1
Изо1бретение от носится к способу лолучения -продуктов ал1килирования а-роматичеоких сое|ДИнений олефинами, которые .могут -быть использованы для переработ1ки в дезинфидиру|ющие средства (детергенты).
Известен способ .пол-учения алкилароматических углеводород ОБ, .заключающийся в том, что углеводороды смешивают с кислотным катализатором и алкилирующим агентам, полученную смесь вводят ,в (первую реакционную зону, из которой кислая эмульсия углеводородов поступает во вторую зону, куда подают дополнительный олефиновый реагент. Алкилирование ведут при О-38°С. Недостатком такого способа является образование большого количества побочных продуктов.
С целью у страненйя указанного недостатка предложено алкилирование на второй ступени вести при С с подачей отработанного .при этом катализатора иа первую стадию алкилирования, «а которой алкилирование ведут при температуре не .менее чем на 3,6° С ниже температуры второй стадии.
Алкилирование на второй стадии желательно вести в 1присутствии фтористоводородной кислоты, содержащей не менее 83 вес. % HF.
Сырьем для реакции алкилирования является, в основном, линейный 1моноолефин, содерлсащий -10-15 атомов углерода, предпочтительно 11 -14, который предпочтительно
(Получают прямым дегидрированием его соответствующего я-:парафппового соединения. Этот .моноолефин используют в качестве алкилирующего агента дл.я соединения, способного алкилироваться, преимущественно для ароматического соединения, содержащего гидрофобную -группу в составе детергента. Подходящими ароматическими соединенияЛ1и могут быть бензол, толуол, ксилол, фенол И мононитробензол.
Алкилирование осуществляют в прис тствии катализатора, активирующего реакцию конденсации. Предпочтительным катализатором является фтористоводородная кислота,
содержащая не менее 83 вес. % HF, лучше 1не менее 90 вес. %.
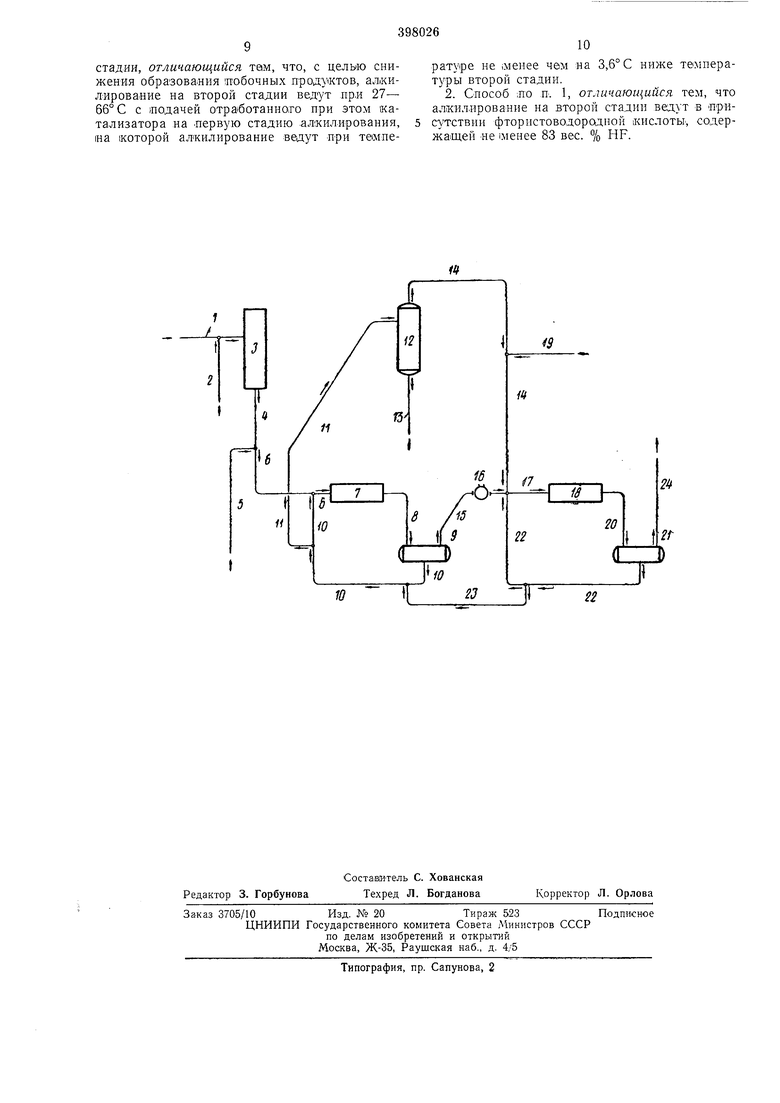
Преп.муществом предлагаемого способа является применение на первой стадии алкилирования катализатора, который раиее был использован на второй стадии этого процесса. Таким образом (катализатор перемещается в направлении, противоположном направлению перемещения углеводородных реагентов. Первую стадию реаКцпи осуществляют предпочтительно при более низкой температуре, чем 1вторую. Поддерживание относительно низкой температуры на первой стадии .позволяет свести к минимуму нежелательные побочные реакции, та.кие, Как реакция .полимеризации. Одна.ко низкая тем.пература, предпочтительная для первой стадии, способствует образованию нежелательных количеств алкилфторидов, загрязняющих Получаемый углеводородный лродукт. Относительно высокая температура, иоддерживаема.я на второй стадии, вызывает частичное разложение их; при этом образуется продукт очень высокой степени чистоты и с очень больш.шм выходом. В промышленности дезинфицирующих средств требуются в достаточной степени бесцветные линейны-е алкилароматичеокие соединения без ол«финовых загрязнений. Поэтому бромное число лолучаеiMoro ал:килата должно быть |менее 30, лредЛОчтительно 10, хотя в некоторых случаях достаточно i6poMHoe число 10-20. При грубом прибл1ил ении бромное число примерно равно количеству (в ррт) олефиновых углеводородов, присутствующих в продукте. Установлено, что слабоокрашенные сульфонаты мотут быть лолучены в том случае, если -моноалкилат имеет индекс по стандартнаму калориметРУ менее 15, преимущественно .менее 10. Моноалкилат, лолученный по лредлагаемому способу, 1ка:к лравило, Иамеет индекс - 5. Первую стадию алкилирования желательно проводить TaiK, чтобы н-олефино,вый алкилирующий агент ло -возможности более лолно вступал в реак1цию, т. е. олефиновый углеводород реагировать с выходом 98%, но менее 100%- Условия троведения второй стадии алкилирования должны быть выбраны TaiK, чтобы оставшийся олефиновый агент был полностью израсходован, а различные алкилфториды, присутствующие в лродукте, полученном лосле лервой стадии, были частично разлол ены. Олефиновый углеводород расходуется преимущественно в количестве 99,9 вес. %. На второй стадии алкилирования в каталитической фазе образуется Лишь небольшое количество де:гтеобразного запряз«яющето вещества; это сводит к минимуму возможность за гряз1не1-шя требуамото .моноалжилата окрашенным вещество.м, таким, «ак ;занесенный из зоны деготь или .продукты лолимеризации. Частично дезактивированный кислый lкaтaлJ-iзaтop из второй стадии реажщии пригоден для активирования «аталитичеокой реакции олефиновым и ароматическим углеводородами, протекающей на лервой стадии, 50 с достаточно высоким выходом. Температура в лервой реакционной зоне лоддерл иваться на относительно низком уровне либо с помощью лригодных теплоо.б;менных средств, таких, как водяное охлаж- 55 дение внутри реактора, либо путем лредварительного охлаждения реагирующих веществ и катализатора. Таким образом, в лервой реакционной зоне должны быть следующие услови.я: температура 4-49° С, пр едп очтительн о 38° С, выдерл :ка в лределах 5-25 мин, лучше 15 мин, объемное отнощение катализатора к углеводороду 0,2 : 1 - 10 : 1, как лравило, 2:1. Для получения максимального выхода .моноалкилата из исходного алкилирующего агента 65 необходимо, чтобы молярное отношение ароматического соединения .« алкилирующему агенту -было больше, чем I : 1, а лучше 2: 1 - 15; 1. Кроме того, молярное отношение ароматичеакого углеводорода к сумаш олефинового углеводорода и алкилата быть 3:1, предпочтительно 8:1. Верхний предел этого отношения диктуется экономикой процесса. Температура во второй реакционной зоне должна быть преимущественно на 3,6° С выше температуры лервой реакционной зоны. Таким образом, условия в этой зоне следующие: тбмлература 27-66° С, лучще 49° С, выдержка в лределах 5-25 мин, лредпочтительно 15 мин, объемное отношение катализатора к углеводороду 0,2 : 1 - 10 : 1, как правило, 1:1. Молярное отношение ароматического углеводорода к cyMiMe олефинового углеводорода и алкилата должно быть более 2:1, лреимущественно 7:1. Контрольной точкой кислотности катализатора (процент фтористого водорода) является весовое содерлсаиие кислоты в лродукте, загружаемом в зону регенерирования катализатора. Кислотность кислого .катализатора в лервой реакционной зоне составлять 86-92 вес. %, лреимущественно 90 вес. %. Катализаторы, кисччотность которых выше или этого предела, в некоторых случаях могут использоваться, однако кислотность не доитжна быть ниже 83%. Кислотность катализатора второй реакционной зоны должна быть больше 90 вес. %, лреимущественно 93-100 вес. %, лучше 93-94 вес. %. Тер:мин «свежий катализатор, используемый здесь для удобства, обозначает ка.к новый катализатор, поступа.ющий извие, так и регенерированный катализатор, подаваемый из зоны 1каталичеокой регенерации. Катализатор, поступающий в зону регенерации, должен иметь концентрацию 90 вес. %, чтобы получить регенерированный катализатор с концентрацией 94 вес. %. На чертел ;е изображена схема :получения алкилароматичеоких углеводоро.дов. н-Нарафиновый углеводород с числом ато,мов углерода И-14 (степень чистоты 98%) л од а ют в зону реакции ио линии 1, где при необходимости его смещивают с дополнительной лорцией рециркулированного н-парафина. поступающего .по линии 2. Суммарное количество углеводорода поступает в зону дегидрирования 3, которая представляет собой неподвил ;ный слой .катализатора, поддерживаемый в сравнительно (МЯ.гжих условиях: темпе ратура 466°С и давление 2,6 атм. Затем систему добавляют водород в тако:м количестве, чтобы .молярное отношение водорода к сум1марной загрузке углеводорода было равно 8. Желательно, чтобы в сум1марнам поступающем :потоке содержание воды составляло 2000 ррт. Продукт реакции соответствующего линейного олефинового углеводорода, содержащий - 95% моноолефина, удаляют из зоны 3 ло линии 4. Оставшиеся 5% вещества .представляют собой в основном диеновый углеводород с незначительны количеством ароматических утлевадородов. Побочным прод}жто1М дегидрирования является водород (степень чистоты 96%), удаление которого из зоны 3 на чертеже не обозначено.
Катализатор, используемый в 3оне 3, активирует дегидрирование парафинов до моноолефинов без изомеризации нормальных парафинов или поллчаемых моноолефинов до соответствующих анало-гов с разветвленной цепью. Подходящими :катализатора1ми, которые способствуют мияимальной изомеризации, являются нейтральные окиси элементов VI группы И сульфиды ИЛИ окиси металлов VHI группы Периодической системы. Наиболее предпочтительным катализатором дегидрирования Парафиновых углеводородов с нормальной цепью являются благородные металлы или сое:.1инения металлов, таких, (как .платина или палладий, осажденные на нейтральной или основной подложке, та.кой, как алюминий.
Продукт, .поступающий -из зоны 3 в лшнию 4, смещивается с бензолом из линии 5, и смесь моноолефинов с бензолом направляется по линии 6 в тервую зону алкилирования 7, из которой продукт ПО линии 8 етостлпает в зону разделения 9, 1где в результате отстаивания кислая каталитическая фаза отделяется от углеводородной. Кислая каталитическая фаза удаляется из этой зоны л о линии 10 и возвращается в зону 7 в смеси с продуктом, поступаюшим по линии 6. Частично использованный катализатор отводится по необходимости из линии 10 и направляется .по линии И IB зону регенерации 12 катализатора.
Регенерация обычно сопровождается десорбированием кислыот катализатором углеводорода в виде inapa в условиях, достаточных для разложения ал-килфторидов и удаления регенерированного кислого 1катализатора в виде пара. Оставшееся дегтеобразное вещество удаляется из зоны 12 по линии 13.
Регенерированный катализатор (названный здесь свежим катализатором) из зоны 12 направляется по линии 14 для смешения с углеводородной фазой, пропущенной через зону 9 и линию 15. Выделенная углеводородная (Ьаза, в значительной степени свободная от кис.лоты, по линии 15 поступает в обогреваЮщее л-стройство 16, где температуру повышают -по крайней мере на 3,6°С по сравнению с температлфой зоны 7. Подогретая углеводородная фаза и кислый Катализатор направляются по линии 17 ПРИ относительно высокой теМПературе во вторую зону алкилирования 18. Обработанный соответствующим образом катализатор добавляют в зону реакции по .тинии 19.
Прод 1ктьт реа КЦии. вытекающие из зоны 18, удатяют я по линии 20 и направляются в ЗОНА пяз.деления 21, где кислота отделяется от -леводородов. Отделивщаяся кислая фаза ИЗ зоны 21 поступает по линии 22 в зону 18 в смеси с продуктом, направляемым в эту
зону по линии 17. Некоторое Количество частично дезактивированного в линии 22 кислото (катализатора постуПает по линия;м 23 и 10 обратно в зону 7. Таким образом, единствен1НЫМ источником (КИСЛОГО катализатора для первой реакционной зоны является частично дезактивированный катализатор, который ранее был использован во второй реакционной зоне.
У.гловодородная фаза из зоны 21 поступает по линии 24 в регенерирующие устройства (на чертеже не показаны). Моноалкилатный продукт с бромным числом Менее 30, преимл-щественно 10-20. выделяют из смеси в Линии24.
. Проводят три опыта. В первом опыте алкилирование ведут при 38°С, молярном отношении бензол : олефин 10:1, с использованием в Качестве катализатора безводного фтористого водорода (содержание HF
99-100 вес. %), при объемном отнощении HF к углеводородам 2, а во втором - при 60° С И Прочих равных условиях. В третьем опыте алкилирование ос}Ществляют в две стадии. При этО:М на второй стадии (на которой углеводородной загрузкой является вьтделенная углеводородная фаза реакции первой стадии) в качестве катализатора используют свежий безводный Лтористый водород, а на первой стадии - 93-94%-ную фтористоводородную
кислоту, регенерированную из Продукта реакции второй стадии процесса:, вторая стадия осуществляется при температуре на 6° С выше температуры первой стадии.
В опыте 1233 мл бензола, пригодного для
нитрации и свободного от тиофен, высущенного до содержания воды менее 50 прт, загружают при 21° С в охлаждаемый водой реактор с т -рбомещал1кой (скорость вращения рабоче о колеса 1500 об/мин), охлажденный
до 10° С с пОМощью теплообменного змеевика в стенках реактора. После охлаждения до 0°С добавляют 4000 жл безводного HF и содержимое реактора иатревают до 38° С. Затем в турбомешалку (при скорости вращения рабочего колеса 1500 об/мин в течение 30 мин с равномерной скоростью за.-ружяют 2000 мл ннмоноолефино-парафиновой омеси, содержащей 10 вес. % моноолефинов, образованных дегидрогениз: цией н-парафинов с числом
углеродных атолшв в пени 10-15 и средним Молекулярным весом 174,6, после чего смесь лопо.ттнительно перемешивают 15 мин при 38° С. Давление в реакторе 1-3 ата.
Содержимое peaiKTopa охлаж.дают до 10° С и отделивщуюся при стоянии фтористоводорадную фазу отделяют от верхней уг.тезодородной фазы. Углеводороднмо фазу, содержащую растворенный HF, нейтрализуют углекислым калием. Продукт перегоняют на следующие фракции: бензол. Фракция из w-napaфинов, фракп я из алкилбензолов, кипящих при 289-335° С. Фракция донного остатка, состоящая из высо:кокипящих полиалкилбензолов, остается в перегонной колбе,
Изучение регенерированной етарафиновой фракции с 10-15 атомами углерода доказало, что весь олефин лрореагировал в обеих партиях, .причем бромное число обеих парафиновых фракций -было менее 2.
Выход ал1килата (в расчете на прореагировавшие олефиныО в первом оцыте 89,6%, во вторам 90,6%. Отношение веса ал1кил1ата к весу загруженного олефина соответственно 1,378 и -1,392.
Показатели регенерированного (рекуперированного) алКИЛата приведены в таблице.
Рост разветвленности боковой цепи указывает на потерю способности к биологическому распаду детергентного продукта, полученного из алкилата.
Цвет сульфонированного продукта является первичным показателем качества, поскольку в нем соединяются белизна с чистотой. Содержание олефинов в алкилатной фракции (как показывает бромное Число) является поэтому обратной мерой качества алкилата вместе с качественным отношением роста разветвленности алкильной боковой цепи, которая также находится в обратной зависимости от склонности к биологическому распаду.
В опыте 3 алкилирование осуществляют в две стадии, лричем на первой стадии свежие бензол и олефин находятся в (контакте с фтористоводородным катализатором, лредварителъно иопол Ьзован1НЫ1М на второй стадии реакции и выделенным из алкилирующей смеси этой стадии. Первую стадию проводят при 38° С, а вторую - при 44° С, используя в качестве катализатора первой -стадии фтористоводородную кислоту со второй стадии. С целью получения катализатора для лервой стации свежий бензол и олефин, содержащий в цепи 10-15 атомов углерода (продукт дегидрогенизации к-ла(рафина, содержащего в це1ПИ 10-15 атомов углерода, в котором находится 10 об. % «-олефинов) алкнлируют при отношении бензола к олефину 10 : 1 в присутствии 100%-ной фтористоводородиой кислоты, при отношении HF к суммарному количеству углеводородов 2 :1, давлении 3 ата и средней продолжительности контакта (между кислотой и углеводородами 45 мин. Продукты реакции отделяют и регенерируют фтористоводородную кислоту, содержащую (в вес, %): 93 HF, 1,2 воды и 5,8 углеводородов.
Первая стадия процесса в опыте 3 начинается при использовании 93%-ной фтористоводородной кислоты, регенерированной (рекуперированной) из вышеприведенной реакции алкилирования, а затем из реакционной смеси второй стадии двухстадийного процесса. 233 мл бензола, пригодного для нитрации, загружают в реактор с турбомещалкой (1500 об/мин) при 2ГС, охлаждают до 10°С, а
затем смешивают с 4100 мл использованной при алкилировании фтористоводородной кислоты, регенерированной, как было описано выше. Смесь «а-трева-ют до 38° С и равномерно в течение 30 мин загружают в турбомешалку (1500 об/мин) 2000 мл н-1моноолефина с длиной цепи атомов углерода (средний молекулярный вес 174,6), после чего омесь дополнительно перемешивают 15 мин при 38° С. Давление по,ддерживают на уровне
3-4 ата. Далее реакционную смесь разделяют на верхний углеводородный слой и на нижний слой использованной катализаторной кислоты, который осушают с целью регенерации катализатора. Углеводородную
фазу снова перемешивают со скоростью 1500 об/мин при paBHOMepHOjM введении при 44°С в продолжении 10 мин 4000 мл 100%ного фтористоводородного катализатора, после чего продолжают перемешивать гари 44° С
в течение 6 мин.
Катализаторную фазу в виде использованной кислоты удаляют из реактора и сохраняют для следующего процесса, в котором катализатор используется дл.я первой стадии алкилироваиия. Углеводородную фазу верхнего слоя про1мьгвают водой, содержащей , с целью нейтрализации растворенного HF, после чего высушивают над безводным К2СОз. Продукт второй стадии алкилирования перегоняют сначала под атмосферным давлением для рекуперации И3быт1ка бензола и н-парафинов, а затем под давлением 2 мм рт. ст. с целью регенерации (рекуперации) алкилбензолъного продукта из остатков перегонки,
содержащих алкильные и диалкильные тетралины, нафтены и другие высококипящие продукты. Фракцию, кипящую в пределах 280-328° С (соответственно атмосферному давлению), получают с выходом 91,3% (в расчете на вес за1грузки олефинов). Этот алкилат характеризуется :бромньш числом менее 2 и содержит 8 ррт фторидов. Отмечено повышение разветвленности в баковой цепи на 5,4%. При сульфонировании 20%-ным олеуiMOM при температуре О-10°С и нейтрализации едким натром алкилат образует детергент в виде алкилбензолсульфоната натри.я почти белого цвета.
Предмет изобретения
1. Способ получения алкилароматических углеводородов путем алкилирования бензола н-олефина1ми, содержащими 10-15 атомов углерода в (молекуле, в присутствии катализатора - фтористоводородной кислоты в две
стадии, отличающийся там, что, с целью снижения образования иобочных продлжтов, алкилйроваиие на второй стадии ведут пр.и 27- 66° С с подачей отработанного ири этом катализатора на .первую стадию .алкилирования, 1на которой алкилирование ведут п-ри температуре не ;менее чем на 3,6° С ниже температуры второй стадии.
2. Способ ло п. 1, отличающийся тем, что алкиллрование на второй стадии ведут в присутствии фтористоводородной КИСЛОТЫ , содержащей не 1менее 83 вес. % HF.



| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ АЛКИЛАРОМАТИЧЕСКИХ УГЛЕВОДОРОДОВ | 1971 |
|
SU316245A1 |
| СССРОпубликовано 07.Х11,1972. Бюллетень № 1за 1973Дата опубликования описания 5.III.1973УДК 665.652.4(088.8)Иностранец | 1973 |
|
SU361576A1 |
| СПОСОБ ДВУХСТУПЕНЧАТОЙ ГИДРООЧИСТКИ БЕНЗИНОВ ВТОРИЧНОГО ПРОИСХОЖДЕНИЯ | 1973 |
|
SU404273A1 |
| СПОСОБ ПОЛУЧЕНИЯ ОЛЕФИНОВЫХ УГЛЕВОДОРОДОВ | 1971 |
|
SU309505A1 |
| В П Т Б | 1973 |
|
SU399144A1 |
| ВПТБ | 1973 |
|
SU400075A1 |
| СПОСОБ РЕГЕНЕРАЦИИ ФТОРИСТОВОДОРОДНОГО КАТАЛИЗАТОРА | 1971 |
|
SU291406A1 |
| Способ получения алкилбензина | 1982 |
|
SU1101440A1 |
| Способ получения высокоокта-НОВОгО КОМпОНЕНТА МОТОРНОгО ТОп-лиВА | 1976 |
|
SU799642A3 |
| КАТАЛИТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЖИДКОФАЗНОГО АЛКИЛИРОВАНИЯ ОЛЕФИНОВ И СПОСОБ ЖИДКОСТНОГО АЛКИЛИРОВАНИЯ ОЛЕФИНОВ (ВАРИАНТЫ) | 1993 |
|
RU2104087C1 |


Авторы
Даты
1973-01-01—Публикация