1
Изобретение относится к способу полу- | чения новых соединений - производных триазолбензодиазепинов формулы
где R - атом водорода или алкил с
1-3 атомами углерода; R -R - атом водорода, алкил с 1-3
1 о
атомами углерода, фтор, хлор, бром, нитроили цианогруппа, трифторметил, алкоксигруппа с 1-3 атомами углерода, амино- J 25
или алканоиламиногруппа, где алканоиль- | ная группа содержит 1-3 атома углерода, алкилтио-, алкилсульфинил или диалкилами- ногруппа, в которых алкильная группа содержит 1-3 атома углерода.
Эти соединения обладают ценными физиологически активными свойствами.
Предлагаемый способ является многостадийным и основан на реакциях получения бензотриазо/ioB, расщепления хинолинового цикла и образования бензодиазепинового цикла.
Предлагаемый способ заключается в том, что 2-хлор-4-фенилхинолин (юрмулы
15
И
ОА
где R -F} имеют указанные значения,I
нагревают с гидразингидратом до температуры -кипения, образующееся производное 2-гидразино-4-фенилхинолина формулы
III
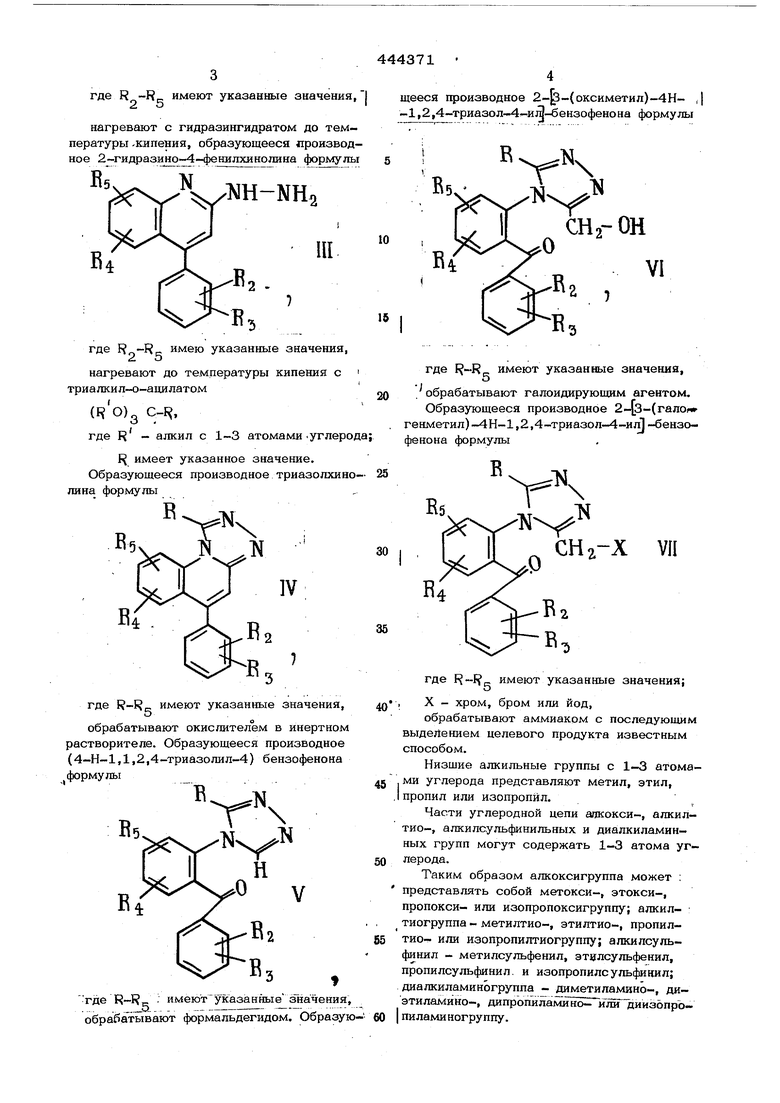
2 щееся производное (оксиметил)-4Н- ,| -1,2,4-триазол-4-и; -ёензофенона формулы где F -R имею указанные значения 2. о нагревают до температуры кипения с триалкил-о-ацилатом (ROQ С-Ц, где R - алкил с 1-3 атомами .углер f имеет указанное значение. Образующееся производное триазолхин лина формулы где R-Rc; имеют указанные значения, о обрабатывают окислителем в инертном растворителе. Образующееся производное (4-Н-1,1,2,4-триазолил-4) бензофенона формулы V где R-1 имеют указанныезначения обрабатывают формальдегидом. Образу где имеют указанные значения, 5 обрабатывают галоидирующшл агентом. Образующееся производное (галоя генметил)-4Н-1,2,4-триазол-4-ил -бензофенона формулы Y TL N- СНг-Х VII где R-R имеют указанные значения; X - хром, бром или йод, обрабатывают аммиаком с последующим выделением целевого продукта известным способом. Низщие алкильные группы с 1-3 атомами углерода представляют метил, этил, пропил или изопропйл. Части углеродной цепи апкокси-, алкилТИО-, алкилсульфинильных и диалкиламинных групп могут содержать 1-3 атома углерода. Таким образом аякоксигруппа может : представлять собой метокси-, этокси-, пропокси- или изопропоксигруппу; алкилтиогруппа - метилтио-, этилтио-, пропилтио- или изопропилтиогруппу; алкилсульфинил - метилсульфенил, этилсульфенил, пропилсульфинил. и изопропилсульфинил; диалкиламиногруппа - диметиламино-, диэтиламино-, дипропиламино Г ишГдиизбпрЬпи лами ногру ппу.
I Алканоиламинная группа с 1-3 атомами углерода состоит из формамидо-,
О
II
(-NH-C-H)
)
ацетиламидо- или пропионамидогруппы.
Получаемые предлагаемым способом кислото-аддитивные соли соединений фор- 10 мулы I представляют собой гидрохлориды,, гидробромиды, гидройодиды, сульфаты, фосфаты, циклогексансульфаматы, метансульфонаты и т. п., получаемые взаимодействием соединения структурной формулы 1с 15 избытком соответствующей кислоты.
2-хлор-4-фенилхинолин формулы Д нагревают с гидразингидратом до темпера- , туры кипения, однако реакцию можно вести и при 25-118°С. Реакцию проводят в 20 течение 1-18 час в среде растворителя или без него. В качестве растворителя t можно Применять низший алканол, например метанол, этанол, 1- или 2-пропанол. При п эедпочтитеяьном варианте достаточно25
1 часа нагревания при температуре в атмосфере азота. По окончании ре- . акции смесь концентрируют, выливают в воду, нерастворимый продукт отфильтровывают. Очистку производят обычным спо- 30 собом, например экстрагированием, хроматографией или перекристаллиза 1ией, после чего получают соответствующий 2-гидразино-4-фенилхинолин (Ш).
Соединение формулы П1 превращают в 35 соответствующий 1-замещенный-5-фенил- - -триазол (4,3-а)хинолин (ГУ) нагреванием с о-низшим алканольным сложным эфиром карбоновой кислоты, например триметил- или триэтил-о-ацетатом. При этой 40 реакции целесообразна температура 80- ; 170 С. В качестве растворителей можно применять гептан, октан, метилциклогексан, бензол, толуол, ксилол (о-, м-, или ft -). Предпочтительно реакцию проводят 5 в атмосфере азота в высококипящем растворителе, например ксилоле, при температуре реакционной смеси. Низшие алканолы, образующиеся в течение реакции вследствие распада орто-сложных эфи- 50 ров, можно удалять дистилляцией. Продукт (1У) регенерируют и очищают обычными способами, например концентрацией реакционной смеси досуха, экстрагированием, . хроматографией и/или перекристаллизацией. 55
Окислением соединения 1У в завиЪимЬсти от окислителя и условий реакции получают 2-(3-замещенный-4Н-1,2,4-триазол-4-ил)бензофенон (У) и/или 4-(2-бензоил Нил)-5-замещенный-4Н-1,2,4-триазол-3- 60
-карбоксальдегид. Окисление можно осуществлять перйодатом натрия с перманганатом натрия или двуокисью рутения д качестве катализатора или озоном и т. п. При применении озона,кроме указанных соединений, получают также 1--эвмеш н1{ый-$-фе 1ил- S -триазол-(4,3-а)-хинолин.-4(5Н)-он. Окисление с помощью двуокиси рутения и перйодата натрия проводят при 0-3 0°С в течение 2-24 час. Перйодат натрия применяют в б-ЮО-кратном весовом избытке по сравнению с двуокисью рутения. В качестве растворителей применяют смеси воды и ацетона. . Реакционную смесь можно фильт.ровать или вначале кбнцентрировать и затем 1фильтровать. Чистые вещества можно получать обычными способами, например экстрагированием, хроматографией, перекристаллизацией, комбинацией этих способов., и т. п. Реакцию можно прекращать также добавпеншем йодида и тиосульфата натрия. Этот последний способ целесообразен при использовании в качестве окислителя органического реактива. При способе окисления озоном применяют температуры 0-3О°С в течение 12-24 час; в качестве растворителя или системы растворителей применяют инертные органические растворители (метанол, этанол, хлористый метилен, хлороформ) или их сочетание.
Соединение У превращают в соответствующий 2-j3-(оксиметил)-б-аамещенный-4П-1,2,4-триазол-4-ил -бензофенон (У1) нагреванием его с формальдегидом в растворителе. Рекомендуется применять водный формальдегид при 1ОО-15О° в течение 318 час в герметичной рабочей систему.
Предпочтительно используют избыток па- раформальдегида в инертном растворителе, как толуол, ксилолы, изооктан с т. кип. 10-140 С. При этой температуре для реакции требуется 3-18 час. Продукт (У1) выделяют и очищают обычными способами (хроматографией, экстрагированием, перекристаллизацией).1
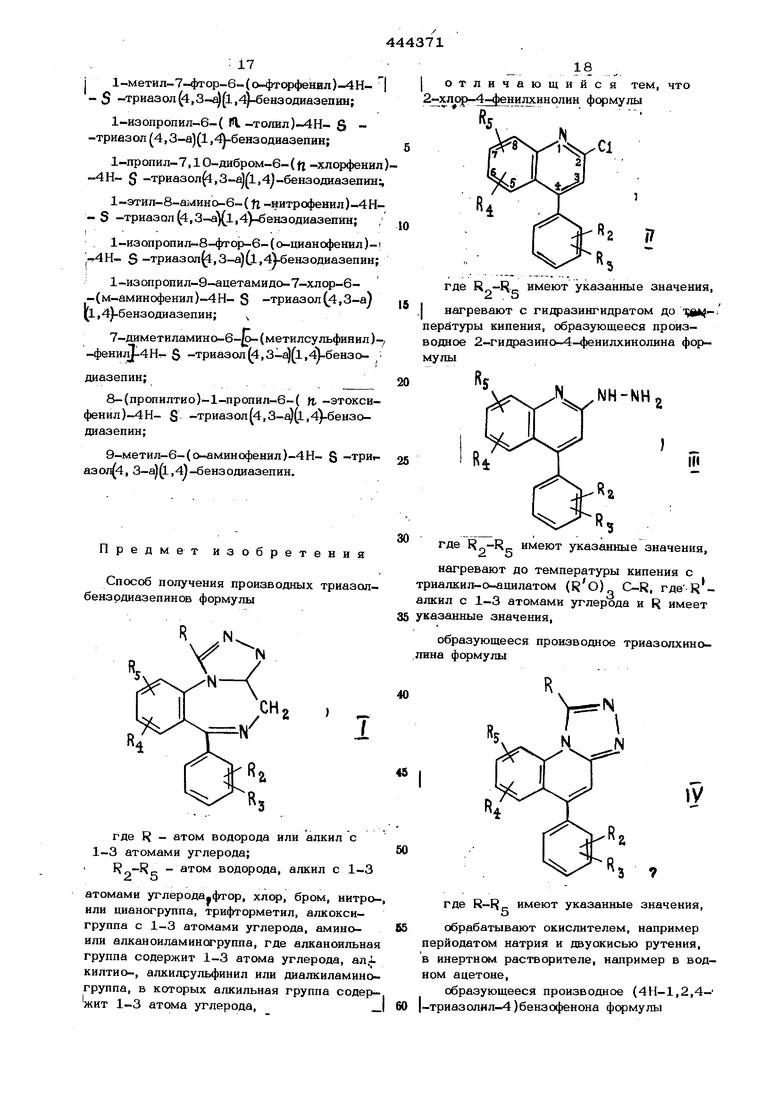
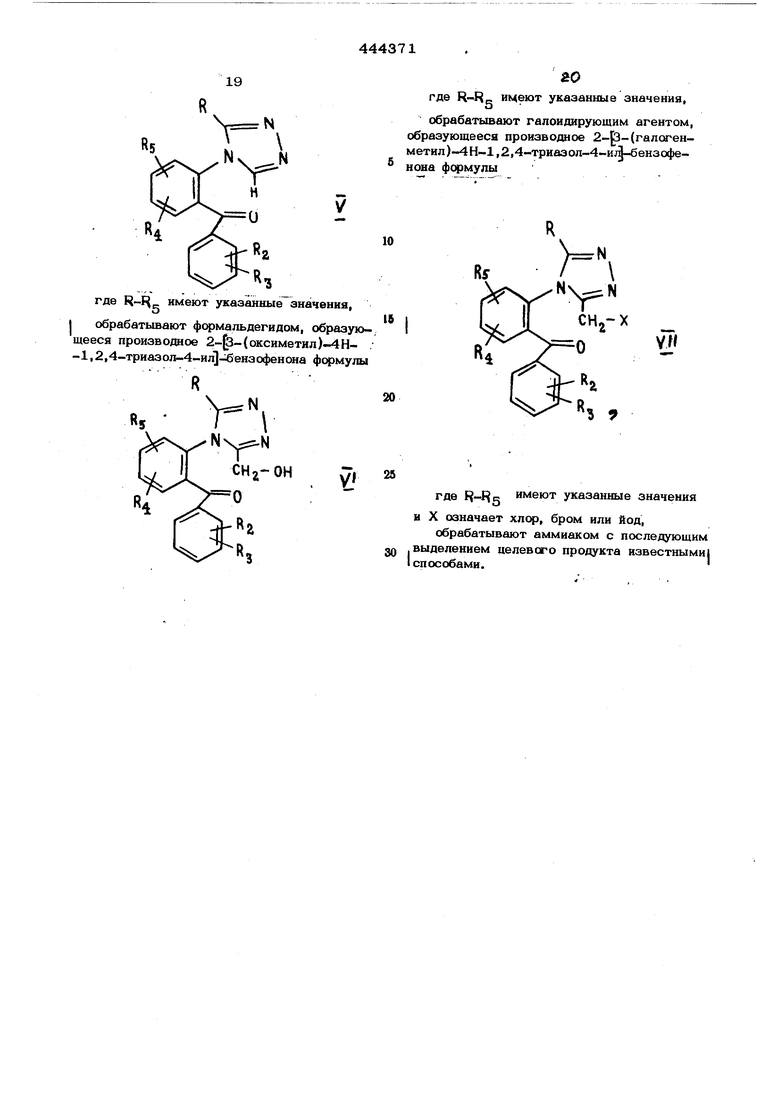
Соединение У Г превращают в (галогенмётил)-5-замещенный-4Н-1,2,4-триазол-4-ил бензофенон (УИ) путем обработки раствора соединения У1 галоидируюшим агентом, как хлористым или бромистым тионилом, оксихлоридом фосфора, трихлористым.трибромистым или трийодистым фосфором, в качестве инертных растворителей в этой реакции применяют например, бензол, толуол, -хлористый метилен, хлороформ, четыреххлористый углерод и т. п. При применении хлористого тионила, предпочтительна температура 50-80°С, при применении галоидов фосфора в хлорированных углеводах - 0-25°С. ; Нодид структурной формулы УП можно также получит реакцией обмена, например обработкой хл рида структурной формулы УП йодидом натрия в ацетоне в течение 2-8 час при 25-55 С. По окончании реакции продукты структурной формулы УП выделяют и очищают обычным способом, например хроматографией, экстрагированием, перекристал лизацией и т. п. Соединение УП подвергают циклизации путем обработки его неводным раствором аммиака. Предпочтительно можно использовать - етрагидрофуран, метанол, этанол, хлористый метилен, эфир и т. п., применим также безводный аммиак без растворителя при его температуре кипения (-33 Предпочтительно растворитель применяют при 0-ЗО°С в течение 18-72 час. Соединение (УШ) выделяют и сушат по окон чании реакции обычными способами, например экстрагированием, хроматографией перекристаллизацией и т. п. Пример 1. 6-Улор-2-гидразино.-4-фенияхинолин. Размешиваемую смесь 2, 7 г (0,01 м ля) 2,6-дихлор-4-фенилхинолина и 6,8 г гидразингидрата разогревают до температуры кипения в атмосфере азота в течение 1 часа, затем концентрируют в вакуу ме. Остаток взвешивают в теплой воде, твердое вещество отфильтровывают, высу- шивают и перекристаллизовывают из этилацетата скеллисольв-В-гексанов, получая 1,81 г (67%ОТ теоретического) 6-хлор-2-гидразино-4-фенилхинолина с т. пл. 156-157°С. Вычислено, %: С 66,79; П 4,49; С1 13,15; N15,58. %: С 67,15:, Н 4,65-., Найдено, N 15,32. С1 13,19; Пример 2. 7-5 лор-1-метил-5-фенил- S -триазол(4,3-а)хинолин. Размешиваемую смесь 1,4 г (. ля) 6-хлор-2-гидразино-4-фенилхинолина, 0,925 г (О,ОО57 моля) триэтил-о-ацетата и 100 мл ксилола разогревают до температуры кипения в атмосфере азота в течение 2 час 40 мин. Образующийся при этом этанол удаляют дистилляцией через короткую наполненную стеклянной спираль .колонну. Затем смесь концентрируют в ва кууме досуха, остаток выкристаллизовыва ют из метанол этилацетата, получая l,0 7-хлор-1-метил-5-фенил- S -три азолЙ-3 Ual-хинолина О.26 г с т. пл. 253-255 - I . 1 V . ход 83,9%). Аналитическую пробу выкристаллизовывают из хлористого метилена/ме- танола, получая т. пл. 252,5-253,5 С, Вычислено, %: С 69,50; Н 4,12; С1 12,07 N14,31. Найдено, %: С 69,39; Н 4,04; N14,49. С1 12,105, Пример 3. 5-)блор-2-(.3-метил-4Н-1,2,4-триазол-4-ил)-бензофенон (окисление 7-хлор-1-метил-5-фенил- S -триазол(4,3-а)хинолина). Размешиваемую взвесь 7-хлор-1-метилl-5-фенил- S -триазол(4,3-а)хинолина (2,94 г, 0,01 моля) в 110 мл ацетона охлаждают в ледяной бане и медленно обрабатывают раствором, полученным добавлением 2 г перйодата натрия в размешиваемую взвесь двуокиси рутения (2ОО мг) в 35 мл воды. Смесь темнеет. Затем в течение следующих 15 мин добавляют дополнительно 8 г перйодата натрия. Ледяную баню удаляют, смесь еще размешивают 45 мин. Добавляют еще 4 г перйодата натрия, смесь еще размешивают в течение 18 час при температуре окружающей среды и фильтруют. Твердое вещество промывают ацетоном, комбинированные фильтраты кон- I центрируют в вакууме. Остаток взвешивают в воде и экстрагируют хлористым метиленом. Экстракт высушивают над безводным карбонатом натрия и концентрируют. Остаток хроматографируют на силикагеле (100 г) с 10% метанола и 90% этилацетата:, получают 50 мл фракций. Продукт элюируют и выкристаллизовывают из этилацетата, получая О,4О5 г с т. пл. и 0,291 г с т. пл. 167,5(выход составил 23,4%) 5-хлор- i 1-2 (3-метил-4Н-1,2,4-триазол-4-ил )-бенЗофенона. Аналитическая проба имеет т. , :пл. 168°С. I Вычислено, %: С.64,54; Н 4,06; 1С1 11,91; N14,11. ICl6 l2 3° I,..... .. Найдено, %: С 64,56; Н 4,35; С1 11,97; 11,93; N 14,29. j Пример 4. Окисление 7-xnop-l-метил-5-феиил- 5 -триазол(4,3-а)хино-( лина.. Размешиваемую взвесь 2,94 (0,61 моля) 7-хлор 1-метил- 5-фенил- S -трйазол- (4,3-а)хинолина и 20О мл ацетона охлаждают в ледяной бане, затем по каплям .воздействуют в течение 15 мин раствором, {полученным из 200 мг двуокиси рутения, ( : 9. 4 г перйодата натрия и 35 мл воды. Наблюдается легкая экзотермическая реакция и потемнение смеси. Через 10 ми в течение следующих 1О мин добавляют 29 мл раствора перйодата натрия (12; г) в 70 мл воды. Смесь затем в течение 2 час размешивают, после чего добавляю раствор (41 мл) перйодата натрия в течение следующих 3 час. Смесь концентри руют в вакууме в целяхудаления ацетона Оставшуюся водную смесь экстрагируют хлористым метиленом. Экстракт промывают водой, высушивают над безводным сульфатом магния и концентрируют. Остаток хроматографируют на силикагеле (150 г) с 2% метанола и 98% хлорофсрма. Получают 60 мл фракций. Регенерированный исходный материал, элюируют во фракциях 11-14 и выкристаллизовывают из метанола-хлористого метилена, по лучая 0,069 г вещества с т. пл. 251,5- 253,5°С. Смесь двух продукте элюирую во фракциях 15-39. Выкристаллизовьшанием этой смеси из этилацетата получают 618 г (2О,8%) 5-хлор-2-(3-метил-4Н-1,2,4-триазол-4-ил)бензофенона с т. пл 165,5-168°С. Кристаллизацией маточного раствора из метанола получают 0,126 продукта с т. пл. 108-112°С и 0,588г продукта с т. пл. 101,5-105,5 С (с раз ложением). Выход метанолеольвата 4-(2-бензоил-4-хлорфенил)-5-метил-4Н-1,2, 4-триазол-3-карбоксальдегида составил 100-101,5 h. Вычислено, %: С 62,68; Н 3,72; С1 10,89; N12,90. Найдено, %: С 59,37; Н 4,89; С1 9,75; N11,30. Исправлено для МеОН и Н О%: С 61,9О; Н 4,06; С1 1О,80; N12,52 I Разогревание сольвата в эксикаторе пр 7О С/15 мм рт. ст. в течение 72 час дает чистый 4-(2-бензоил-4-xлopфeнил)-5-метил-4Н-1 , 2,4-триазол-3-карбоксаль дегид. Пример 5. Окисление 7-хлор,-1-метил-5-фенил- S -триазол,3-а)хинолина. I: В течение 12 час в размешивамый, охлажденный льдом раствор 31,1 г ( (0,106 моля) 7-хлор-1-метил-5-фенил- S -триазол(4,3-а)хинолина в 750 мл метанола и 500 мл хлористого метилена вводят сильную струю озона в- кислороде . 10 (Образующуюся смесь фильтруют, фильтрат | добавл5пот в ледяной раствора йодида натр1 я-(47,5 г) и уксусной кислоты (63 мл) в 20О мл воды. Раствор обеспечивают добавлением тиосульфата натрия и концент-т рируют в вакууме. Остаток смешивают с водой и экстрагируют хлористым метиле- , ном. Экстракт промывают водой, высушивают над безводным сульфатом магния и концентрируют Остаток хромато- графируют на силикагеле (1,5 кг); получают 175 мл. фракций. Фракции 1-128 алютруют 1% метанола и 99% хлсроформа, а фракция 129-168 - 5% метанола и 95% хлорофсрма. Первое соединение элюи1руют во фракциях 49-6О и выкристалли- . зовьшают из метанола-этилацетата, получая 0,769 г с т. пл. 229г5-231°С (с с разложением) и 0,535 г с т. пл. 228с (с разложением) 7-хлор-1-метил-5-фенил- - S -триазол 4,3-а)хинолин-4(5Н)-она. Аналитическая проба имеет т. пл. 232233°С. Вычислено, %: С 65,92; Н 3,91; С1 11,44; N13,57. 3° Найдено, %: С 65,46:, Н 3,72; С1 11,48; N13,59. Регенерированный исходный материал элюируют во фракциях 66-78 и выкристаллизовьшают из хлористого метилена-метанола, получая 0,737 г продукта с т. пл. 251-253,. Смесь оставшихся двух про. дуктов элюируют во фракциях 73-168. Кристаллизация этой смеси из этилацетата дает 1О,8 г с т. пл. 166,5-167,5°С; , 0,987 г с т. пл. 166-167°С и 2,52 г с т. пл. 164-165,5°С (выход 45,3%) 5-хлор-2-(3-метил-4Н-1,2,4-триазол-4-ил)-бензофенона. Кристаллизация маточного раствс а из метанола дает 5,62 г ст. ал. 140-141,5°С; 1,23 г с т. пл. 10О,51О2,5 С (с разложением) и 1,О4 г с i т. пл. 105-137,5°С (выход 20,8%) 4-(2-бензоил-4-хлорфенил)-5-метил-4Н-1,2,4-триазол-З-карбоксальдегида. Пример 6. 5-Хлор-2- 3-(оксиметид)-5-метил-4Н-1,2,4-триазол-4-ил)}-бензофенон. Размешиваемую смесь 2,98 г (0,01 моля) 5-хлор-2-(3-метил-4Н-1,2,4-триазол-4-ил)-бензофенона, 3 г параформальдегида и 10О мл ксилола разогревают 7 час в атмосфере азота в бане 125°С. Затем смесь концентрируют в вакууме. Остаток хроматографируют на силикагеле (150 г) метанола и 97% хлороформа. Получают 50% фракций. Продукт элюируют во фракци$1х 2О-44. Фракции концентрируют, остаток кристаллизуют из этанола-этилацв тата, получая 1,64 г с т. пл, 138-142°С 0,316 г с т. пл. 138,5-141°С; 0,431 г с т. пл. 139-1410С (выход 72,8%) 5-хлор-2- З-(оксиметил)-5-метил-4Н-1,2, 4-триазол-4-ил}-бензофенона. Аналитическая проба имеет т. пл. .38-139°С. Вычислено, %: С 62,ЗО; Н 4,30; Ci 10,81; N12,82. 17 l4 N3°2 Найдено, %: С 62,23; Н 4,22; С1 10,82; All 1,73. Пример 7.5-xлop-2-jЗ-{бpoммe-тил )-5-метил-4Н-1 , 2,4-тpиaзoл-4-ил1-бeнзoфeнoн. Раствор 328 г (О,О01 моля) 5-хлор-2-| - (оксиметил )-5-метил-4Н-1,2,4-триазол-4-ил1-бензофенона в сухом стабилизированном углеводом хлороформе (5 мд) охлаждают в ледяной бане и обрабатывают трибромистым фосфором (0,1 мл). Бесцвет ный раствор выдерживают в ледяной бане 55 мин при температуре окружающей среды (22-24°С) в течение 5 час. Образующийся желтый раствор выливают в смесь льда и раствора бикарбоната натрия. Эту смесь экстрагируют хлороформом. Экстрак промывают рассолом, высушивают над безводным сульфатом магния и концентрируют Остаток кристаллизуют из хлористого ме- тилена-этилацетата, получая 0,285 г с т. пл. 200-24О°С (с разложением) и 0,ОЗО г с т. пл. 200-220°С (с разложением ) 5-хлор-2- -(бромметил)-5-метил- -4Н-1,2,4-триазол-4-ил|-бензофенона. Ан литическая проба имеет т. пл. 2ОО-24О°С Вычислено, %: : С 52,, Н 3,35; ВГ 2О,46; С1 9,08; М10,76; C,H,BrClN,0 Найдено, %: С 52,13; 52,45; Н 3,77 3,66; ВП 20,44; С1 9,20; N10,43, . Пример 8. 5-хлор-2- 3-(хлорметил )-5-метил-4 Н-1,2,4-триаз ол-4-ил1-бензофенон. 328 г (0,001 моля) 5-хлор-2-|3-(оксиметил)-5-метил-4Н-1,2,4-трназол-4-и4 -бензофенона, растворенного в хлсфйстом тиониле (2 мл), разогревают в течение 4О мин до температуры бани 78°С и выдерживают 1 час 25 мин при 78-83°С. Затем раствор, охлаждают и выливают в ледяную воду. Смесь нейтрализуют бикарбонатом натрия и экстрагируют хлороформом. Экстракт промьшают.рассолом.высущивают ёезподным сульфатом магния и концентрируют в вакууме. Остаток кристаллизуют из этилацетата-скеллисольв-В-гек- санов, получая О,24Ог с т.ш1.144,5-147 С и 0,045 т. пл. 144,5-146, 5-хлор-2- 3-(хлорметил )-5-метил-4 Н-1,2,4-триазол-4-ил) -бензофенона. Аналитиче- ,JОекая проба имеет т. пл. 139-140 С. Вычислено, %: С 58,96; Н 3,78; i С1 20,48; 12,44. Найдено, %: С 59,22; Н 3, С1 20,66; N11,91. Пример 9. 5-хлор-2-ГЗ-(йодметил)-. 5-метил-4Н-1,2,4-тpиaзoл-4-илl-бeнзoфeнoн. 346 г (0,ОО1 моля) добавляют в размешиваемый раствор ЗОО Mj (0,002 моля) йодида натрия в ацетоне. Образовав- щуюся смесь ,6 час 54 мин размешивают при температуре окружающей среды, затем выливают в ледяную воду. Смесь экстрагируют. Остаток кристаллизуют из хлористого метилена-этилацетата, получая 0,227г, с т. пл. 185,5-192°С (с разложением) 5-хлор-2- 3- (йодметил )-5-метил-4Н-1,2, 4-триазол-4-ил}-бензофенона. Аналитическая проба имеет т. пл. 185-2ОО С (с разложением). Вычислено, %: С 46,65; Н 2,99,: С1 8,10; 29,00; N 9,60. : Найдено, %: С 46,78; Н 2,88; С1 8,59; 326,98; N9,23. Пример 10. 8-хлор-1-метил-6- -фенил-4Н- S -триазолЙг,,4)-бензодиа зепин.I Размешиваемую взвесь 391 мг (0,001 моля) 5-хлор-2 3-(бромметил)-5- -мети л-4 Н-1,2,4-триазол-4-и -бензофенона в 15 мл тетрагидрофуране охлаждают в ледяной бане и обрабатывают насыщенным раствором аммиака в метаноле 1(12,5 мл). Образовавшемуся раствору дают нагреться .що температуры окружающей среды и выдерживают 24 часа. Затем его концентрируют в вакууме. Остаток взвешивают в воде, обрабатывают небольшим количеством бикарбоната натрия и .экстрагируют хлористым метиленом. Экст.ракт промывают рассолом, высушивают
13 j безводным карбонатом натрия и концентркьруют. Остаток кристаллизуют из хлористого метилена-этилацетата, получая О ,22Ог сырого продукта с т.ш1.227-228,5°СЛере таллизацией этого вещества из этилацетата получают 0,142 г с т. пл. 228-229,5°С и 0,021 гот. пл, 228-229,5°С 8-хлор-1 -метил-6-фенил-4 Н- S -триазол (4,3-а) 1,4)-бензодиазепина. Реакция 5-хлор-2- -(хлорметил)-5- -метил- 4Н-1,2,4-триазоп-4-ил|-бензофенона с аммиаком в метаноле также дает 8 -хлор-1-метил-6-фенил-4Н- § -триазол (4,3-ау1,4 -бензодиазепин, но реакция про текает медленнее. Для ее окончания потребовалось более двух дней. Таким же образом 782 мг (0,ОО2 моля) 5-хлор-2- - (бромметил )-5-метил-4Н-1,2,4-триазол-4-и -бензофенона в хлористом метилене по охлаждении в бане из сухого льда и метанола дают ,с безводным аммиаком 515 г 8-хлор-1-метил-6-фенил-4Н- S -триазол,,4)-бензодиазепина с т. пл. 226-227°С. Пример 11. 6-хлЬр-4-(2,6-ди фторфенил)- 2-гидразинохннолин. . Аналсяично примеру 1 соединение 2,6-дихлор-4-(2,6-дифтсчзфенил)-хинолин подвергают реакции обмена с обратным холодильником с гищэазингидратом, получая 6-х.лар-4- (2,6-дифторфенил )-2-гищзaзинxинo лин. ... ,.f... Пример 12. 7-хлор-1-метил-5-(2,6-дифторфенил)- S -триазол(4,3-а)хинолин. Аналогично примеру 2 соединение 6- -хлор-4-(2,6-дифторфенил )-2-гидразинохинолин и триэтил-о-апетат кипятят при температуре кипения в ксилоле, получая 7-хлор-1-метил-5-(2,6-дифторфенил)- S -триазолЙ, 3-а|хинолин. 1 Пример 13. 5-хлор-2,6-дифтор-2-(З-метил-4 Н-1,2,4-триазол-4-ил )-бензофенон. Аналогично примеру 3 соединение 7-хлор-1-метил-5-(2,6-дифторфенил)- $ -триазо(Й,3-шхинолин окисляют при низкой темг1ературе перйодатом натрия и двуокисью рутения, получая 5-хлср-2,6-дифтор-2-(З-метил-4 Н-1,2,4-триазол-4-и л )бензофенон. Пример 14. 5-хлор-2,6-дифтор-2-|Ь-(оксиметил)-5-метил-4Н-1,2,4-триазол-4-ил1-бензофен(ж. Аналогично примеру 6 соединение 6,514, -.хл(Ч) -дифтор-2-(3-меГИЛ-4Н-1,2,4тpиaзcмI-4-ил)-бензофенон разогревают с парафс мальдегидом при , получая ,5-хлор-2,6-дифтор-2 -(оксиметил)-5 зМетип.-4Н-1,2,4-триазол-4-ип1-бензофенон. Пример 15. 5-хлор-г,6-дифтор-2-fe-(бромметил )-5-метил-4 Н-1,2,4-триаз ол-4-ил -бензофенон. Аналогично примеру 7 соединение 7,5-хпар-2, 6 -дифтор-2- 3- (оксиметил) -5-метил-4Н-1,2,4-триазол-4-ил1-бензофенон обрабатывают трибромистым фосфором, получая 5-хлор-2 6-дифтор-2- -Хбромметил)-5-метил-4Н-1,2,4-триазол-4-ил|- i -бензофенон. Пример 16. 8-хлор-1-метил-6-(2.6-дифторфенил)-4И- S -триазол(4,3|1, 4 -бензодиазепин. Аналогично примеру 10 соединение 5-хлор-2,6-дифтор-2-{3-(бромметил)-5-метил-4Н-1,2,4-триазол-4-ил1-бензофенон подвергают реакции обмена с насыщенным раствором аммиака в метаноле, получая 8-хлор-1-метил-6- (2,6-дифторфенил)-4Н- S -триазол|4,,4}-бензо- диазепин. LПример 17. 6-хлор-4-((-хлор-) , фенил)-2-гифазинохинрлин. Аналогично примеру 1 соединение 2,6,-дихлор-4- (о-хлорфенил-хинолин) разогре-. вают с обратным холодильником с гищ)а- зингидратом, получая 6-хлор)-4-(о-хлорфенил )-2-ги/фазинхинолин. Пример 18. 7-хлор-1-метил-5-(о-хлорфеннл)- S -триазол 4,3 -хинолин. Аналогично примеру 2 соединение 6-хлср-4-(о-хлорфенил )-2-ги/фазинхинолин и триэтил-о-ацетат разогревают при температуре кипения в ксилоле, получая 7- -хлор-1-метил-(о-хлорфенил)- § -триазол J4.3хинолин. Пример 19. (2;5-дихлор-2-(3-метил-4 Н-1,2,3-триаз ол-4-и л)-бензофенон. Аналогично примеру 3 соединение 7-хлор-1-метил-5-(о-хлорфенил- S -три- зо;,3-а)хинолин. сжисляют при низкой температуре перйодатсял натрия и двуокисью рутения, получая 2,5-дихлор-2-(3-метил 4Н-1,2,4-триазол-4-ил )-бензофенон. Пример 20. 2 -дихлор-2-р-(оксиметил )-5-метил-4 Н-1,2,4-триазол-4-илТ -бензофенон. I Аналогично примеру 6 соединение 2J5-I |-дихлор-2-(3-метил 4Н-, 1,2,4-триазол-4-ил)-бензофенон разогревают с параформальдегидом при 125 С, получая 2,5 -дихлор-2- 3- (оксиметил )-5-метил-4 Н-1, 2,4-триазол-4-ил -бензофенон. Приме р-21. 2,5-дихлор-2-(бррм метил)-5-метия-4Н-1,2,4-триазол-4-и; -бензофенон. Аналогично примеру 7 соединение 2,5 -дихлор-2- -( оксиметил )-5-метил-4Н-1,2,4-триазол-4-ил|-бензофенон обрабатывают трибромистым фосфором, получая 2,5-дихлор-2- 3-{бромметил)-5-метил-4Н-1,2,4-триазол-4-ил}-бензофенон. : Пример 22. 8-хлор-1-метил-6-(-хлорфенил)-4Н- $ -триазол(4,3-(1,4J бензодиазепин. Аналогично примеру 2 соединение 5-нитро-6-пропил-4-(м-трифторметил-4Н-1,2,4-триазол-4-ил -бензофенон подвергают реакции обмена с насыщенным jiacT- вором аммиака в метаноле, получая 8-хлор-1-метил-6-(о-хлорфенил)-4Н- S -триазолйг, 3-a(l ,4у-бензодиазепин. Пример 23. 5-нитро-6-пропил-4 - (м-трифторметилфенил)-2-гидразинохиноАналогично примеру 10 соединение 2 -дихлор-2-|3-(бромметил)-5-фторметилфенил)-хинолин разогревают с обратным холодильником с гидразингидратом, получая 5-нитро-6-пропил-4-(м-тpифтopмeтилфeни -2-гидpaзинoxинoлин. Пример 24. 6-нитро-7-пропил-1-этил-5-(м-трифторметилфенил)- S -триазол(4, зХ-хинолин. О Аналогично примеру 1 соединение 2- -хлор-5-нитро-6-пропил-4-(м трифенил)-2-гидразинохинолин и триэтил-о-пропион I разогревают до температуры кипения в ксилоле, получая 6-нитро-7-пропил-1-эти 5-(м-трифторметилфенил)- S -триазол (4,3-а хинолин. Пример 25. 6-нитро-5-пропил-2-(3-этил-4Н-1,2,4-триазол-4-ил)3(трифторметил)-бензофенон. Аналогично примеру 3 соединение 6- -нитро-7-пропил-1-этил-5-(м-трифторметилфенил)- S -триазол,3-а)х:инолин окис ляют при низкой температуре перйодатом натрия и двуокисью рутения, получая 6-нитро-5-пропил-2-( 3-ЭТИЛ-4Н-1,2,4-триазол-4-ил)-3-(трифторметил )-бенз о- I фенон. 71 i Пример 26, 6-нитро-5-пропил- I (оксиметил )-5-этил-4 Н-1,2,4-триаз ол-4-ил -3-(трифторметил-)-бенз офен он. Аналогично примеру 6 соединение 6-нитро-5-пропил-2-(3-этил-4Н-1,2,4- -триазол-4-ил)-3-(трифторметил)-бензофенон разогревают с параформальдегидом при 125 С, получая 6-нитро-5-пропил-2-1 -( оксиметил )-5-этил-4 Н-1,2,4-триазол-4-ил}-3-(трифторметил)-бензофенон. Пример 27. 6-нитро-5-пропил-2-|3-(бромметил)-5-этил-4Н-1,2,4-триаз ол-4-и З- (трифторметил-)-бенз офен он: II 1 Аналогично примеру 7 соединение 6-нитро-5-пропил-2-|3-(оксиметил4-5-этил-4 Н-1,2,4-триазол-4-и З-(трифторметил )-бензофенон обрабатывают трибромистым фосфором, получая 6-нитро-5-пропил-2- 3-(бромметил)-5-этил-4Н-1,2,4-триазол-4-ип1-3-(трифторметил)-бензофенон. Пример 28. 7-нитро-8-пропил-1-этил-6-(м-трифторметилфенил)-4Н-S -триазол,3-(1,4У-бензодиазепин. Аналогично примеру 10 соединение 6-нитро-5-пропил-2- 3- (бромметил) -5-этил- -ЛН-1,2,4-триазол-4-ил|-3-(трифторметил) -бензофенон подвергают реакции обмена с насыщенным раствором аммиака в метаноле, получая 7-нитро-8-пропил-1-этил-6-(м-тпифхорметилфенил)-4Н- S -триазол ,,4)-бензодиазепин. Аналогично способам, приведенным в описанных примерах, можно получить еле- дующие соединения: 8т хлор-1-этил-6-фенил-4Н- S -триазол-(l, 3-a)(l, 4)-бенз одиазепин ; 8-хлор-6-фенил- 4Н- S -триазол,3р. ,4)-бензодиазепин; 8-трифторметил-1-метил-6-фенил-4Н- -триазол,3-а)р,4 бензодиазепин; 8-хлор-1-метил-6-(о-фторфенил)-4Н- , -S -триазол,3-а)(1,4)-бензодиазепин; 7-(этилтио)-1-пропил-6-(о-бромфенил)-4Н- S -триазол(4,3-аУ1,4)-бензодиазепин-, 10-(тоифторметил )-6-lrt-(пропионилами- но)-фенилр-4Н- S -триазол,3-1(1,4 -бензодиазепин; 9-пропокси-8-бром-1-этил-6- м-(этилсу льфинил)-фенил)-4Н- S -триазол(4,3-3) l ,4)-бензодиазепин; 9-нитро-8-этил-1-пропил-6- с -(этилсульфинил)-фени;3-4Н- § -триазол,3-а) (1,4)-бензодиазепин:, j 1-.метил-7-фтор-6-(о-фтсффенил)-4Н- S -триазол(4,3-)(1,4)-бензодиазепин; 1-изопропил-.6-( Л -толил)-4Н- S -триазол (4,3-а)(1 .- бензодназепин; 1-пропил-7,10-дибром-6-( fi -хлорфенил) -4Н- S -триазол,.,4 -бензодиазепин:, 1-этил-8-амино-6-( tl -нитрофенил)-4Н-S -триазал,3-а)(1,4)-бензодиазепин; , 1-изопропил-8-фтор-6-(о-цианофенил)-4Н- S -триазол,3-а)(1,4)-бензодиазепнн; 1-изопропил-9-ацетамидо-7-хлор-6-(м-аминофенил)-4Н- S -триазол (4,3-а) ,4}-бензодиазепин; 7-днметиламино-6- (метилсульфипил)-, -фенип|14Н- S -триазол (4,3-(1,4)-бензодиазепин;8-(пропилтио)-1-пропил-6-( ц -этоксифенил)-4Н- S -триазол(4,3-(1,4)-бензодиазепин;9-метил-6-(о-аминофенил)-4Н- S -тригазол(4, 3-а)(1,4)-бензодиазепин. Предмет изобретения Способ получения производных триазолбензрдиазепинов формулы где R - атом водорода или алкил с 1-3 атомами углерода; F -R - атом водорода, апкил с 1-3 2 о атомами углерода.фтор, хлс, бром, нитроили цианогруппа, трифторметил, алкокси- группа с 1-3 атомами углерода, аминоили алканоиламиногруппа, где алканоильная группа содержит 1-3 атома углерода, алд. КИЛТИО-, алкилрульфинил или диалкиламиногруппа, в которых алкильная группа содержит 1-3 атома углерода, отличающийся тем, что 2--хлсу-4-фенилхинолин формулы N. - Ci где R -Нд имеют указанные значения, 2 . 5 I нагревают с ги;чразингидратом до Щ перйтуры кипения, образующееся производное 2--гифазино-4-фенилхинолина формулыNH-NH . где R -R имеют указанные значения, о нагревают до температуры кипения с риалкил-о-ацилатом (Ro) C-R, гдеR лкил с 1-3 атомами углерода и R имеет казанные значения, образующееся производное триазолхиноина формулы где R-Rp имеют указанные значения, обрабатывают окислителем, например перйодатом натрия и двуокисью рутения, в инертнслл растворителе, например в водном ацетоне, образующееся производное (4Н-1,2,4|-триазолил-4)бензофенона формулы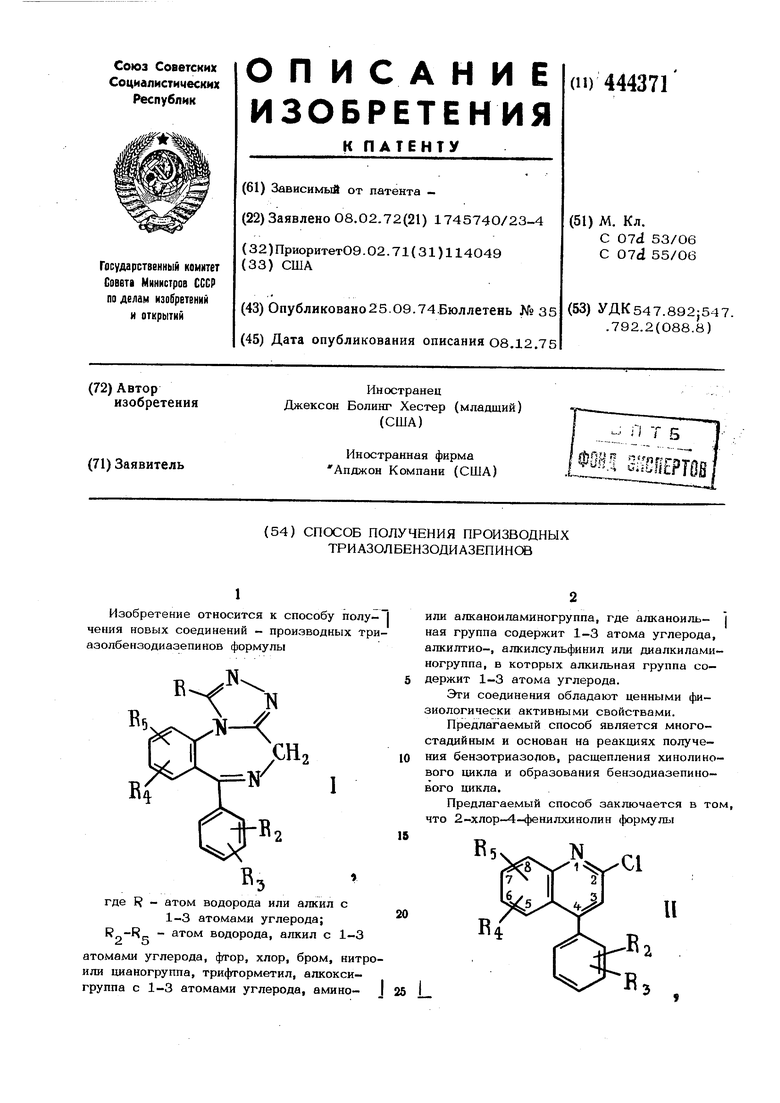








Авторы
Даты
1974-09-25—Публикация
1972-02-08—Подача