1
i Изобретение относится к способу получения производных 5-иминометил-2-нитроимидазола, обладающих биологической активностью.
Основанный на известной реакции конденсации альдегидов с азотсодержащими соединениями, предлагаемый способ получения производных 5-иминометил-2-нитро- имидазола общей формулы
Г
И
г
m
Т1
где f - низщий алкип; у -замещенный
иминометил, 2-бензимидазолил или 5-амино-1,3,4-тиадизол-2-ил, заключается в том, что альдегид общей формулы. J
к
II
онс
R
где f - как указано выше,
обрабатывают аминами, гидразинами, тиосе, микарбазидами, гидроксиламинами или их солями в присутствии акцептора кислоты и, когда У - 2-бензимидазолил или 5-ам1И1о-1,3,4-тиадиазол-2-ил, соответствующие основания Шлффа или тиосемикарбааоны окисляют слабыми окисга1телями и ьыделн- ют целевой 1фодукт обычными приемами. Для окисления можно исполь::ювать теграацетат свинца, атмосферный кислород, окись ртути, двуокись марганца, соли дну-валентной меди и соли трехвалентного /к леза.
I В получаемых соединениях алкил содс-р1жит 1-4 атома углерода, а замеиюниый
1иминометил может представлять собой производнь1е 1-алкил-2-ниТро-5-имидазолальдегида, такие, как незамещенные гидразоны, MOiio- и диалкил-, аралкил-, циклоал- кил-, моко- и диарил-, оксиалкил-, ацил- замещенные гидразоньг,, семикарбазоны,
тиосемикарбазоны, гуанилгидразоны, окси- мы, замещенные оксимы, нитроны, алдазины, основания Щиффа и з(мещэнные гидразоны, у которых второй атом азота входит в состав 5-7-членного гетероцикла, который может содержать и другие гетероатомы, например азот, кислород или серу. Реакцию обычно проводят в интервале
температур от комнатной до температуры кипения растворителя, в качестве которого используют низший алкай, воду или их О
перечисленные в табл. 1. При использовании солей гидроксиламина к реакционной
си, предпочтительно при эквимолярном соотношении между компонентами.
Пример 1. -{1-Метил-2-нитроимидазол-5-ил)- (У -метилнитрон.
Смесь 0,25 г 1-метил-2-.нитро-5-имидазолальдегида, 0,150 г гидрохлорида , метилгидроксиламина и 0,15О г бикарбоната натрия в 80 мл безводного этанола киптят 2 час с обратным холодильником, фильтруют, упаривают до небольшого объема и охлаждают. Выход 0,24 г, т. тек. 208-2О9°С.
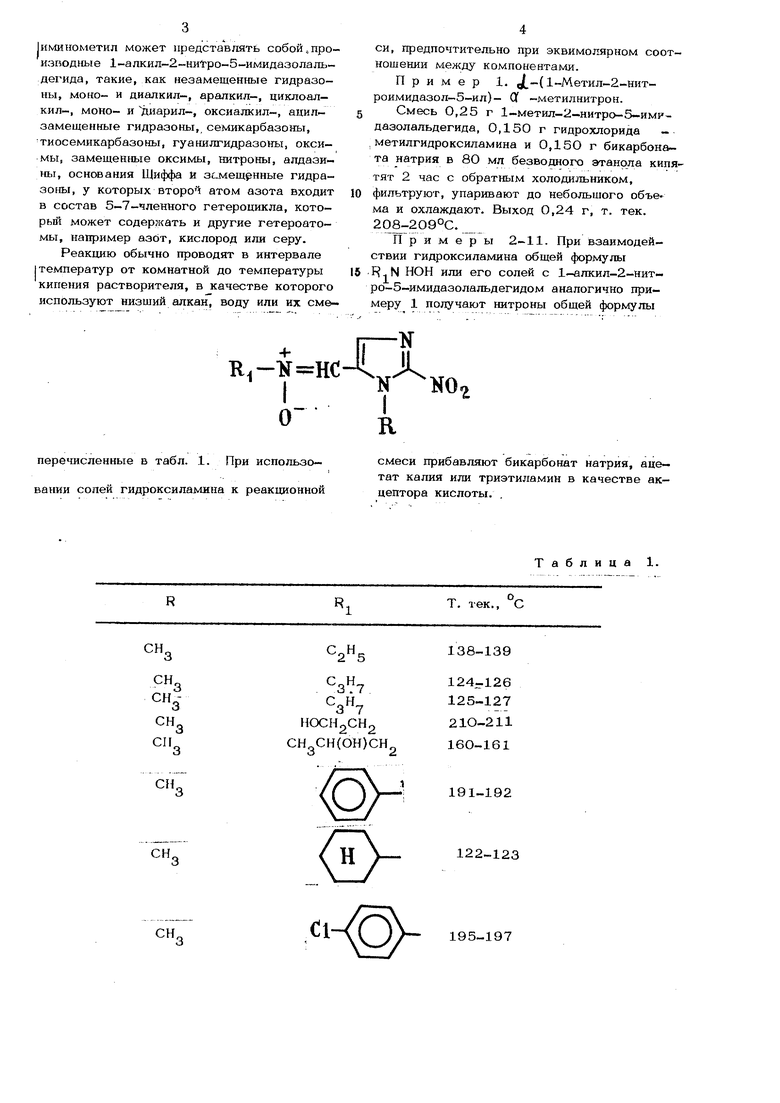
Примеры 2-11. При взаимодействии гидроксиламина общей формулы R N НОН или его солей с 1-алкил-2-нит-. ро-5-имидазолальдегидом аналогично примеру 1 получают нитроны общей формулы
1 II
|
N I R
N0.
смеси прибавляют бикарбонат натрия, ацетат калия или триэтиламин в качестве акцептора кислоты.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 2-нитроимидазола | 1972 |
|
SU466684A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ИМИДАЗОЛА | 1973 |
|
SU385445A1 |
| ЗАМЕЩЕННЫЕ АРИЛАЛКИЛТИОАЛКИЛТИОПИРИДИНЫ ДЛЯ БОРЬБЫ С БАКТЕРИЯМИ HELICOBACTER | 1995 |
|
RU2139286C1 |
| Способ получения производных пиразола | 1975 |
|
SU582758A3 |
| Способ получения производных акриловой кислоты | 1985 |
|
SU1395139A3 |
| Способ получения N-/бициклических гетероцикло)-4-пиперидинаминов, фармацевтически приемлемой соли присоединения кислоты или стереохимически возможной изомерной ее формы | 1987 |
|
SU1694064A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЬЗАМЕЩЕННОГО 5-НИТРО-2-ИМИДАЗОЛА | 1973 |
|
SU385446A1 |
| ТИОПИРИДИНЫ ДЛЯ БОРЬБЫ С БАКТЕРИЯМИ HELICOBAKTER | 1995 |
|
RU2142459C1 |
| Способ получения имидазолов, их солей или -окисей | 1974 |
|
SU542473A3 |
| Способ получения 1,2-гидроксиламинооксимов | 1981 |
|
SU977453A1 |

СИ,
СИ,
С1
СН,
Таблица 1.
191-192
122-123
195-197
Продолжение табл.1
Пример 12i 1-Метй№-2-ннтро- -5-имидазолальдегидоксим
К раствору 0,4 г гидрохлорида гидроксиламина в 15 мл метанола при комнат- I ной температуре прибавляют 0,4 г 1-ме- тил 2-нитро-5-имидазолальдегида в 2Омл этанола и 0,810 мл триэтиламина, остав-, ляют на ночь, упаривают до небольшого объема, фильтруют, кристаллизуют осадок из воды и получают 0,10 г целевого соединения, т. пл. 2ОЗ-205°С.
Пример 13. 1-Метил-2-нитро-5-имидазолальдегид-О- дешшоксим.
К раствору 0,3 г 1-метил-2-нитро-5-имидазолальдегида в 74 мл метанола прибавляют 0,335 г О-децилгидроксиламина, выдерживают в течение ночи, фильтруют и получают 0,228 г продукта, т. тек. i70°C.
этил)-2-амино-5-этиламидазола и О, J 75мг этилата натрия в 2,89 мл этанола, выдерживают в течение ночи, отделяют тверд).1Й осадок и промывают его водоГк Выход
I О,269 г, т. тек. 18S-1874:.
I i
Пример 17. 1-Метил-2-11И1ро-Г - -имидазо7Юльдегид-2-оксиэтилгидразон.
Раствор 0,3 г 2-оксиэтилгидрази11а и 0,4 г 1-метил-2-нитро-5-имидазолальде гида в 20 мл метанола выдерживают дьа дня, фильтруют, промывают осадок и получают 0,245 i целевохо продукта, т. rcii l38-14O°C.
Пример ы 18-48. При взаимо/ц-й-ствии альде1ида обшей форму.чы
N1
30
П р и м в р 14. 1-Метил-2-нитро-5-имидазолальдегидтиосемика эбазон.
Водный раствор 1,42 г тиосемикарбазида прибавляют к раствору 1,8 г 1-ме- тил-2-нитро-5-имидазолальдегида в метанле и получают 2,2 г продукта, т. тек. 282-287°С.
П р и м е р 15. 1-Этил-2-нитро-г5имидазолальдегидтиосемикарбазон.
При взаимодействии 1-этил-2-нитро-5-и ми дазо ла льде гида с тиосемйкЪрбазпдом, проводимом аналогично примеру 14, полу4ajQT целевое соединение, т. тек. 220222 0..
Пример 16. 1-Метил-5-|1-(2-оксиэтил)-5-этил-2-имидазо7ш;3-иминометил-2-нитроимидазол. .
I К раствору 0,4 г 1-метил-2-нитро-5-имидазолальдегида в 25 мл этанола прибавляют 0,494 г гидрохлорида 1-(2-окриОНС N NOn I
R
с амином общей формулы П N Ч
njni t.l I
солью в ирисутсгвии акцептора кисло ы, например ацетата, бикарбоната, карбона Ia гидроокиси ИШ1 алкоголята щелочно1о ьи;Талла, триэтиламина, пиридина, iiojfjUJiKnсоединения обшей формулы
-N
11
.
К
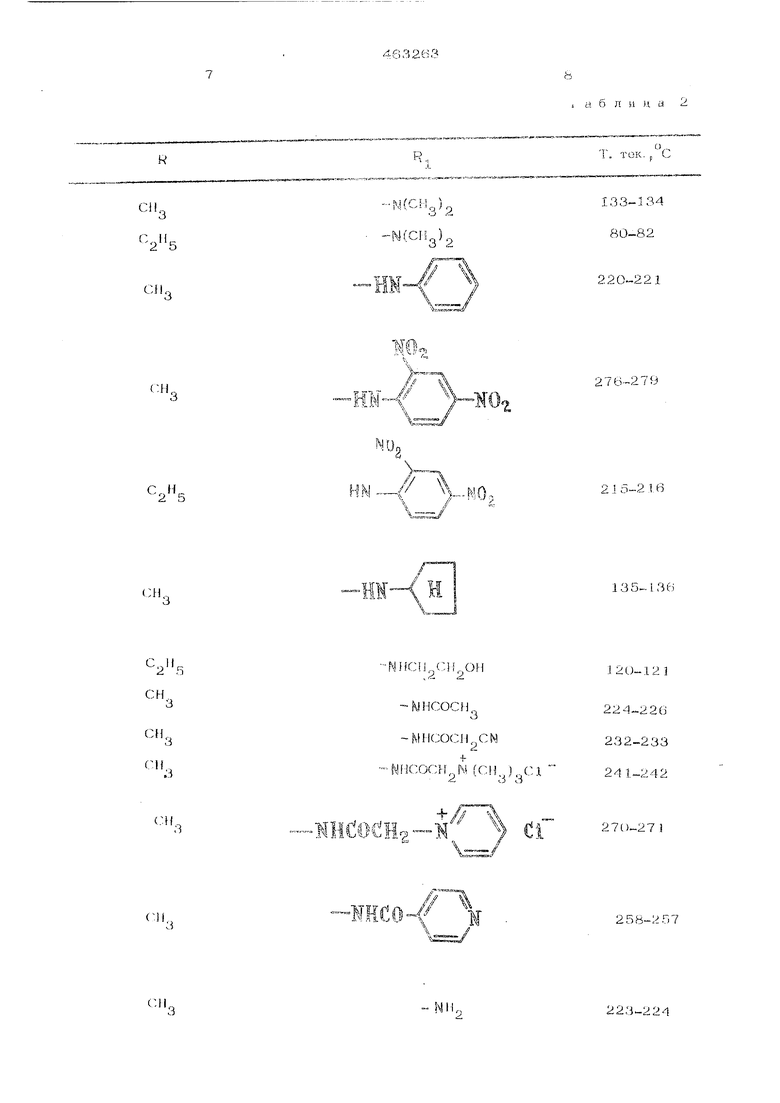
свойства которых приведены в табл. 2.
R
а б л И ц а 2
Т. тек.р С
220-221
СИ,,
т-€
21 5-21В
СН,
3
з
СИ .
(:н
NHcn,
-МНСОСН,
224-226
-WHCOCH CN 232-233 NHCOCH N (Cli, ),. СЛ 241-242
/rit5 о
27()-27 I
258-257
Nii.,
223-224
9
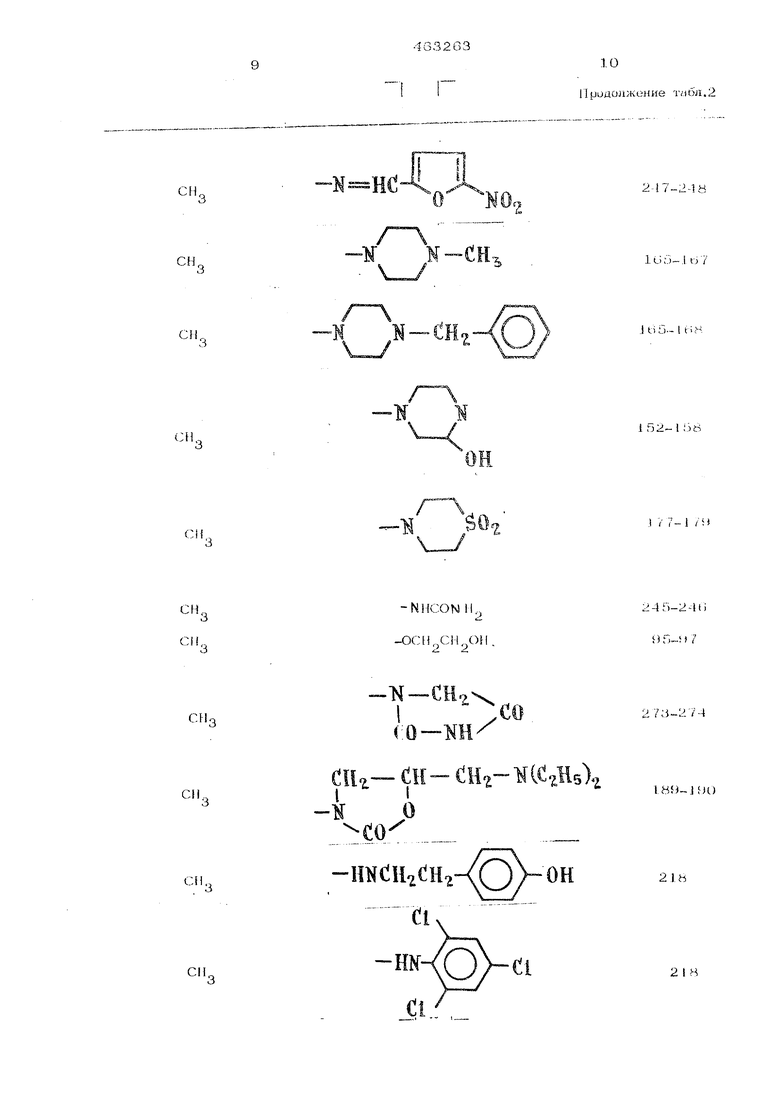
Придолжелие Г1лбп.2
СИ,
217-2-18
:н.
си
3
CH,
3
Clb
СПгi j
СП.
X-riA/
Cii.,
СИ
3
М-СН
1и5-.1 Ь7
ь
н
I tiO- 1 tiH
1 52-i i.iS
77-1 /i
2
-NKCON II,,
245-2-Ui НГ.Я 7
-ОСИ,.,СН,ОИ
К
273-2/4
2
tU)
HK(ll2(Hr
OH
11
СИ,
3
- NHCS N
СИ,
12
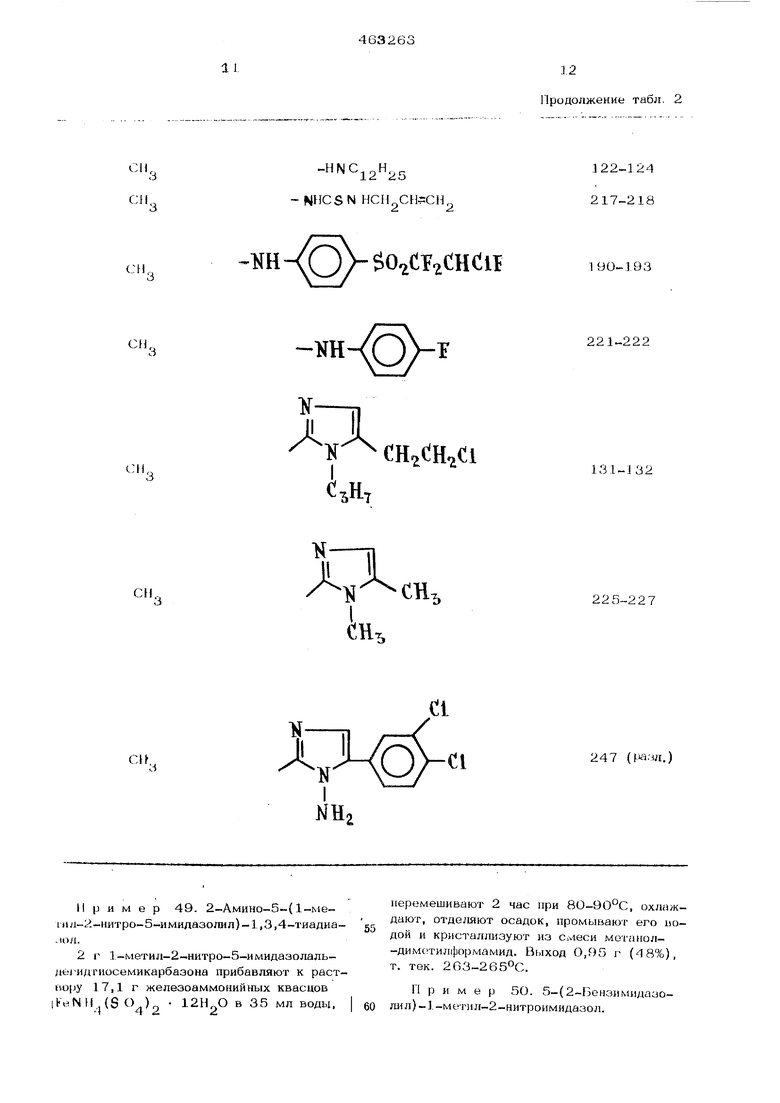
Продолжение табл. 2
122-124 217-218
си.
SO Cr CHClI
1УО-103 -NH СА
1
,,
Пример 49. 2-Амино-5-(1-меп1л-2-нитро-5-имидазолил) -l,3,4-тиaдиa.oл.
2 г 1-метил-2-нитро-5-имидазолальде1-идг11осемикарбазона прибавляют к раст1Юру 17,1 г железоаммонийных квасцов
lKeNH,j(SO)2
12Н О в 35 мл воды, CH« CHoCl
225-227
перемешивают 2 час при 80-9О°С, охлаждают, осадок, промывают его водой и кристаллизуют из смеси мета но л-димотилформамид. Выход 0,95 г (48%), т. тек. 203-2650С.
Пример 5О. 5-(2-Бензимидазолил)-1-метил-2-нитроимидазол. 221-222 131-J32 Раствор 0,5 г 1-метип-2-нитро-5-имидазолапьдегида и 0,348 г о-фенипенпиамнна в 10 мл этанола кипятят 2 час с обратным хрдодильником, фргльтруют, промывают осадок этанолом, растворяют его в 10 мл уксусной кислоты, добавляют 0,75Ог тетраацетата свинца РЬ (СН„СОО) , нагревают 2О мин до 50 С, охлаждают, разбавляют 5О мл воды, отделяют осадок, пере кристалгшзовывают его из ацетона и полу- I. I чают 0,15 г целевого соединения, т. тек. 268-27О°С.
сн осн сн„оN сно
сн Генном -н
с Н оси сн ON-sCHт: у.,
,OCH2CH20KJ CHТаблица 3
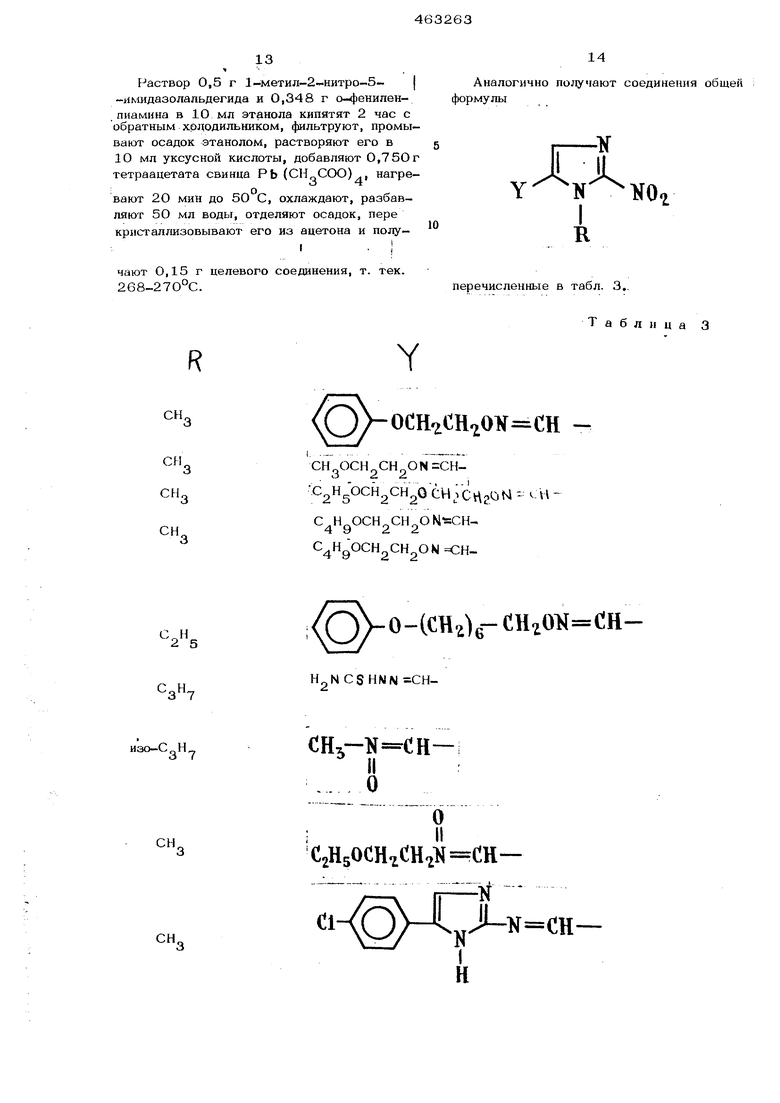
Аналогично получают соединения общей ормулы еречисленные в табл. 3,.
0-(СИг)б- гОК с:НH NCSHNN CHСз 7
СНл-К -С FiО
iИ
СгНзОСН СН Ш- ll
О
-
15
16
СИ,,
(Н500ССНгШ К(Н-
(Нь(ООС2Н 1 СНСН - {-N CHНК
си,.
0. О
/-
СИ
3
(o)
2 о
(Ul--СИ
3
сн.о
СИз
11
о
17
18
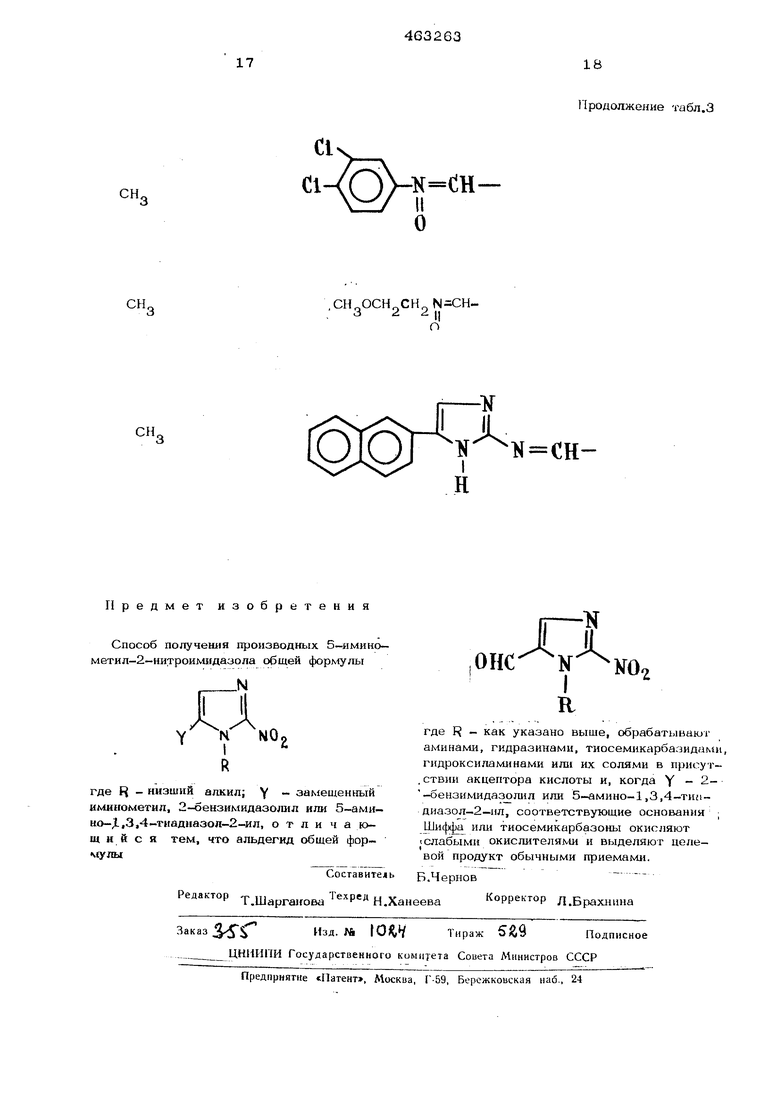
Продолжение табл.З
СН,
., J II
О
СН,
Авторы
Даты
1975-03-05—Публикация
1972-07-25—Подача