Изобретение относится к способу получения новых, обладающих биологической активностью проиэьЪцных флуоренона, которы могут применяться в фармацевтйчёской промышленности и медицине. Известен способ получения производных флуоренона общей формулы R-dH-CHg-A Гриньяра Hal-Mj-CH2-CH(R)-CH2-A, где Hal - атом галогена, А и Ц имеют указанное уже значение. Для го лучения иовьсх фоизвсцных флуоренона известной общей формулы . OCORg O-CHg-CH-CJHg-lfHRi I - алкил, который мс(жет быть заме ОДНИМ или несколькими атомами галогена циклоалкил, который может быть замещен одним или несколькими алкилами, фенил, замещенный в соответствующем случае галогеном, метилом или метоксигруппой, 5или 6-членный гетероциклический остаток содержащий гетероатом кислород или азот фенилалкил или карбалкоксиалкил, или ах содей, дебензилируют известным способом например, каталитическим гидрированием, соединения общей формулы ОСОЕп СН II O-dHg- H- Hg- -Ei где { и { имеют гзначения, указанные для ошцей фрмупы 1, с последующим выделением известным способом целевого пр аукта в виде основания или соли. Процесс ведут вприсутствии катализарю ра, предпочтительно палладиевого катализа тора, в инертном, в реакционных услови ях , органическом растворителе, например в сложном уксус-ном эфире, ледшюй уксусной кислоте, циклическом простом эфире или гростом эфире с открытой цепью, как в простом диэтиловом эфире, п редпочтительно при комнатной температуре и нормально давлении. После окончания гидрирования отфильтровывают катализатор и упаривают фильтрат досуха. Пример 1. Получение 4-(3-трет. бутила ино-2-пивалоилоксипропокси) -9-флуоренона. 5 г 4-(2,3-эпоксипропокси)-9-флуоренона и 16,15 г N-бензил-трет. бутиламина в 25 мл диоксана нагревают 16 час в автоклаве до 180 С. Упаривают при пониженном давлении досуха, причем одновреме но отгоняется избыточный N -бензил-трет. бутиламин. Извлекают остаток обработкой простым эфиром и 1 н. раствором винной кислоты, при о.хлаждении доводят затем виннокислые фазы 5 н. раствор.ом едкого натра до щелочной реакции и экстрагиру- ют метиленхлоридом. После упаривания метилеихлорица получают маслянистый -бензил, трет. бутиламино)-2-оксипропокси -9-флуоренон. Гидромалеат этого соединения выкристаллизовывается из этанола/сложного уксусного эфира: т. пл. 167-168°6. О 4,37 г полученного основания в 16 г триметилуксусной кислоты перемешивают с 1J72 г ангидрида триметилуксусной кислоты в течение 16 час при комнатной температуре. Выливают смесь на лед и прибавляя 10%-нВ1й аммиачный раствор доводят ее до щелочной реакции, экстрагируют метилентслоридом и упаривают растворитель при пониженном давлении. Получают масляпгистый N -бензил.трет.бутил- амино)-2-пивал{ илоксипропокси}-9Ц луоренон, его гидромалеат кристаллизуется из этанола/сложного уксусного эфира, который затем подвергают дебензилированию, т. пл. 180-182 С. 2,15 г полученного соединения растворяют в 50 мл тетрагидрофурана, и в присутствии О,5 г палладиевого катализатора (10% угле) дебензилируют полученный раствор с помощью 1 моля водорода. Это соединение чистят хроматогра- фией на силикаг.еле метилекхлоридо я и кристаллизацией из бензола/бензина; т. пл. 82-85с. Пример 2. Получение 4-(2-ацетокси-3-трет.бутиламинопропокси)-9-флуоренона. Дебензилируют 4- 2-ацетокси-3-( N -бензил-трет-бутиламино)-пропокси}-9-флуоренон по примеру 1. Гидромалеат, полученного соединения, имеет т. пл. 167169°С. Пример 3. Получение 4-(3-трет.-бутиламино-2-гептаноилоксипропокси)-9-флуоренона. Дебензилируют ( |у -бензил-трет. бутиламино)-2-гептаноилоксипропокси -9-флуоренон по примеру 1. В результате получают соединение. Гидрохлорид имеет т. пл. 169-171°С. Пример 4. 1 Получение 4- з-трет.бутиламино-2-(4-хлорбутирилокси)-пропокси -9-флуоренона. Проступают так, как было описано в примере 1, и дебензилируют 4-СЗ-( N гбензил.рет.-бутиламино) -2-( 4-хлорбу тирнлокси) ропокси -9-флуоренон. В результате полуают соединение. Гидрооксалят имеет т пл 193-195 с. Пример б/Получение 4-(2- eri3oилокси-3-.трет.бутиламвнопропокси)-9-флуоренона. Поступают так. как было описано в примере 1, и дебенаилируют 4-С2-бенаоилокси- 5 3-( -бена1л-трет:бутиламино)пропокси|-9-флуоренона. В реаупьтате получают. соединение. Гидромалеат имеет т. пл. 212-214 С. Пример 6. Получение 4-(3-трет. бутиламино-2-циклогексилкарбонилоксипропокси)-9-флуоренона. Поступают так, как было описано в примере 1, и дебенаилируют 4-(3-( N -бенаил-15 -трет. бутиламино)-2-циклогексилкарбонилоксипропокси -9-флуоренон. В реаультате получают соединение. Гидромалеат имеет т.
пл. 206-208 С. Пример 7. Получение 4-(-трет. бутиламино-2-пивалоилоксипропокси)-9-флу ренона. Поступают так, как было описано в при ре 1, и дебенаилируют ( N-бенаил-т бутиламино)-2-пивалоилоксипропокси -9.-флуоренон. В реаультате получают соедин ние. Гидро.хлорид имеет т. пл. 228-231 0 Пример 8. Получшие 4-(3-трет. бутиламино-2-(2,2-диметилбутирилокси)-пропокстЛ -9-флуоренона. Поступают так, как было описано в при мере 1, и дебенаилируют N -бенаил-трет. бу ти ламино) -2-{ 2,2-диметилбутирилокси)-.пропоксиЗ-9-флуоренон. В реаультате получают соединение. ГидрооксаI лат имеет т. пл. 159-162°С, Пример 9. Получение 4-(3-трет. бутиламино-2-,хлорацетоксипропокси)-9-флуоренона. Поступают так, как было описано в при мере 1, rf дебенаилируют 4-(3-( N -бенаил-трет. бутиламино)-2-хлорацетоксипророкси -9-флуоренон. В реаулвтате получают соединение. Гидро.хлорид имеет т. пл. 204-207°С. Пример Ю. Получение 4-(3-трет бутиламино-2-ди.хл орадетоксипропоксв) -9-флуоренона. Поступают так, как было описано в примере 1, и дебензилируют -бенаил-трет. бутйламино} -2-дихло рацетоксипропоксиЗ-9.-флуоренан. В результате получают соединение. Гидро,хлориц имеет т. пл. 218-220 С.
127-129 С. Пример 11. Получение 4-(3-трет. бутиламино-2-каприноилоксипропокси)-9-флуоренона. Поступают так, как было описано в примере 1, и дебенаилируют 4-(j3-( N енаил-трет. бутиламино)-2-каприноилоксипропокси}-9-флуоренон. В реаультате получают соединение. Гидрохлорид имеет т. пл. 115-118 С П р и м е р 12. Получение 4-(3-трет. бутиламино-2-стеароилоксипропокси)-9-флуоренона. . Поступают так, как было описано в примере 1, и дебенаилируют ( N -бенаил-трет. бутиламино)-2-стеароилоксипропокси -9-флуоренон. В реаультате получают соединение. Гидрооксалат имеет т. пл. 13. 4-(2- хлорПримердетокси-3-иаопропиламинопропокси)-9флуоренона. Поступают так, как было описано в приере 1, и дебенаилируют 4-{3-( N -бенаил-иаопропиламино)-2-хлорацетоксипр оокси -9-флуоренон. В реаультате получат соединение. Гидро.хлорид имеет т. пл. 210-214°С. Пример 14. Получение (3пентиламино)-2-пивалоилоксипропокси -9н|шуоренона. Поступают так, было описано в при.Г мере 1, и цебенаилируют. 4-.Q3-( N -бенаил...3-пенталамино)-2-пивалоилоксипропокси -9- ф1уоренон. В результате получают : соединение. Лдррмалеат имеет т. пл. 155-157. Пример 15. Получение 4-{р-трет. бутиламино-2- (2-бром-2-метилпропионилокси)-пропокси}-9-флуоренона. Поступают так, как было описано в примере 1, и дебенаилируют ( N -бенаил-трет.бутиламино) -2-{ 2-бром-2-метилпропионилокси)-пропоксиЗ-9-флуоренон., В результате получают соецинение.Оксалат имеет т. пл. 193-196°С. Пример 16. Получение 4-{3-трет. хлорибензоилокси)-фопо1 см (ёутиламино-.2-( 2-9-ч})луоренона. Поступают так, как было описано в примере 1, и дебензилируют ( N -трет, бутиламино)-2-(2-.хлорбензоилокси)-пропокси -9-4луоренон., В результате получают соединение. Гидро.хлорид имеет т. пл. 209211°С.
: Пример 17 Лолученйё 4- з-трет. . бутиламино 2- (4-толуоилокси) -пропокси -Э-флуоренона.
Поступают так, как было описано в примере 1, и дебензнлирую ( N -бенанл-трет. бутиламино)-2-(4-толуоилокси) пропокси -9-(}и оренон. В результате получают соединение. Гидрохлорид имеет т. пл. 225228°С.
1Пример 18. ,|1олучение 4-(3-трет.
бутиламино-2- (Зг-метоксибензоилокси):-пропокс1 9-флуоренона., Поступают так, как было описано в примере 1, и дебензилируют ( { -бензил-трет. бутиламино)-2-(3-метрксибензоилокси)-пр опоке (,,флуорёнрр. В результате получают соединение. Гидрохлорид имеет т. пл. 203-206°С.Пример 19. Получение 4-(3-циклогекс иламино-2-пива лоилоксипропоксн) -9-флуоренона.
Поступают так, как было описано в примере 1, и дибензилнруют ( N -бензил -циклогексилактно) -2-пивалоилоксипропокси-9-флуоренон. В результате получают соединение; т. пл. 97-98°С.
Пример 20. Получение 4-(3-трет бутиламинот2-фенилацетоксТ1пропокси)-9 -флуоренона.
Поступают так, как было описано р примере 1, и дебензилируют 4-{.3-( -бензил-трет. бутиламин0)-2-фенил -ацеток снпропокси7-9-фпуренон. В результате полчают соединение. Гидрохлорид имеет т.пл. 191-193°С.
Пример 21. Получение 4- 3-трет буткламино-2-(4-тетрагидропиранилкарбо- йи локси)-л ропокси -9-флу оренона.
Поступают так, как было описано в примере 1, дебензилируют ( N -бензил-трет. бутиламино)-2-(4-тетрагидропиранилкарбонилоксиТ-пропокси}-9-флуоренон. Ё результате получают сое некие. Гидро
оксалат имеет т. пл, 214-216 С.
Пример 22. Получение зложного этил- 3-трет. бутиламинс -1-(9-оксо-4-флуоренилокси)-пропил -эфира малоновой кислоты.
Поступают так, как было описано в
примере 1, дебензилируют сложный эгйл{3-( N -Jбeнзил-тpeт,бyтилaминo)-l-(9-оксо-4-флуоренилоксв)-пропил эфир малоновой кислоть. В результате получают соединение. Точка плавления гидрохлорида имеет т, пл. 185-186°С.
Пример 23. Получение 4-(3-трет.бутила ино-2-никотиноилоксипропокс и) Ш.9-ФЛУ оренона.
Поступают так, как было описано в примере 1, и дебензилируют 4-(j3-( N -бензил-трет. бутиламино) -2-никотиноилоксипропокси -9-флуоренон; В результате получают соединение. ГицрЪрксалат име« вт т. пл. 223°С.
Пример 24. Получение (З-фенил-1-пропиламино)-2-пиБалоилоксипропокси) -9 -флу орено на.
Поступают так, как было описано в примере 1, и дебензилируют -бензил-(3-фенил-1- 1ро1галамино)-2-пивалоилоксипропокси}-9-флуоренон. В результате получают соединение, т. пл. 8385°С.
Пример 25. Получение сложного этилового эфира 2-метил-2-(Ъ-(9-оксо-4-флуоренилокси5-2-пивалоилоксипропиламино)-пропионовой кислоты.
Поступают так, как было описано в примере 1, и дебенэилиру1бт сложный
этиловый эфир 2-|N -бензил з-(9-оксо-4-флуоренилокси)-2-пивалоилоксипропиламино |1 -2-метилпропионовой кислоты. В результате получают соединение. Гидрооксалат имеет т. пл. 169-170°С.
Приме р 26. Получение (2-метил-4-фенил-2-бутиламино)-2-пивало1Ялоксипропокси -9-флуоренона.
( N - ензил-2-метил-4-фенил-2-бути лам ино) -2-окс ипр опокси2 -9-флу оренон растворяют в тетрагидрофуране и де- бензилируют водородом в присутствии палладиевого катализатора (10% палладия на угле). В результате получают соединение. Гидромалеат имеет т. пл. 198-2ОО°С.
Пример 27. Получение 4-ГЗ-тре бутиламино-2-( 1-метилциклогексилкарбонилокси)-пропокси -9-флуоренона.
( N -бензил-трет. бути лам ино)-2г-( 1-метилциклогексилкарбокси) -пропокси -9-флуоренон растворяют в тетрагидрофкр не и дебензилируют водородом в прЬсутст ВИИ палладиевого катализатора (10% палладия на угле). В результате получают содинение. Гидро.хлорид имеет т. пл. 182. 184°С.
485589
9
10
Предмет изобретения
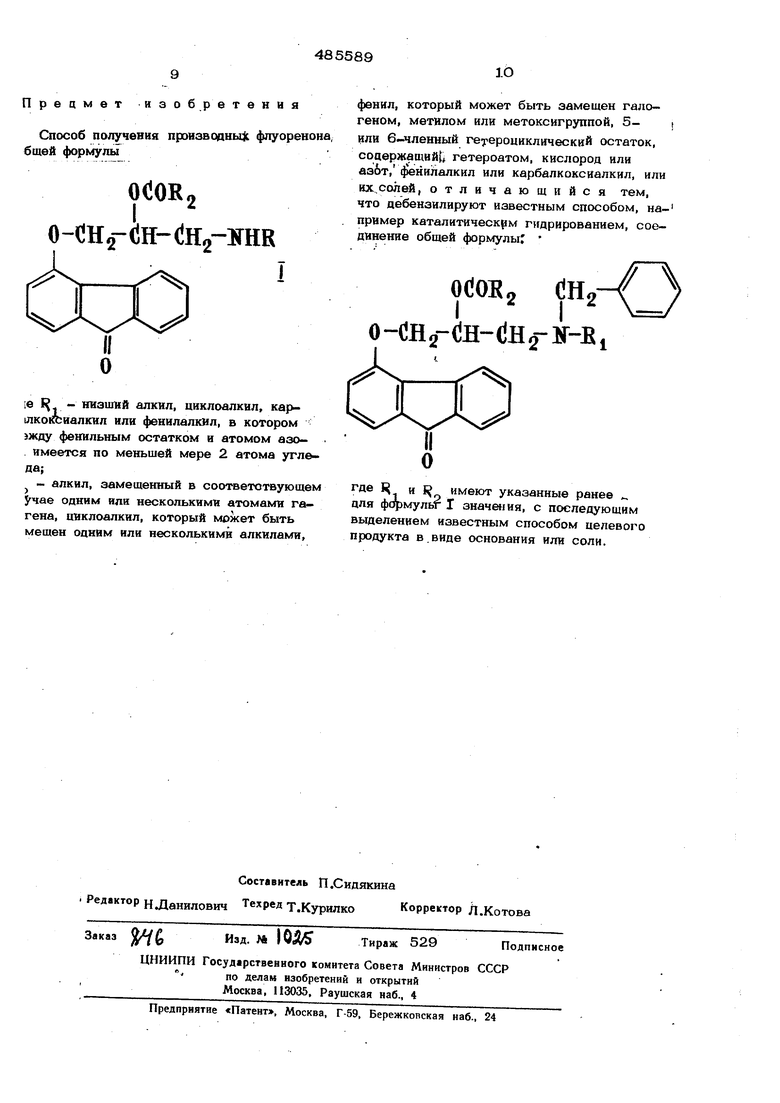
Способ получения производньцс фпуоренона, бщей формулы
OCOR2
I
o-CHs-iiH-dHgJTHR
6 1 - низший алкил, циклоалкил, карлкоксиалкил или фенилалкил, в котором 5жду фенильным остатком и атомом азоимеется по меньшей мере 2 атома угледа;
- алкил, замешенный в соответствуюшем Jrnae одним или несколькими атомами гагена, циклоалкил, который может быть мешен одним или несколькими алкилами.
фенил, который может быть замешен галогеном, метилом или метоксигруппой, 5- или 6-членный гетероциклический остаток, соаержвщвй гетероатом, кислород или азЬт, 1Й нилалкил или карбалкоксйалкил, или их солей, отличающийся тем, что дебензилируют известным способом, например каталитическрм гидрированием, соединение общей формулы;
ОЙОЕп ЙНо
II
O-CHg-tiH-teg-iT-Ei
где Ц и { имеют указанные ранее „ для формульг I значения, с последующим выделением известным способом целевого продукта в.виде основания или соли.





Авторы
Даты
1975-09-25—Публикация
1972-05-24—Подача