(54) СПОСОБ. ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
БЕНЗОЦИКЛОГЕПТЕНА ИЛИ ИХ СОЛЕЙ Изобретение относится к способу получения новых производных бензоцик логептена общей формулы OCHiCHCH NHRi i« /2 .|-(СНг)п tC«iu (СВ.5)р( где либо |э О, п 1 или 2 и m « 1; либо р 1, п 1;ИП1 О или 1; либо , R -алкил Сз-7 фенилалкил, феноксиалкил или фенилтиоалкил Cg, которые в фениль ном кольце имеют заместитель алкилили алкоксигруппу С « атом галоида трифторметил или цианогруппу, причем фенилрадикал отделен по крайней мере двумя атомами углерода от атома азота, с которым связан R и R 3 либо вместе образуют неразвётвленный С -С -алкилен, либо К и R% каждый представляет собой атом водорода или алкил . причем, если р равно О, а m и h равны 1, то Ra и R3 не могут сразу обозначать два атома водорода; R и RK- каждый представляет собой атом водорода или алкил С,. Описываемые соединения обладают блокирующим воздействием на адренергические 5-рецепторы и поэтому могут применяться для профилактики и терапии коронарных заболеваний. Известны различные производные бензоциклогептена. Известен способ получения 10-С2-окси-3-(2,2,5,5-тетраметил-1-пирролидинил)-пропоксиЗ-4Н-бензо-Е4,5 J -циклогепта 1,2-ЬЗтиофен-4-она, заключающийся в том, что смесь 10-(2,3 -эпоксипропокси)-4Н-бензо 4,5 -Циклогепта-С1,2-ь}тиофен-4-она и 10-(3-хлор-2-окси-пропокси)-4-она кипятят с 2,2,5,5 тетраметилпирролидином в метаноле L13« Согласно способу получения производных бензоциклогептена общей формулы I или их солей соединение формулы I I
х
t (г
01 ;(СНг) (СМ5)р-Ч
где , Pi пит имеют указанные значения, а R представляет собой группу.
-ся-сн, ч/- г
о
-СН-СНхУ
Ьн
где У - галоген или группа Ry-SOj -O, где Ry-фенил, толил или низший алкил подвергают взаимодействию с первичны амином формулы III
,
I Ь .
где R имеет указанное значение. Целевой продукт выделяют в виде свобод ного соединения или соли, которые могут быть в форме рацемата или оптичеки активного антипода.
Процесс проводят преимущественно в инертном органическом растворителе например в диоксане, при температуре киг1ения реакционной смеси, кроме тех случаев, когда реакция происходит в расплаве.
Пример 1. 1-(3-трет.-Бутиламино-2-гидроксипропокси)-6,7,8,9 .-тетрагидро-7,7 ДИметил-5Н-циклогептен-6-он. 2,2 г сырого 1-(3-хлор-2-гидроксипропокси)-6,7,8,9-тетрагидро-7 7-Диметил-5Н-бензоциклогептен-6-она кипятят в 20 мл диоксана и 10 мл трет.-бутиламина в автоклаве в течение 20 ч при ,.затем.концентрируют и растворяют в 10%-ном водном растворе винной кислоты и эфира. Водную часть экстрагируют с помощью эфира (т.пл. кислого малеината 186-188°С - из этанола).
Количество полученного конечного продукта 2,2 г.
Исходные реагенты могут быть получены следующим образом:
а) К суспензии, состоящей из 21 г гидрида натрия в тетрагидрофуране, добавляют по каплям раствор ,0 г 5-метокси-1-тетралона в тетрагидрофуране. После этого смесь подвергают
взаимодействию с г метилиодида в тетрагидрофуране. В. результате получают 5-метокси-2,2-диметил-1-тетралон (т.кип. 162-170 С при ; 12 мм рт. ст.).
б)Смешивают раствор метилмагнийиодида(получен из 69,7 г метилиодида и 11,9 г магния в эфире) с раствором 66,5 г 5-метокси-2,2-диметил-1-тетралона в эфире, далее примешиваю раствор из б2 г хлорида аммония а воде, полученный карбинол экстрагируют с помощью эфира, повторно раствряют в бензоле, в котором находится 0,5 г толуол-П-сульфоновой кислоты. После хроматографической очистки с помощью петролейного эфира получают метил-1 -(5,6,7,8-тетра гидро-6,6-диметил-5-метиленнафтил)-эфир (сырое масло - прямо может обрабатываться).
в)125 г таллиумтринитрат-тригидрата в метаноле подвергают взаимодействию с 55 г метил-1-(5,6,7,8-тетрагидро-6,6-диметил-5 метилен-нафтил)-эфира в бензоле, выпадающий тринитрат таллия отфильтровывают и раствор экстрагируют с помощью метиленхлорида. 6,7,8,9-Тетрагидро-1-метокси-7,7-диметил-5Н-бензоциклогептен-6-он плавится при 58-59 С (из гексана),
г)4,0 г 6,7,8,9-тeтpaгидpo-1-мeтoкcи-7 , 7-диметил-5Н-бензоциклогептен-6-она кипятят вместе с 45 мл уксусной кислоты и с 5 мл 0%-ного раствора брома в воде в продолжение 20 ч, потом раствор сгущают, далее его разбавляют водой и экстрагируют с помощью эфира. 6,7,8,9-тетрагидро-7,7-диметил-6-оксо-5Н-бензрциклогептен-1 , остающийся после удаления растворителя,плавится при 152-15 С (из толуола).
д)К раствору из 1,8 г 6,7,8,9 -тетрагидро-7,7-ДИметил-6-оксо-5Н-бензоциклогептена-1 и 8 мл эпихлоргидрина добаёляют 2 капли пиперидина и перемешивают в течение ч при . Раствор выпаривают, вносят в эфир, фильтруют и сгущают, причем остается 1-(3-хлор-2-гидроксипропокси)-6,7,8,9-тeтpaгидpo-7,7-Димeтил-5H-бeнзoциклoгenтeн-б-oн.
Пример2. 8 -(3-тpeт.-Бyтилaминo-2-гидpoкcипpoпoкcи)-cпиpo | циКлогептан-1 ,2 - (1 -Н)-нафталинЗ-4(зн)-он.
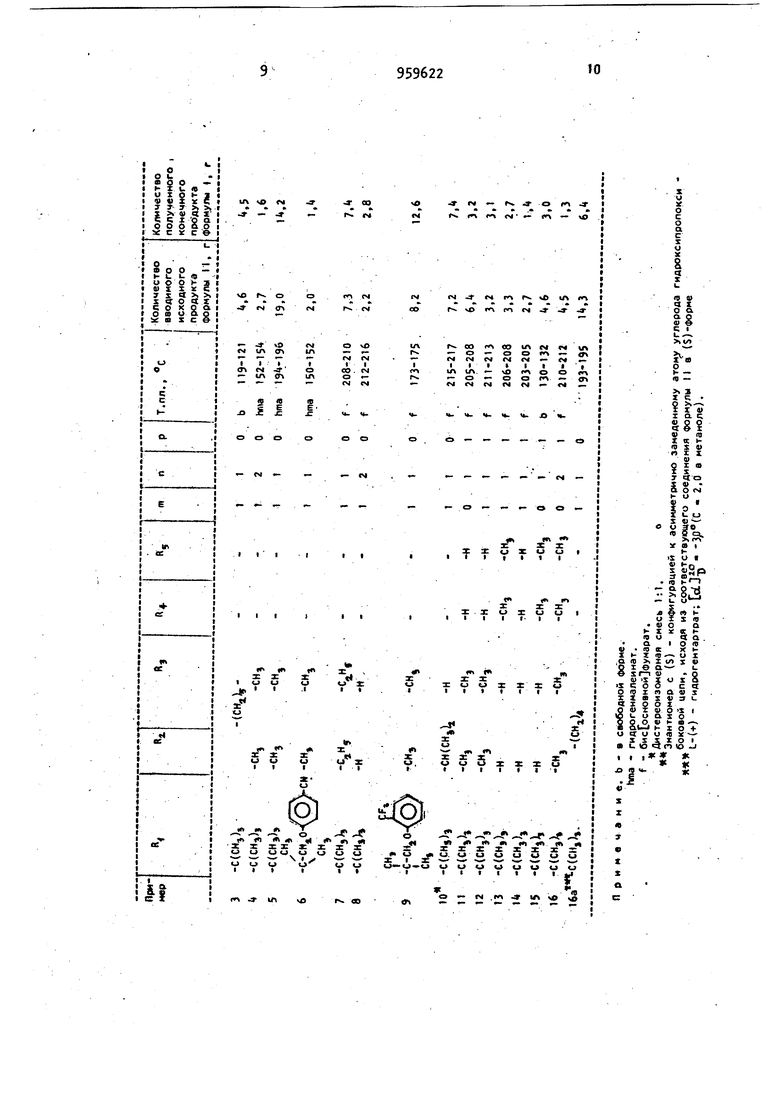
Аналогично примеру 1 из 4,6 г 8 -(З-хлор-2-гидроксипропокси)-спи5ро циклопентаи-1,2(1-Н)-нафталин -« (ЗН)-она получают 4,5 г целевого соединения,(т.пл. гидрогенмалеината 188-190°С - из этанола). Исходное вещество может быть полу чено следующим образом: а)К раствору 2-метоксибензилмагнийхлорида (получен из 5,3 г магния и 31,2 г 2-метоксибензилмагнийхлорида, растворенных в jOO мл эфира) по каплям добавляют раствор 39,9 г циклопентилиденциануксуснокислого этилового эфира в 350 мл тетрагидрофурана. Смесь в течение 2 ч перемешивают при комнатной температуре. Далее смесь перемешивают с 300 мл 15 -ного раствора хлорида аммония, продукт экстрагируют, с помощью эфи.рэ и эфирный раствор сгущают. В результате получаюто -циано-(1 - 2-метоксибензилЗ-циклопентан J-уксуснокислый этиловый эфир, который перегоняют при I O-lBO C, 0,002мм рт. (сырой продукт может подвергаться дальнейшей обработке). б)К раствору из 32, гоС-Циано-J l- 2-метоксибензилД-циклопентан}-уксуснокислого этилового эфира и 300 мл этиленгликоля добавляют 33,6 гидроокиси калия и раствор перемешивают в течение 40 ч при . Раствор охлаждают, а нейтральные побочные продукты удаляют путем эфирного экстрагирования. Водную часть подкисляют соляной кислотой и экстрагируют с помощью эфира. После упаривания растворителя остается (2-метоксибензил) циклопентан}ук.сусная кислота (т.лл. 85-87 с - в гексане). в)5,7 г f1-(2-метоксибензил)циклопентан уксусной кислоты перемешивают с 30 г полифосфорной кислоты при температуре 1 в течение 10 мин. Раствор охлаждают и добавляю 250 мл водц. Путем экстракции с помощью эфира и концентрирования эфирного экстракта получают 8 -метокси-спиро циклопентан-1,2(lH)-нaфтaлин -4 (ЗН)-он (т.пл. б2 -6бС, непосредственно сразу подвергается дал нейшей обработке). г)Аналогично примеру 1 (абзац г) из 8-метокси-спиро| циклопентан-1,2 (1н)-нафталин -4 (3Н)-она получают 8-гидрокси-спироГциклопентан .-1,2 (1Н)-нафталин -4(Зн)-он (т.пл. 163-165°С - из толуола). .д) Аналогично примеру 1 (абзац д) из 4,6 г 8 -гидрокси-спиро1 циклопен22 - тйн-1,(1H)-нaфтaлинJ-4-()-она получают 8-(3 хлор-2-гидроокси пропокси)-спироГ-Циклопентан-1,2 -(1н)-нафталинЗ- -(3н)-он (сырой) Примеры 3-1ба. Аналогично примерам 1 и 2 путем взаимодействия соответствующих соединений формупы I I , где R означает -CHCH/jrOP , t соединением формулы til (в избытке) получают соединения формулы К представленные в таблице. Пример 17. 1-(3-трет.-Бутиламино-2-гидроксипропокси)-6,7,8,9 -тетрагидро-7,7-Диметил-5Н-бензоциклопентен-6-он. Аналогично примеру 1 из 1,7 г 1-(2,3-этоксипропокси)-6,7,8,9-тетра гидро-7,7-диметил-5Н-бензоциклопен-6-она получают 1,6 г целевого соединения (т.пл. кислого малеината 186188 С - из этанола). . Исходный продукт получают анало-. гично примеру 1е путем обработки в течение 1 ч после реакции превращения с эпихлоргидрином полученного сырого продукта с эквивалентом трет, -бутилата калия в абсолютном тетрагидрофуране при комнатной температуре. Пример 18. 1-(3-трет.-Бутиламино-2-гидроксипропокси),8,9 -тетрагидро-7,7-диметил-5Н-бензоциклопентен-6-он. Аналогично примеру 1 из 2,3 г 1-Ч 3-бром-2-гидроксипропокси)-6,7,8,9-тетрагидро-7,7-яиметил-5Н-бензоциклогептен-6-она получают 2,1 г це-; левого соединения (т.пл 186-188 C из этанола). Исходный продукт получают аналогично примеру 17 при использовании эпибромгидрина вместо эпихлоргидрина. Пример 19. 1-(3-трет.-Бутиламино-2-гидроксипропокси)-6,7,3,9 -тетрагидро-7,7-Диметил-5Н-бензоциклопентен-6-он. Аналогично примеру 1 из 1,6 г 1-(2-гидрокси-3-мезилоксипропокси)-6,7,8,9-тетрагидро-7,7-диметил-5Н-бензоциклогептен-6-она получают 1,3 г целевого продукта (т.пл. 186188 С - из этанола). Исходный продукт получают аналогично примеру 17 при использовании 1,2-эпокси-З-мезилЬксипропана вместо эпихлоргидрина. П р .и м е р 20. 1- (Зтрет.-Бути ламино-2-гидроксипропокси )-6,7,8,9 -тетрагидро-7,7,Яиметил-5Н-бензоциклопентен-6-она. Аналогично п-римеру 1 из 2,7 г 1-(2-гидрокси-3 П тозилоксипропокси) -6,7,8,9-тетрагидро-7,7-Диметил-5НбензЬциклогептен-6-она получают 2,3Г целевого соединения (т.пл. t86 - из этанола). Исходный продукт получают анало- ; гично примеру 17 при использовании 1,2-эпокси-3- -т6зилоксипропана вместо эпих оргидрина. , 95 2 Пример 21. 1-(3-трет.-Бутиламино-2-гидроксипропокси)-6,7,8,9 :-тетрагидро-7,7 диметил-5Н-бензоциклогептен-6-он. Аналогично примеру 1 из 2,2 г 1-(3 бензолсульфонилокси-2-гидроксипропокси)-6,7,8,9-тетрагиДро-7,7-диметил-5Н-бензоциклоГептен-6-онаполучают 1,9 г целевого соединения (т.пл. 186-188 С - из этанола). Исходный продукт получают аналогично примеру 17 при использовании Збензолсульфонилокси-1,2-эпоксипропана вместо эпихлоргидрина. Формула изобретения Способ получения производных бен циклогептена общей формулы 1: OCHiCHCH UHKi Чснг1п ч ъ о I ., )p-- где либо {) 0, п 1 или 2, m 1; либЬ р 1, п 1, тп О или 1; либо ,, R-алкил , фенилалкил, феноксиалкил или фенилтиоалкил Cg:., которые в фенильном кольце в случае необходимости имеют заместитель алкил- или алкоксигруппу атом галоида, трифторметил или цианогруп пу, причем фенилрадикал отделен по крайней мере двумя атомами углерода от атома азота, t которым связан R Rj и Rj либо вместе образуют неразветвленный С |-алкилен, либо R 1 каждый представляет собой атом водорода или алкил приче если р равно О, а m и п равны 1, то R и R-J не могут сразу обозначать д атома водорода; 12 R. и Re каждый представляет собой атом водорода или алкил С ., , или их солей,,о т ли чающий с я тем, что соединение формулы II г 1 . -(,N. Э ,1т (CR,)p-4 где , р, п и m имеют указанные значения, а R- представляет собой группу -СН - СН,, -СН -СН.,У X / Л I о он где У - галоген или группа R -SOj-O, где R - фенил, толил или низший алкил, подвергают взаимодействию с первичным амином формулы III кгда где имеет вышеуказанное значение с последующим выделением целевого продукта в виде свободного соединения или соли. Источники информации, принятые во внимание при экспертизе 1. Патент СССР № 537337, кл. С 07 D 205/0, 1975,






Авторы
Даты
1982-09-15—Публикация
1978-03-23—Подача