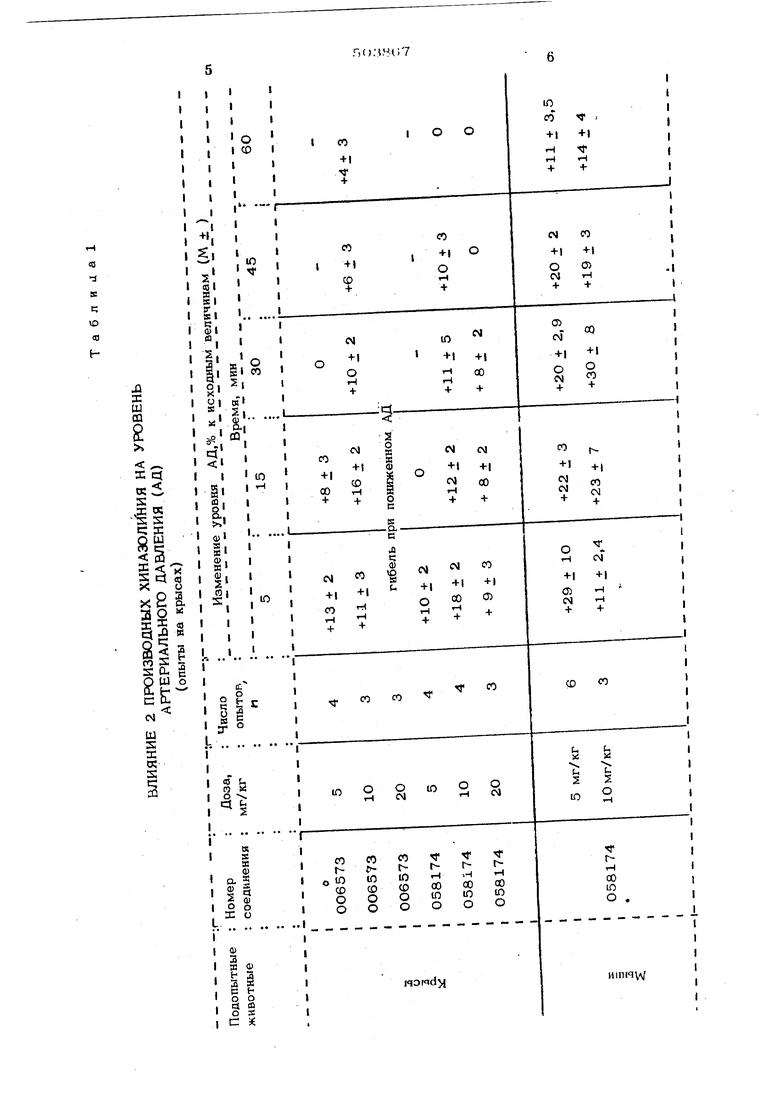
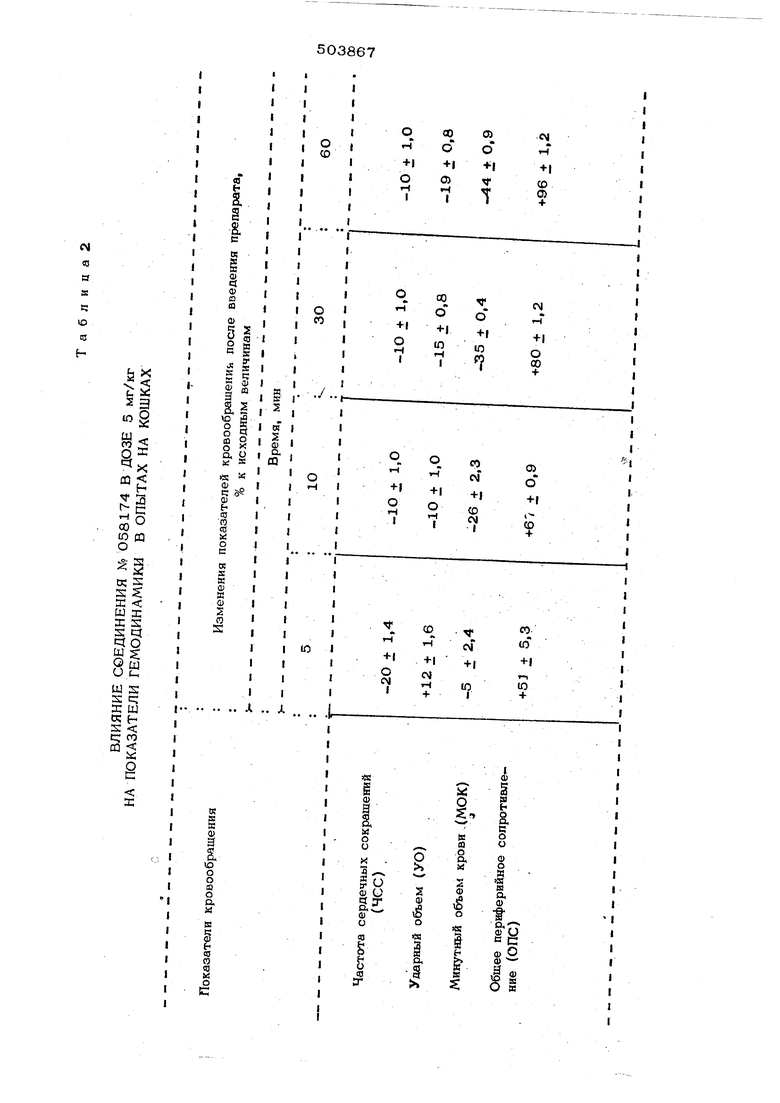
З-метил-3,4 дигидро-4-оксихиназишн: (П) -псевдооснование соединения Т. иелью изобретения является синтее йодистого и хлористого 3-метил-3,4гйигидро--4 - (3-иидолил) -хиназолиниясредств сердечно-сосудистого действия. Полученные соли нредставлякт собой высокоплавкие бесцветные кристаллические вещества, растворяющиеся в полярных органических растворителях, воде, кристаллизуются. Способ получения йодистого 3 -метил-3, - дигидро - (3 -индолил) - хиназол иния заключается в конденсации индола с йодистым 3 - метилхиназолинием при 100110°С,I Процесс следует вести в высококипяще полярном растворителе, предпочтительно в бутиловом спирте. Выпавшие из реакционной массы кристаллы отфильтровывают, кристаллизуют. Хлористый 3-метил-3,4 -дигидро-4 -(3-индолил)-хиназолиний получают взаимодействием гидрохлорида 3-метил-3,4 -дигидро -4 -оксихиназолина -псевдооснова имя соединения I с индолом в спирте при 100 - 11О°С. Строение синтезированных соединений доказано данными элементного анализа, методом Уо и ПМР спектроскопии и хим ческим путем. Нарушение ароматичности пиримидиновой части молекулы йодистого 3-метил-3,4 -дигидро -4 -(з-индолил) -хиназолин проявляется; в УФ - спектре в гипросхром ном сдвиге полосы поглощения с А weX 23О нм (.З), характерной для йодмет лата хиназолина, до 215 нм. При присое динении индола к йодметилату хиназолина исчезают кольцевые токи в пирамидиново фрагменте, что отражается в спектре ПМР полученного соедоюния в смещении сигналов 2-Н ( 9,45 м.д.) и 4-Н ( «9,96 м. д. ), характерных для четвертич ной соли хиназолина, в значительно более сильное поле: .2-Н ( 8,75 м.д.) и 4-Н ( 6,5О м.д.). Протонирование молекулы приводит к появлению сигнала 3-Н в слабом поле ( 5 8,70 м.д. ). Сигналы ароматических гфотонов о.ннели- рованного бензоядра в хиназолиновой части молекулы, а также в индоле проявляются в виде мультинлета ( S 6,8-7,7 м.д.). Строение хлористого 3 -метил -3,4 дигидро - 4 -( индолил) - хиназолиния подтверждено химическим путем. К 3- летил-3,4-дигидро-4- (3-индолил)-хиназолину, выделенному после под- шелачивания водного раствора йодистого 3-метил-3,4 рдигидро -4 -(З-индолил) хиназолиния до рН 8, добаншяют концентрацию НС t до рН 1. Образовавшийся олевой продукт идентифицирован с ранее олученным хлористым 3-метил-3,4-диидро-4-(З-индол ил)-хиназол инием по / ( ) и отсутствию депрессии пробе смещения. Влияние соединений на уровень артерильного давления (АД) определяют в остых опытах на крысах (наркоз нембутаовый) и кошках (наркоз уретан-хлоразопа); бщепринятым методом. Вещества вводят в дозах 1, 5, 1О и 2О мг/кг. Менее токсичное и перспективное oeдиj«eниe - йодист ый 3 -метил -3,4 -диидро - 4 - ( 3 - индолил ) - хиназолиний . ; ; № 058174 ,) изучается более подробно. Как показывают проведенные опыты на крысах, соединения № 058174 i. №006573 (хлористый хиназолиний) вызывают заметное повыщение уровня артериального давления (см, табл. 1). Гипертензия кратковременная при введении 5 мг/кг и болэе длительная.при введении 10 мг/кг. В опытах на кощках наблюдается высокая активность соединения № 058174 по сравнению с опытами на крысах. Выраженное повыщение АД отмечается уже 5 мин. после введения вещества в дозе 5 мг/кг и продолжается 45-60 мин. При увеличении дозировки до lO мг/кг установлено болеет позднее появление гипертен- зии (АД повыщается лищь через 15 мин, после введения), что очевиднс объясняется ослаблени.ем работы сердпа в первые минуты после введения.. В опытах зарегистрированы изменения ряда показателей кровообращения (см. табл.2)-урежается частота сердечного ритма, уменьщается ударный объем (УО) и сердечный кыброс - (минутный объем крови) - (МОК), повыщается общее периферийное сопротивление (ОПС).
CQ i
S
e;
Ю D
H
Л
3:
Ш CQ
X cl
к
«
-I
s
I
E: X
01
з: s
rf C( CO
X
и
xB
2§
1
0 №
g
rt S S Cu Ш
2Щ о b-c:fc
CM
Ш
s
ОС CR S
I
I I I
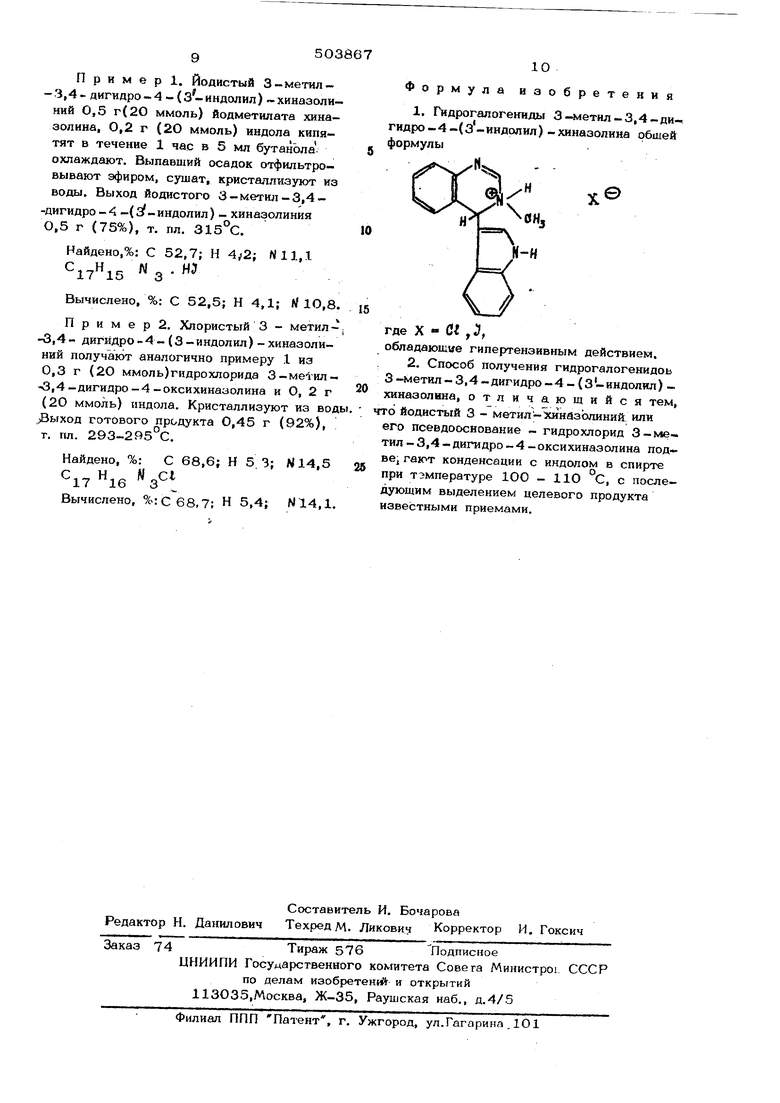
I t I I 5О3 Пример. Йодистый 3-метил- 3,4 дигидро 4 - (З- индолил) хиназолиний 0,5 г(2О ммоль) йодметилата хиназолина, 0,2 г (2О ммоль) индола кипятят в течение 1 час в 5 мл бутанола охлаждают. Выпавший осадок отфильтровывают эфиром, сушат, кpиcтav лизyJoт из воды. Выход йодистого 3-метил -3,4-дигидpo-4 -(Sf-индолил) - хиназолиния 0,5 г (75%), т. пл. З15с. Найдено,%: С 52,7; Н 4/2; N11,1 N 3 . Н Вычислено, %: С 52,5; Н 4,1; И 10,8 П р и м е р 2. Хлористый 3 - метил-5,4- дигидро-4- (3-индолил) -хиназолиний получают аналогично примеру 1 из 0,3 г (2О ммоль)гидрохлорида 3-метил-3,4-дигидро-4-оксихинааолина и О, 2 г (20 ммоль) индола. Кристаллизуют из вод JBыxoд готового продукта 0,45 г (92%), т, пл. 293-2 . Найдено, %: С 68,6; Н 5,3; N14,5 17 l6 Вычислено, %:Се8,7; Н 5,4; N14,1 10 Формула изобретения 1. Гидрогалогениды 3- 1етал-3,4-ди-. гидро -4 -(3 -индолил) - хиназолина обшей формулы -Ч где X - С , 3, обладающие гипертензивным действием. 2. Способ получения гидрогалогенидоь 3 -метил - 3,4 - дигидро - 4 - (3 - индолил) хиназолина, отличающийся тем, то йодистый 3 - метил-Хиназолиний или его псевдооснование - гидрохлорид 3-ме тил - 3,4 - дигидро - 4 -оксихиназолина подве, гают конденсации с индолом в спирте при тэмпературе 100 - 110 °С, с последуюшим выделением целевого продукта известными приемами.



Авторы
Даты
1976-02-25—Публикация
1974-12-31—Подача