(54) СПОСОБ ОПРЕДЕЛЕНИЯ ТРИГЛИЦЕРИДОВ В ВЕЩЕСТВАХ

| название | год | авторы | номер документа |
|---|---|---|---|
| Реактив для определения тригицеридов | 1976 |
|
SU641884A3 |
| Реактив для определения триглицеридов | 1973 |
|
SU639487A3 |
| Реактив для турбидиметрического определения липазы | 1980 |
|
SU1367867A3 |
| СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ТРИГЛИЦЕРИДОВ | 1973 |
|
SU371734A1 |
| СПОСОБ ОПРЕДЕЛЕНИЯ ПОЛИВАЛЕНТНОГО АНТИГЕНА В БИОЛОГИЧЕСКОЙ ЖИДКОСТИ | 1989 |
|
RU2032906C1 |
| Способ определения свободного связанного холестерина в биологических жидкостях | 1973 |
|
SU637097A3 |
| Реактив для определения общего холестерина в сыворотке крови | 1974 |
|
SU717994A3 |
| 4-ЦИКЛОАЛКИЛЗАМЕЩЕННЫЕ ПРОИЗВОДНЫЕ ТЕТРАГИДРОХИНОЛИНА И ИХ ПРИМЕНЕНИЕ В КАЧЕСТВЕ ЛЕКАРСТВ | 2005 |
|
RU2393151C2 |
| СПОСОБ ДИАГНОСТИКИ ХРОНИЧЕСКОГО ПАНКРЕАТИТА, РАЗВИВШЕГОСЯ НА ФОНЕ ЯЗВЕННОЙ БОЛЕЗНИ ДВЕНАДЦАТИПЕРСТНОЙ КИШКИ | 2002 |
|
RU2249433C2 |
| Реактив для определения глицерина фотометрическим методом | 1981 |
|
SU1554765A3 |

Изобретение относится к способам определения триглицеридов в веществах и может быть использовано как при анализе пищевых продуктов, так и в медицинских целях.
Известен способ определения триглицеридов в веществах, например пищевых продуктах, предусматривающий их ферментативное омыление путем добавления к пробе липазы и последующее измерение количества образовавшегося глицерина.
Недостаток ферментативного расщепления по известному способу состоит в том, что омыление протекает продолжительное время и, кроме того, при осуществлении этого способа необходимо использовать значительные количества дорогого фермента. Для того чтобы реакция протекала в приемлемый промежуток времени, необходимо в одну пробу добавлять около 1 мг фермента. Время реакции превышает 30 мин, поэтому способ мало пригоден для проведения быстрых лабораторных исследований, в частности при частых определениях. Наконец, выделившаяся в свободном состоянии кислота жирного ряда образует с ионами кальция и .магния нерастворимые мыла, которые, если не проводить центрифугирование, приводят к помутнению и, следовательно, искажению результатов измерения.
С целью упрощения и уменьшения времени определения предложено наряду с липазой к пробе добавлять карбоксилэстеразу и алкилсульфат щелочного или щелочноземельного металла, содержащего в алкильном остатке от 10 до 15 атомов углерода. Алкилсульфат рекомендовано добавлять в количестве от 0,001 до 0,1% (вес/объем), а омыление проводить при рН от 6 до 9. При этом желательно наряду с карбоксилэстеразой и алкилсульфатом в пробу дополнительно вводить альбумин сыворотки в количестве от 0,1 до 2,0 мг/мл.
Количество липазы, необходимое для одного определения, составляет около 20 мкг. Определение проводят при комнатной температуре. В качестве липазы предпочтительно использовать липазу из Rhizopus arrhizus, а в качестве карбоксилэстеразы (БС 3.1.1.1) карбоксилэстергидролазу - препарат, получаемый из печени млекопитающих, в частности из печени свиньи.
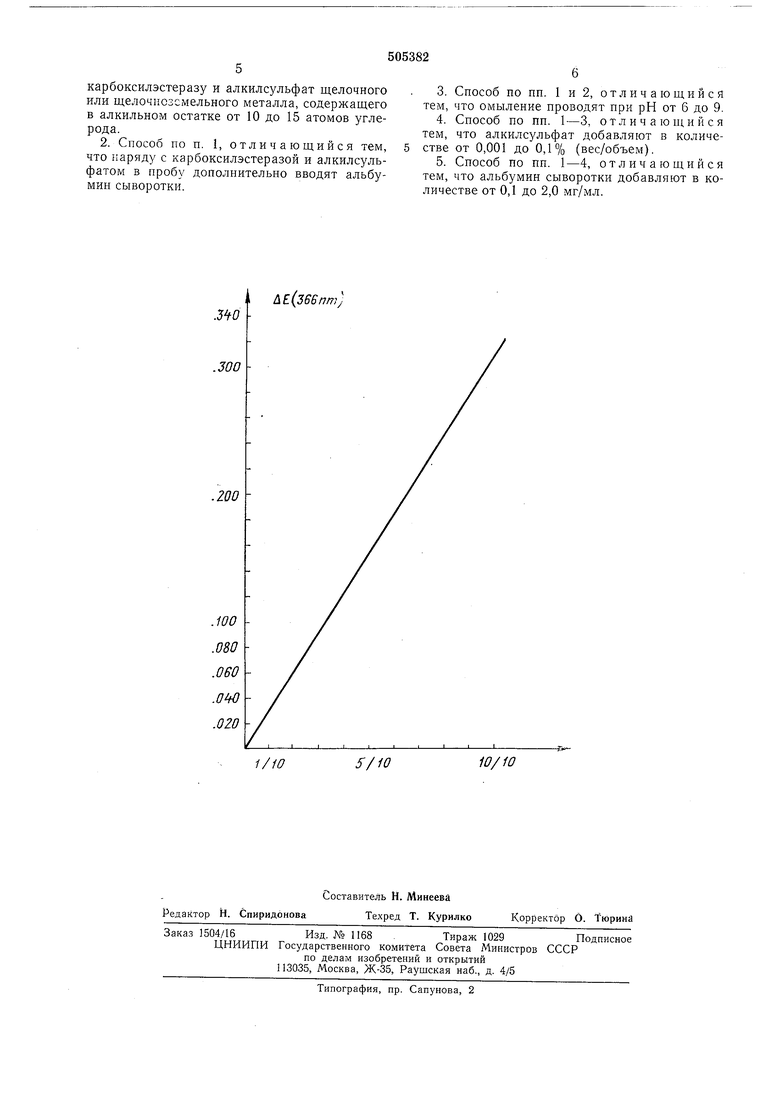
Однако применение могут находить также и другие карбоксилэстеразы. Вполне достаточно использовать приблизительно 100 мкг эстеразы на одно определение. Среди алкилсульфатов желательно использовать соли щелочных металлов, так как они не образуют нерастворимого мыла с выделяющимися жирными кислотами. При добавлении альбумина сыворотки в пробу можно использовать алкилсульфаты щелочноземельных металлов, например додецилсульфат в количестве до 0,001 % (вес/объем). Количества более 0,1% приводят к образованию пены и некоторому замедлению реакции. По этой причине нецелесообразно применять алкилсульфат в таких количествах. Определение можно проводить при рН от 6до 9. Оптимальная область рН лежит между 7и 8,5, что позволяет проводить омыление и измерение количества образовавшегося глицерина в одной реакционной смеси. Ионы кобальта и/или магния оказывают активирующее действие на липазу и эстеразу и поэтому могут быть добавлены к реакционной смеси для еще большего ускорения реакции. В качестве буферов могут быть использованы все эффективные в указанной выше области значений рН буферы, кроме фосфатного. Пригодными буферами являются триэтаноламиновый, амидазольпый, вероналовый, глициновый, трис-буфер, а также, что менее желательно, амидольный, бо атный и коллидиновый. Пример 1. Готовят состоящий из пяти компонентов реактив, который можно хранить в течение 1-2 дней. Компонент I0,1 М триэтаноламиновый буфер (рП 7,6), содержащий 3 ммоля сернокислого магния, 1,5мг/мл альбумина сыворотки крупного рогатого скота и 0,1 мг/мл додецилсульфата натрия. IIРаствор, содержащий 6 ммолей НАДН, 33 ммоля АТФ и 11 ммолей фосфоэнолпирувата в дистиллированной воде. IIIСуспензия кристаллов, содержащая 2 мг/мл лактатдегидрогеназы и 1 мг/мл пируваткиназы. IVРаствор, содержащий 0,2 мг/мл липазы из Rhizopus arrhizns и 4,0 мг/мл карбоксилэстеразы. VСуспензия кристаллов, содержащая 2 мг/мл глицеринкиназы. Смешивают 2,9 мл компонента I, 0,1 мл компонента П и 0,02 мл компонента III, и смесь нагревают до 25°С. Затем добавляют 0,1 мл сыворотки, которая содержит триглицериды, подлежащие определению, и полученную смесь выдерживают 5 мин при указанной температуре. После этого к реакционной смеси добавляют 0,1 мл компонента IV, смесь выдерживают 15-20 мин при указанной температуре и Никотинамидадениндинуклеотид в гидрированной форме. Аденозинтрифосфат. сразу же после этого определяют поглощение при 366 нм или 340 нм. Найденное значение обозначают EI. После этого к пробе добавляют 0,02 мл компонента V и через 10 мин опять определяют поглощение. Измеренное значение обозначают Eg. Через 10 мин снова определяют поглощение и полученное значение обозначают ЕЗ. Расчет проводят по уравнению: АЕ (Е,-Е,}-(Е,-Е,}. Общее содержание глицерина в триглицеридах (в мг на 100 мл) равно ДЕ-89,1. Вышеописанное определение повторяют 9 раз, причем каждый раз прибавляемое количество сыворотки уменьшают на 0,01 мл. При нанесении на график полученных значений ДЕ по отношению к добавленному количеству сыворотки получают прямую линию (см. чертеж). Из найденных значений рассчитывают пропорциональность сг 0,9986. Сравнение сг (идеальн.) 1000 показывает высокую точность метода. Пример 2. Опыт, описанный в примере 1, повторяют с использованием стандартного раствора триглицеридов. В опыте 1 в реакционную смесь не добавляют карбоксилэстеразу и додецилсульфат, в опыте 2 - додецилсульфат, а в опыте 3 - карбоксилэстеразу. Результаты определения количества триглицеридов представлены в таблице как процентное отношение экспериментально полученных значений к тем концентрациям триглицеридов. которые добавлены в реакционную смесь. Приведенные данные показывают, что при соблюдении выбранных условий в отношении концентрации липазы лишь соответствующая предлагаемому способу комбинация компонентов пригодна для количественного определения. Формула изобретения 1. Способ определения триглицеридов в веществах, например пищевых продуктах, предсматривающий их ферментативное омыление утем добавления к пробе липазы и последущее измерение количества образовавщегося лицерина, отличающийся тем, что, с цеью упрощения и уменьшения времени опрееления, наряду с липазой к пробе добавляют
карбоксилэстеразу и алкилсульфат щелочного или щелочноземельного металла, содержащего в алкильном остатке от 10 до 15 атомов углерода.
(Z6Bnm
.0
.300
1/10
10/W
/10
Авторы
Даты
1976-02-28—Публикация
1973-06-19—Подача