подвергают взаимодействию со спиртом общей формулы R - ОН(З), где F имеет указанные значения, в кислой среде, полученное соединение, если 5 - атом галогена или роданогруппа И - ацильный остаток, в присутствии . 3 органического основания, предпочтительно диэтиламина, восстанавливают водородом, расходуемым в количестве одного эквивалента, до образования соответствующего С-3-метильного соединения, ацильную груп пу омыляют известным способом, а конечный продукт выделяют обычными методами Возможно также сначала производить омыленйё ацильной группы и непосредственно после этого восстанавливать галогенметиПьну}о группу в метильный остаток. Соединение, соответствующее формуле 2, вводят во взаих одействие со спиртом преимущественно в присутствии соляной кислоты, и -толуолсульфокислоты или кислоты Льюиса. Предпосылкой к проведению реакции цик , которая может быть осуществлена в кислой, преимущественно спиртовой, среде, или к получению ыиклогепта(с)пирана является наличие в цис-положении циклопентанового кольца С-7 гидроксильной группы и пиранового кольца, а также нал ичие реакционоспособной аллильной состемы у углеродных атомов е-3, С-4, С-6. Формально циклизация происходит в результате присоединения кислорода гидроксильной группы к С-7 и С-3, что сопровождается аллильной перегруппировкой и отщеплением НХ. Поскольку реакцию проводят в Присутствии спирта и кислого катализатора, например хлористого водорода, и. -толуолсульфокислоты или кислоты Льюиса, то в результате алкоголиза может быть осуществлена замена | -остатка у С-1алкоксиль ным или арнлалкоксильным остатками, соо(Тветствующими применяемому спирту. В. промежуточном соединении общей фор мулы СНз- R, гае Si,, - галоген, Yf - ацильный r.c-i-aацилоксильный остаток, расположенный у . сначала может быть омылен до гигфоксильной группь, после чего может быть произведено каталитическое восстановлениё лагогенметильной группы у в метильный остаток. ЕСЛИ F,- ацильный ос. . . . .J. таток, циклопента(с )пираны формулы 2 могут быть получены из гидровальтре1та и его гомологов посредстврм переведения эпоксидного соединения в соответствующий гидрин. Если в качестве исходного соединения используют циклопента{с)пиран, в котором Е, - и -D-глюкозидный остаток, -..,,, ,., ... Rr, и F - атом водорода, то соединение ; . ,, . . формулы 1 получают циклизацией в результате реакции со спиртом в кислой среде. 1Диклопеита{с)пиран, в котором I -и Г-глюкоэидный остаток, содержится в корнях и ризомах растений типа валерианы и может быть выделен из них экстракцией такими полярными растворителями, как вода, спирты, ацетон, ЭТИЛОВЫЙ уксусной кислоты или смесь указанных растворителей, или смесь галогенированных. углеводородов и спирта, причем в некот фых случаях для получения вещества в чистом виде экстракт хроматографируют на силикагеле или окиси алюминия лри использовании в качестве элюирующего средства смеси этилового, эфира уксусной кислоты и спирта или экстракт подвергают гельфильтрации на молекулярных ситах, способных набухать в органических растворителях. В больщинстве случаев при синтезе соответствующих настояшему изобретению веществ также можно использовать неочищенные. экстракты гидровальтрата и аналогичных и -Л-глюкозидов., П р им ер 1. Получение 4-ацетокси-3-галоген(или родано)метил-10-метилен-8-метокси-2,9-Диоксатрицикло( 4,3,1,0 ) -декана. 2О г 1-изоваперокси- -изовалероксиметйл-6-ацетокси-7-гидрокси-7 - йодметил циклопента (сУпирана растворяют в 25 мл метилового спирта и полученный раствор смешивают при наружном охлаждении льдом с 1О мл метилового спирта, содержащим 19 г хлористого водорода в растворенном состоянии. Раствор постепенно окращивается в темный сине-зеленый цвет. После выдерживания в течение 1 часа при комнатной температуре реакционную смесь разбавляют водой, а затем тщательно экстрагируют диэткловым эфиром, после чего производят I.efiтрализациюэфиряо фазы к)к;лым углекнслым натрием. После сушки над сернокислым натрием, обесцвечивания небольшим количеством угля и упаривания раствора в вакууме (при 50 G/7 мм рт. ст.) до получения остатка постоянного веса или до исчезновения запаха метилового эфира изовалериановой кис лоты получают 13. в г маслообразного {фодукта,. окрашенного в светло- коричаевый ове который после раст&орения в небольшом количестве смеси метилового спирта и эфира постепенно кристаллизуется на холоде. Полученный 4-aиeтoкcи-3-йojaмвтил-10- метилен-8- метокси-2,9-диоксатриаик ло-(4.3,1,о )-декан представляет собой кристаллическое вещество с кристаллами в форме призм и имеет следующие физические характеристики: С, (мол. вес 380.19): т. пл. 104-106°С; (в метиловом спирте). Аналогично получают следующие соеди нения: 4-ацетокси-3-бромметил 1О-К1етилен-8-метокси--2,9-диоксатрицикло-(4.3, -декан: С, кН. 0„В4 (мол. вес 333.2): С Н Id 17 5 20 т. пл. 101-102 C:Mjj + 8О (в метилоBOM спирте); 4-ааетокси-3-хлорметил-10-метилен-8-метокси-2.9-ДиоксатрИцикло-(4.3,1.0 (мол. вес 288,74) -декан: С „Н.„0„С о т. пл. 9О-91°С: Ид + 8l (в метиловом спирте): 4-ацетокси-3-раданометил-10-метилеН - 8-метокси-2,9 диоксатрицикло-( 4.3.1.СГ -декан со следующими физическими констан(мол, вес 311,34): тами: С. ао .„о . т. пл, 118-12О°С: в тиловом спирте). Т}рк замене метилового спирта другими спиртами, например этиловым, цропиловым, бутиловым или бензиловым, можно получить соответствующие 4-ацетокси-3-галогенметил-10-метилен- 8- алкокси (или арилалкокси)-2,9-ди(Жсатрицикло-( 4, .) -деканы. П р и м е р 2. Получение 4-окси-З-метИл-10-метилен-8-метокси-2 9--Дйок атрицикло-(4,3,1,О- )-декана, К суспензии OrО8 г никеля Ренея в 2О мл метилового спирта прибавляют раствор 0.7 г 3 -ацетокси-3-йодметил-1О-метилен-8-метокси-2,9-ДИОксатриЦикло-( 4.3,1,0 -дeкaнa, полученного аналогично при- меру 1, в 2О мл метилового спирта, содержащего 0,5 мл диэтиламина, и приготовленную смесь ,при встряхивании при комнатной температуре и атмосферном давлении гядрируют в течение 9О мин одни экБиралекгом гюдорода. После фильтрованна з, через асбест фильтрат упаривают до сухого состояния и полученный остаток экстрагируют хлороформом. Из промытого водой хлороформного экстракта поеле его сушки над сернокислым магнием и упаривагчя в вакууме (при 5О С/7 мм рт. ст.) получают р,426 г 4 -ацетоксй З-метил-1О-метилен-8- метокси-2.9-)Е оксатрицикло-( 4,3,1, )-декана в бесцветного маслообразного продукта, ьыход 9О.% от теоретического. Непосредственно после этого маслообразнь1й продсгкт растворякхг в 25 мл метилового спирта JJ полученный раствор смешивают с 5 мл 1 н. раствора гидроокиси натрия. После выдерживания в течение 1 часа п комнатной температуре смесь разбавяяют войой„ после чего производят экстрагирсшайие этиловым эфиром уксусной кислоты. Из -нейтрализованного и высушенного над сернокислым магнием раствора продукта в этиловом эфире уксусной кислоты после ynaj iBaHHH в вакууме Ьри 5О С/7 мм рт. ст.) получают 0.292 г 4 -окси- 3-метвл-1 О метилен-8-метокси-. -2,9-диоксатрииикпо--(4,3.1,0 )-декана в яиде бесцветйого маслообразного продукта: С .j.. (мол. вес 212,2а): of 42° (в метиловом спирте) 1.5096. Пример 3. Получение 4-окси-З-метиЛ 10-метилен- 8- апкокси- 2,9-диoкcaтpициклo-(4.3.1,O )-деканов при использовании 1- j3 -В-глюкозидо-4-изовалероксиметил-6.7-Диокси- 7-метил-1,4 а, 5.6,7,7 а- , -гексагйдроциклояента с)пирана. 1 Г 2- jS -I -гл oкoзидo-4-изoвaлepoкcи.мeтил-6,7 Яиокс:и-7-метил-1, 4а, 5.6,7.7 агексагидроышслеттента(с)пирана раствсфяют в 20 мЛ спирта и приготовленный раствор смешивают с 5О мг а -толуолсульфокислотЫ. После кратковременного нагревания при 40®С реакаиояйую смесь разбевляют водой, затем нейтрализуют кислым углекисль1м натрием, после чего экстрагируют этиловым эфиром уксусной кислоты, рбъединеиные экстракты сушат над сернокислым натрием. После упаривания в вакууме получают окрашенное в светло-коричневый цвет маслообразное вещество, которе подвергают очистке с помощью препаративной хроматографии в тонком слое на пластинках с силикагвлем. Элюй{5уюшая смесь состоит из 24 ч. этилового эфира уксусной кислоты, 60 ч. н -гексна я 6 ч, н-пропилового спирта. При бэльишх количествах очистку проводят на хроматографической колонке, заполненной окисью алюминия, при использовании в качестве элюируюшей смеси диэтилового эфире (соответственно посредством пе регсинки в вакууме). В завнсимости от исходного спирта формулы 3 попуч ают следующие соединения: - гокси-З-метил-10-метилен-В метокси-2.б -диоксатрицикло- 4,3.1,о )-аекан: . С, ;Н. „О. (мол. вес 212,25);ВДп% 42 И 1о 420 (в метиловом спирте); KU 1,5О96: 4-окси 3-метил-10- метилен-&-этокси-2.9-ДИ Жс п иаикло(413,1.0 )екан: С -Н дО (мол, вес 226,28) + 55 50 (в метиловом спирте); rtj 1,4983; 4-сжси-Зг-метип-10-метилен-8-(н-буГ си)-2.9-йиоксатрицнкло-( 4.3,1, )-декан С„ . ( мол. вес 254.33): j 14 22 430 ( 39 (в метиловом спирте);K,j 1,49О №:хоаный 1- |J -Bгглt6кoэидo-4-изoвaлёpиoKcвiмeтtш-6 ,7 диокси-7-метил- 1, 4а, 5, 6,7, 7 гексагидроциклсшента(с)лиран полуHcaot слёяукнцим способом, 6 Kf И0к1еяьчешш1х кЬрней к риэомЦгиSMitno. Щ €&вАИ тщательно нерколируют в пёрколяФсфе снаяала н-гексаном при добавленви 1% уксусной кислоты. Первый перкодат выбрасывают. Непосредственно после этого noBtqpHyro перколяцию смесью хлороформа я метилового спирта, взятыми соотношении 5t2. Перколят нем «Horcv упаривают и затем три раза промывают ьоаой. 1.сяользуй для каждойпромывки поЮ Л. Органическую фазу отбрасывают, а водную фазу после насыщения сернокислым аммонием четыре раза экстрагируют атйлшмм уксусной кислоты, исполь я для каждой экстракции по 5 л. Затем эфирную фазу сушат над серйокисjiuM магнием И непосредственно после этого упаривают до получения сухого остатка. Полный вес остатка 199 г или 3.31% в расчете на вес сухого растительного сырья . Фракцию, состоящую в основном из растворимых в воде эфироглюкозидов, для дальнейшей очистки подвергают хроматографированиЮ на колонке: Ю г остатка, полуHeHHWo после упаривания этилового эфира уксусной кислоты, растворяют примерно в loo мл влажного этилового эфира уксусной кислоты и после выдерживания в течение 1 часа отфильтровывают нерастворимые составные части. Фильтрат вводят В заполненную 250 г силикагздя колонку (размер частиц 0.2 - 0,5 мм). Проводят взмучивание Силикагеля, а затем элюируют сначала влажным этиловым эфиром уксусной кислоты, после чего элюирование продолжают этиловым эфиром уксусной кислоты при добавлении метилового спирта, Собирают фракции по 1ОО мл, 1- р -Б-глю кпзидо-4-изовалероксиметил-6,7-Диокси-7-метил-1. 4а, 5,6.7,7 а-гекс аги дроцикл опента(с)пиран находится в фракциях 17-27. Суммарно из этих фракций выделяют после упаривания 3,65 г глюкозида в виде аморс} юго порошка, жрашенного в желтоватый цвет, .. . Формула изобретения 1. Способ получения 8-производных-4-окси- 3-метил-1 (-м- илен- 2,9-диокс атрииикло-(4.3,1.О )-декана общей формулы 1: : в которой {J - алкоксигруппа с 1-4 атомами углерода или бензилоксигруппа, т ли чаю щ и и с я тем, что циклоента(с)пиран общей формулы 2,в которой X - ацилоксигруппа: Е - ацилоксигруппа или 6 -D-глюкоидная группа; f} - атом водорода или галогена или оданогруппа; - атом водорода или ацил, о подвергают взаимодействию со спиртом бшей формулы 5R - ОН , где ff имеет указанные значения, в кислой среде и выделяют целевой про дукт или образующийся промежуточный про дукт обще0 формулы 4г: СЯз-й, -- ; где .имеет указанные значение, - втом гадогена или родано. / .б ..- , группа и Р ацнл. - /: л,- ; ,-.- . . переводят в ; -н 4е п1л лройзврдное каталитическвц Г1шр) эквивалентным когшиествоц врдорсрз е присучхгтвии органа еокш о есцован)1Я например диэтнламина, за «мЬ1а5шт ашшЫ1ук группу и выделяют пвлевс продукт известшь{мн приемами. 2. Способ по п. 1, q т л и чаю щ и и с я тем, «гто соединение формулы 2 яодаергюот азанмоДеЙствик) со спиртом формулы 3 в н| йсутствии соляной кислоты, t -топуопсульфокиспоты или кислоты Льюиса., 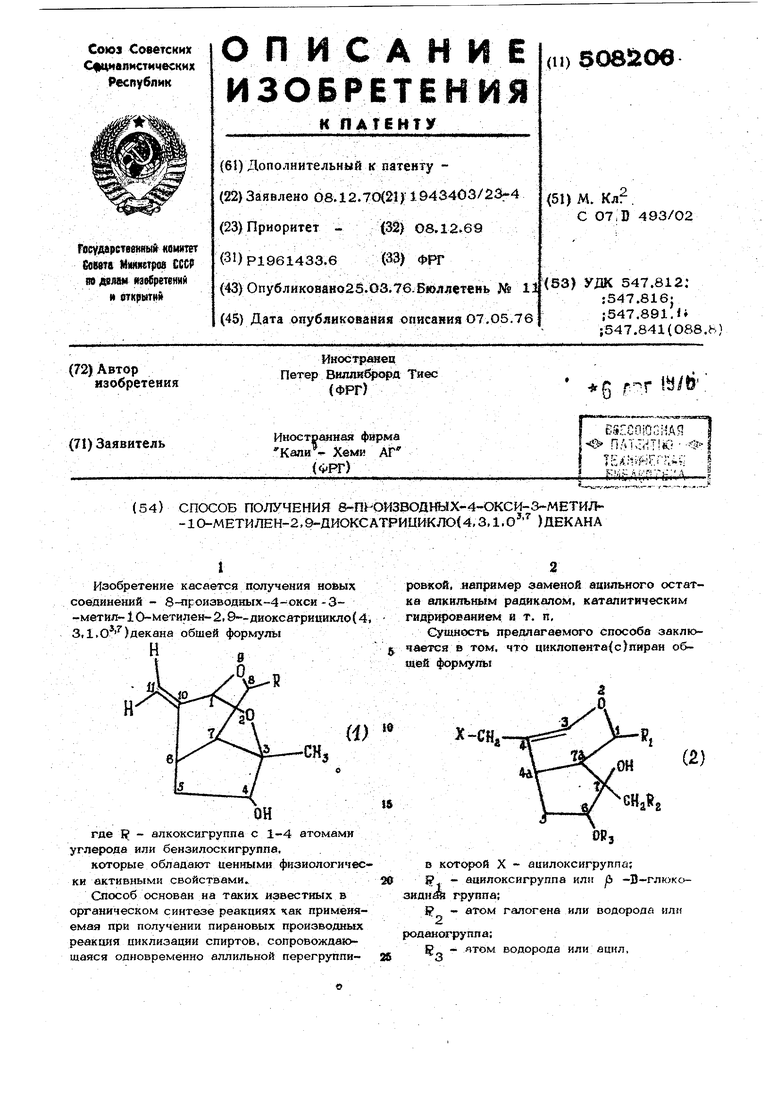




Авторы
Даты
1976-03-25—Публикация
1970-12-08—Подача