(54) СПОСОБ ПОЛУЧЕНИЯ 2а - ДВУОКИСЕЙ 2,13БЕНЗОТИАДЙАЗИН-4-ОНА
результатов, а при более низкой температуре, например при 25°С, происходит только незначительная циклизация.
В качестве исходных сс даиений формулы П предпочтительны следующие о супьфамидобензойные кислоты: N - метил - N - этил, N - и - пропил, N - н - бутил, N изобутил, N - изопропил-, N трет - бутил-, N - шклогексил-, N - циклопентил-, N циклооктнл N - о - карбоксифенил сульфамид.
Проводят циклизацию при максимальной температуре , предпочтительно от -20 до- -25С, F частности от -6 до ШС, ..од давлением или без давления, прерьшно или непрерывно.
В качестве основания употребляют двузамещенный у атома азота амид к боновой кислоты или третичный амин, предпочтительно в количестве 5-25 вес.% в пересчете иа фосген. Для циклизаида употребляют и CMeoi указанных оснований. Предпочтительными основаниями являются: триметиламин, триэтиламин, пиридин, N - диметиланилин, N - дизтила1шлин, N - зтилпиперидин, N - метилпирролидин, а -, /3 - и 7 пиколин, N - пропилпиперидин, хинолин, изохинолин, хиназолин, хиноксаяин, т|жамиламин, три - н - бутиламин, и - пропилдиизопропиламин, трифурфуриламин, тригексиламин, N метили ми дазол, N - метилпиррол, N - диметилШ клогексиламин, пиримидин, акридин; диметилф(мамид диэтилформамид, N - метиланилид муравиной кислоты, N,N - диметилацетамид - N - метилпирролидон.
Целесообразно проводить циклизацию в присутствии растворителей. Предпочитают растворнтели с датольньпм моментом выше 1,2. В качестве растворителей используют галоидированные углеводороды, как метиленхло1жд, 1,1-- и 1,2 - дихлорэтан, 1,2 цис дихлорэтилен, н - бутилхлорид, 2 -, 3 - и изобутилхлорид, хлорбензол, бромбензол, йодбензол, о - им - дихлорбензол, о -, м дибромбензол, о -t м , п хлортолуол, 1,2,4 трихлорбензол, хлор - 1,3,5 триметилбензол, 1,10 дн омдекан, 1,4 дабромбутан; N, N - двузамещгнныв амиды карбоновой кислоты, как днметилформамид; кетоны, как ацетон, адэтофенон, цнклопентанон, инклогексанон; сложные эфиры, как метилацетат, изоёутяладетат, сложный метиловый эфир бензойной кислоты, фенилацетат; «ктроуглеводороды, как нитрометан, нитрозтан, нитробензол, о -, м -, п хлорнктробензол, о шггротхшуол; , как ацетонитрил, беюовитрвл, fn хлорбензоннт жл; третичные амины, как пирндан. N димепищиклогексиламин, N диметяящоишн, а -, /3 , 7 пиколин; хннолин, изохинолкн, пирнмиднн или соответственные смесн. Ис. 1гомьзуют также и смеси растворителей, |га1фнмер кет(жов, с ароматическими или алифатическими углеводорода1«1, шш{Н1мер ацетон и толуол или лигроин или хлорбензол и ацетон. В соответствующем случае могут быть использованы и пошфные растворители j дапальным моментом выше 1, например хлороформ. Полярный растворитель целесообразно использовать в количестве 250-400 вес.% в пересчете на исходное соединение. Часто вьподно употреблять основание одновременно и в качестве растворителя для образования реакционной среды, причем соответственно повышают количество основания.
Проводят реакцию следующим образом. Смесь исходного соединения обшей формулы 11,. фосгена, основа1шя и, в соответствующем случае, растворителя выдер:нкивают в течение 8-16 час при реакционной температуре. Затем удаляют растворитель и избыточный фосген и из остатка вьщеляют конечный продукт известным образом, например растворе1шем в одном из указанных растворителей, осаждением путем прибавления воды и фильтрацией. Можно и экстрагировать реакционную смесь натровым щелоком, в соответствующем случае после отделения избыточного фосгена
н/или части растворителя подкислять отделенную щелочную фазу н отфильтровьшать образовавшийся конечный продз ст.
Можно получать исходное соединение формулы 11 любым известным способом и проводить
циклизацию в реакционной смеси, не отделяя образоваршегося исходного соединения формулы П.
Получают исходное соединение формулы 11 предпочтительно следующим образом. Сначала подвергают антраниловую кислот шш одну из ее солей
реакции взаимодействия с галогенангидридом сульфаминовой кислоты, в частности с хлоранпщридом
обшей формулыX
IR-NH-SO И/
в которой R имеет указанные значения н X представляет собой галогенный атом, в присутствии полярного органического растворителя при 15-40° С.
11редпочитаемыми соединениями формулы 1П
являются те, в структурах которых символ R имеет значения и X обозначает атом брома или, в частности, атом хлора. Целесообразно проводить реакщ{ю взаимодействия при 15-25° С в присутствии указанных полярных, органическнх растворителей с
дапольным моментом выше 1,2 или указанных смесей растворттелей и в присутствии двузамещенного амида карбоновой кислоты или третиоюго амина, особенно одного из указанных оснований. По окончании этой первой реаКцнй прибавляют
фосген и в соответственном случае основание н предлагаемым способом доводят циклизацию. Пример.
А. Перемешивая, при температуре - 15С прибавляют 2S вес.ч. фосгена к суспензии.51,7 вес.ч. N изопропил - N - (о карбокси) - фенилсульфа1«шда в 190 вес. ч. хлороформа и 5,2 вес.ч. диметилформамида. Перемешивают смесь 14 час прн 5-8°С. После отделения избыточного фосгена и хлороформа растворяют маслянистый остаток в Швее. ч.
ацетона н прибавлением 250 вес. ч. воды выкрнсталлизовьшают его. Получают 41,8 части (87% от теоретического) 2,2 - двуокиси 3 - изопропил-2,1,3 бензотиадиазин - 4 она; т.пл. 125-129°С.
Б. При употреблении смеси растворителей из 87 вес. Ч- толуола.и 33 вес. ч. ацетона и 2,62 вес. ч. диметилформамида получают по примеру 1А; выход 91% от теоретического конечного продукта формулы Г; Т.Ш1. 125-129° С.
П р и м е р 2. Перемешивая, при -20°С 14,5 вес.ч. фосгена прибавляют к суспензии 25,8 вес.ч. N - изопропил - N - (о - карбокси) фенилсульфамида в 43 вес. ч. толуола, 16 вес. ч. ацетона в 6,1 вес. ч. N - диметиланилина. Перемешивают.смесь 14 час при комнатной температуре.
Затем концентрируют раствор, растворяют его в 100 вес ч. натриевого щелока (10 вес. %) и фильтруют. Подкисляют щелочную фазу и отсасьшают осадок. Получают 20 вес. ч. (83% от теоретического) 2,2 - двуокиси 3 - изопропил - 2,1,3 - бензотиадиазин-4-она; т.пл. 129-131°С.
ПримерЗ.
А. Интенсивно перемешивая, при 15° С через подведенные трубы медленно прибавляют в течение 1 час 4,68 вес. ч. хлоранй1Дрвда 4 - изопропилсульфаминовой кислоты и 3,78 вес. ч. диметилциклогексиламина к суспензии 3,62 вес. ч. антршшловой кислоты в 18,2 вес. ч. хлорбензола и 2,54 вес. ч. aujeTOHa. Выдерживают смесь 1 час 20° С. Добавляют 0,230 вес. ч. диметялфс мамнда и затем добавляют в течение 6 час. 3,9 вес. ч.
при -6°С. Перемешивают смесь 9 час при -6°С и 4 час при 20° С. Затем отсасьтают избыточный фосген и ацетон при 30° С и под давлением 80 торр. После этого экстрагируют раствор смесью 3,8 вес. ч. гидроокиси натрия и 54 вес. ч. воды, k отделенной щелочной фазе, перемешивая, добавляют 26 вес. ч. соляной кислоты (13вес.%), фильтруют и сушат остаток от фильтрации.
- Получают 4,94 вес.ч. (78% от теоретшшского) 2,2 - двуокиси 3 - изопропил 2,1,3 - бензотиадиазин-4-она; т.ш1. 124-130 °С.
Б. По примеру 3 А можно без ущерба отказаться от экстракции оргайической фазы натровым щелоком. Если удаляю фисген и растворитель н перемешивают остаток с 80 вес. ч. воды, то растворяется образовавшийся шдрохлорид диметилдаклогексиламина, в то время как одновременно осаждается 2,2 - двуокись 3 - изопропил - 2,1 - 3 бензотиадиазин - 4 - она примерно 97%-ной чистоты.
Получают 4,83 вес.ч. (76% от теоретического конечного продукта формулы I).
В. По примеру ЗА проводят реакцию взаимодействия ври 15-20°С. Получают тот же самый выход конечного продукта,
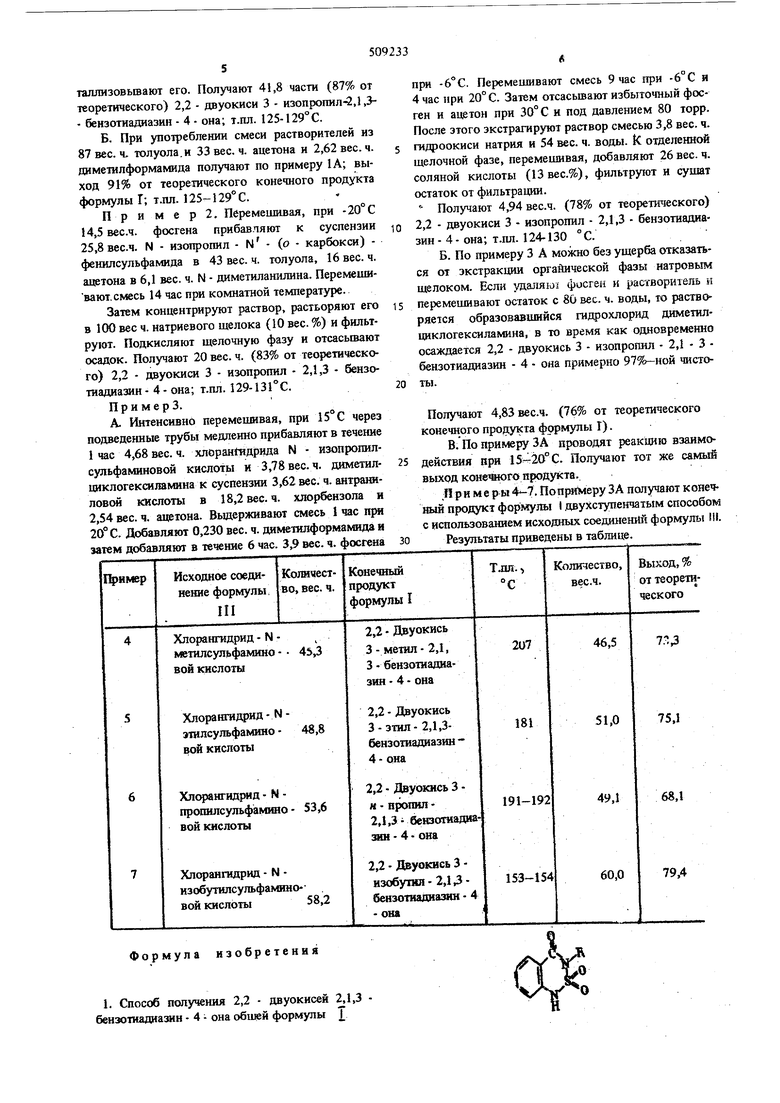
Я р и меры 4-7. По примеру ЗА получают к онечный продукт формулы I .двухступенчатым способом с использованием исходных соединений формулы 111. Результаты приведены в таблице.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 2,1,3-тиадиазин-4-он-2,2-диоксида | 1978 |
|
SU715021A3 |
| Способ получения двуокисей 1-циано- 2,1,3-бЕНзОТиАдиАзиН-4-OHA-2,2 | 1979 |
|
SU843747A3 |
| Гербицидное средство | 1974 |
|
SU688106A3 |
| Способ получения 2,2двуокисей 2,1,3- бензотиадиазин4-она | 1974 |
|
SU514571A3 |
| Способ одновременного получения 1,3-дизамещенных мочевин и 1,2-диолов | 1978 |
|
SU856379A3 |
| Гербицидная композиция | 1975 |
|
SU603316A3 |
| Способ выделения 3-изопропил-2,1,3-бензотиадиазин-4-он-2,2-двуокиси | 1982 |
|
SU1261565A3 |
| Способ получения галогеналкиламиносульфонилгалогенидов | 1975 |
|
SU604483A3 |
| Гербицидный состав | 1977 |
|
SU710498A3 |
| Гербицидное средство | 1974 |
|
SU540550A3 |

Формула изобретения
гбе R - низший 8ЛКИЛ с t-6 атомами углерода, окклоалкил с S-8 атомами углерода, путем Шпслизлшт о супьфамвдобензойных кислот в п|жсутCTBmt 1Шклиэую1Х1его агента, отличагоши ся мм, что. с целью повышения выхода и чистоть овлевого продукта, о сульфамвдобенэойную кясitory обшей формулы И
-сош
rjae И - имеет указанные значения, подвергают цикяалавл я присутствия фосгена я дизюмещенного у
атома азота амида карбоновой Ю1слоты и/шш третичного амина при температуре от -20°до- -50С.
качестве органического растворителя.
до-|-251. 

Авторы
Даты
1976-03-30—Публикация
1972-02-07—Подача