тилтриптофан (2), ацетилтирозин (3), ацетилглутамин (4). Биологическое дейотние предлагаемых соединений сравнивали с андростаназолом.
Испытываемые стероиды в дозе 2 мкм в спиртово-масляном растворе вводили подкожно крысам, «астрированным .в 30-дневном .возрасте (.вес 55-60 г), на протяжении 9 дней, начиная с 21-го дня .после орхидэ.ктомии. Спустя 22-24 ч после девятой инъекции жи.вотных декапитирО:Вали, извлекали т. levator ani вентральную долю предстательной железы, семенные пузырьки и устанавливали их вес iB мг. Аидрогенная активность определялась по реакции семенных пузырьков и вентральной доли предстательной железы на введение вещества; анаболическая миотропная- по реакции т. levator ani. Андрогенная и анаболическая активность N-ацилпроизводных стероидопиразолов
Анаболичеокий индекс вычисляли по формуле:
Вес т. levator ani подопытных крыс - Вес т. levator ani контрольных. Вес семейных пузырьков подопытных крыс - вес сел:снных пхзырьков контрольных крыс.
Контролем служили крысы того же веса, кастрированные в те же сроки и находившиеся в тех же усло.виях, что и по-допытные живетные, но получавшие лишь раст1БОритель в том же объеме 0,4 мл.
Результаты исследова-ния приведены в табл. 1, где PI-для разницы между данными опыта
и контроля;
Ро - для разницы между данными под влиянием андростаназола и исследуемыми соединениями.
Таблица t 

| название | год | авторы | номер документа |
|---|---|---|---|
| СТЕРОИДНЫЕ ЭФИРЫ N-ДИ(2-ХЛОР-ЭТИЛ)-АМИНОФЕНИЛ-N-АЦЕТИЛАЛАНИНА, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ, АНДРОГЕННОЙ И АНАБОЛИЧЕСКОЙ АКТИВНОСТЬЮ | 1984 |
|
SU1266111A1 |
| СОЕДИНЕНИЯ SARM И СПОСОБЫ ИХ ПРИМЕНЕНИЯ | 2011 |
|
RU2571421C2 |
| В ПФОНД а^а^лгп1и^ | 1973 |
|
SU404235A1 |
| Способ получения -галогеноалкил -нитрозокарбаматов или галогеноалкил- -нитрозоаллофанатов стероидных соединений | 1974 |
|
SU512714A3 |
| Способ получения производных триаминоандростана,их солей или четвертичных аммониевых солей | 1976 |
|
SU967276A3 |
| СПОСОБ ПОЛУЧЕПИЯ17а-(БУТИНЕНИЛ-1,3)-17р- | 1971 |
|
SU320486A1 |
| 17α-АЦЕТОКСИ-3β-ФЕНИЛПРОПИОНИЛОКСИ-6-МЕТИЛПРЕГНА-4,6-ДИЕН-20-ОН, ОБЛАДАЮЩИЙ ГЕСТАГЕННОЙ АКТИВНОСТЬЮ, И ЛЕКАРСТВЕННОЕ СРЕДСТВО НА ЕГО ОСНОВЕ | 2001 |
|
RU2200165C1 |
| Способ получения 9 - метилстероидов | 1971 |
|
SU493962A3 |
| ПРИМЕНЕНИЕ ГЕТЕРОЦИКЛИЧЕСКИХ ГИДРАЗОНОВ В КАЧЕСТВЕ СРЕДСТВ, ОБЛАДАЮЩИХ АНТИГЛИКИРУЮЩЕЙ АКТИВНОСТЬЮ | 2016 |
|
RU2658819C2 |
| Способ получения 9 -метилстероидов | 1971 |
|
SU488405A3 |

Из полученных данных следует, что по анаболическому действию Ы-ацетилтирозин17а-метил-17-р - оксиандростано (3,2-с) пиразол и N-aцeтил:глyтaмин-ди- 17a - .метил-17роксиандростано (3,2-с) пиразол почти соот.ветствуют андростаназолу. N-ацетилфенилаланин-17о-;метил-17|3 - аксиандро.стано (3,2-.с) пиразол и Н-ацетилтриптофан-17а-;метил-17роксиандростано (3,2-с) лиразол обладают более высо.кой анаболической активностью. После их введения вес мышцы увеличен отчетливее, чем после андростаназола. Андрогенные свойства указанных соединений ниже, чем у андростана.зола и только N-а.цетилфенилаланин-17а-метил-17(3 - оксиандростано (3,2-с) пиразол отличается |более выраженным андрогенным действием. Однако, несмотря на то, что для К-ацетилфенилаланин-17а-метил-17|3оксиандростано (3,2-с) лиразола андрогенная активность выше, чем для андростаназола, по анаболическому действию он значительно .превосходит последний. Таким образом, анаболические индексы предлагаемых веществ составляют; N-ацетилфенилаланин-17а-метил - 17|3 - оксиандростано (3,2-с) пиразола (1) 0,68, N-ацетилтриптофан-17а-метил-17|3-оксиандростано (3,2-с) пиразола (2) 1,44, М-ацетилтирозин-17а-метил17|3-о,ксиа«дростано (3,2-с) пиразола (3) 1,17 и М-а|Цетилглютамин-ди- 17а-метил-17р-о«сиандростано (3,2-с) пиразола (4) 1,28. Токсичность заявленных веществ изучалась в острых опытах на мышах-самцах весом 18-22 г. Заявленные вещества и андростаназол в спиртово-масляном растворе вводились внутримышечно. Контрольные животные получали лишь растворитель в том же объеме. Наблюдения за 1животными проводились ,в течение 30 дней. Данные этих исследований приведены в табл. 2. Таблица 2 Токсичность N-ацилпроизводных стероидопиразолов в острых опытах на мышах Вещество ЛДзо, лг/кг Ы-Ацетилфеннлалаиии-17 а-метлл-17/З-окспаидростано (3,2-с) пиразол8100 К-Ацетплтриитофан-17 «-метил-17/3-оксиандростано (3,2-с) пиразолj2500 N-Aцeтилтиpoзин-17 а-метил-17 /3- -апдростаио (3,2-с) пиразол3000 N-Ацетилглутамин-ди 17 а-метил-17 ;3-оксиандростаио (3,2-с) пиразол 1650 Андростаиазол3700 Для андростаназола ЛДао, вычисленная по методу Личфельда и Уилкоксона, составляет 3700 мг1кг. Как видно из табл. 2, токсичность всей предлагаемой группы соединений весьма незначительна. Кроме того, если учесть, что применяе|Мые в клинике дозы для андростаназола - 0,1-0,5 веса, а курс лечения длится обычно около .месяца, то их .можно считать практически нетоксичными. Синтез предлагаемых биологически активных стероидов был осуществлен взаимодействием 2-оксиметилен-17а - метилдигидротестостерона с соответствующими гидразидами: N-апетилфенилалаиина, N-ацетилтриптофана, N-ацетилтирозина, N-ацетилглютаминовой кислоты, с последующей дегратацией полученного 3-гидразона путем нагревания при 150-160° С, при 5-7 мм рт. ст. в течение 5 ч. Примеры получения М-ацилпроизводных 17а-метил-17р-окси-5а-андростано (3,2,-с) пиразолов фор.мулы I. Пример 1. Ы-а.цетилфенилалапин-17а.метил-17р-оксиандростано (3,2-с) пиразол. 2 г оксиметилен - 17а - метилдигидротестостерона и 1,6 г гидразида N-а.цетилфенилаланина (т. пл. 167° С) растворяют в 20 мл метилового спирта и кипятят с обратным холодильником 5 ч. Охлажденный раствор разбавляют 300 мл насыщенного раствора NaCl и оставляют стоять до следующего дня. Затем осадок нагревают с э.фиром (30 мл) в течение 15 мин, отфильтровывают, промывают несколько раз эфиром. Выделяют 3,2 г 3(Nа.цетилфенилаланин) гидразон-2-оксиметиле.н17а-метил-17|3-оксиандростана с т. пл. 125- 127° С. ИК-снектр: 3400, 3310, 1680, 1550, 1350 слг-. Я.макс. 232-234 н.м. 2,89 г полученного 3гидразона нагревают 6 ч при температуре масляной бани 140-150° С при 5-7 мм рт. ст. После дегидратации выделяют 2,63 г (95,9% от теоретического) N-ацетилфенилаланин17а-метил-17р-оксиандростаио (3,2-с) пиразола с т. пл. 137-139° С. ИК-спектр: 3420, 3300, 1730, 1670, 1590, 1550, 1450 слг-. Хмак. 230-234 им. Пайдено, %: N 8,67; Вычислено, %: N 8,12. Пример 2. N-ацетилтриптофан-Па-метил-17|3-о.ксиандростано (3,2-с) пиразол 1,06 г 2-оксиметилвн-17а-.метилдигидротестостерона, 1 г гидразида Ы-ацетилтриптофана, 20 мл метилового спирта обрабатывают аналогично примеру 1. Выделяют 1,62 г 3(Nацетилтриптофап) гидразон - 2 -оксиметилен17а-метил-17 5-оксиандростана с т. пл. 163- 165° С. ИК-спектр: 3430, 3320, 1670, 1600, 1530, 1505, 1460, 1245, 1010, 920 см. Хмакс. 278-280 нм. После нагревания в вакууме 1,6 г полученного гидразона выделяют 1,54 г N-ацетилтри.птофан - 17а - метил - 17р -оксиандростано (3,2-с) пиразола (99,3%) т. пл. 174-178°. ИК-спектр: 3420, 1670, 1600, 1530, 1470, 1450, 1350, 1020, 920 см . 7.чакс. 270-280 нм. Найдено, %: N 10,63. Вычислено, %: N 10,035. Пример 3. Ы-ацетилтирозип-17а-метил17р-оксиандростано (3,2-с) пиразол. Смесь 1,16 2-оксИМетилен-17а-метилгидротестостерона, 1 г гидразида N-ацетилтирозина, 20 мл .метилового спирта нагревают в течение 5 ч. После аналогичной обработки выделено 2,00 г 3-гидразона с т. пл. 168-173° С. ИК-спектр: 3500, 3400, 3320, 1660, 1525, 1355 с.и-. .„ак-с- 227 нм. Из 1,67 г 3-гидразона после дегидратации в вакууме при 140-150° С получено 1,58 г М-ацетилтирозин-17а - метил-17р - оксиандростано (3,2-с) пирозала (98,1% теорет.) с т. пл. 174-178° С.
ИК-спектр: 3430, 3300, 1730, 1670, 1600, 1480, 1453, 1355 cлt-.
чако- 226-227 НМ.
Найдено, %: N 8,22.
Вычислено, %: N 7,688.
Пример 4. N-a;ueTH.firjyTaMHH-6«c- 17аметил-Пр-сксиандростано (3,2-.с) пиразол.
Из 1,3 г 2-оксиметилен-17а-метилдигидротестостерона, 1 г дигидразида N-ацетилглутаминовой кислоты и 20 мл метилового спирта в анало.гичных условиях выделено 1,840 г 3-(К -ацетилглутамнн)-бис-(гидразон-2 - оксиметилен - 17а-метил-17р - оксиандростана) с т. .пл. 170-172° С.
ИК-спектр: 3400, 3300, 1675, 1540, 1356 с.иИз 1,59 г 3-гидразона после дегидратации получено 1,460 г К -ацетилглутамин-бцс- 17аметил-17|3-0ксиандр0стано (3,2-с) пиразола (94,2% теорет.) с т. пл. 194-200° С.
ИК-спектр: 3430, 3300, 2670, 1550, 1460, 1350 см-.
А макс- 234-236 НМ.
Найдено, %: N 8,9. вычислено, %: N 9,1.
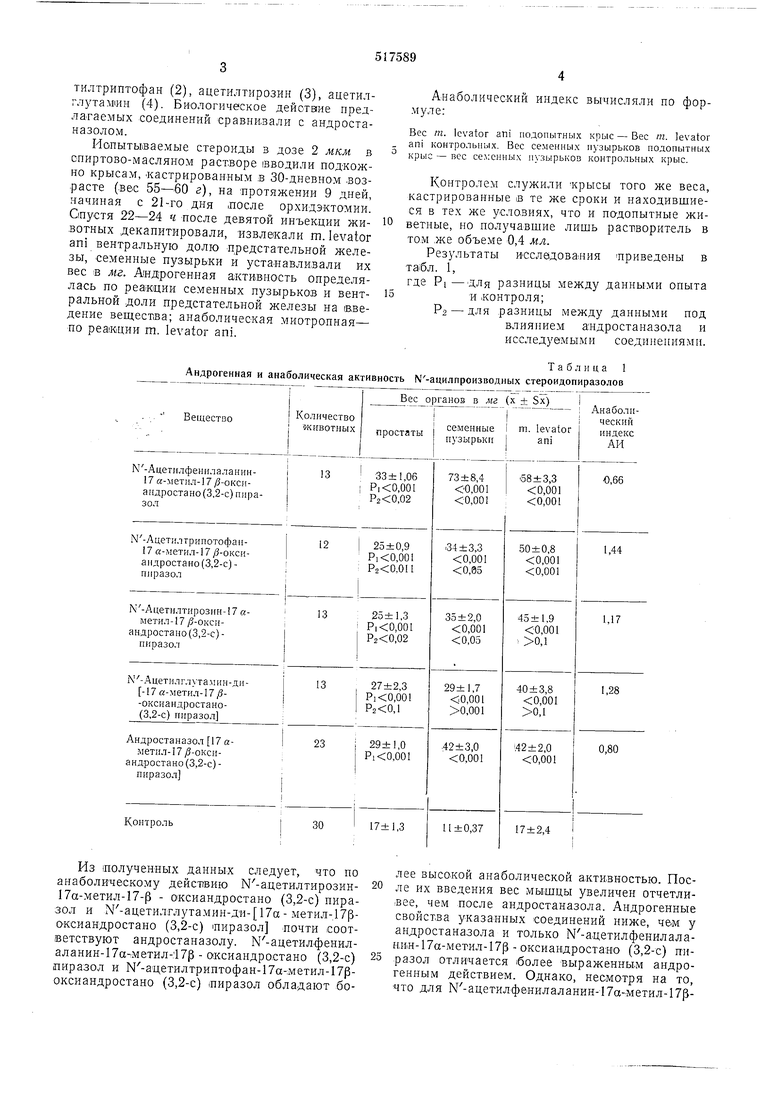
Формула изобретения
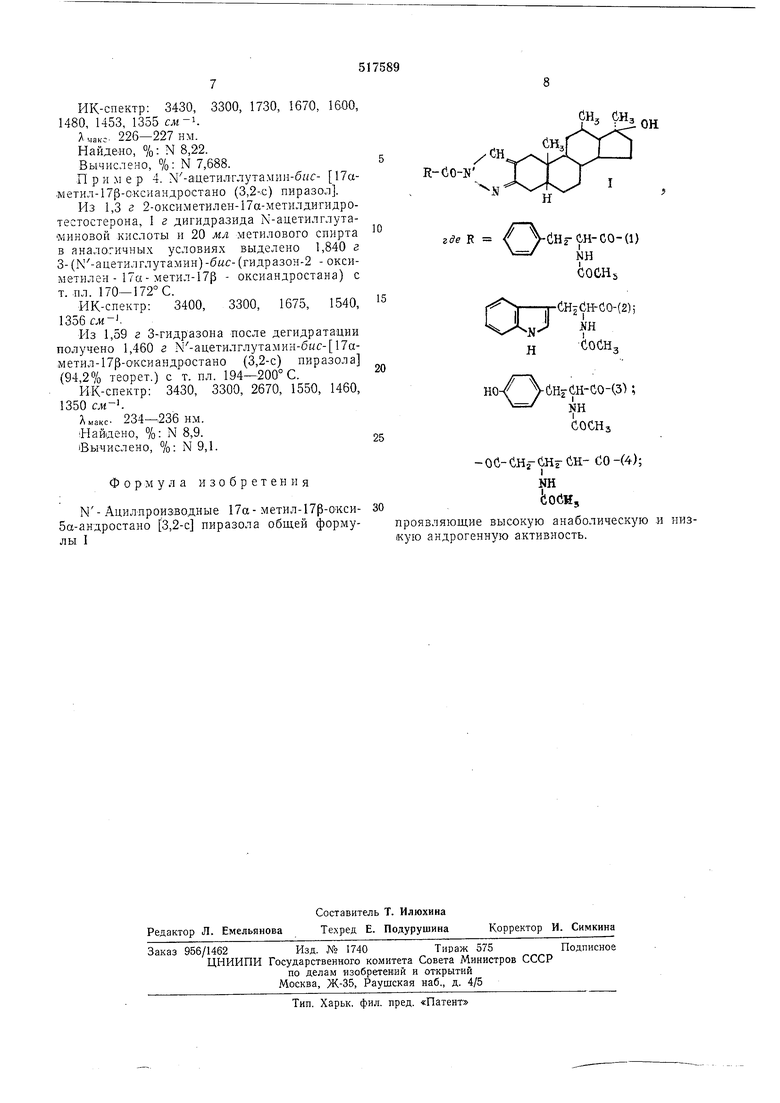
N-Ацилпроизводные 17а-метил-17р-окси- 30 5а-андростано 3,2-с пиразола общей формулы I
СНз (Нзо
CO-JJ
-СНгС-Н-СО-Ц)
где F NH COCHs
11 11 CH2CH-GO-(2)i
.j,J т
COCHg
бнгсн-сочз);
СОСНз
- ос- CHj- СНГ СН- со -(4); NH (10СНз
проявляющие высокую анаболическую и низкую андрогенную активность.
Авторы
Даты
1976-06-15—Публикация
1973-12-10—Подача