1
Предлагается способ получения новых соединений, которые могут найти применение в медицине.
В литературе широко известны методы дегидратации в кислой среде о
Целью изобретения является разработка способа получения новых производных пиперидина, обладающих фармакологической активностью.
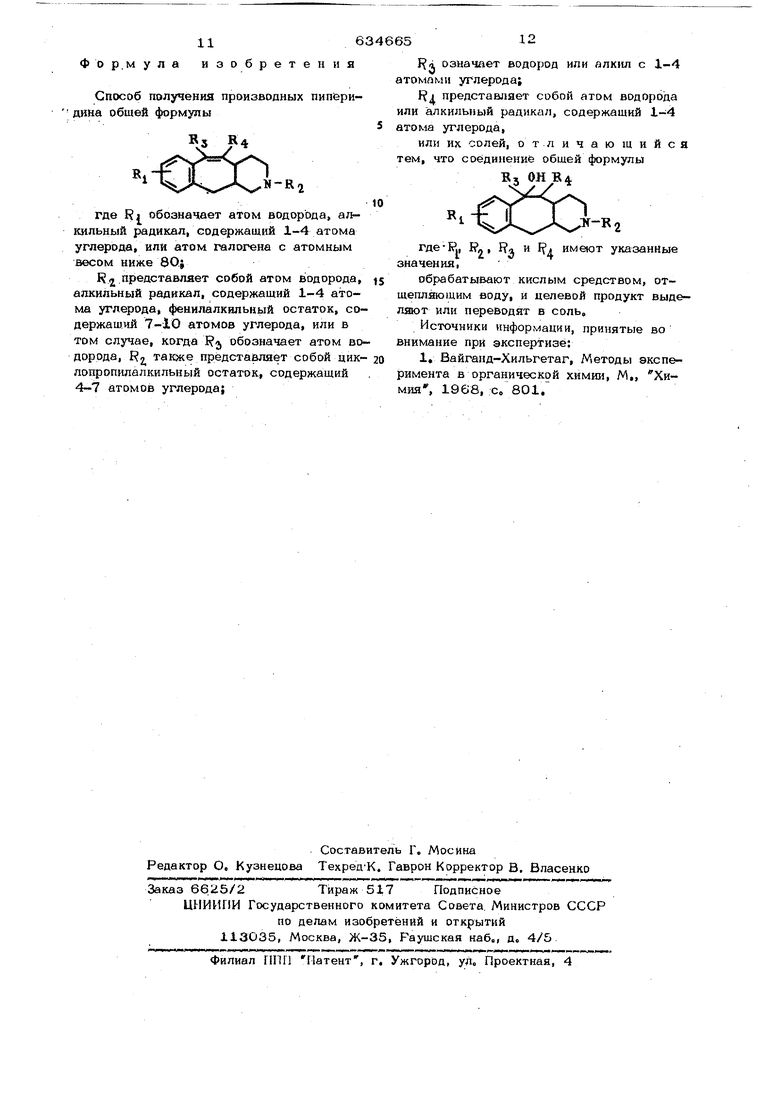
Предлагаемый способ получения произ- водных пиперидина общей формулы
том случае, когда обозначает атом водорода, R также представляет собой циклопропилалкильный остаток, содержащий 4-7 атомов углерода,
означает водород или алкил с 1-4 атомами углерода;
- атом водорода или алкильпый радикал, содержащий 1т-4 атома углерода.
Способ заключается в том, что соединение общей формулы
Rj ОН R4 б циклогепта Г1,2-с пиридин-6-ола в 30 мл концентрированной соляной кислоты и ЗО мл воды нагревали в течение 15 мин при тем пературе кипения с обратным холодильником. Затем реакционную смесь охлаждают, разбавляют ее 2ОО мл воды и подщелачивают (рН 14), прибавляя 2О %-ный раствор гидроокиси натрия Выделившийся в осадок маслообразный продукт экстрагируют хлористым метиленом, органическую фазу промывают водой до нейтральной реакции промывных вод, сушат над сернокислым натрием и затем упаривают. Полученный в результате этого маслообразный остаток растворяют в 2О мл этилового спирта, полученный раствор смешивают с раствором, содержащим 6,0 г фумаровой кислоты в 40 мл этилового спирта, и выделившийся в виде кристаллического продукта гидрофумарат соединения, указанного как целевой продукт, отфильтровывают после охлаждения смеси. Полученный продукт перекристаЛлизовьшают из этилового спирта, его т, пл, 215-21бс, Исходный материал может быть получен следующим, образомАО В раствор, содержащий 136 г триэтилового эфира фосфоноуксусной кислоты в 125 мл диметилформамида, прибавляют порциями при охлаждении льдом 67 г трет-бутилата калия, Реакцонную смесь выдерл шают в течение 1 ч при комнатн.ой температуре и затем смешивают по каплям с раствором 105 г этилового эфира 3-бензил-4-оксо-1-пиперидинкарбоновой кислоты в 90 мл абсолютного толуола так, чтобы температура внутри реакционного сосуда не превышала 35 С После завершения прибавления по каплям указанного раствора реакционную смесь перемешивают в течение 18 ч при температуре ТО С затем охлаждают до О-lOc и по каплям охлажденную реакционную смесь смешивают с 40О мл 2,5 н, раствора соляной кислоты. После разбавления 8ОО мл бензола смесь дополнительно перемешивают в течение ЗО мин, органическую фазу отделяют, промывают ее 10°/о-ным раст вором углекислого калия и водой, сушат над сернокислым, натрием и упаривают,Остаток порегогшют в высоком вакууме, при- чем этиловый эфир 1-зтоксикарбЬнил-З-бензил-4-пиперидилиденуксусной кислоты перегоняется, при 160-165 С О, О 05 мм рт.ст. Б, Раствор, сод жащий 114 г этилово го эфира 1-этоксикарбонил-3-бензил-4-пиперидилвденуксусной кислоты в 120 мл этилового эфира уксусной кислоты, гидрируют в присутствии 15 г 10%-ного палладия на угле при давлении 10 ати и температуре 50 С в течение 18 ч. После отделения катализатора растворитель отгоняют от фильтрата при пониженном давлении. Полученный в виде остатка этиловый эфир 1-этоксикарбонил-3-бензил-4-пиперидинуксусной кислоты (смесь изомеров) без дополнительной очистки применяют на последующей стадии. В, Смесь, состоящую из 114 г этилового эфира 1-этоксикарбонил-3-бензил-4-пиперидинуксусЯой кислоты и 2 л концентрированной соляной кислоты, нагревают при перемешивании в течение 24 ч при температуре кипения смеси. Затем полученный раствор упаривают досуха и в течение 2-3 ч остаток сушат в высоком вакууме при 100°Со Полученный в виде остатка неочищенный гидрохлорид З-бензил-4-пиперидинуксусной кислоты (смесь изомеров) применяют для осуществления последующей стадии. Неочищенный продукт может быть перекристаллизован из ацетона, в результате чего может быть получен ос -изомер, 178-179Со Гс Смесь, состоящую из 95 г гидрохлоридй З-бензил-4-пиперидинуксусной кислоты (смесь -изомеров), 30 мл концентрированного раствора аммиака, .90О мл 33%- ного раствора формальдегида и 140 мл 9О%-ной муравьиной кислоты нагревают в течение 18 Ч при температуре кипения реакционной массы. После охлаждения до комнатной температуры и смешения со 120 мл концентрированной соляной кислоты смесь упаривают досуха при пониженном давлении и полученный остаток сушат в высоком вакууме в течение 5 ч при 1ОО С, Полученный неочищенный гидрохлорид 3-бензилг-1-метил-4-пиперидинуксусной кислоты (смесь изомеров) без даль- ней1дей очистки используют на следующей стадии, Д, Полученный неочищенный гидрохлорид растворяют в 2,5 л абсолютного этилового спирта, раствор смешивают с 12мл концентрированной серной кислоты, реак-ционнузо смесь нагревают в течение 24 ч при температуре кипения, затем еще раз производят примешивание 12 мл концентрированной серной кислоты и снова реакционную массу нагревают в течение 24 ч при температуре кипения. Непосредственно йосле этого реакционную смесь упаривают при пониженном давлении приблизительно до 500 МЛ| остаток смешивают с 2 л воды со льдом, массу промывают диэтиловым эфиром и пощелачивают затеме прибавляя концентрированный раствор гидроокиси натрия. Выделившийся в осадок маслообразный продукт извлекают диэти- ловым эфиром, экстракт промывают водой сушат над сернокислым натрием и затем упаривают. Полученный остаток перегоняют в высоком вакууме, причем этиловый эфир 3-бензил-1-метил-4-пиперидинуксусной кислоты (смесь изомеров) перегоняется при 120-125°С/О,О2 мм рт, ст. Е, К 25О г предварительно нагретой до 1ОО С полифосфорной кислоты медленно прибавляют 27 г этилового эфира 3- -бензил-1-метил-4-пиперидинуксусной кис лотыа Затем температуру повышают до и реакционную смесь выдерживают при указанной температуре в течение. 2 ч. После охлаждения реакционной массы до комнатной температуры ее выливают в 1 л воды, га)лу{енный раствор промывают диэтиловым эфиром и затем подщелачивают, прибавляя раствор углекислого капня (рН 9-1О). Выделившийся в виде маслообразного продукта 1, 2,3,4,4а,5,11,11а -октагидро-2-метил-бН-бензо 5,б1 цикло- гепта ,2-с|пиридин-6-он экстрагируют диэтиловым эфиром, экстракт промывают водой, сушат над сернокислым натрием, упаривают и полученный остаток перегоняют в высоком вакууме. Температуре кипения смеси изомеров 135-140 С/0,5 мм рт,ст. Разделение изомеров. Раствор 95 г смеси изомеров в ЗОО мл этилового спир та смешивают с раствором 48 г фумаровой кислоты в 1ООО мл этилового спирта и смесь выдерживают в течение 48 ч при комнатной температуре, причем проиоходит кр к:таллизадия гидрофумарата транс -1,2,3,4,4а,5,11,11а-октагидро-2 метил -6Н бензо Г5,б|циклогепта Г1,2- ;1пиридин-6-она. Температура шювленкя продукта 2О1202 С (после перекристаллизации из этилового спирта). Образовавшийся после первой перекрис таллизация маточный раствор упаривают досуха, остаток смешивают с водой и хло ристым метиленом и смесь подщелачивают, прибавляя гидроокись натрия. После отделения органического раствора водную фазу три раза экстрагируют хлористым метиленом, объединенные органичес1ше растворы промывают водой, сушат над углекислым натрием и упаривают. Полученный остаток растворяют в изопропиловом спирте и продукт переводят в его гидро- хпоркд под действием эфирного растворп хлористого водорода, Пос:ле вьщержиппния в течение нескольких часов . гидрохлорид цис-1,2,3,4,4x3,5,11,11а-октагидро-2-метил-6Н-бензо 5,б циклогепта i,2-c пиридин-6-она отфильтровывают и затем перекристаллизовывают из изопропилового спирта, его т, пл, 241-243-С, Ж, К суспензии 8,0 г литийалюминийгидрида в 550 мл безводного эфира при комнатной температуре прибавляют по каП- лям раствор, содержаший 1О,О г транс-1,2,3,4,4а,5,11,11а-октагидро-2-мети№-бН-бензо 5,б1циклогепта||1,2-с| пирндин-6 -QHa в 2ОО мл безводного диэтилового эфира. Реакционную смесь перемешивают в течение 1 ч при указанной температуре и затем смешивают по каплям с 15О мл этилового эфира уксусной кислоты при О- 10 С, После прибавления по каплям 80 мл воды отфильтровывают неорганический остаток, промывают его диэ илавым эфиром, от фильтрата отделяют воду и эфирный раствор сушат над сернокислым машием,, После отгонки растворителя полученный транс-2,3,4,4а,5,6,11,11а-октагидро- -2-метил-1Н-бензо 5,6 циклогепта i,2-clпиридин-6-ол можно было перекристаллизовывать из ацетона, его т, пл, 193194°С. Пример 2о Шс-2,3,4,4а,11,11а-гексагидро-2-метил-1Н-бензо 5,6j цикло- гепта 1,2-с пирвдин. Аналогично примеру 1 из 8,5 г цис- -2,3,4,4а,5,6,11,11а-октапщро-2-метил-1Н-бензо| 5,бТциклогепта i,2-c7 пиридин-6-ола (получен по аналогии с примером 1Ж посредством восстановления цис-1,2, 3,4,4а,11,11а-октагвдро-2-метил-6Н-бен30-5,6-цикл о гепта |l,2-cj пиридин-6-она, т, пл, 14О-144с), 26 мл концентрированной соляной кислоты и 26 мл воды получают указанное соединение, которое выделяют в виде гидрофумарата с т,-пл, 116- -12ОС (из смеси этилового спирта и диэтилоаого эфира) Пример 3, Транс-2,3,4,4а,11, 11а-гексаг1щро-2,6-диметил-1Н-бензо 5, бДциклогепта Г1, пиридин, 12,5 г транс-2,3,4,4а,5,6,11Д1а-октагидро-2,6-диметил-1Н-бензо 5,б7 ЦИКЛО гепта LI,2-с1 пирвдин-6-ола нагревают в течение 15 мин в 18О мл концентрированной соляной кислоты и 12О мл воды прда температуре кипения смеси. Затем смесь упаривают досуха при пониженном давлении и полученный в виде твердого аешест- ва остаток, представляющий собой гидрохлорид указанного целевого соединения, два раза перекристаллизовывают из ацетона. Полученный продукт плавится при 234- 236 С, Исходное соединение получают следующим образом. А, К раствору 73 мл 2М раствора метиллития в диэтиловом эфире и 250 мл безводного эфира в течение 1 час прибавляют при комнатной температуре раствор, содержащий 13,О г транс-1,2,3,4,4а,5, 11,11а-октагидро-2-метил-6Н-бензо , б цнклогепта jl,2-сТпиридин-6-она в 2 50 мл безводного бензола, Реакционную смесь перемешивают в течение 5 ч при комнатной температуре, затем выливают ее в 70О мл 20%-ного раствора хлористого аммония, органическую фазу отделяют, а водную фазу экстрагируют хлористым метиленом. Объединенные органические раст воры промывают водой, сушат над сёрнокислым натрием и упаривают. Полученный транс-2,3,4,4а,5,6,.И,11а-октагидро-2,6 -диметил-1Н-бензо Г5,б1 цикпогепта 1,2-с пирвдин-6-ол непосредствегтоподвергают дальнейшей переработке. Пример 4, Транс-2,3,4,4а,И, 11а Гексагидро-2,5,6-триметил-1Н-бензо Г5,б1циклогепта ri,2-cj пиридиНо 7,0 г транс-2,3,4,4а,5,6,11,11а-октагидро 2,5,6 триметил-1Н-бензо| 5,б| ди логепта Г1,2-с7 пиридин-6-ола нагревают в iOO мл концентрированной соляной кислоты и 70 мл воды в течение 30 мин при температуре кипения реакционной сме си, после чего ее охлаишают до , Не посредственно после этого реакционную массу обрабатывают аналогично примеру 1 и полученное в виде маслообразного ве щества указанное целевое соединение переводят в гидрофумарат, который затем перекристаллиаовывают. Продукт плавится при i84-185 С (из изопропилового спирта). Исходный продукт получают следующим образом, Ае К предварительно нагретому до 5О раствору 1О,О г транс-1,2,3,4,4а,5,11. На-октагидро-2-метил-бН-бензо 5,б ци логепта 1,2-с1пиридин-6-она в ЗОО мл иклогексана медленно прибавляют при пеемешивании 5,9 г трет-бутилата калия. Реакционную смесь перемешивают при указанной температуре в течение 15 мин, охлаждают затем до 2О С, смешивают по каплям с 7,2 г йодистого метила, и непосредственно после этого дополнительно перемешивают в течение 4 ч при кокшат- ной температуре. После добавления ЗОО мл воды и 200 мл бензола отдел5Пот органический раствор, который промывают водой, суша над сернокислым натрием и упаривают. Полученный в виде остатка транс-1,2,3,4,4а,5,11,11 а-октагидро-2,5-диметил-бН-бензо 5,6Jцикпогепта 1, пиридин-6-ол два раза перекристаллизовывают из смеси эфира и гексана, бго т.пп. 101-102°С, Аналогично примеру ЗА из 6,5 г указанного раньше продукта в 120мл безводного бензола и 34,5мл 2М метиллития в эфире и 120 мл безводного эфира получают траис-2,3,4,4а, 5,6,11,11а-октагидро-2, 5,6-тримет-ил-1Н-бензо Ъ,б1циклогепта 1, 2-с1пиридин-6-ол, который в неочищенном виде подвергают дальнейшей переработке, Аналогично примерам 1-4 также получают и другие производные 2,3,4,4а,11, На-гексагидро-1Н-бензо ,б7циклогеп- та 11,2-CJ пиридина посредством отщепления воды от соответствующих 2,3,4,4а,5,в,11, 11а-октагидро-1Н-бензо 5, б7циклогепта 1,2-сТпиридин-6-олов, Соединения.приведенные в таблице, могут быть получены аналогично примерам 1-4, но при соблюдении следующих условий:применяют этанольный, изопропанольный или водный раствор соляной или серной кислоты и способ осуществляют при комнатной температуре, применяют уксусный ангидрид или ангидрид пропионовой кислоты и способ осуществляют при температуре, лежащей в интервале между 50 С и температурой кипения реакционной смеси, применяют хлористый тионил в пиридине и способ осуществляют при О-20 С,
н
(С
а
.
о, а
О)
ю
н
I
г
ю н





ь
а: I
п;
S
у
CJ
ti
W
о
§ §
5-55 т 1
со со со 1163 Фор.мула изобретения Способ получения производных пиперидина общей формулы где обозначает атом водорода, алкипьный радикал, содержащий 1-4 атома углерода, или атом галогена с атомным весом ниже 8О R 2 представляет собой атом водорода, алкильный радикал, содержащий 1-4 атома углерода, фенилалкильный остаток, содержащий 7-10 атомов углерода, или в том случае, когда обозначает атом водорода, Ц2, также представляет собой циклопропилалкильный остаток, содержащий 4-7 атомов углерода; 65 означает водород или алкил с 1-4 атомами углерода; предсташ}яет собой атом водорода или алкильиый радикал, содержащий 1-4 атома углерода, или их солей, отличающийся тем, что соединение общей формулы В, ОН В4 где-I., К. , и имеют указанные значенияI обрабатывают кислым средством, отщепляющим воду, и целевой продукт выделяют или переводят в соль. Источники информации, принятые во внимание при экспертизе: 1, Вайганд-Хильгетаг, Методы эксперимента в органической химии, М,, Химия, 1968, с. 801.
Авторы
Даты
1978-11-25—Публикация
1975-10-16—Подача