Изобретение относится к способу получе ния новых имидазогетероциклических соединений, которые обладают антидепрессивной активностью и поэтому MorjT найти применение в фармацевтической промышленности. В литературе известен целый ряд производных имидазотиазолов или имидазотиази- нов и способов их получения. Например, известен способ получения 3-ария-5,в--ди- гидроимкдазо..() тиазолов обшей форгде АГ - арил; обладающих, как и предлагаемые соединения антидепрессивной активностью. Согласно настоящему изобретению предл гается способ получения имидазогетероциклических соединений общей формулы (1) 1 Ч-N-,(сн,) ЛЛ J в которой R - незамещенный фенил, нафтил, фурил, тиенил, пиридил или фенил, замещенный 1 или 2 заместителями, выбранными из группы, содержащей атом гапогека, алкил, галоидалкил, алкокси-или алкилтиогруппу, содержащую в алкильной части от 1 до 4 атомов углерода, диалкил амино- или арил аминогруппу, каждая из которых содержит до 6 атомов углерода, нитрогрупп .; R -алкил, содержащий от 1 до 6 атомов углерода, алкенил или алкинил, содержащий до 6 атомов углерода, фенилалкил, содержащий до 8 атомов углерода; П- целое число от 1 до 2j юш их солей, которые отличаются от известных соединений значениями радикалов и обладают улучшенными свойствами по сравнению с известными соединениями. Предлагаемый способ получения соединений формулы (Г) основан на известной реакции и заключается в том, что соединение общей формулы ( Л ) N-(CH,), ГО где R , п имеют вышеуказанные значения;R - атом водорода, алкил,содержащий от 1 до 6 атомов углерода; подвергают взаимодействию с соединением общей формулы R, t или , в которых RJ, имеет вышеуказанные значения; , -хлор, бром, йод. Реакцию проводят в среде растворителя, например эфира или тетрагидрофурана. Повышение температуры приводит к ускорению или завершению реакции. Полученные соединения выделяют в свободном виде или в виде солк, в виде смеси изомеров или отдельных изомеров или опти чески активных антиподов. Подходящими кислотно-аддитивными сол ми являются хлоргидрат, бромгидрат, фосфа сульфат, цитрат, ацетат, оксалат, метансул фонат, толуол-п-сульфонат, тартрат, малеа глюконат. Пример 1. Раствор транс-6-ацетил -5- {3,4-дихлорфенил )-2 ,3,5,6-тетрагидроимидазо-(2,1-6)-тиазола (0,63 г) в сухом тетрагидрофуране (50 мл) осторожно добав ляют в атмосфере азота к реактиву Гринья ра, полученному из магния (0,14 г) и ме- тилйодида (0,38 мл) в эфире. Смесь перемешивают при 20°С в течение 1 час, раст воритель отгоняют выпариванием, и одну часть остатка растворяют в этилацетате, а другую - в 0,5 н. растворе гидроокиси натрия. Этилацетат выпаривают и остаток хроматографируют на силикагеле, используя в качестве элюента этил ацетат/ метанол. Получают транс-6-( 1-окси-1-метилэтил)-5-( 3,4-дихлорфенил) -2,3,5,6-тетрагидроимидазо-(2,1-&-тиазол, т. пл. 126-128°С перекристаллизацией из петролейного эфира (т. кип. 80-10О С) и ацетона. П р и м е р 2. Процесс, описанный в примере 1, повторяоЕОТ, используя в качестве исходного продукта эквивалентное количество цис- или транс-6-этоксикарбонил-5 енш1-2,3,5,6-тетрагидроимидазо-(2,1- Ь -тиазола вместо гранс-6-ацетил-5- (3,4-дихлооФенил)-2,3,5,6-тетрагидроимидазо-(2,1-& -тиазола, а также двойное количебт во подходящего реактива Гриньяра вместо метилмагниййодида, и не применяя колоночной хроматографии. Получают соединения общей формулы конкретные представители которых даны в табл. 1. Таблица.
Продолжение таблицы 1.




| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения имидазогетероциклических производных, их солей или их оптически-активных производных | 1974 |
|
SU520051A3 |
| Способ получения производных имидазо /2,1-в/ тиазола | 1973 |
|
SU518133A3 |
| Способ получения имидазо-2,1-8-тиазолин-или-тиазин-производных в виде смеси или отдельных изомеров или их кислотно-аддитивных солей | 1979 |
|
SU893134A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТИАЗОЛА | 1972 |
|
SU357730A1 |
| Способ получения производных имидазо/2,1-в/тиазолина или имидазо /2,1-в/тиазина или их кислотно-аддитивных солей,в виде смеси изомеров или отдельных изомеров | 1979 |
|
SU873887A3 |
| Способ получения аминов, или их солей, рацематов или оптическиактивных антиподов | 1976 |
|
SU602112A3 |
| 0-АЦИЛ-4-ФЕНИЛЦИКЛОАЛКАНОЛЫ, ИХ ЦИС/ТРАНСИЗОМЕРЫ ИЛИ ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ | 1994 |
|
RU2130921C1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ МОРФОЛИНА | 1970 |
|
SU422159A3 |
| СПОСОБ РАЗДЕЛЕНИЯ НА ОПТИЧЕСКИ АКТИВНЫЕ | 1971 |
|
SU318223A1 |
| i^" "БИБЛИОТЬНА I ^.fox-:^ | 1973 |
|
SU373945A1 |

Винил
Бензил
Реакционную смесь нагревают с обратным холодильником в течение последних двух часов. рН доводят до 10 перед экстракцией эфиром.
Реактив Гриньяра готовят из магния и этилйодида.
Сырой продукт вначале кристаллизуют из ацетона и получают транс-6-( l-oкcи-н-пpoпил)-5-фeнил-2,3,5, 6-тетрагидроимидазо-{2,1-)-тиааол, т.пл. 176 С. Маточный раствор обрабатывают эфирным раствором НСЕ, и из осадка кристаллизуют хлоргидрат. Реактив Гри- ньяра готовят из магния и этилйодида.
Реактив Гриньяра готовят из магния и Нт-пропилбромида и нагревают с обратным холодильником 2 час. Из сырого продукта перекристаллизацией выделяют хлоргидрат.
Реактив Гриньяра готовят из магния и бензилбромида. Сырой продукт очищают хроматографией на силикагеле, элюируют этилацетатом.
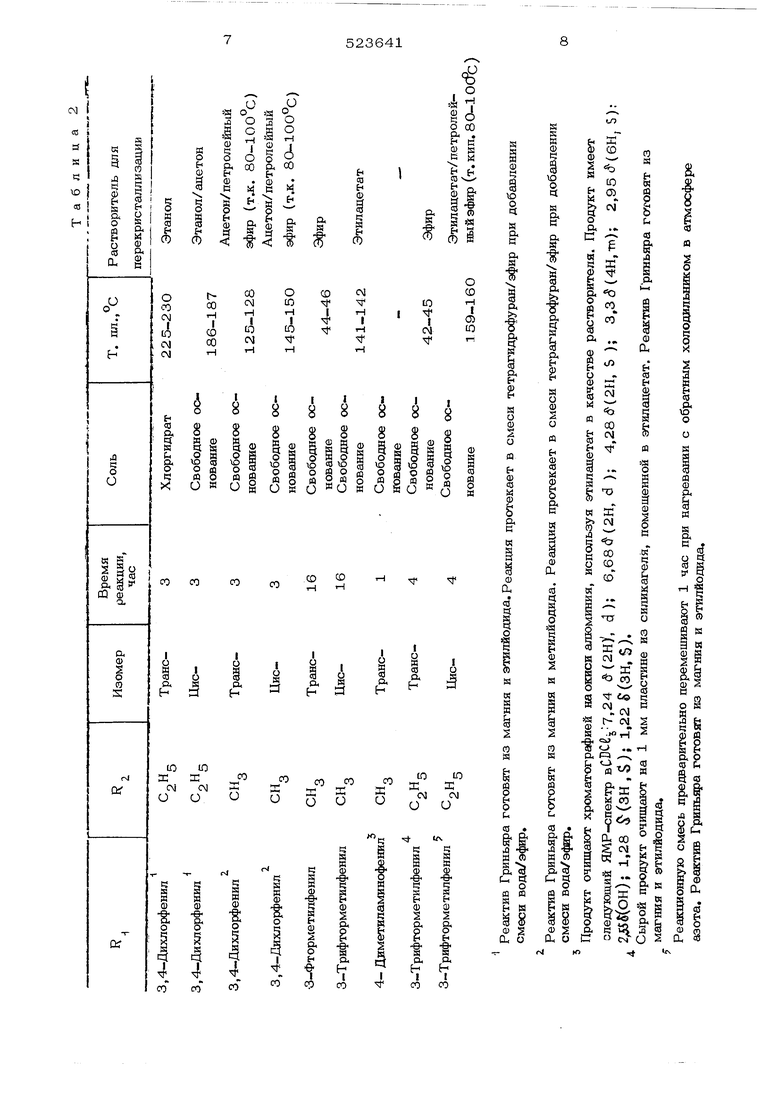
Реактив Гриньяра готовят из магния и бензилбромида. Сырой продукт очищают хроматографией на 1 мм пластине из силикагеля, помещенной в хлороформ/этиладетат (1:1). П р и м е р 3. Процесс, описанный в примере 2, повторяют, используя в качеств исходного продукта эквивалентное количест во 6-этоксикарбонилпроизводного, и получают соединения общей формулы t. - конкретные представители которых приведены в табл. 2, П р и м е р 4. Суспензшо комплекса из литийадетиленида и этилендиамина (1,84 г в сухом диоксане (130мл) насыщают сухим ацетиленом. Транс-6-этоксикарбонил-5-(3,4-дихлорфешш)-2,3,5,6- тетрагидроамидазо-(2,)-тивзоп (1,7 г) в сухом диоксане (50 мл) добавляют быстро к насыщенному раствору, и смесь перемещивают при 2О С в течение 2 час. Через смесь барботируют зот, отгоняя избыток ацетиле на. Добавляют воду (1 мл), растворители oTTOHsnoT упариванием, одну часть остатка растворяют в этиладетате, другую - в 2 н. НС1. Кислотный слой отделяют, подщелачивают и экстрагируют этилацетатом. Остаток очищают хроматографией на колонне с сили. кагелем, используя этиладетат как растворитель. получают транс-в-(1-этинил)-оксипроп-2-имил-5-(3,4-дихлорфенил)-2,3,5, 6-тетрйгидроимидазо-(2,1- 6)-тиазол в виде хлоргидрата с т. пл. более 3301 (из смеси этилацетат / этанол).
Транс140-144
Ацетон
184-187
Этанол
ТрансП р и м е р 5. Раствор 0,0-ди-п-толусил- ( D )-винной кислоты (7,6 г) в изопропаноле (100 мл) добавляют к раствору рацемического транс-5-(3,4-дихлорфе НИЛ )-6-(1-окси-1метилэтил)-2,3,5,6-тетра гидроимидазо-(2,)-тказола (6,2 г) в изопропаноле (1ОО мл). Смесь затравливают и оставляют на ночь. Смесь отфильтровывают и осадок перекристаллизовывают из этанола (50 мл), получают кислый тартрат (+) изомера с т. пл. 149 С. Эту соль помещают в смесь этилацетата (100 мл) и раствора 0,5 н. гидроокиси натрия (80мл). Этилацетатный слой отделяют, промывают водой, сущат, упаривают и получают хорощо кристаллизующийся сироп. Обработкой последнего петролейным эфиром (т. кип. 40-60°С) получают (+)-транс-5-(3,4-дихдорфешш -6-( 1-окси-1-метилэтил)-2,3, 5,6-тетрагидроимидазо-(2,1-)- тиазол, т. пл. 135-136°С, ГоС + 155° (, в этилацетате). Изопропанольный фильтрат, полученный при приготовлении соли, упаривают и получают вязкий гель, который обработкой О,5н, гидроокисью натрия и экстракцией этилацетатом превращают в (-) -основание, которое имеет вид сиропа. Перекристаллизацией из эфира получают (-)-транс-5-(3,4-дихлорфенил)-6-( 1-окси-1-метилэтил)- 2,3,5,6-тетрагидроимидазо-(2,1н6 )-тиазолс т. пл. 135°С, Ы25 (с 2, в этилацета)и ,
| - О
О
о
CO
CO
Ю iH
гЧ
t
.
t
CM
.со со
CO
со
со
g
0
я
ЕЮ
со
со
со со
со
см
к Е
и
о
о о
о
о
CD
тН
05 Ю
-
о.
со Ю
Xп:
см см
ои
с;
g Ф 2
о.
о.
со Пример 6. Смесь2-аминотиазолина(10,Ог), триэтипамина (25,0 мл) и этил-2,3-.дибро -3-фенилпропионата в этилацетате (40 мл нагревают с обратным холодильником в атмосфере азота в течение 20 час. Охлажден ную смесь фильтруют, и фильтрат хорошо промывают водой, затем обрабатывают 1 н НС1, Кислый экстракт подщелачивают 2 н. гидроокисью натрия и экстрагируют этилац татом. Этилацетат отгоняют выпариванием и остаток хроматографируют на силикагеле, используя в качестве эпюента этилацетат. Перекристаллизацией из ацетона получают цис-6-этоксикарбонил-5 енил-2,3,5, 6-тетрагиароимиаазо-(2,1- ) - тиазол, т. па. 99°С, и транс-6-этоксикарбонил-5-фенил-2,3,5,6-тетрагидроимидазо-( 2,1-) -тиазол, органическую фазу перемешивают с 1 н. НС1 (1,5 л), охлаждают смесь ниже 10 С. Выпадает осадок, который отфильтрОБывают, и перекристаллизацией из этанола получают цис-5-(3,4-дихлорфенил)- 6-втоксикарбонил-2,3,5,6-. тетрагидроимидазо-( 2,1-§)-тиазол гидрозшорид с т. пл. 226-230 С. Обработкой этой соли щелочью получают свободное основание с т. пл. 125-130 С (перекристаллизовано из адетонпетролеиного эфира, т. кип. 80-100 Маточный раствор, полученный после выпадения в осадок цис изомера, отделяют, водную фазу охлаяэдают менее, чем на 10° подщелачивают 4 н. гидроокисью натрия и экстрагируют дважды этилацетатом. Объединенные экстракты выпаривают досуха, и остаток перекрксталлкзовывают из смеэфир (т. кип. 80си ацетонпетролейный 1ОО С. Получают транс-5-(3,4-аихлорфенил) -6-этоксикарбонил-2,3- 5,6 -тетра- гидроимидазо-(2,1-S)-тиазол, т. пл, 65-68°С. Пример. Смесь этил-3-(3 трифторметилфенил) -2,3-дибромпропионата (8,0 г), 2-аминотиазолина (2,2 г) и триэтиламина (4,0 г) в этилацетате нагревают с обратным холодильником в атмосфере азота в течение 7 час. Охлажденную смесь фильтруют, фильтрат охлаждают до 10 С и добавляют 1 н. НС1 (40 мл). Смесь перемешивают 15 мин, осадок отфильтровывают, обрабатывают щелочью и получают цис-6-этоксикарбонил-5-(З- рифторметилфенил) -2,3,5,6-тетраги дроимид азо-(2,1-6)-тиазол, т. пл. 120-122°С (пер кристаллизован из петролейного эфира, т. кип. 80-100 С). Подкисленный фильтрат охлаждают до 10 С, добавляют щелочь, и полученный тве дый фильтрат перекристаллизовывают из петролейного эфира (т. кип. 80-100 С) с получением соответствующего транс-изоме111-113 С. с т. Ш1. Прим е р 8. Раствор метил-2-бром-3-(4-диметиламинофенил)-акрилата(1,4 г), триэтиламина (0,7 мл) и 2-аминотиазолина (0,5 г) в диоксане (50 мл) нагревают с обратным холодильником в атмосфере азота 2 2 час. Охлажденную смесь выпаривают досуха, одну часть остатка растворяют в воде, другую - в этилацетате, и этилацетатный экстракт хроматографируют на силикагеле с использованием этилацетата в качестве элюента, получают транс-5-(4-диметиламинофенил) -6-метоксикарбонил-2,3,5,6-тетрагидроимидазо-(2,1-)- тиазол в виде масла; HA-iP в CDCtg : 7,(2Н, d); 6,7 5 (2Н, d ); 4,8 d (IH, d ); 4,6 d (IH, d ); 3,75(3H, S ); 2,8 (У (4H, m); 2,95 6 (6H, S ). Формула изобретения Способ получения имидазогетероциклических соединений обшей формулы (1) -(CH,L где -незамещенный фенил, нафтил, фурил, тиенил, пиридил или фенил, замещенный 1 или 2 заместителями, выбранными из группы, содержащей атом галогена, алкил, галоидалкил, аякокси- или алкнлтио- группу, содержащую в алкильной части от 1 до 4 атомов углерода, диалкиламино- или ариламиногруппу, каждая из которых содержит до 6 атомов углерода, нитрогруппу; R j -алкил, содержащий от 1 до 6 атомов углерода, алкенил или алкинил, содержащий до 6 атомов углерода, фенилалкил, содержащий до 8 атомов углерода; Т1 -целое число от 1 до 2; или их солей, отличающийся тем, что соединение общей формулы ( (1 ) н.Д-(сн,„ RjOjC S где имеют вышеуказанные значения, R - атом водорода, алкил, содержащий т 1 до 6 атомов углерода; одвергают взаимодействию с соединением бщей формулы 1И Ri g- илиR2 Li, в которых R имеет вышеуказанные знаения:
523641 1112
it-хлор, бром, йод;нием продуктов в свободном виде, или в вив среде растворителя, например эфира,де соли, в виде смеси изомеров или отдельтетрагидрофурана, с последующим выделе-ных изомеров, или оптических антиподов.
Авторы
Даты
1976-07-30—Публикация
1975-03-25—Подача