(54; СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ З-СУЛЬФОНИЛ-2-АЗАЯНТАРНОЙ КИСЛОТЫ ИЛИ ИХ СОЛЕЙ имеет указанное значение, гпиоюсиповую кнспоту формулы}Х 1| СООД и эфир карёаминсшой кислоты общей формупы IV H.N Ц. имеет указанное значенне, в любой последовательности в среде орг нического |раствсфйтеля или в водной среде при 5-1ОО С с последующим вьвделение целевого продукта в свободном виде или в виде солв Радикалы J и Я могут быть однократно или многократно замешены. Целевой продукт .быть получен в виде соли. Из неорганических с.опей предпочтительными являются соли с катионами первой и второй гл«1Вной группы, в особенности аммониевые, литиевые,натриевые, калиевые, кальциевые и медные соли. Из солей с органическими катионами предпочитаются соли, ;являюшиеся производными от органичесю1х оснований, триметипамина, триэтиламина, триэтаноламина, морфолина, пиперидина, брудина, пирролидина и анилина Соединения общей формулы .1 могут быть получены следующим образ:ом. А. Сульфиновую: кислоту-обшей формулы И в пригодном растворител|ё подвергают взаимодействию с глио1а;иловой кислотой и получают при этом оксисульфонилуксусную КИСЛОТУ общей формулы.У R-$02H CHO соонсоон я1 Затем, оюсисульфонилуксусную кислоту oe щей формулы V в случае необходимости после ее выделения подвергают взаимодей ствию с эфиром карбаминовой кислоты обш формулы IV и получают целевой продукт общей формулы 1 K-S02- J1101H-H2 COOR I СООНS - R S02- iH--XH OORj еоон Обычно оксисульфонилуксусные кислоты |0бщей формулы V не особенно термоусто чивы, поэтому обычно рекомендуется процесс проводить при температуре не 50 С. Б. Супьфиновую кислоту общей формулы II, глиоксиповую кислоту и эфир карбамиНОВОЙ кислоты подвергают взаимодействию в пригодном растворителе R-SOeH-b ОСН4- H2N- СООКГ B-SOg-CH-NH-COORy в качестве растворителей применяют предпочтительно ледяную уксусную кислоту,, муравьиную кислоту, спирты с 1-4 атомами углерода, воду, диметилформамид, диме- тилсульфоксид или смеси растворителей, в частности смеси указанных растворителей. Обычно три компонента: 1 сульфиновую кислоту, глиоксиловую кислоту и эфир к аминовой кислоты размещивают в применяемом растворителе при 5-1ОО°С. Сульфиновую кислоту можно, например, применять. также в виде ее соли, предпочтительно кали-евой или натриевой. Целевой продукт осаждается в виде кристаллов, причем после вы| деления их Mogaio перекристаллизовывать из пригодного растворителя. В этом случае обычно пол чают продукт с хорошим выходом, однако в некоторых случаях он неудовлетворителен, так как ре- ашия между соединением общей формулы V. которая к согласно этому способу явля-i ется промежуточной, и эфиром карбаминовой кислоты протекает настолько медленно, что соединения общей формулы U1 разлагаются уже при температуре реакции. В. Сначала эфир карбаминовой кислоты общей формулы IV подвергают взаимодействию с глиоксиловой кислотой и получают соединение общей формулы VI ОСИ н- H2N - COOBi - СООН - HO-CH-NH-COOBi Эту реькшю ведут в пригодном растворителе или смеси растворителей. В качест|. ве растворителей можно использовать, .например, воду, ледяную уксус}1ую кислоту, муравьиную кислоту, этиленхлорид, диметилформамид, диметилсульфоксид, спирты с 1-4 атомами углерода и их с мое и. Реакцию можно осуществлять при доволы но жестких условиях, например при температурах до 150 С и выше, в результате чеговозможно также взаимодействие инертных и/или труднорастворимых эфиров карбаминовой кислоты общей формулы IV. Затем соединение VI в случае необходимости после его выделения подвергают взаимодействию с сульфиновой кислотой общей формулы и при мягких условиях реакции и в пригодном растворителеR-S02H+ НО - СН NH- COOR яYL - И - S02- CH-NH - COOR. в качестве растворителей можно использ вать, например, воду, спирты (С,-С ), муравьиную кислоту, ледяную уксусную КИСЛО1У диметилформамид, диметилсульфоксид или их смеси. Температура реакции 0-80 С. Так же и при вариантах А и В сульфиновую кислоту И можно применять в виде соли. Все три варианта А, Б и В позволяют применять и глиоксиловую кислоту в виде соли например натриевой, калыщевой, триэтиламмониевой, триэтаноламмониевой или калиевой соли. Кроме того, в некоторых случаях альдегидная группа может быть ацетализи- рованной. В качестве сульфиновых кислот или их солей можно использовать, например, метан- пропан-, бутан-, бензол-, П -толуол-, п - -хлорбензол-, 4-метоксибензол-, 3-трифтор метилбензоп-, 4-нитробензол-, З- цианбенЗОЛ-, 4-ацетаминобензол-, 3,4-дихлор-, 2,5-дихлор- иди 2,6-дихлорбензол-, 2,3,4-трихпорбензол-, 2,5-дим.етоксибензол-, 3,4,5-триметоксибензол-, 2-метокси-5- -хлорбензол-, 2-xnop-5 HHTpo6eH30J -, 2-хлор-5-трифторметилбензол-, 2-хлор-6-ме- тилбензол-, 2- иофен-, 2-нафталинсульфиновые кислоты. Если необходимые в качестве исходных соединений сульфиновые кислоты Ц и эфиры карбаминовой кислоты IV неизвестны, то их можно получать известными способами. Сульфиновые кислоты можно получать, например, восстановлением, соответствующих сульфохлоридов (которые в свою очередь получают путем взаимодействия соответству ших замещенных основных соединений с хлор сульфокислотой или из соответствующих замещенных ариламинов путем, модифицированной реакции Зандмейера по Меервейну) или путем непосредственной реакции Зандмейера с получением сульфиновой кислоты. Таким образом получают, например, еще неизвестную 2-хлор-метилбензолсульфиновую кислоту (т.пл. 110 С (разложение), исходя из 2-хлор-6-метиланилинов через 2-хлор-6- -метил-бензолсульфохлорид (т.кип. 117°С/ /1,3 мм рт. ст. В качестве эфиров карбаминовой кислоты (называемые также уретанами) можно использовать, например метил-, аллил-, н-бутилфенил-, бензил-, 4-метоксибензил-, циклогексил-, 3-фенилпропил-, пропинил-, феноксиэтилкарбаматы и др. Эфиры карбаминовой кислоты можно легко получать, например, из соответствующих спиртов и мочевины или из соответствующих эфиров хлормуравьиной кислоты и аммиака. Из соединений общей формулы I можно получать соли известным способом путем взаимодействия с другими неорганическими или органическими основаниями. Прим ер 1. (Вариант В), 7,5-метилкарбамата, 17,8 г натриевой соли П -толуолсульфинокислоты, 26 г глиоксиловой кислоты (40%-ной) в воде, 100 мл воды и 2О г муравьиной кислоты (85%-ной) в течение 5 час размешивают при 40 С. По истечении 2 час раствор мутнеет в результате начала кристаллизации продукта вза- имйдействия. По окончании реакции охлаждают до +10 С, отсасывают и промывают ледяной водой. После сушки над полупятиокисью фосфора получают 29,5 г (76% от теоретического) метиловый эфир 3-( я -то- лилсульфонил)-2-азаянтарной кислоты с т.пл. 1О1 С в виде рацемата. Это соединение посредством оптически активных оснований можно разделять на его оптические антиподы. Посредством триэтиламина в спирте получают соль тризтиламмония с т.пл. 90 (разложение), которая превосходно растворяется в воде и также в органических растворителях, например хлороформе, этиловом эфире уксусной кислоты, спирте, диметилформамиде. Другие соли метилового эфира 3-( ц -толипсульфонил) -2-азаянтарной кислоты получают следующим образом. Литиевая соль. Кислоту при 20 С растворяют в воде и нейтрализуют карбонатом лития. Сущат над полупятиокисью фосфора при 20 С. Получают бесцветную отличЬно растворимую в воде литиевую соль с т.пл. 19О (разложение). Подобным споробом получают натриевую и калиевую соли с применением карбоната натрия или калия.
Медная с о л ь. 14,3 г (5О ммолр,й) суклшната при 7О растворяют в 200 мл воды. К воде добавляют 100 мл холодного насыщенного раствора из pacTDOJpa ацетата кюди (I) . Охлаждают до 20 С, и поспе выдержки в а чение ночи отсасыва ют труднорастворимую в воде медную сопь. Получек м елто--зепеные кристаллы, -которцч разлагаются при температуре выше 150 С без ппавдения.
Аниииновая сопь. 14,3 г (во ммолей) сукюшата растворяют в ISOijin изопропанола. Размешивая при комнатной температуре, по каплям добавляют 6 г |(60 ммопей) анилина, растворенного в 4 О мн иэопропанода. После 3 час перемеигАвания отсасывают анилиновуто соль (17 г, 90% от теоретического) и промывают эфиром. Получают бесцветные кристаллы с т.пл. 180 (разложение).
Пример 2. (Вариант А). 24 г 3,4. -дихлорбензопсупьфинокислого натрия ра;тв | ряют в -7 О мл воды и 5О мл муравьиной. кислоты (65%-ной) при О С. Озшажда- ют до 20 С и добавляют 26 г глисяссило-. вой кислоты (4О%-ной) в воде. Перемешивают в течение 3 час при ЗО С и затем добав/шют 12 г ti -бутипкарбамата и продолжают перемешивать еще 5 час при. 20-
1; )
30 с. Охлаждают па ОС, п nwuie п..шерж. ки в течение ночи огсгчсывают об тазовав- яиеся кристаллы и промьпзают ледяной о- дои. Можно перекрнстпллизовыватьиа изопропанода. Получают 26 г (70% от теоретического) бутилового э({|ира 3-(3,4-дихло1 фенилсульфонИ71)2 азаянтарной кислоты с т. пл. 118 С (разложение).
П р и м е р 3. (Вариант В). 13,7 г фенилкарбамата, 26 г глиоксиловой кислота (40%-ной) в воде и 5О мл воды в течение 5 час размешивают при 85 С. Получают прозрачный раствор. Охлаждают до 40 С и при размешивании добавляют раствор ИЕ 18 г tl -толуолсульфинокислого натрия в 6О мл воды и 30 мл муравьиной кислоть (85%-«ой). После дальнейшего 6-час перемешивания при 40 С выкристаллизовьтает ся продукт. Охлаждают до О С с целью завершения кристаллизации. Получают 22,2 г (б4% от теоретического) фенилового эфира 3-(tl -толилсуль ннл)«2-азаянтарной кисло ты с т. лл. 192 (р ложение) в виде радемата.
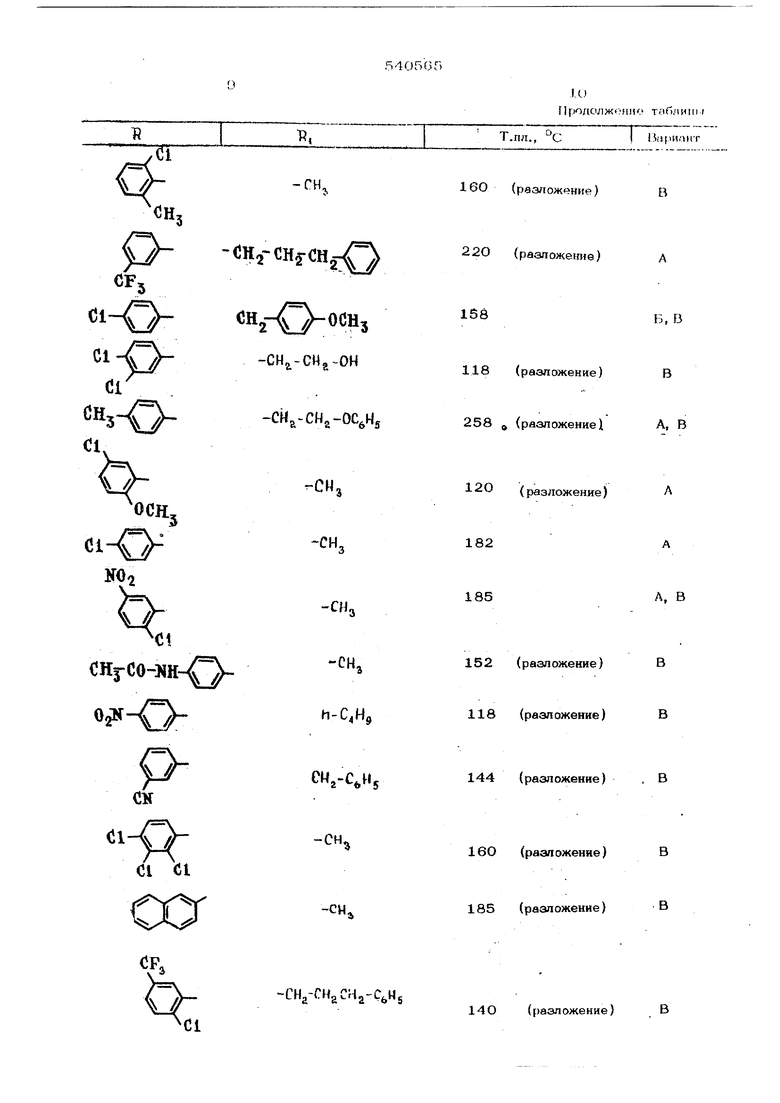
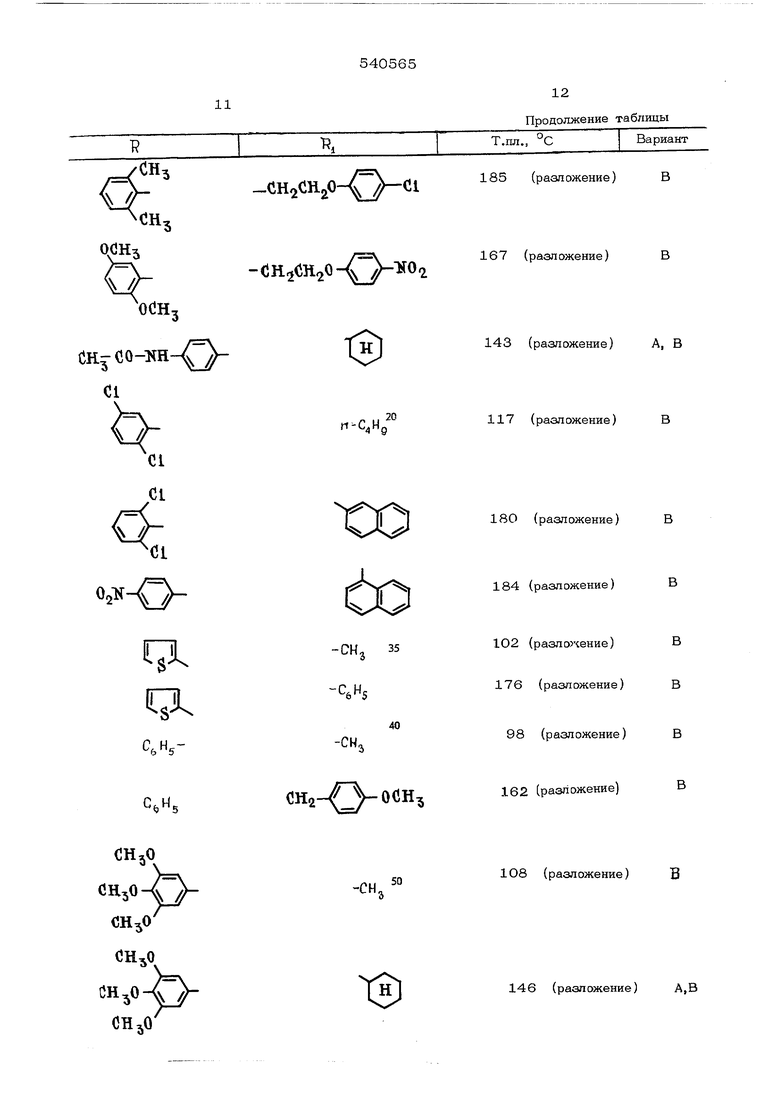
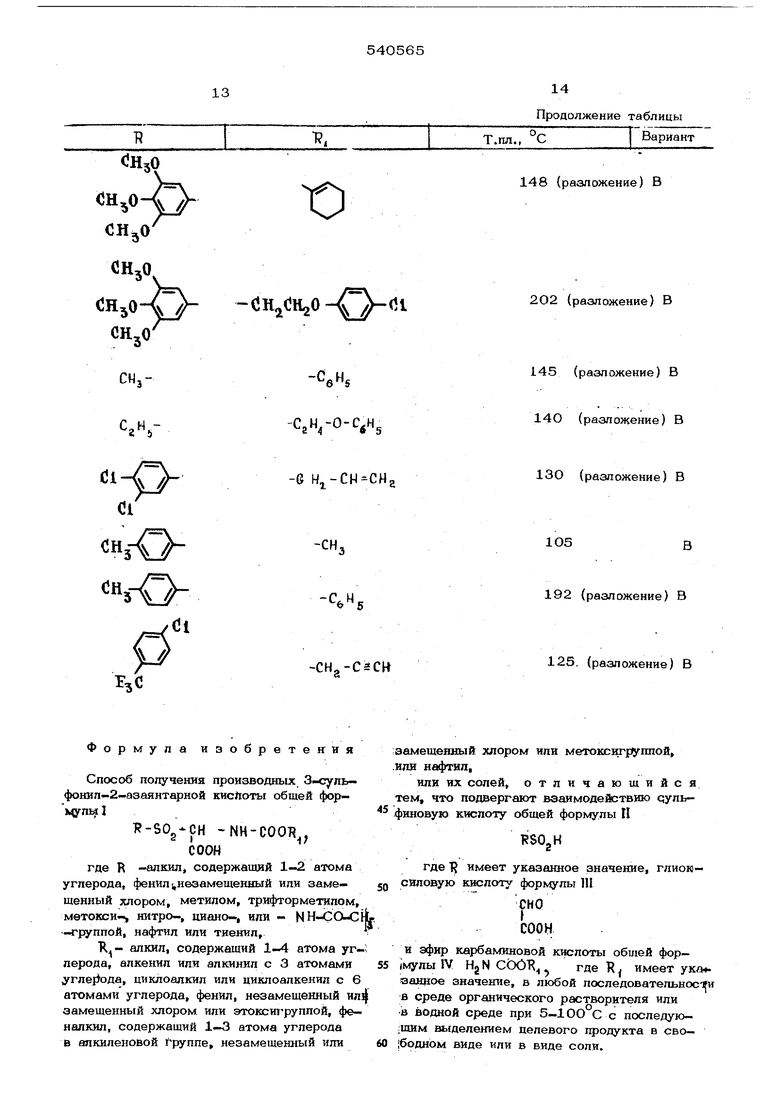
Аналоги рймй спосрбамн получают соеК -СН-НН-СООК форйуиямJ . .: :... . CQOH
.характеристика которого дад.а в таблице.




-СН.
-СН,
з-Л //
128
В, Б
145 (разложение)
В
176
в
196
в
22О (разложение)
в
ОСН.
160
л,в
f 1рОЛОЛЖМ1ЛО тебя ИИ I
-сн.
16О (разложение)В
-OH -CHfCH
22О (рааложе(шв)
-СН -СНа-ОН
158Б, ГЗ
118 (разложение)В
-CHj,-CH2-OC M5
зЛ
-CM,
осн.
-сн.
-сн.
С
-СИ, .
СН,.С,Н5
-СН,
-сн.
CF,
-СНд-СИаСИа-С Н.
258 (разложение А, В
12О (разложение)
182
Л. В
185
152 (разложение)В
118 (разп ожение)
144 (разложение), В
160 (разложение)В
185 (разложение)В
14О (разложение)В
11
12
Продолжение таблицы
-.,/-С1
185 (разложение)В
-ОН2 1Н20-4 O-l
167 (разложение)В
143 (разложение)А, В
117 (разложение)В
180 (разложение)В
184 (разложение)В
-СНз 35
-С,Н5
-сн.
с.н,(Зл -/ -ОСНх
1О2 (разло чение)
В
176 (разложение)В
98 (разложение)В разложение)В
1О8 (разложение)В
-СН,
146 (разложение)А, В
Авторы
Даты
1976-12-25—Публикация
1972-06-02—Подача