Изобретение относится к производству ветеринарных биологических препаратов и представляет собой новый ijJTaMM лептоспир, который может использоваться для приготовления вацин против лептоспироза сельскохозяйственных и промысловых животных.
Высокая иммуногенная активность штаммов лептоспир, из которых изготавливается вакцина, является одним из основных условий, обеспечивающих получение активной вакцины против лептоспироза животных . Б настоящее время в биологической промышленности изготавливают убитую вакцину против лептоспироза из 24-39 штаммов лептоспир, относящихся к 6 серологическим группам, в том числе содержащую 5 щтаммов серологической группы Иктерогеморрагия, в частности, штаммы И-1496, И-542, Белоусов, Судьин и Вайнберг l .
Недостатком известных штаммов является их низкая иммуногенная активность, кроме того, получение вакцины из них трудоемко, так как необходимо выращивать каждый штамм в баллонах (10-12 л).Целью изобретения является штамм лептоспир серологической группы Иктерогеморрагия, обладающий высокоактивными в иммуногенном и антигенном отношении свойствами,который можно использовать для приготовления поливалентной вакцины против лептоспироза животных,и позволяющий реализовать менее трудоемкий реакторный метод выращивания лептоспир при изготовлении вакцины.
0
Штамм лептоспир Иктерогеморрагия ВГНКИ-2 выделен от свиньи в Московской области в 1972 г. и хранится в коллекции микроорганизмов ВГНКИ ветпрепаратов МСХ СССР под № 2.
5
Штамм лептоспир Иктерогеморрагия ВГНКИ-2 характеризуется следующими признаками.
Морфологические признаки. Обладает характерными для лептоспир мор0фологическими признаками.
При микроскопии в темном поле микроскопа представляет собой серебристо-белые плотные спирали с утолщениями в виде крючков на концах.
5 .Витки спирали незаметны при увеличении в 200-400 раз, но они хорошо видны в электронном микроскопе. Длина лептоспир 8-17 мкр, диаметр 0,1-0,15 мкр. Наиболее отчетливо
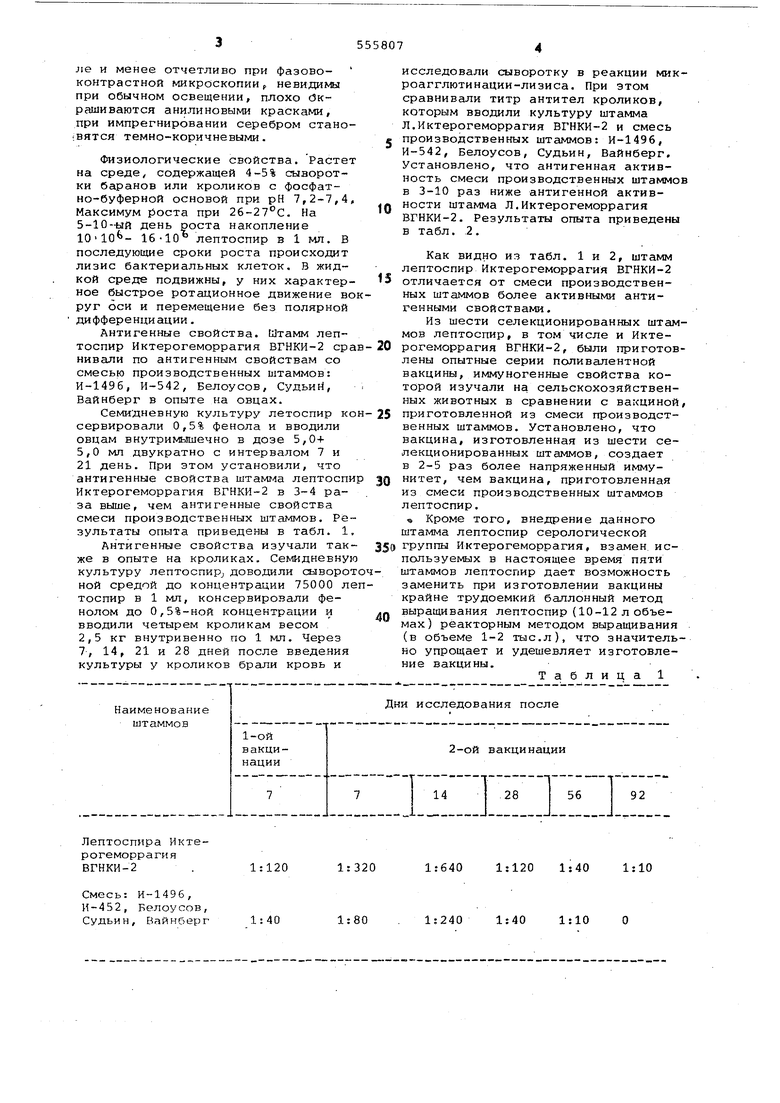
0 видны при микроскопии в темном поJie и менее отчетливо при фазовоконтрастной микроскопиир невидимы при обычном освещении, плохо С5крашиваются анилиновыми красками, при импрегнировании серебром стано:вятся темно-коричневыми. Физиологические свойства. Растет на среде, содержащей 4-5% сыворотки баранов или кроликов с фосфатно-буферной основой при рН 7,2-7,4 Максимум роста при 26-27 0. На 5-10--ый день роста накопление 10-10 - 16-10° лептоспир в 1 wi, В последующие сроки роста происходит лизис бактериальных клеток. В жидкой среде подвижны, у них характерное быстрое ротационное движение во руг оси и перемещение без полярной дифференциации. Антигенные свойства. Штамм лептоспир Иктерогеморрагия ВГНКИ-2 ср нивали по антигенным свойствам со смесью производственных штаммов: И-1496, И-542, Белоусов, Судьий, Вайнберг в опыте на овцах. Семидневную культуру летоспир к сервировали 0,5% фенола и вводили овцам внутримышечно в дозе 5,0+ 5,0 мл двукратно с интервалом 7 и 21 день. При этом установили, что антигенные свойства uiTaMr/ia лептосп Иктерогеморрагия ВГНКИ-2 в 3-4 раза выше, чем антигенные свойства смеси производственных штаммов. Ре зультаты опыта приведены в табл. 1 Антигенные свойства изучали так же в опыте на кроликах. Семидневну культуру лeптocпиpJ доводили сыворо ной средой до концентрации 75000 л тоспир в 1 мл, консервировали фенолом до 0,5%-ной концентрации и вводили четырем кроликам весом 2,5 кг внутривенно по 1 мл. Через 7-, 14, 21 и 28 дней после введения культуры у кроликов брали кровь и исследовали сыворотку в реакции микроагглютинации-лизиса. При этом сравнивали титр антител кроликов, которым вводили культуру штамма Л.Иктерогеморрагия ВГНКИ-2 и смесь производственных штаммов: И-1496, И-542, Белоусов, Судьин, Вайнберг. Установлено, что антигенная активность смеси производственных штаммов в 3-10 раз ниже антигенной активности штамма Л,Иктерогеморрагия ВГНКИ-2. Результаты опыта приведены в табл. .2. Как видно из табл. 1 и 2, штамм лептоспир Иктерогеморрагия ВГНКИ-2 отличается от смеси производственных штаммов более активными антигенными свойствами. Из шести селекционированных штаммов лептоспир, в том числе и Иктерогеморрагия ВГНКИ-2, были приготовлены опытные серии поливалентной вакцины, иммуногенные свойства которой изучали на сельскохозяйственных животных в сравнении с вакциной, приготовленной из смеси производственных штаммов. Установлено, что вакцина, изготовленная из шести селекционированных штаммов, создает в 2-5 раз более напряженный иммунитет, чем вакцина, приготовленная из смеси производственных штаммов лептоспир. « Кроме того, внедрение данного штамма лептоспир серологической группы Иктерогеморрагия, взамен, используемых в настоящее время пяти штаммов лептоспир дает возможность заменить при изготовлении вакцины крайне трудоемкий баллонный метод выращивания лептоспир (10-12 л объемах) реакторным методом выращивания (в объеме 1-2 тыс.л), что значительно упрощает и удешевляет изготовление вакцины. Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Штамм LертосрIRа ромоNа ВГНКИ-6 | 1976 |
|
SU555665A1 |
| Штамм LертоSрIRа caNIcoLa ВГНКИ-3 | 1976 |
|
SU555666A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПОЛИВАЛЕНТНОЙ ВАКЦИНЫ ПРОТИВ ЛЕПТОСПИРОЗА ЖИВОТНЫХ | 1996 |
|
RU2096042C1 |
| Способ изготовления вакцины поливалентной против лептоспироза лошадей | 2023 |
|
RU2815538C1 |
| Способ получения поливалентной вакцины против лептоспироза животных | 1975 |
|
SU555664A1 |
| Поливалентная вакцина ВГНКИ против лептоспироза животных и способ ее получения и использования | 1979 |
|
SU828459A1 |
| ВАКЦИНА ИНАКТИВИРОВАННАЯ КОМБИНИРОВАННАЯ ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА, ВИРУСНОЙ ДИАРЕИ И ЛЕПТОСПИРОЗА КРУПНОГО РОГАТОГО СКОТА | 2009 |
|
RU2395297C1 |
| ВАКЦИНА ИНАКТИВИРОВАННАЯ КОМБИНИРОВАННАЯ ПРОТИВ ИНФЕКЦИОННОГО РИНОТРАХЕИТА, ВИРУСНОЙ ДИАРЕИ, РОТА-, КОРОНАВИРУСНОЙ БОЛЕЗНЕЙ И ЛЕПТОСПИРОЗА КРУПНОГО РОГАТОГО СКОТА | 2009 |
|
RU2395299C1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ЛЕПТОСПИРОЗА И ПАРВОВИРУСНОЙ ИНФЕКЦИИ СВИНЕЙ | 1987 |
|
SU1538305A1 |
| АССОЦИИРОВАННАЯ ВАКЦИНА ПРОТИВ ЛЕПТОСПИРОЗА И КАМПИЛОБАКТЕРИОЗА КРУПНОГО РОГАТОГО СКОТА | 1992 |
|
RU2021818C1 |

1:120 1:320 1:640
1:401:80. 1;240
1:10
1:120 1:40
1:10
1:40
Таблица 2
Авторы
Даты
1983-01-30—Публикация
1976-01-30—Подача