(54) СПОСОБ ПОЛУЧЕНИЯ 5а-БРОМ-6 |3-ФТОРПРОИЗВОДНЫХ ПРЕГНАНА В качестве основания Льюиса применяют обычно тетрагидрофуран (ТГФ) или диметилформамид, а в качестве галоидалкана - хлористый метилен или хлороформ. Пример. Sen-Бром -6)3- фтор -16а- метил -3/3- На- диокси -5а- прегнан-20- он. В полиэтиленовый реактор вводят 35 мл (1,75 моль) безводного фтористого водорода, охлаждают до -70° С, добавляют 55мл (0,68моль) ТГФ, приливают раствор 1,86 г (0,0065 моль) 1,3-дибром -5,5- диметилгидантоина в 120 мл хлористого метилена, медленно добавляют 3,45 г (0,01 моль) 16о;-метил-3/3, 17а-диокси-5- прегнен -20-она и перемешивают Зчас при (-70) - (-50)° С. Реакционную смесь нейтрализуют 20%-ным водным раствором аммиака, экстрагируют хлороформом, промьшают экстракт водным раствором сульфата натрия и водой, сушат безводным сульфатом натрия, вьшаривают досуха и остаток (4,4 г) кристаллизуют из этанола, получая 3 г хроматографически чистого целевого соединения, т.пл. 208-210°С; -72,8° (0,2%, хлороформ) . Вычислено, %: С 59,32; Н 7,69. С22Нз4ВгРОз. Найдено, %: С 59,71; Н 8,03. В примерах 2-11 проводят опыт, как в примере 1, и получают хроматографически чистый продукт (во всех примерах). Пример 2. 5№Бром-6/3- фтор -3)3, 16а; 17а-триокси -5о:- прегнан- 20- он. Используя 35мл (1,75 моль) безводного фтористого водорода, 70 мл (0,86 моль) ТГФ, раствор 1,79 г (0,013 моль) N -бромацетамида в хлороформе и 3,48 г (0,01 моль) 3/3, 16а, 17о;- триокси -5-прегнен -20- она, получают реакционную смесь, которую нейтрализуют, экстрагируют смесью хлороформ - бутанол и остаток (4,4 г) после вьшаривания кристаллизуют из смеси бензол - циклогексан. Выход 2,8 г, т.пл. 171-174°С; 53,2° (0,5%, метанол). П р и м е р 3. 5а:-Бром -б/З-фтор -16а- метил.. - 3)3- окси- 5а- прегнан- 20- он. Из 60 мл (3 моль) безводного фтористого водорода, 60мл (0,74 моль) ТГФ, раствора 1,8 г (0,0063 моль) в хлористом метилене и 3,3 г (0,01 моль) 1 бес-метил -3(3- окси -5- прегнен -20-она, растворенного в хлористом метилене, получают продукт-сырец, который кристаллизуют на смеси ацетон -циклогексан. Выход 2,2 Гт.пл. 195-200°С; Q: Jp -117° (1%, хлороформ). Вычислено, %: С 61,54; Н 7,98. С22Нз4ВгР02. Найдено, %: С 61,33; Н7,97. П р и м е р 4. 5а -Бром -6/3-фтор -16о; 17а-изопропилидендиокси -3)3- окси -50- прегнан-20- он. Применяя 60 мл (3 моль) безводного фтористого водорода, 30 мл (0,37 моль) ТГФ, раствор 1,86 г (0,0065 моль) 1,3-дибром -5,5- диметилгидантоина в хлористом метилене и 3,9 г (0,01 моль) 160, 17о:-изопропилидендиокси-3/3-окси -5- прегнен -20-она, получают 4,7 г продукта-сырца, который кристаллиззют из 80%-ного водного этанола. Выход 2,85 г; т.пл. 226-227 С; -12,4° (1%, хлороформ). Вычислено, %: С 59,14; Н7,44. С24НзбВгР04. Найдено, %: С 59,44; Н 7,38. П р и м е р 5. 3,16-Диацетат 5о:-бром -6)3-фтор-3(3, 16а, 170 -триокси -5о:- прегнан-20-она. Из 34 мл (1,7 моль) безводного фтористого водорода, 51мл (0,63 моль) ТГФ, раствора 1,86 г (0,0065 моль) 1,3-дибром-5,5- диметилгидантоина в хлористом метилене и 4,3 г (0,01 моль) 3,16-диацетата 313, 16а, 17о:-триокси -5- прегнен-20- она получают 5,3 г продукта-сырца, который кристаллизуют из 95%-ного водного этанола. Выход 3,8 г; Т.ПЛ. 204-207° С; ог -56,0° (1%, хлороформ). Вычислено, %: С 56,50; Н 6,83. СзаНзбВгРОб. Найдено, %: С 56,93; Н 6,92. П р и м е р 6. 21-Ацетат 5о;-бром -6)3- фтор -3)3, 17о; 21-триокси -5о:- прегнан -20-она. Используя 8 мл (0,4 моль) безводного фтористого водорода, 8,0мл (0,1 моль) ТГФ, 0,51 г (0,0018 моль) 1,3-дибром-5,5- диметилгадантоина и 1,17 г (0,003 моль) 21-ацетата 3)3, 17о; 21-триокси-5- прегнен -20- она, растворенного в хлористом метилене, получают 1,4 г продукта-сырца, которьш кристаллизуют из смеси ацетон-циклогексан. Выход 0,95 г; т.пл. 173-177°С; а -15,5° (0,4%, хлороформ). Вычислено, %: С 56,45; Н 7,00. С2зНз4ВгРО5. Найдено, %: С 56,48; Н 7,08. П р и м е р 7. 3,21-Диацетат 5а-бром -60 -фтор-3)3,17а, 21-триокси прегнан -20-она. Бромфторирование 3,21-диацетата 3)3, 17о; 21-триокси -5- прегнен -20-она проводят, как в примере 6, используя те же молярные количества реагентов, и получают 1,5 г продукта-сырца, который кристаллизуют из смеси ацетон-циклогексан. а -6,5° Выход 1г; т.дл. 195-197°С; (1%, хлороформ). П р и м е р 8. 3,17, 21-триацетат 5о -бром -6(3фтор -3/3, 17)3, 21-триокси -5а -прегнан -20- она. Бромфторирование 3,17, 21-триацетата 3)3, 17а 21-триокси -5- прегнен -20- она проводят аналогично примеру 6, применяя те же молярные количества реагентов, и выделяют 1,7 г продукта-сырца, который кристаллизуют из ацетона. Выход 1,1 г; т.пл. 182-183°С; OL -44,6° (1%,хлороформ). П р и м е р 9. 3-Ацетат 5а:-бром -6/3-фтор-3)3-окси- 16-прегнен-20- она. Из 8 мл (0,4 моль) безводного фтористого водорода, 12 мл (0,15 моль) ТГФ, 1,6 г (0,0055 моль) 1,3дибром -5,5-диметил -гидантоина, 40мл хлористого метилена и 3,56 г (0,01 моль) 3-ацетата 3/3-окси -5,16- прегнадиен -20- она получают 4,5 г
продукта-сырца, который кристаллизуют из метанола. Выход 3,2 г; т.пл. 182-184°С; а -29,4° (1%, хлороформ); Хшкс 238 нм; EI см 1% 213.
Вычислено, %: С 60,66; Н 7,09.5
СззНзаВгРОзНайдено, %: С 60,54; Н7,12.
Примерю. 3- Ацетат 5о:-бром -6j3- фтор -3/3окси -16- прегнен -20-она.
Бромфторирование 3-адетата 3/3-окси -5,16- ю регнадиен -20- она проводят, как в примере 9, но ри температуре (-10) - (-20)°С в течение 0 мин. Выход 3,1 г; константы те же, что и в римере 9.
Пример 11. 3 - Ацетат So:-бром-6 -фтор- и
3|3 - окси - 16 - прегнен - 20 - она.
Бромфторирование 3 - ацетата 3/ -окси - 5,16прегнадиен -20- она проводят аналогично примеру 9, но используя 1,45 г (0,005 моль) бромируюего агента и проводя реакцию при (-5) - 5°С 20 течение 30 мин. Выход 2,7 г, константы те же, что и в примере 9.
Пример 12.3- Ацетат 5й; - бром - 6j3 - фтор 3|J- окси - 16 - прегнен- 20 - она.
В полиэтиленовый реактор добавляют 3,56 г 25 (0,01 моль) 3-ацетата 3/3-окси -5,16- прегнадиен-20- она, приливают 40 мл хлороформа, при перемешивании охлаждают до (-20) - (-40) ° С, добавляют 4мл (0,15 моль) 60%-ного водного раствора фтористого водорода и 1,6 г (0,0055 моль) 1,3-дибром- зО -5,5- диметилгидантоина, перемешивают 30 мин при указанной температуре и, как в примере 9, вьщеляют 3,1 г продукта; т.пл. 180-183°С; -30,4° (1%, хлороформ); Хма1«Г238нм; EjCM 202.35
П р и м е р 13. 5о -Бром -6/3-фтор -3/3-окси -16прегнен-20-он.
Бромфторирование 3|3-окси -5,16- прегнадиен-20- она проводят подобно примеру 9, применяя те же .молярные количества реагентов, и кристалли 40 зуют продукт-сырец из 70%-ного водного этанола. Выход 3 г; т.пл 183-185°С; -38,2° (1%, хлороформ); Хмакс238нм; EJCM 227.
Вычислено, %: С 61,02; Н 7,31.
2 1 2
Найдено, %: С 60,92; Н 7,25.
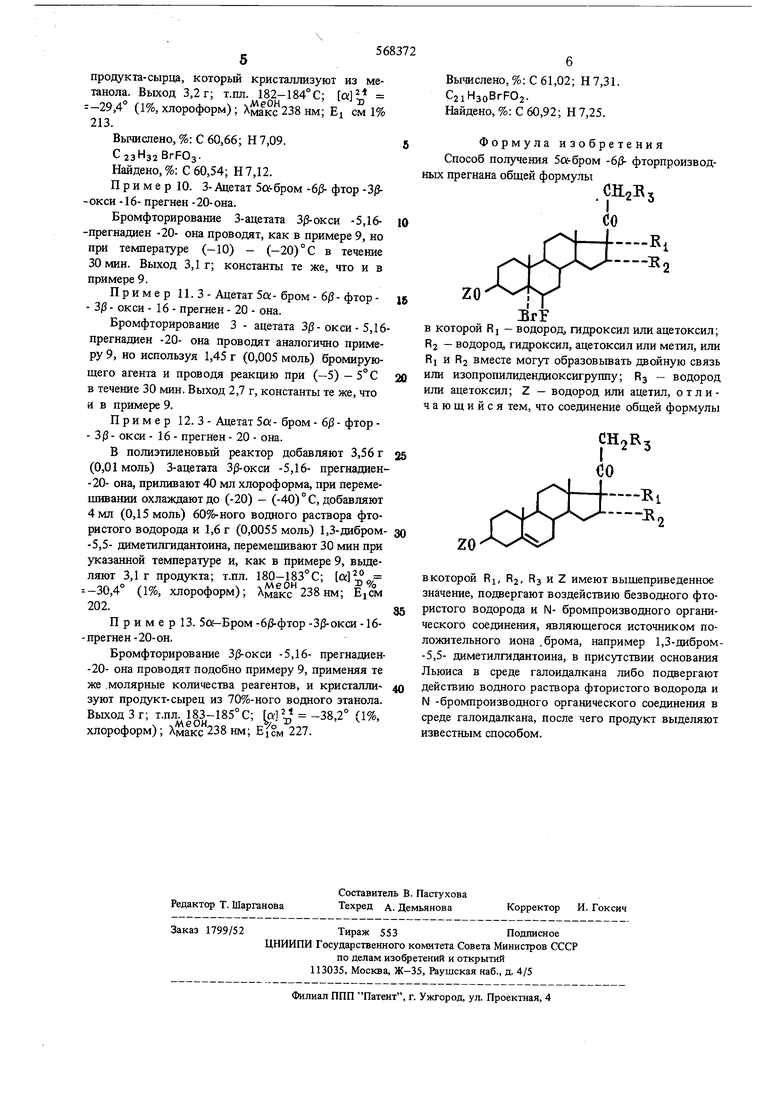
Формула изобретения Способ получегшя 5о:-бром -6/S- фторпроизводых прегнана общей формулы
.
со
.--Ri
Во
ВгГ
в которой RJ - водород, гидроксил или ацетоксил; R2 - водород, гидроксил, ацетоксил или метил, или RI и R2 вместе могут образовьшать двойную связь или изопропилидендиоксигруппу; RS - водород или ацетоксил; Z - водород или ацетил, отличающийся тем, что соединение общей формулы
вкоторой RI, R2, из и Z имеют вышеприведенное значение, подвергают воздействию безводного фтористого водорода и N- бромпроизводного органического соединения, являющегося источником положительного иона .брома, например 1,3-дибром-5,5- диметилгидантоина, в присутствии основания Льюиса в среде галоидалкана либо подвергают действию водного раствора фтористого водорода и N -бромпроизводного органического соединения в среде галоидалкана, после чего продукт выделяют известным способом.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 21-ацетокси-6 фтор-4-прегнен-3,20-дионов | 1973 |
|
SU524522A3 |
| Способ получения 5-бром-6-фторстероидов | 1971 |
|
SU422242A1 |
| Способ получения 21-ацетокси-6 -фтор-4-прегнен3,20-дионов | 1973 |
|
SU525432A3 |
| Способ получения производных прегнановой кислоты | 1974 |
|
SU622411A3 |
| Способ получения д-гомостероидов | 1974 |
|
SU517263A3 |
| Способ получения стероидных (16 ,17- )-2",3"-дигидро-/1,4/диоксинов или их 1,2-дегидропроизводных | 1975 |
|
SU581874A3 |
| Способ получения производных 16-метилпрегн-16-ен-20-она | 1986 |
|
SU1401864A1 |
| Способ получения 16,17-замещенных 5 -бром-6 фтор-21-ацетоксипрегнанонов-20 | 1972 |
|
SU438262A1 |
| 6 -Фторциклогексано (1",2",16 ,17 ) -прегн-4-ен-3,20-дион,обладающий гестагенной активностью и способ его получения | 1976 |
|
SU555116A1 |
| Способ получения 6,6-дифтор-11 , 16 ,17 -триокси -4 прегнен-3, 20-диона | 1972 |
|
SU438181A1 |


Авторы
Даты
1977-08-05—Публикация
1972-11-01—Подача