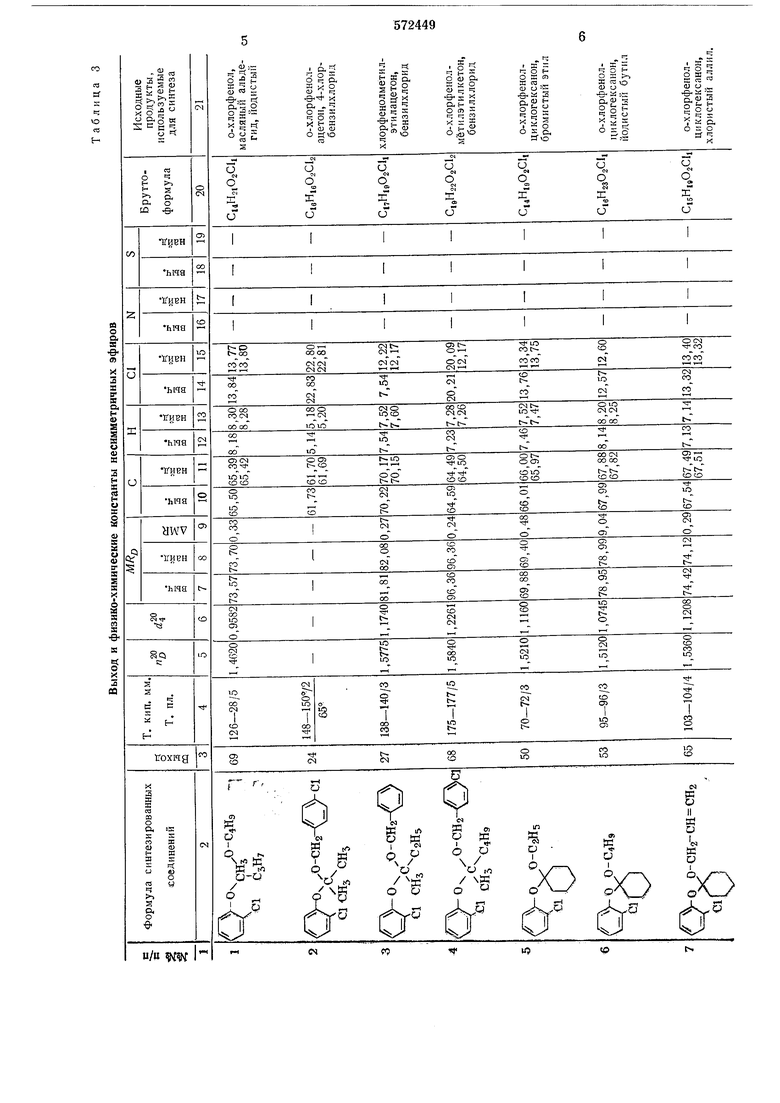
Изобретение Относится к новому способу получения неописанных в литературе фенилалкил- или фенилариловых эфиров гемгликолей, которые могут найти Нриме«ен«е в сельском хозяйстве. Известен способ получения фенилалкиловых или феНИларИловых эфиров метиленгликоля путем взаимодействия а-хлорметилфениловых эфиров с алкоголятами -или фенолятами в среде безводното адетона при температуре кипения :раствО|рителя 1. к- дНедостатком известного способа является использование а-галоидэфн.ров, которые являются малодоступными, что ограннчивает получение :неси1мметрнчных эфиров гемгликолей. Кроме того, имеет место низкий выход целевого продукта из-за образования побочпых симметричных эфиров. Предложенный способ иолучелия несиммстричных эфиров гемгликолей обгцей формулы I Целевой продукт выделяют известными приемами, например перегонкой в вакууме. Выход конечного продукта достигает 70% от теории. Данный способ позволяет получить несимметричные фенилалкиловые или фениларИловые эфиры гемгликолей п-ри Варьиров1ан1ии заместителей R, R,R в формуле I и оксосоедипепий, .в результате последовательных операций в одной системе, без обработки И выделения промежуточных продуктов. Предлагаемый способ иллюстрируется ниж е п p«iB еден н ы м и пр и м ер а мИ. Пример 1. Получение н-бутилового 2хлорфенилового эфира 1,1-|Циклогекоилиденгликоля. В трехгорлую реакционную колбу, снабженную механической мешалкой, капельной воронкой, термометром и водоотделением с обратным холодильником помещают 26 г (0,2 г-м) 2-хлорфенола, 150 мл бензола и лри псреА1СШИвании прикалывают 60% водный раствор едкого кали в количестве 20 г. Смесь при усиленном перемешивании нагрев ают в условиях конденсации бензола до прекращения выделения воды. Реакция длит.ся 3 часа. После выделения 11 мл воды отгоняют основную часть бензола и -к полученному безводному кристаллическому 2-хлорфеноляту калия прибавляют 50 мл (0,5 г-м) циклогексаHOiHa и смесь акеремеш.ивают в течение 1 ч при 90°С до полного растворения 2-хлорфе«олята -калия. К полученной массе добавляют 46 г (0,26 г-м) бутилиодида и смесь неремеш ивают при 80-90°С в течение 3 ч с последуюЩИм отделением в виде осадка, соли иодида калия, который затем промывают на фильтре циклогексаноном. Из фильтрата отгоняют бензол и цИКлогексанон при помощи водоструйного насоса, а остаток в количестве 100 г подвергают вакуумной (мм рт. ст.) перегонке. В табл. 1 нриведены фиэико-химические копстанты нолученного эфира. Т а б л II ц а 1


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ЧЕТВЕРТИЧНЫХ АММОНИЕВЫХСОЕДИНЕНИЙ | 1969 |
|
SU242177A1 |
| Способ выделения 2,4-дихлорфенола | 1982 |
|
SU1625862A1 |
| Способ получения производных интерфенилен-9-тиа-11-оксо-12-азапростановой кислоты | 1978 |
|
SU952104A3 |
| Способ получения 4-циано-2,3,5,6тетрафтордифениловых эфиров | 1975 |
|
SU614085A1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-МЕТОКСИИЗОБУТИЛИЗОЦИАНИДА | 1990 |
|
RU2026857C1 |
| СПОСОБ ПОЛУЧЕНИЯ 2-ВИНИЛПИРИДИНА | 1973 |
|
SU379572A1 |
| Способ получения несимметричных ацеталей амидов кислот | 1977 |
|
SU732236A1 |
| Способ получения моноэфиров гексадииндиола-1,6 | 1973 |
|
SU447398A1 |
| Способ получения производных @ -дигалоидвинилциклопропана | 1978 |
|
SU1075972A3 |
| Способ получения бензофеноналкилкарбоновых кислот | 1975 |
|
SU645551A3 |

Результаты мнкроэлементного анализа. Пайдено. %: С 67,80; 67,82; Н 8, 20; 8,26; С1 12,60; 12,55.
Ci4H2l02Cli.
Вычислено, %: С 67,96; Н 8,14; С1 12,57.
Индивидуальность полученного целевого продукта установлена хроматографически. Анализ проводился на хроматографе ЛХМ7А. Длина колонки - 1 м. В качестве жидкой фазы использован полиэтиленгликоль-4000, нанесенный на кирнич ИНЗ-600 в количестве 5% детектора 190А. Выход целевого продукта в расчете на 2-хлорфенол составляет 35 г (62%), селективность процесса 100%.
Пример 2. Получение бензилового 2хлорфенилового эфира 1,1-циклогексилиденгликоля. В реакционную колбу, описанной выше установки, помещают 26 г (0,2 г-м) 2хлорфенола, 150 мл бензола и 12 г (0,2 г-м) сухого и непорошкообразного едкого кали. Смесь усиленно перемепгивают без нагрева в
течение 1 ч (20-45°). Затем перемещивание продолжают при нагревании в условиях конденсации бензола до прекращения выделения
воды. Реакция длится 2 ч и за это время выделяется 4 мл воды. Затем отгоняют основную часть бензола и к полученному безводному 2-хлорфеноляту калия прибавляют 70 г (0,7 г-м) циклогексанона. К полученной жидкости по каплям прибавляют 26 г (0,2 г-м) бензилхлорида и смесь перемешивают при 80-90°С в течение 3 ч. В охлажденную реакционную смесь добавляют 250 мл бензола и смесь при перемешивании разлагают водой.
Верхний слой отделяют от нилснего водного слоя, и который один раз экстрагируют бензолом и соединяют с верхним слоем. Органический слой два раза промывают 5%-ным водным раствором едкого кали и один раз
водой, после чего сушат над безводным Na2S04. После сущки и отгонки растворителя остаток в количестве 97 г перегоняют под вакуумом. В табл. 2 приведены физико-химические константы полученного эфира.
Таблица 2
Результаты микроэлементарного анализа: Найдено, %: С 72,00; 71,98; Н 6,70; 6,75; С1 11,07; 11,03.
Ci9H2lO2Cli.
Вычислено, %: С 72,04; Н 6,63; С1 11,22.
Индивидуальность полученного целевого продукта установлена хроматографически. Анализ ироводился на хроматографе ЛХМ7А. При вышеописанных условиях выход целевого эфира в расчете на о-хлорфенол составляет 38 г (60%).
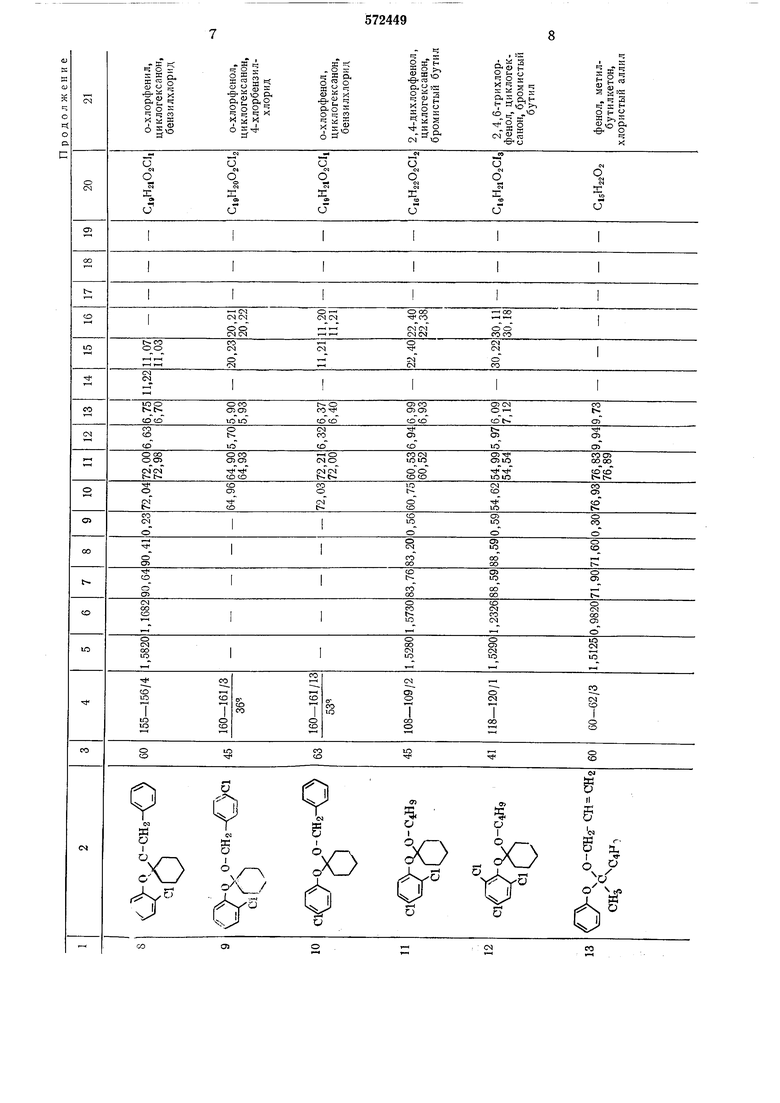
Выход и физико-химические константы несимметричных эфиров гемгликолей представляют в табл. 3.
Формула изобрет-еиия
Способ получения несимметричных эфиров гемгликолей общей формулы
As ,OR
R
где R,R-H,C1,
R-CjHs.-CiHgj-CHs™KD -СИг-СН ОН2
iNO2;
Д- f tifпород uflu epQ X-H, CHj-, - -алкид
ИЛИ X И Y
вместе с атомом углерода, с которым они связаны, представляют циклогексил, отличающийся тем, что соответствующий фенолят щелочного металла подвергают взаимодействию с оксосоединеннем в безводной среде, полученный при этом продукт обрабатывают алкил- или арилгалогенидом в бензоле при 80-90°С с выделением целевого
продукта.
Источники информации, принятые во внимание при экспертизе

Авторы
Даты
1977-09-15—Публикация
1975-07-17—Подача