г)удельное вращение 54 , (с - 0,2 метанол), определяемое при 25°С; д)ИК - спектр поглощения в хлороформе ее следующими максимумами поглощения; 2,85; 3,34; 5,83; 6,84; 7,22; 7,53 (слабый), 5,78 (слабый), 8,76 (сильный), 8,95 (сильный),9,15; 9,50 (сильный), 9,55 (сильный), 9,60; 9,85; 10,15; 10,45 и 10,70 (слабый) мк; е)в его УФ - спектре в этаноле только концевое поглощение ниже 200 ммк; ж)спектр ЯМР в дейтерохлороформе со следующими характеристиками: 66,01; 4,21; 4,11; 3,99; 3,89; 3,80; 3,67; 3,65; 3,57; 3,55; 2,83; 2,66; 2,58; 2,56; 2,30; 2,22; 1,96; 1,90; 1,85; 1,70; 1,62; 1,31; 1,25; 1,18; 0,95; 0,93; 0,77; 0,75; 0,73; 0,68 и 0,66 ч/млн; з) титруемую группу при величине рКд 7,9 в 80% - ном водном диметипформамиде; и) рентгенограмму, полученную методом дифракции рентгеновых лучей на образце в порошке (Си - радиация, 1,5405Х, никелевый фильтр), имеющую следующие межплоскостные расстояния j в ангстремах (d); Значение Rf 0,11 Вода, насыщенная 0,41 Вода,насыщенная кислоты и 1 % пип Вода- метанол-ац NH4OH до рН 10,5 1% МИБК, 0,5% Ы 17,4 г К2НР04, 30 Бензол, насыщенн Вода Вода-МИБК-этил м) кислотную функцию, способную образовать соли и эфир; н) одну по крайней мере гидроксильную группу, способную к этерификации. Изобретение предусматривает также.Cj-Cs -ациловые эфиры и физиологически приемлемые соли этих факторов. II. Фактор В антибиотика А-28086 - кристаллическое соединение белого цвета, когда кристаллизовано из смеси ацетона и воды, растворимо в низших спиртах, диметилформамиде, диметилсульфоксиде, этнлацетате, хлороформе, ацетоне и бензоле; но мало растворимо в гексане и нерастворимо в воде. Соединение имеет следующие характеристики: а)Т.ПЛ. 150-153С; б)молекулярный вес 762, определяемый масс спектрометрией с высоким разрешением; в)эмпирическую формулу С4зН-;оО11. определяемую масс - спектрометрией с высоким разрещением;г)ИК - спектр в хлороформе со следующими различными максимумами поглощения: ,82; 3,30; Система рас dОтносительная интенсивность 12,00100 10,1050 9,2590 8,0040 7,5015 6,9290 6,4040 5,9805 5,6815 5.2040 4,9840 4,6240 4.2120 3,4810 к) Rf 0,24 при хроматографии в тонком слое на силикагеле в системе растворителя бензол-этилацетат (3:2) с применением Bacillus subtilis АТСС 6633 в качестве обнаруживающего организма; л) значение RfjB указанных ниже системах при хроматографии на бумаге с применением Bacillus subtilis АТСС 6633 в качестве обнаруживающего организма: ителя илизобутилкетоном (МИБК) К, плюс 2% паратолуолсульфоина(12:3:1) с добавлением ем НзГО4 до рН 7,5 в воде этанола на литр воды одой ат (98:1:1) ,77; 5,85; б,80; 7,20; 7,50 (слабый), 7,72 (сла8,57 (сильный), 8,68; ый), 7,80 (слабый), 9,50;9,83 (сильный), 9,90; ,90 (сильный), 9,10; 10,43 (слабый), 0,10; 10,17 (сильный), 11,35 (слабый). 0,80 (слабый), 11,20 (слабый), 11,73 (слабый) и 12,03 (слабый) мк; д) наблюдаемый максимум в этаноле в его УФ пектре при 220 ммк (E 137,5; ,477); е) спектр ЯМР в дейтерохлороформе со слеующими характеристиками: 5 7,20; 7,09; 6,26; 6,15; 4,19; 4,12; 4,05; 3,95; 3,89 3,52; 3,48; 2,81; 1,91; 1,84; 1,71; 1,18; 1,11; 0.96: 0,94; 0,90; 0,74 и 0,68 ч/млн; ж)величину fif 0,42 при хроматографии в тонком слое на силикагеле в смеси бензол - этилацетат (3.2) с применением Bacillus subtilis АТСС 6633 в качестве обнаруживающего организма;з)величины Rf в указанных ниже системах при хроматографии на бумаге с применением Bacillus subtilis АТСС 6633 в качестве обнаруживающего организма: G
RfСистема растворителя
Вода, насыщенная МИБК, плюс 2% паратолуолсульфокислоты
и 1% пиперидина Вода-метанол-ацетон (12:3:1) с добавлением
NH40H до рН 10,5, затем НзР04 до
рН7,5
1%МИБК, 0,5% NH40H в воде
Бензол, насыщенный водой
Вода
Вода-МИБК-этилацетат (98:1:1) и) кислотную функцию, способную образоват соли и эфиры; к) две кетогруппы; л) одну по крайней мере гадроксильнуг группу. Предусмотрены и физиологически приемлемые соли фактора, III. Фактор D антибиотика А - 28086 - кристаллическое соединение белого цвета, когда кристаллизовано из смеси ацетона и воды, растворимое в метаноле, этаноле, диметилформамиде, диметилсульфоксвде, этилацетате, хлороформе, ацетоне и бензоле, но только мало растворимое в гексане и нерастворимое в воде; т.пл. 96-98°С. Соединение имеет следующие характеристики: а)молекулярный вес 778, определяемый массспектрометрией высокого разрешения; б)примерный элементарный состав: 67,59% углерода, 9,38% водорода и 22,77% кислорода; в)эмпирическую формулу C4 H740i 1, определяемую - спектрометрией высокого разрешения;г)удельное вращение - 56° (с 0,1 метанол) , определяемое при 25° С; д)ИК - спектр в хлороформе со следующими максимумами поглощения: 2,89; 3,39; 3,43; 3,50; 5,88; 6,90; 7,25; 7,60; 7,84; 9,00; 9,26; 10,31; 10,58; 11,10 и 11,49 мк; е)УФ - поглощение в 95%-ном водном этаноле не наблюдается; ж)спектр ЯМР в хлороформе со следующими характеристиками:5 6,00; 4,20; 4,10; 4,00; 3,98; 3,92; 3,86; 3,83; 3,79; 3,67; 3,64; 3,57; 3,54; 2,88; 2,81; 2,71; 2,62; 2,58; 2,48; 2,37; 2,29; 2,21; 2,15; 2,10; 2,04; 1, 1,89; 1,83; 1,76; 1,68; 1,61; 1,58; 1,55; 1,47; 1,39; 1,30; 1,25; 1,18; 0.95; 0,90; 0,88; 0,84; 0,74 и 0,68 ч/млн; Значение Rf Вода, насьц 0,10 Вода, насы 0,26 и 10% пипе Вода-мета NH4OH до до рН7,5 1% МИБК, 17,4 г К2Н Бензол, на
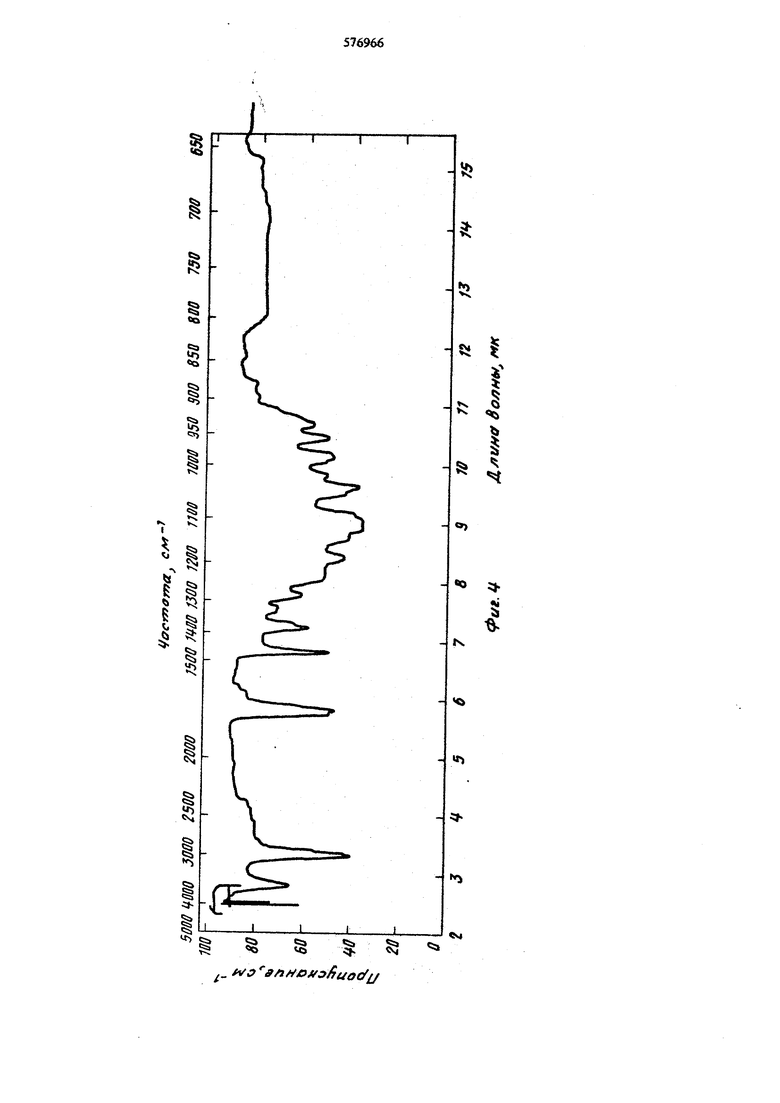
576966 з) титруемую группу с величино1 рКс 8,67 в 80%-ном вЬдном диметилформамиде; и) рентгенограмму, полученную методом дифракции рентгеновых лучей на образце в порошке ( радиация, 1,5405Х, никелевый фильтр), имеющую следующие межплоскостные расстоя1шя, в ангс:фемах (d): Относительная интенсивность 100 к) значения Rf в указанных ниже системах при хроматографии в тонком слое в силикагеле с применением Bacillus subtilis АТСС 6633 в качестве обнаруживающего организма: Значение RfСистема растворителя 0,26Бензол-этилацетат (3:2) 0,66Этилацетат-диэтнламин(95:5) л) значения Rf в указанных 1шже системах при хроматографии на бумаге с применение Вас1Ии$ subtilis АТСС 6633 в качестве обнаруживающего организма: ма растворителя я метшшзобутилкетоном (МИБК) я МИБК, плюс 2% паратолуолсульфокислоты а цетон (12:3:1) с добавлением ,5, затем НзР04 H4OH в воде 0 мл этанола на литр воды ный водой м) кислотную функцию, способную образоват;соли и эфиры; и) по крайней мере одну гидроксильную групну, способную к этерификации. Прегцусмотрены и Cj-Cg - аниловые эфиры и физиологически приемлемые соли этого фактора. Факторы А,В и D антибиотика А - 28086 Лвые члены группы полиэфирных антибиотиков. К членам этой гру1П1ы относятся монерпзин, дианэмицин (нигерцин) и салиномицин. Термин антибиотический комплекс означает смесь совместно ; образующихся индивидуальных антибиотических факторов. Отношение ИНДИЕЙдуальных получаемых факторов в антибиотическом комплексе может изменяться в зависимости от примене1шых условий брожения. Комплекс антибиотика А - 28086 получают при выращивании нового штамма Streptomyces aureofaciuns-NRRL 5758 при брожении в аэробных условиях в толстом слое до достижения значительного уровня антибиотической активности. Этот антибиоти получают также при вырашивании еще одного нового штамма Streptomyces aureofaciens NRRL 8092. Полученный|с помощью S.aureofaciens NRRL 5758 или S.aureofaciens NRRL 8082 антибиотик экстрагируют из бродильного бульона и отделяют от мицелия полярнык-ш органическими растворителями. Экстрагированную смесь разделяют при концентрировании растворов, добавлении к концентрату петролейного эфира для осаждения посторонних примесей с последующим фильтрованием и выпариванием фильтрата до получения смеси антибиотика А - 28086. Эту смесь дополнительно очищают и разделяют на индивидуальные факторь методом хроматографии на колонке. Содинения А - 28086 замедляют рост орга газмоЕ, патогенных для животных и растений. Соединегая А - 28086 являются агентами, замедляющими рост кокцидий и, кроме того, они являются антибакте альными,антивирусными;,активнымипротив органи мов, вызывающих пневмонии, инсектициднь1ми акарицидными агентами, а также веществами, повьпШющими эффективность использования корма жвачными животными. На фиг. 1-8 изображены ИК - спектры поглощения в хлороформе. На фиг. 1 - фактора А антибиотика А - 28086; на фиг. 2 - фактора В антибиотика А - 28086; на фиг.-З - ацетилового эфира фактора А антибиотика А- 28086; на фиг. 4 - пропионилового эфира фак-тора А антибиотика А - 28086; на фиг. 5 - бутириловс го эфира фактора А антибиотика А - 28086; на фиг. 6 - валерилового эфира фактора А антибиотика А - 28086; на фиг. 7 - капроилового эфира фактора А антибиотика А - 28086 и на фиг. 8 - ИК -спектр поглощения фактора D антибиотика А - 28086. Ь v БК-этилацетат (98:1:1) Факторы А - 28086 структурно похожи друг на яруга. Во время брожения совместно образуются по крайней мере четыре фактора в BH/te смеси. Факторы отделяют один от другого и факторы А,В нО вьщеляют в виде индивидуальных соединений. Смесь факторов А - 28086 растворима в больнгей части органических растворителей , но нерастворима в воде. Фактор А кристаллизуют из смеси ацетона и водь1. Он имеет температуру плавления У8100° С, отверждается и снова плавится при 195-200° С. ЭлементарньЕЙ анализ фактора А дает следующий состав: углерод 66,69%,водород9,85; и кислород 23,10%. Эмпирическая формула этого фактора С4зН72011 Фактор А имеет молекулярный вес приблизительно 764, определяемый масс - спектрометрией. На фиг. 1 показан ИК - спектр фактора А. Наблюдались следующие максимумь поглощения: 2,85; 3,34; 5,83; 6,82; 7,22; 7,5з (слабый), 7,78 (слабый), 8,75 (сильный), 8,95 (сильный), 9,15; 9,50 (сильный), 9,55 (сильный), 9,60; 9,85; 10,15; 10,45 и 10,70 (слабый) мк. . УФ - спектр фактора А в этаноле показывает только концевое поглощение ниже 220 ммк. Спектр ЯМР фактора А в дейтерохлороформе показал следующие характеристики: 66,01; 4,21; 4,11; 3,99; 3,89; 3,80; 3,67; 3,65; 3,57; 3,55; 2,83; 2,76; 2,74; 2,68; 2,66; 2,58; 2,56; 2,30; 2,22; 2,17; 2,10; 2,05; 1,96; 1,90; 1,85; 1,70; 1,62; 1,60; 1,47; 1,39; 1,31; 1,25; 1,18; 0,95; 0,93; 0,90; 0,88; 0,85; 0,77; 0,75; 0,73; 0,68 и 0,66 ч/млн. Фактор А, кристаллизованный из смеси ацетона и воды. Имел следующую рентгенограмму, полученную методом дифракции рентгеновых лучей на образце в порошке ( радиаиля, 1,5405Х, никелевый фильтр, d - межплоскостное расстоя гие а ангстремах): dОтносительная интенсивность 12,00100 10,1050 Удельное вращение фактора А -- 54° (с 0,2 метанол) , определяемое при 25° С.
Электрометрическое титрование фактора А в 80% - ном водном растворе диметилформамида показывает присутствие титруемой группы с рК 7,9.
Фактор А растворим в таких органических растворителях, как метанол, этанол, диметилформамид, диметилсульфоксид, этилацетат, хлороформ, ацетон и бензол, но мало растворим в таких непопярных органических растворителях, как гексан, и не растворяется в воде.
Фактор А антибиотика А 28086 имеет кислотную функцию, способную к образованию солей и эфиров, а также по крайней мере одну гидроксильную группу, способную этерифицироваться.
Фактор В антибиотика А - 28086 - кристаллическое соединение белого цвета (при кристаллизации из смеси ацетона и воды), имеет т.пл. 150 Ч53° С.
Масс - спектрометрией с высоким разрешением установлено, что фактор В имеет молекулярный вес приблизительно 762 и предполагаемую змпиричесКуЮ формулу С4зН7о011.
На фиг. 2 показан ИК - спектр фактора В в хлороформе. Наблюдались следующие максимумы поглощения: 2,82; 3,30; 5,77; 5,85; 6,80; 7,20; 7,50 (слабый), 7,72,(слабый), 7,80 (слабый), 8,67 (сильный), 8,68;8,90 (сильный), 9,10; 9,50; 9,83 (сильный), 9,90; 10,10; 10,17 (сильный), 10,43 (слабый), 10,80 (слабый), 10,20 (слабый), 11,35 (слабый), 11,73 (слабый) и 12,03 (слабый) мк
УФ спектр фактора В в этаноле показьшает максимумы поглощения при 220 ммк (Е 137,5; ,477).
Спектр ЯМР фактора В в дейтерохлороформе показал следующие характеристики; 6 7,20; 7,09; 6,26; 6,15; 4,19; 4,12; 4,05; 3,95; 3,89; 3,78; 3,62; 3,59; 3,52; 3,48; 2,81; 2,73; 2,63; 2,54; 2,52; 1,99; 1,91; 1,84; 1,71; 1,64; 1,55; 1,43; 1,33; 1,18; 1,11; 0,96; 0,94; 0,90; 0,87; 0,77; 0,74 и 0,68 ч/млн. .
Фактор В антибиотика А - 28086 растворим в таких органических растворителях, как, например, метанол, этанол, диметилформамид, диметилсульфоксид, этилацетат, хлороформ, ацетон и бензол; мало растворим в неполярных растворителях, например в гексане, и непастворим в воде.
Хотя химическая структура фактора В не выяснена однако физические и химические свойства показывают, что фактор В имеет одну группу карбоновой кислоты, две кетонные группы и одну или более гидроксильных групп.
При получении с помощью S, aureofaciens NRRL 8092 фактор D составляет до 10% вьщеленной антибиотической активности; при получении с помощью S. aureofaciens NRRL 5758 он является наименьшим из факторов..
Фактор D антибиотика А - 28086 - кристаллический продукт белого цвета ( при кристаллизации из смеси воды и ацетона) с т.пл. 96-98° С. Кажуищйся молекуля1: 1п,1й вес 778 (определяется массспектрометрией с высоким разрешением). Элементарный состав пика в масс-спектре натриевой соли фактора D 800,5050 (вьпшслено для €44473011 800,5050). В масс - спектре фактора О
в форме свободной кислоты наблюдали небольшой максимум при 778 и больший максимум при 760, 5117 ( вычислено для C44H720io ); м/з 760 в масс - спектре свободной кислоты является результатом потери воды из молекулярного
иона. Поэтому состав молекулярного ио1И фактора D в форме свободной кислоты C44H74Ol 1
Предполагаемая эмпирическая формула фактора D C44H740i 1 Элементарный анализ фактрра D дал следуюшлй состав: 67,59% углерода, 9% водорода и 22,77% кислорода.
Теоретически для C44H74Oi i требуется 67,87% углерода, 9,51% водорода и 22,77% кислорода.
Фактор D в 95%
ном водном этаноле не поглощает УФ лучей.
Спектр ЯМР фактора D в дейтерохлороформе имеет следующие характеристики: 5 6,00; 4,20;
3,67; 4,10; 4,00; 3.98; 3,92; 3,86; 3,83; 3,79;
2,71; 3,64; 3,57; 3,54; 2,88; 2,91; 2,62; 2,58; 2,48; 2,43; 2,37; 2,29; 2,21; 2,10; 2,04; 2Д5; 1,97; 1,89; 1,83; 1,76; 1,68; 1,58; 1,55; 1,61; 1,47; 1,39; 1,30; 1,,18; 0,90; 0,88; 0,95; 0,84; 0,74 и 0,68 ч/млн.
Фактор D, кристаллизованный из смеси ацетона и воды, имеет следующую рентгенограмму, полученную методом дифракции рентгеновых лучей на образце в порошке (Си - радиация, 1,5405 X, никелевый фильтр), d - межплоскостное расстояние в ангстремах:
dОтносительная
интенсивность
100 70 90 30 10
100 20 20 20 10 20 40 30 10 10 05 05 05
Удельное вращение фактора D - 56 (с - 0,1 метанол) , определяемое при температуре
Электрометрическое титрование фактора в 80% ном водном диметилформамвде показало присутствие группы с рКа 8,67. Фактор D растворим в таких оргаяинорителях, как метанол, этанол, диметелферЛ:я диметилсульфоксид, этилацетат, хлороформ, ац и бензол; мало растворим в таких неполяр органических растворителях, как, например, сан, и нерастворим в воде. Фактор D имеет кислотную функцию, спо Т сличина Rf фактор А фактор В бактор D 0,11 0,09 0,410,160,26 0,540,460,36 0,480,360,39 0,150,33 . 0,25 0,240,510,26 0,240,110,09 0,750,610,64 Величины Rf для факторов А, В и D в двух системах при хроматографии в тонком слое на силикагеле (предварительно покрытые пластины Величина Rf ФакюрА факторов факторЮ 0,240,420,26 0,540,340,66 Одновременно с комплексом антибиотика А-28086 образуется другое вещество, произвольно названное А-28086-1. Это вещество, не активное микробиологически, структурно родственно факторам антибиотика А-28086, А -28086 - 1 - кристаллическое соединение белого цвета (при кристаллизации из смеси ацетона и воды) имеет т.пл. 160-162° С. Сравнительное исследование спектров ЯМР и других свойств А -28086 - 1 и синтетически приготовленного метилового эфира фактора А доказьгеают, что А - 28086 представляет собой метиловьш эфир фактора А или очень близкое соединение, т.е. стереоизомер. Хотя А - 28086 - 1 осаждается совместно с активными факторами антибиотика А - 28086, однако он легко отделяется хроматографией на ошикагеле. А - 28086 - 1 имеет величину Rf, равную примерно 0,53 при хроматографии в тонком слое на силикагеле с этиладетатом в качестве элюента и при применении винилового реагента для опрыскивания (3% ванилина в метаноле плюс 0,5 мл концентрированной серной кислоты на Шбмл раствора) с целью обнаружения. После опрыскивания винилином и нагревания А - 28086 - 1 дает синее пятно, в то время как факторы антибиотика А - 28086 дают яркие розовые пятна, которые быстро становятся темными, коричневатосиними. Факторы А, В и D, а также указанные эфиры карбоновой кислоты и факторов А и D способны Сис Бен Эти гую образовать соли и фиры и но крайней мере одну гидроксильную группу, способную этерифини МЩ; роваться. етон Значения ,Rf факторов А, В и D в разных систеныхмах хроматографии на бумаге с применением гекBacillus subtilis АТСС 6633 в качестве обнаружисобвающего организма, показаны ниже. Система растворителя Вода, насыщенная мети)шзобутилкетоном (МИБК) Вода, насыщенная МИБК, плюс 2% наратолуолсульфокислоты и }% пиперидина Вода-метанол-ацетон (12:3:1) при добавлении NH40H установлено, а затем снижено до рН 7,5 НзРО4. 1%МИБК,0,5%МН40Нвводе 17,4 г К2НР04,30 мл этанола в литре воды Бензол j насыщенный водой Вода Вода-МИБК-этилацетат (98:1:1). .Мерк, Дармщтат Г - 254, толщина слоя 0,25 см) ри применении В. subtilis АТСС 6633 в качестве бнаруживающего организма с едующие. астворителя тилацетат (3 : 2) ат-диэтиламин (95 : 5) образов ьшать соли Физиологически приемлемыми солями, которые приемлемы также как фармацевтические средства, являются соли, у которых токсичность в отношении теплокровных животных не превыщает токсичности несолевой формы соединений. Пригодными солями факторов А и В являются соли натрия, калия, лития, дезия, рубидия, бария, кальция и магния. К пригодным аминовым солям факторов А и В относятся соли аммония, первичного, вторичного к третичного Ci-С4 - алкиламмония и окси - - алкиламмония. Сояи щелочных и щелочноземельных металлов факторов А, В и D: также ациловые эфиры факторов А и D получают обычными способами приготовления солей. Например, фактор в форме свободной кислоты или эфира растворяют в подходящем растворителе, например теплом метаноле или этаноле, и к раствору добавляют раствор, содержащий стехиометрическое количество неорганического основания в водном метаноле. Полученную соль можно выделить обычными способами, например фильтроBaiffleM или выпариванием растворителя. Таким же способом можно получать соли с органическими аминами. Например, газообразньш или жидкий амин можно добавить к раствору фактора в подходящем растворителе, например ацетоне, а затем выпарить растворитель и избыток амина. Формулу соли можно выбирать в записимости от упобсгва применения, токсичносги и 3jcoномии. Фактор А образует эфиры карбоновых кислот. Этерификация происходит у одной из гидроксильных групп фактора А при обработке ангидридом или хлорангидридом Cj -С кислоты. Такие эфиры обычно получают при реакции фактора А с соответствующим ангидридом кислоты при комнатной температуре. Такие эфиры также пригодны в качестве антибиотиков и агентов, повышающих эффективность использования корма. Ацетиловый эфир фактора А - кристаллическое соедине1ше белого цвета (при кристаллизации иэ смеси ацетона и воды) имеет т.пл. 100-103 С и эмпирическую формулу €4 j Н, г Молекулярный вес его равен примерно 807 в соответствии с эмпирической формулой, предложенной для фактора А. Элементарный анализ ацетилового эфира фактора А дает следующий процентный состав: Вычислено,% С 66,97; Н 9,24; О 23,79. C4sH74O| 1 Найдено,%: С 67,67; Н 8,71; О 23,13. ИК - спектр ацетилового эфира фактора А в хлороформе показан на фиг. 3. Наблюдались следующие максимумы поглощения: 2,85; 3,36; 3,38 (сильный), 5,80; 6,83; ./7,25 (сильный), 7,60 (слабый), 7,80 (сильный), 8,45 (сильный) 8,80 (сильный), 8,95 (сильный), 9,10 (сильный), 8 20; 9, 9,80.(сильный), 10,12 (слабый) и 10,50 мк. УФ - шектр (фактора А ацетилового эфира) в этаноле показывает только концевое поглощение. Электрометрическое титрование ацетилового эфира фактора А в 80% - ном водном диметилформамиде показывает присутствие титруемой груП|ПЫ с рКа 8,5. Пропиониловый эфир фактора А - кристаллическое вещество белого цвета (при кристаллизации из смеси ацетона и воды) с т.пл. около 96-98° С. Пропиониловый эфир фактора А имеет эмпирическую формулу C47H7sOij и молекулярный вес около 821, вычисленный по эмпирической формуле, предложенной для фактора А. Элементарный анализ пропионилового эфира фактора А дал следующий процентный состав: Вычислено,%: С67,29; Н9,33; О 23,38 С4бН7бО,, Найдено,%: С 66,06; Н 9,17; О 23,41. ИК - спектр пропионилового эфира фактора А в хлороформе показан на фиг. 4. Наблюдались следующие максимумы поглоще1шя: 2,85; 3,33; 3,38 (сильный), 3,45 (сильный), 5,75 (сильный), 5,82; 6,81; 7,22; 7,30 (сильный), 7,50 (слабый), 7,60 (слабый), 7,80; 8,43; 8,75 (сильный), 8,90; 9,05; 9,15 (сильный), 9,50 (сильный), 9,63; 9,83 (слабый), 10,05 (сильный), 10,13; 10,20 (сильный) ; 10,45 и 10,68 мк. УФ - спектр пропио1шлового эфира фактора А в этаноле показал только концевое погло1це1ше. Бутнриловый эфир фактора А - кристаллическое соедииеш1е белого цвета (при крнстял,чи:иции из смеси ацетона и воды) с т.пл. с.коло96-98С. Этот эфир имеет эмпирическуто формулу C47H-)gOij, молекулярный вес около 835 и примерный состав:С67,60%,П 9.41%, 022,397г., вычисленный по эмпирической формуле факто{1а А. ИК - спектр бутирилового эфира фактора А в хлороформе показан на фиг. 5. Максимумы поглощения следующие: 2,89; 3,40; 3,45; 3,51; 5,85; 5,92 (сильный), 5,97 (сильный), 6.90; 7.30; 7,84 (слабый), 8.55; 8,85 (слабый), 9,01 (сильный),9,26; 9,76; 9,95; 10,31 и 10,64мк. Валериловый эфир из фактор гА и валериановой кислоты - кристаллическое соединение белого цвета (при кристаллизации из смеси ацето1и и воды) с Т.ПЛ. около 173 - 175°С имеет эмпирическую формулу G48HgoOij, молекулярный вес около 849 и примерный состав: С 67,89%; Н 9,50%; О 22,61%, как вычислено по предложенной эмпирической формуле фактора А антибиотика А - 28086. ИК - спектр валерилового эфира фактора А в хлороформе показан на фиг. 6. Максимумы поглощения следующие: 2,90; 3,40; 3,45; 3,51; 5,87; 5,92 (сильньп), 5,99 (сильный), 6,81; 7,30; 7,69 (слабый), 7,87 (слабый), 8,16; 8, 8,85 (слабьга),9,26; 9,76; 10,00 (слабый), 10,31 и 10,64 мк. Эфир капроновой кислоты и фактора А, капрсяловый эфир - кристаллическое соединение белого цвета (при кристаллизащда из смеси ацетона и войы) с т.пл. около 163-167° С имеет эмпирическую формулу C49H82Oj2, молекулярный вес около 863 и примерный состав: С 68,18%; Н9,58%; О 22,24%, определенньп1 по эмпирической формуле фактора А. ИК - спектр капроилового фактора А показан m фиг. 7. Максимумы поглощения:2,90; 3,40; 3,45; 3,51; 5,87; 5,92 (сильный), 5,97 (сильный), 6,90; 7,30; 7,66 (слабый), 7,84 (слабьш), 8,16; 8,58; 8,85 (слабый), 9,05 (сильный), 9,17; 9,72; 9,96; 10,29 и 10,62 мк. ИК спектр фактора D (фиг. 8) имеет следующие максимумы поглощения: 2,89; 3,39; 3,43; 3,50; 5,88;6,90; 7,27; 7,60; 7,84;9,00; 9,26; 9,62; 10,31; 10,57; 11,10 и 11,49 мк. В результате ацилирования фактора А происходят следующие изменения спектра I ядерного магнитного резонанса: карбо1шльный резошнс, происходящий примерно при 4 ч/млн, перемещается примерно до 5,3 ч/млн ( точное положение немного изменяется в разных ацилпроизвощ ых); смещаются также сигналы виниппротона. Эти характерные изменения представлены в частнч ой структуре: и где R представляет Ci - -Cs - алкнл. Эти частичные ст.уктуры полностью соответствуют aKcnopiiNiemaM но1 roNioMo;ieK ;iHpnoMv разъединению и ЯМР - шектру 13 зфйрйз уьссусяс; и пропионовой . ятттьа эфир фактора А растворим в таких органичесясих расгворитёлях, как метанол этанол, диметияформамид, даметилсульфоксид этилацетат, | хлороформ, ацепш и беиэоп, но мало рассорим в I неполярных i органических раствори телях, например в гексане, и {«растворим в воде. Каждый Cj-Сб - ацеловый эфир антибиотика А -28086 имеет кислотную ф)гшсцию, шособнуго образовывать соли и эфиры. Новые анти&ютики получают при выращивании штамма Streptomycer aureofacJens, образувнцего А 28086 в аэробных условиях глубинным |способом подходящей питательной среде до образования зна чительной антибиотической активности- Антибиоти ки выделяют, используя разные, обычно приме няемые способы вьщеления и очисткиХарактеристика NRRL 5758 в разных средах. JSP|3 2 (дрожжевой экстрактсолодовый ркстракт) iSP/33 (овсяная мука) ISPj34 (неорганическая соль - крахмальный агар) JSPp5 (глицерин-асшрапшовый агар) Томатная паста - агар с овсяной мукой Глицерин-глициновьш агар Глюкоза аспарагиновый агар Пищевой агар Один из организмов, пригодных для приготовления антибиотиков А - 28086, был выделен из образца почвы, собра1шой на Арарате, Typimn. Этот opraiffl3M классифицирован как штамм Streptomy5 ces aureofaciens Дутгара. Культуры выращивали при 30° С в течении 14 дней, кроме особо отмеченных случаев. Характеристика штамма NRRL 5758, образующего А - 28086. {ОМорфология Гифы, образующие споры, состоят из блоков, петель и открьггых спиралей. Наблюдался также морфологический представитель типа рек тис эластичный. Споры короткие и щишндрические, 15 образуют I цепи из 10-50 спор. Размер спор 1,3 X 1,75 /;в пределах от 1,3 до 1,96 х 1,3 д. Поверхность cnoip, наблюдаемая с помощью злектронногс микроскопа, гладкая. Характеристика Обильный рост; обратная сторона желтая; воздугщп ш мицелий и спорообразование от удовлетворительного до хорощего; мицелий белый (w) 13 Ьа и темно - серый (Gy), 3ih; j нерастворимый пигмент. Рост хорощий; обратная сторона зеленовато желтая (11В2); удовлетворительный воздущный мицелий (Gy) темно-зеленый, 3ih; растворимый пигмент светло - коричневый. Обильный рост: обратная сторона светлая желтовато - коричневая (12Е5) ; воздущный мицелий и споры (w) пурпурные и белые 13 Ьа до (GV) светло- серых d нерастворимый пигмент. Рост хороший; обратная сторона светлая, желтовато - зеленая; хорошие воздупшьш мицелий и споры (Gy) желтовато - серые 2dc до светлых серовато - красновато коричневых 5fe; нерастворимый пигмент. Обильный рост; обратная сторона светлая, желтовато- коричневая (13Ш),воздушный мицелий и споры от удовлетворительных до хороших (w), от белого А до (Gy) средне - серого д. Растворимый пигмент светло - коричневый. Обильный рост; обратная сторона темная серовато - желтая (1216) ; хорощие воздушный мицелий и споры (У), светло - желтые 2dbj нерастворимьш пигмент. Обильный рост; обратная сторона серовато зеленовато- желтая (12Е2) обилие воздушного мицелия и спор (Gy) желтовато - серого цвета 2dc; светлый коричневый растворимый пигмент. Рост хороший; обратная сторона серовато желтая (12В2), цвет воздушного мицелия и спор не определен ввиду плохого развития; нерастворимый пигмент. АПШ Беннетга Агар с кальциевой солью яблочной кислоты Агар с раствором Чапек Агар Эмерсона Тнрозиновый агар Триптоново - дрожжев Организм NRRL 5758 определения некоторых стандартным способом.
Свойства Действие на молоко
Нитратное восстановление Пищевой желатин Образование меланинового пигмента на косом агаре с тирозином
пептон Дифко - дрожжевом экстракте - железо - косом агаре
на бульоне с триптоном и экстрактом Необходимая температура ISP среда 02 - косаясреда из щюжжевого и солодового экстрактов
Результаты опытов по определению утшгазавии углерода, проводимых с организмсм NRRL 5758, следующие. Для характеристаки роста применены следующие обозначения:
+ хороший рост положительное использование углерода;
(+) рост от плохого до удовлетворительного
(-) слабый рост, вероятно, без утилизации
- нет роста, нет утилизации.
Источник углерода
Реакция
-I- + + D - глюкоза L - арабиноза D- ксилоза D - фруктоза
+ Сахароза
Характеристики
Молоко пептонизировалось, белое кольцо; прозрачная область рыжевато- коричневая, рН 5,7.
Положительное Разжижение на 30% через 14 дней
Очень слабо положительная (пигмент через 4 дня)
Отрицательная Отрицательная
Хороший рост при 26-30°С; отличный рост и спорообразование при 37°С; слабый вегетативный рост при 45°С; красноватый растворимый пигмент.
D - манчитИзоинозитол
Рамноза+
Рафиноза-
Контроль, без углевода-
Второй новый организм, образующий А- 28086, был получен из S. aureofaciens NRRL 5758 путем селекционирования, сопровождаемого химической л утацией. Этот организм, идентифицирова1Шый как NRRL 8092, и классифицирован как разновидность Streptomyces aureofaciens Дуггара. Эта классификация была основана на результэтах исследования организме NRRL 8092 ранее описанными методами Классификации Streptomices в таких же условиях поста. Обильный рост; обратная сторона серовато желтая (1ЖЗ) ; скудные воздушный мнцелнй и споры (Gy) желтовато - серый 2dc; нерастворимый пигмент. Хороший рост; обратная сторона серовато коричневая (15С8); нет воздушного мицелия и спорообразования; коричневый растворимый пигмент. Рост хороший, цвет не определен ввиду плохого развития. Обильный рост; обратная сторона серовато - желтая (11,5), нет воздушного мицелия или спор; нерастворимый пигмент. Обильный рост; обратная сторона светлая, слквково- коричневая (14,5) обильные воздушный мицелий и споры от (w) Ь (центр) до (СУ) светлых коричневато-серых; 3fe (по краям) ; очень светло - коричневый растворимый пигмент. Слабый рост; цвет не определен. Характеристика штам щего А 28086 Морфо В питательной среце 1S культура образует ред образом короткие и пря ciiop состоит из не менее 10 Короткие прямые цепн сп Характернстика NRRL (дрожжевой и солодовый экстракт (овсяная мука) 15РД4 ( агар с неорганическими солями и к iSP/35 (агар с гшщери и аспарагином) Агар с томатной пастой и овсяной мукой Агар с глицерином н глицином Агар с глюкозой и аспарагином Пищевой агар Агар Беннета Агар с малеиновокислым кальцием Агар с раствором Агар Эмерсона Агар с тирозином щих средах: ISP/33 в агаре с раствором Чапека и ISP(35. Обильная коремня наблюдалась в агаре Эмерсона. Наблюдения с помощью электронного микроскопа производили на агаре с тирозином (18РД7) и на агаре с глюкозой и аспарагином. Споры были гладкие длиной от 1,2 до 2,0 и диаметром около 1,0 ac. Средний размер пор 1,,0мк. Характеристика Рост удовлетворительный; обратная сторона светлая, желтовато - коричневая (12Н8) ; удовлетворительный воздушный мицелий; плохое спорообразование; мицелий светло - серый; нерастворимый пигмент. Рост разбросанный; обратная сторона прозрачная; нет воздушного мицелия; нерастворимый пигмент. Рост умеренный; обратная сторона серовато желтая (11В2) ; скудньш воздушный мицелий и плохое спорообразова1ше; воздушный мицелий светлый, желтовато-серый; (10А1); нерастворимый пигмент. Рост умеренный; обратная сторона светло - желтая (10Р2) ; удовлетворчтельный воздушный мицелий; скудное спорообразование; мицелий белый (10А1); нерастворимый пигмент. Рост умеренный; обратная сторона сероватая зеленовато - желтая; воздушный мицелий удовлетворительный; средняя степень спорообразования: бледно - серая (55А2); нерастворимый пигмент. Обильный рост; обратная сторона серовато - желтая (11Е4),умере1Шый воздушный мицелий, белый (10А1); спорообразование не происходит; нерастворимый пигмент. Рост умеренный; обратная сторона светло - желтая (lOF): умеренный воздушный мицелий и такое же спорообразование, белый (10AI) мицелий; нерастворимый пигмент. Рост скудный, обратная сторона светло - желтая (10В2); нет воздушного мицелия; нерастворимый пигмент. Рост удовлетворительный; обратная сторона среды желтовато - пунцовая; очень скудный воздушный мицелий; спорообразование не происходит; нерастворимый пигме) т. Рост очеЯь скудный, просвечивающийся; нет воздушного мицелия; нерастворимый пигмент. Рост очень скудный; обратная сторона прозрачная; нет мицелия; нерастворимый пигмент. Рост умеренный; обратная сторона серовато - желтая (1115); пятнистый воздушный мицелий; спорообразования не происходит; нерастворимый пигмент. Рост умеренный; обратная сторона светлая желтовато - кортчневая (12Н6); умеренный возД5Ш1ньш мицелий, светлый слабо - серый край (53А2): центр почти белый; спорообразование 21 Агар с тряптоком и дрожжами Фкзиологические сдрцсгх Свойства Действие ш молоко Нитратное восстановле1ше Пищевой желатин Образование меланинового пигмента на косом агаре с тирозином -бульоне с трилтоном и дрожжевым экстрактом -морковной пробке -картофельной пробке Необходимая температу («SP/32); косая среда- {дрожжевой экстракт и солодовый экстракт Результаты опыте по определению ут углерода приведены ниже. Для указаияя с роста использованы следувопще обозна%в хороший рост; положятелыоя утшшзац (+) рост от плохого до удовлетворительн (-) слабый рост, вероятж), без утшшзащш нет роста, нет упигазащга. Источник углеродаРезу D - глюкоза+ с. - арабиноза-iNRRL 5758
Желтый иа нескольких средах
Стрллылк спорофоры на среде из пасты томатной и овсяной муки; и на среде: неорганические соли крахмал
Рост удовлетворительный, коричневьш с просветлением
Умеренное спорообразование| воздушный мицелий
NRRL 8092
От кремового до светло - желтого цвета
на нескольких средах.
Короткие прямые спорофоры
и случайные крючки
Рост скудный, светлый, без просветлений
Скудное споробразование; мицелий светлый, желтовато - серьги 22 умеренное; нерастворимый пигмент. Рост очень скудный, просвечнвающийся; нет воздушного мицелия; нерзсгворнмын пигмент. NRRL 8092 Характеристики Пептонизнровалось (90%); светло:желтое кольцо; прозрачная область светло-желтая; Положительное Гидролизовался в течение 14 дней на 50% Очень слабо положитешоеи Отрицательная Обильный рост; светло - желтый; без воздушного мивдлия Обильный рост; серовато-белый; без воздушного мицелия, без изменения в пробке. При 25°С обильный рост; удовлетворительный воздушный мицелий; обратная сторона светло - коричневая нерастворимый пигмент. При 30° С обильный рост; удовлетворительный воздушный мицелий; обратная сторон светло - коричневая; нерастворимый пигмент. При 37° С обильный рост; удовлетворительный воздушный мицелий; обратная сторош коричневая; коричневый растворимый пигмент. При 40 С обильный рост; скудный в6з; цшшый мицелий i обратная сторона красновато-коричневая; растворимый пигмент красновато-коричневый. При 45°С удовлетворительный рост; без воздушного мицелия; обратная сторона красновато-коричневая; умеренный красновато-коричневый пигмент. 1У D - ксилоза+ D - фруктоза+ Сахароза- D - маннит- Изоинозитол+ Рамноза+ Рафиноза+ Контроль . без углевода Различия в свойствах организмаNRRL 5758 и ор ганизма NRRL 8092 показаны ниже:
Aiap Беннета
KyjtbTypbi Streptomyces aureofaciens, приходнпые для образования антибиотиков А - 28086, хранятся в коллекгдаи культур Северного исследовательского отдела торговли и питания Министерства сельского хозяйства США, Служба сельскохозяйственного исследования, Пеория, Иллинойс, 61604, номера NRRL 5758 и NRRL 8092.
Для выращивания Strepfomyces :aureofaciens NRRL 5758 или Strepfomyces aureofaciens NRRL 8092 можно использовать любую нз сред. Однако цля и1тимального выхода и легкого выделения продукта предпочтительны определе1шые среды. Например, предпочтительными источниками углеводов для процессов брожения в промышленном масштабе являются декстрин тапиоки и сахароза, хотя можно применять также глюкозу, маисовый крахмал, фруктозу, маннозу, мальтозу, лактозу и т.п. Пригощагми источниками углерода являются также кукурузное масло, арахисовое масло, соевое масло и рыбий жир. Предпочтителыйым источником азота является элзиматический гидролизат казенна, но пригодны также пептоны, соевая мука, мука {ХЛОПКОВЫХ семян, такие аминокислоты, как глу{Пминовая и т.п. К неорганическим солям, которые можно вводить в питательную среду, относятся обычные растворимые соли, способные образовьшать ионы хлорида, карбоната, сульфата, нитрата, натрия, магния, кальция, аммония и т.п.
Для роста и развития организмов в питательную Яреду необходимо включать также микроэлементы.
К питательной среде при ферментации в промышленном масштабе, еслн имеет место вспенивание, необходимо добавлять небольшие количества (т.е. 0,2 мл/л), противовспенивателя, например по: липропнленгликоля.
Количество антибиотика А - 28086, образуемого штаммом Streptomyces aureofaciens, увеличивается при добавлении к среде небольшого количества соевого масла.
Для получения значительных количеств антибиотиков А 28086 Желательно применять аэрацию питательной среды в бродильных чанах. Небольшие количества антибиотиков А - 28086 можно получать при выращивании культуры во встряхиваемой колбе. Так как при инокуляции в больших чанах спорами организмов образование антибиотиков сильно замедляется, то желательно применять вегетативный посевной материал. Такой материал приготовляют при инокуляции небольшого объема питательной среды спорами или обрывками мицелия организма для получения свежей, активно растущей культуры. Затем вегетативный инокулум переносят в большой чан. Для вегетативного роста посевного материала можно применять такую же среду, как используемая при брожегши в большом масштабе, но пригодны и другие среды.
or светло-фиолетового
до серого
Обратная сторона желтая j Обратная сторона розоная
Орга1шзмы, образующие А - 28086, можно выращивать при температуре в пределах примерно от 20 до 40° С. Оптимальный рост А - 28086 происходит, по видимому, при температуре от 27 до 30° С.
Обьтчно в процессах выращивания при аэробных условиях питательную среду продувают стерильным воздухом. Для эффективного роста организма предпочтительный объем воздуха, приме няемый в больших чанах, составляет больше одного Ьбъема на объем среды в минуту. Для эффективного образования антибиотиков А - 28086 в чанах желательно применять аэрацию больше 0,25 объема воздуха на объем питательной среды в минуту. Большие количества растворенного кислорода не ;тормозят юбразование антибиотика.
За образованием антибиотиков можно следить во время ферментации путем отбора проб бульона или экстрактов твердых веществ мицелия. В этих пробах определяют активность в отношении организмов, чувствительных к антибиотикам. Одним из организмов, пригодных для испытания антибиоти,ков данного изобретения, является Bacillus subtil is АТСС 6633. Испытание обычно производят с помощью бумажного диска на агаровых пластинках.
Первоначальная величина рН инокулированной питательной среды зависит от примене1шой среды. Вообще, рН должно быть в пределах от 6,0 до 7,5. В конце ферментации рН обычно несколько выще и пежит в пределах от 6,5 до 8,0.
Антибиотическая активность проявляется на второй день ферментации. Максимальная антибиотическая активность обычно достигается на шестой- седьмой день.
Образовавшиеся в результате брожения антибиотики А - 28086 можно выделять из бродильной среды обышыми способами. Антибиотической активностью обладают как мицелярная масса, так и профильтрованный бульон. Поэтому максимальное выделение антибиотиков А - 28086 достигается при комбинации фильтрования, экстракции и адсорбционной хроматографии. Предпочтительньтм растворителем для вьщеления этих антибиотиков из цельного или профильтрованного бродильного бульона является этилацетат, хотя можно применять и другие растворители, обычно используемые для этой цели.
Особенно выгодный способ вьщеления факторов А, В и D антибиотика А - 28086 состоит в снижении рН всего бродильного бульона примерно до рН 3,0. По этой величине рН факторы А,В и D обычно отделяют фильтрованием совместно с мицелярной массой. Другой способ выделения факторов А - 28086 связан с добавлением к цельному бу;тьону бикарбоната, например, бикарбоната натрия, в количестве равном примерно 1 г/л. Обычно факторы Л-2Я0 отделяют совместно с мицелярной массой в форме солей. Предяочгательным растворителем для отделения антибиотиков от мицелярной массы является кютанол, одндко пригодны и другое низшие спирты в кетоны. Для выделения антибиотиков А - 28086 с успехом можно применить азеотропную перегонку. В этом случае к водному бродильному бульону добавляют органический растворитель, образующий соответствуннций а: еотроп, и полученную смесь подвергают азеотропной перегонке для удаления по крайней мере половины воды из бульона. В результате остается смесь воды и растворителя, при этом антибиотики А 28086 растворены в органическом растворителе. Нерастворимые побочные продукты можно отделить подходящим способом, HanpHMejii, фильтрованием или центрифугированием. Затем антибиотики можнс выделить из органического раствора хорошо известными способами, например выпариванием растворителя, осаждением при добавлении нерастворителя или экстракцией. К органическим растворителям, образующим требуемые азеотропы с водой при процедуре вьщеления, относятся, например, бутиловый спирт, амиловый спирт, гексиловый спирт, бензиловый спирт, бутилацетат, амилацетат, 1,2 - дихлорэтан, 3 -пентанон, 2 - гексанон, бензол, циклогексанон, толуол, ксилолы и т.п. Азеотропная перегонка особенно выгодна при процессах брожения в большом масштабе. Воду и растворитель, отбираемые из верхней части колонны, можно разделять известными способами и возвращать для дальнейшего использования. Отделенная вода не содержит загрязнителей. Выделенный растворитель можно возвращать в процесс. Дальнейшая очистка антибиотиков А - 28086 включает дополнительную экстракцию и адсорбцию. В качестве адсорбентов можно использовать жишкагель, уголь, флорисил ( силикат магния фирмы Флоридин комп.) и т.п. С другой стороны, твердые вещества культуры, включая компоненты среды и мицелий, можно использовать без разделения, но предпочтительно после удаления воды, в качестве источника антибиотика А 28086. Например, питательную среду можно высушить ври лнофилизацик и смешать с кормом. С другой стороны, после окончания ферментации в питательной среде можно отделить мицелий и после сушки его пол чить продукт, используемый непосредственно для приготовления предварительной кормовой смеси. При отделении мицелия для этой цели добавка карбоната кальция (примерно 10 г/л) рбле1-чает фильтрование и дает сухой продукт лучшего качества. Штаммы Streptomyces aureofaciens, названные NRRL 5758 и NRRL 8092, образуют преимущественно фактор А антибиотика А - 28086. Хотя отношение факторов изменяется в зависимости от примененных условий брожения, но вообще фактор А составляет более 99% общей антибиотической активности, выделенной из NRRL 5758 и npiaiepHo 90% антибиотической активности, выделенной из NRRL 8092. Фактор В составляет большую часть остальной активности, выделенной из NRRL 5758, фак тор D является второстепенным. С другой стороны, фактор D составляет примерно 8-10% антибиотической активности, выделенной из NRRL 8092, а фактор В является второстепенным. Факторы А,В и D разделяют и выделяют в виде индавидуальных соединений известными способами, как например, хроматографяя на колонке, хроматография в тонком слое и т.п. Например, для выделения факторов А,В и D применяют хроматографию на колонне с силикагелем и колонну элюируют смесями разных растворителей, например бензола и этилацетата. При применении такой смеси в колонке с силикагелем вначале злюируется фактор В, а затем факторы А и D. Обычно для регулирования процесса элюирования применяют хроматографию в тонком слое. Соединения А - 28086 задерживают рост бактерий и грибов, патогенных в отношении животных и растений. Ниже указана активность фактора А и В антибиотика А - 28086 в отношении ряда микроорганизмов. Испытание производили обычным методом диск - диффузия (6 - миллиметровые толтоны погружали в растворы, содержашие 1 мг соединения в 1 мл; томпоны помещали на агаровые пластины, засеяннью испытуемым орга1шзмом):






















| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения метаболита "а 27 106 | 1974 |
|
SU539538A3 |
| СПОСОБ ПОЛУЧЕНИЯ АНТИБИОТИКА А204 | 1971 |
|
SU296323A1 |
| Способ получения антибиотического комплекса а-35512 | 1977 |
|
SU751332A3 |
| Способ получения полиэфирного антибиотика А 80190 | 1985 |
|
SU1531861A3 |
| Способ получения антибиотика А 42125 и штамм микроорганизма NocaRDIa aeRocoLoNIGeNeS - продуцент антибиотика А 42125 | 1987 |
|
SU1547710A3 |
| Способ получения антибиотика -11743/а | 1976 |
|
SU643085A3 |
| Способ получения баумицина а и в | 1977 |
|
SU867318A3 |
| Б П Т Б Алчп '>&-,'Ю^У'^:''ЛЧ1 | 1973 |
|
SU404186A1 |
| Способ получения антибиотика в 508 | 1977 |
|
SU715034A3 |
| Способ получения антибиотика | 1981 |
|
SU1134120A3 |








3 994ATCC
Зона сдержива1шя роста, мм фактор А фактор В 1921
2831
2616
1212
2366 17
1414
12Не испытывался
27
Соединеши А-28086|осо1б 1шо эффект шно задерживают рост анаэробных бактерий. Ыиаинаюь шя ко1щентрацня, 11ри которс |фактор А задерживает раэлнчных анаэробных Gaxispwiit опре
Испытуемые oftnaHaiijai
АсИтютпусев bovCs Cto&iridiiuin tnocuutn CCostridium perjrtng-ens Ctostridiutn ramofteum CCo&triciium septicum
CtoftiridLuTn septicum bovine Eubacterium aet4)acUns Peptoeoccus anacrobius Peptostreptococcus intermediut PropiotiCbacterCum aene« i
PropiOnibaclerCum acne& 79 BocteroCdes fisp. Bacteraide« /raoriCis ssp. tKetaiotac bacteroldes frag-ceit «sp. Vvtyarit Bocteroidet ssp. vuCg-ari« Fusobacteriutn si mCiObum
Pu«0bacterium necropkorum VeilConctta aCeaCeseens Cj-Ce - ацилевые эфнры фактора А тшкжв обладают антибактериальной и противог1 1бковой активностью. Эти производные обладают повышенной активностью в отношении гра11«1оложителышх микроорганизме. Такая активность некоторых из таких производных сравнима с активностью фактора А. Соединения испытывали нефелометрическим методом на полуавтомаппескш системе. При испытании антибиотиков А - 28086 были использованы следукицие параметры: Sl phylococcus aureus (Н- Хитли) NRRLB- 314 в питательной среде (рН7 инкубировали 4 часа при 37° С. Пробы и эталон растворяли в смеси метанола с водой (10:90). Эталон, фактор А, находился в концентрации 2,3,4 и 5 мкг/мл. Соединения разбавляли до содержания примерно 3 или 4мкг активности в мл перед помещением в аппарат. Ниже показаны относительные активности соединений в сравнении с активностью эталона. Относительная Соединения активность С 1 Фактор А (эталон) етиловьш эфир А - 28.086 - А Пропиониловый эфир А - 28086 - А Бутириловый эфир А - 28086 - А Валериловьгй эфир А - 28086 - А Капроиловый эфир А - 28086 - А
28
ленная стандартным Цетодсж агар - разбавление, следующая показате|ш получены после 24 - часовой .-.
Мншмашьная концентрация, г/мл
0,S 0,5 0,S
4,0 0,5 0,5
4,0 16 Соединения А 28086 обладают также антимикро алыюй активностью в отношешш микоплаэмы. Агенты, активные в отнощении организмов PPLO, особенно необходимы при разведении домашней птицы. Ниже показаны минимальные концентрации фактора А антибиотика А - 28086, задерживающие рост разновидностей микоплазмы, определенные in vitro при исследовании методом разбавления бульона. Организм Минимальная концентрация, мкг/мл М. galiseptjcum 12,5 М. hyorhims М. synovicil М. hypopneumoniae М. hyosynoviae , Растворы,содержавшие всего лишь 10 мкг антибиотика А - 28086 в 1 мл, применялись для дезинфекции поверхностей с целью зашиты животных от разных видов микоплазм. Соединения А - 28086 обладают также способностью нейтрализовать действие вирусов. Фактор А активен в отношегши поливируса типа III, вируса вакциния, лишайного вируса и лесного вируса Семлики. Фактор А активен также в отношении передающегося вируса, вызьшаюшего гастроэнтерит, вирусз, выэывашоего болезиь Нышкасла и вируса, вызывашцего ринотрахеит быков.
Поэтому соединение А 28086 можно давать , местяо или минуя шицеварительный тракт.
Дэза дая предотвращения или лешния вирусного эфбопеваиня изменяется примерно от 1 до S мг/кг веса тела млекопитающего, в зависимости от вируса
к от шзначения лекарства, т.е. с профилактической
нлв терапевпреской целью.
Кроме того, растворы, содержащие соединения А - 28086, предпочтительно совместно с поверхшхгшо;активным веществом, можно применять для обеззараживания участков, инфшдарованных, наа{жмер, вирусом лишая илиполиомиэлита. Для борьбы с вирусом эффективны растворы, содержзщие примеров от 1 до 500мкг/л соединения А - 28086.
Токсичность фактора А антибиотика А - 28086, введенного внутрибрюшинно мышам, определяется как ЛД5.о 7,15 мг/кг.
Соединения А 28086 являются также инсектицидами и аскарнщ1Дзми. Эти соединения активны в отношении таких насекомых, как мексиканские бобовые жуки, жуки молочая и домашние мухи, а также в отношении таких клещей, как двупятнистый паукообразный клещ, при применении в количестве 500 ч/млн. Кроме того, соединения А - 28086 активны в отношении личинок москитов при применешш в количестве I ч/млн
Важньил свойством соединений А - 28086 яв71яется способность их воздействовать на кокцнди. Например, эксперименты по использованию его в кормлении покаэьшают, что при содержании соединения А - 28086 в корме даже в таком небольшом количестве (0,003%) наблюдается увеличение в весе, а при содержании в количестве 0,005% - уменьшается смертность цыплят, заражен. ных кокцидиями.
В табл. 1 , 2 и 3 показаны результаты опытов по применению фактора А для лечения цыплят, зараженных разнь1ми авдами Е i meria.
Таблица 1
31
Средние показатели четы1)ехввшкш: 5 молоденьких петушков в каждом.
) Четыре опыта в каждом случае; 5 молоденьких петушков в каждом опыте.
Для предупреждею1Я или лечения болезни, вызванной кокцидаями, птицам дают ежедневно, предпочтительно через клюв, нетоксичное количество соединения А - 28086. Такое соединение можно применять в разной форме, но лучше всего давать совместно с физиологически приемлемым носителем, предпочтительно в смеш с кормом. Дяя . определения подходящей концентрации соединеташ А - 28086 следует учитывать ряд факторов, но вообще пригодаа коидентрация от 0,003 до 0,4% или предпочтительно от 0,005 до 0,02% веса корма.
576966
32 Таблица 2
Таблица 3
50
1,75
3,5
73 0,9
3,3
Важным свойством соединений А 28086 является также их способность улучшать эффективность использования корма. Например, соединения А - 28086 улучшают эффективность использования корма. Например, соединения А 28086 улучшают
эффективность использования корма жвачных животных, с развитой функцией рубца.
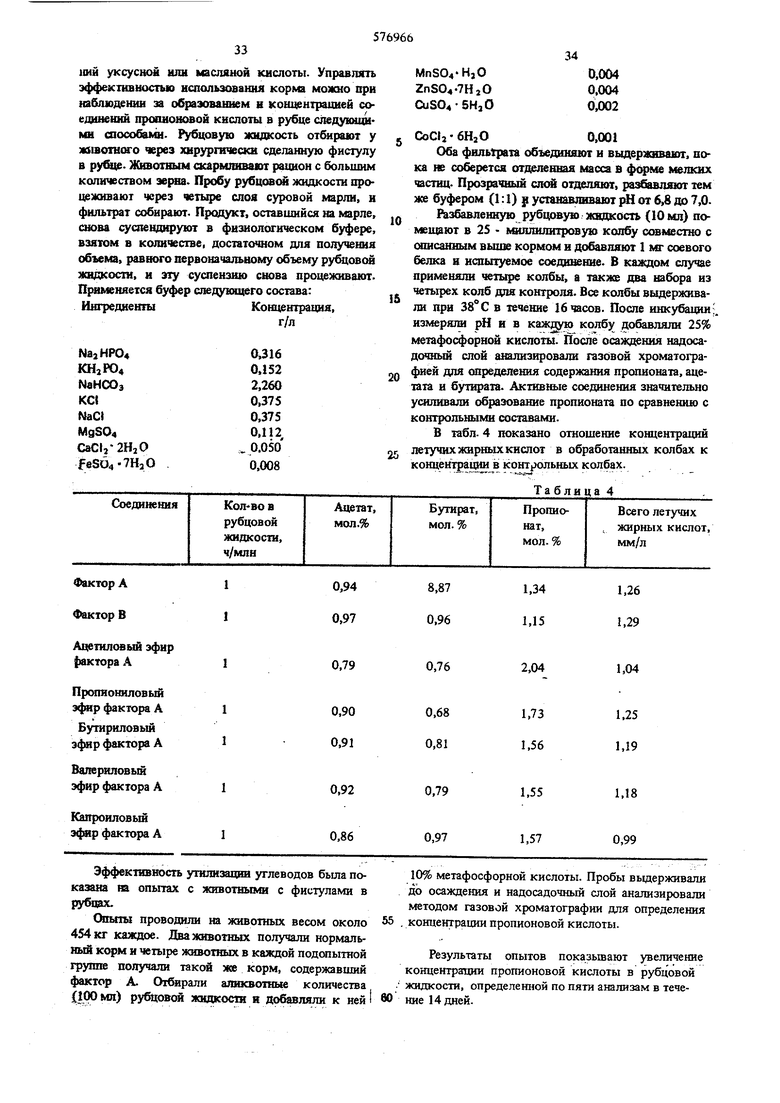
Эффект}шность использования углеводов у жвачных животных увеличивается при стимулировании флоры в рубце животиого к образсяанию
производных пропионовой кислоты, в не соединеЭффективность утилизации углеводов была показана ва опытах с животными с фистулами в рубцах.
Шыты проводили на животных весом около 454кг каждое. Двахототных получали нормальный корм и четыре животных в каждой подсшытной группе получали такой же корм, содержавший фактор А. Отирали аликвотные количества {100 мл) рубцовой жидкости и добавляли к ней 1
10% метафосфорной кислоты. Пробы выдерживали до осаждения и надосадочный слой анализировали методом газовой хроматографии для определения 55 , концентрации пропионовой кислоты.
Результаты опытов показьтают увеличение концентрации пропионовой кислоты в рубцовой . жидкости, определенной по пяти анализам в течевО ние 14 дней. Кроме того СИ1ЫТЫ in vivo показали, что фактор А увеличивает тшшзаци1а1сбрма овцдми. Производаше. фактора О а1Ш11биотшса А - 2SQ86 являются антивирусными агешамн- Фактор D активен в опношении вируса Мэриланд В, поливируса типа III, вируса СХЗЕ, ге петического вируса и лесного вируса Семяики. Фактор D активен также в отношении вируса, вызывающего гастроэнтерит, вируса болезни Ньюкасла и вируса ринотрахеита крупиого рогатого скота. Тот факт, что производные фактора О активны в отношении вирусов и анаэробных бактерий, делает эти соединения особенно благоприятными для профилактики энтеритов у цыплят, свиней, рогатого скота и овец. Соединения фактора О пригодны также для лечения эктеротоксемии у жвачных животных. Важньид свойством соединений фактора D является их активность в отношении кокцидий. Эксперименты in yitro показывают, что фактор D активен в отношении Eiineria tenella. При заражении клеточных культур жизнеспособными спорозоитами с последующим добавлением фактора D были получены следующие результаты. Активность в отношении кокцидий фактора D антибиотика А-28086; Концентрация фактора. Характеристика 1 мкг/мл Результаты двух испытаний. Другой полезной особенностыо производных фактора О является их способность улучшать эффективность утилизации корма жвачными животнымиСоединения эти эффективно увеличивают количество пропионатов н тем самым способствуют эффективной утилизации корма при введении через рот жвачным хошотным в количестве пршдерно от 0,05 до 5,0 мг/кг в день. Наиболее благоприятные результаты достигаются при дозах примерно от 0,1 до 2,5 мг/кг в день. Соединение предварительно смешивают с кормом, но его можно применять также в форме таблеток, шариков и в капсулах. Такие препараты приготовляют способами, хорошо известными в ветеринарной фармации. Каждая отдельная доза должна содержать количество соединения, соответствующее дневной дозе для животного. Антибиотик А - 28086 можно применять в Составе корма, предназначенного для откармлива5JQ 15 20 25 30 35 40 45 50 55 60 ния скота, в количестве от 1 до 30 г соединения н тонну корма Как сказано выш, соеданения А - 28086 представляют собой антиэирусные агенты и активны также в отношении анаэробных бактерий, в частности в отношении Clostridium perfringeusillo3toму такие соединения пригодны для лечения и предупреждения энтеритов цьшлят, свиней, рогатого скота н овец. Они пригодны также для лечения энтеро токсемии жвачных животных. Пример. А. Ферментация А - 28086 при взбалтьюашй в колбе с применением s. aureofaciens NRRL 5758. K nbTypynStfeptomyces aureofaciens NRRL 5758поместихш на косой агар следующего состава: ЙнгредаентыКоличество, Агар20 Декстрин10 Гидролизованный энзимом казеин2 Мясн(ж экстракт2 Дрожжевой экстракт2 Диспшлированная водадо 1 л. Косой агар инокулировали Btreptomyces aureofaciens NRRL 5758 и инкубировали при от 6 до 10 дней. Созревщую культуру покрыли бычьей сьшороткой и стерильной петлей разрыхляли споры. Полученную суспензию шор и обрывков мицелия .в бычьей сьшоротке подвергали лиофилизации. Один из щести лиофилизированных шариков ис; пользовали для инокуляции 50 мл вегетативной среды, имеющей следующий состав: ИнгредиентыКоличество, г Глюкоза20 Соевая крупа15 Водный настой кукурузы10 Углекислый кальций2 Водопроводная водадо 1 л. Инокулированную вегетативную среду в колбе Эрленмейера емкостью 250 мл инкубировали при 30° С в течение 72 часов на аппарате для. встряхивания, вращающемся по дуге диаметром 50,8 мм со осоростью 250 об/мин. ; Б.ферментация А-28086 в чане с применением S. aureofaciens NRRL 5758. Для увеличения объема посевного материала 10 мл полученной инкуГ ированной вегетативной среды использовали для инокуляции 400 мл вегетативной среды второй стадии того же состава. Эту среду в 2-литровой колбе инкубировали при 30° С в течение 24 часов в аппарате, вращающемся по дуге диаметром 50,8 мм со скорстью 250 об/мин. Вегетативную среду второй стадии (1л) использовали для инокуляции 100 л стерильной среды следующего.состава: ИнгредиентыКоличество, г/л Декстрин тапиока60,0 Казеин, гидролизованный энзимом8,0 Меласса15,0 ,О 0.5 CiaCSO, 2,0 5.0 1%1финированаов сооюе касш Деионизированшя вода ml литр После стерилизации в автоклаве в 120 С в течение 30 минут под давлением 1,05 - 1,4кг1ш величина рН была равной 6,7. В 165 - литровом бродильном чане инокулированшя среда подве1иалась брожению в течение 10 дней при температуре 29° С. Бродильную среду аэрировали стерильным воздухом, подаваемым со скоростью 0,4 объема воздуха на 1 объем среды в минуту. Среду перемешивали обычными мешалками со скоростью 250 об/мин. П р и м е р 2. Выделение антибиотического комплекса А - 28086, образованного S. aureofacie NRRL 5758. Сброженный бульон (132л), полученный, как описано в примере 1, профильтровали с помощью фильтра (Гифло Суперцел, инфузорная земля, фирмы Джонс Маквилл Продактс корп.) и получили 97 л фильтрата, который экстрагировали примерно равным объемом этилацетата. Экстракт отде;шли от водной фазы и сконцентрировали до объема, равного примерно 500 мл. Этот концентрированный этилацетатный экстракт добавили : большому избытку петролайного эфира (Скелли Зольв; около 10 л) для осаждения и тем самьин для отделе1шя нежелательного продукта. Отделенный фильтрат вьшарили в,вакууме и получшш комплекс антибиотика А-28086 (6,9 г). Мицелярную часть этого комплекса по лучили при двойной экстракции отфильтрованного мицелия примерно половинными объемами метанола (62 и 59 л). Экстракты объединили и оконцентрировали в вакууме для удаления метанола. После концентрирования осталось примерно 10 л водной фазы, к которой добавили разбавленный раствор гидроокиси натрия до рН 7,5. Полученный раствор дважды экстрагировали примерно одинаковыми объемами этилацетата (9 и Юл). Экстракты объединили и сконцентрировали до объема, равного примерно 400 мл. Этот экстракт добавили к большому избытку петролейного эфирас целью удаления нежелательных продуктов при описанной выше процедуре концентрирования профильтрованного бульошюго экстракта. Мицелярная порция комплекса, полученная из фильтрата, весила 20,6 г. П р и м е р 3. Выделение индивидуальных факторов А и В. Мицелярную порцию комплекса антибиотика А; 280В6 (235 г, как описано в примере 3) растворили примерно в 80 мл бензола. Этот раствор ввели в колонку сияикагеля (9Х 130 см, 8л сшшкагель Мате зона сорт 62). Колонку элюировали разными смесями бензола и этилацетата. Элюирование сопровождалось хроматографией в тонком слое. При применении системы растворителя бензол-этилацетат (90:10) вначале элюировали фактор В, который выделили как индивидуальный фактор. Этот фактор после кристаллизации из ацетона веежн 43 мг и имел тлл. 150-153° L. Продолжая злю 1рование смесягаш бензола и этилацетата, но постепенно увел1яквая отаооггельное количество этилацетата, выдеанзш фактор А. Фракции, содержавшие фактор А, объединюш и сконцентрировали в вакууме. Остаток растворили в ацетоне (примерно 150 мл) к к раствору добавили примерно 160 мл воды. При добавлении 1 н- соляной кислоты установили рН 3 раствора. Подкисленную смесь перемешивали в течение 1 часа, в результате чего образовался осадсчс. Этот осадок отфильтровали и перекристаллизовали (примерно 150 мл) после добавления воды (примерно 60 мл). Продукт сушили в течение ночи в вакууме и полушли фактор А (примерно 6,6 г). После частичного испареиня ацетона из фильтрата получили дополнительк примерно 1,2 г фактора А. П р и м е р 4. Ацетиловый эфир фактора А. Фактор А антибиотика А-28086 (7,41 г) растворили в пиридине (150мл) и к раствору добавшш 50 мл уксусного ангидрида. Полученный раствор тщательно смешали и выдержал в течение ночи при комнатной температуре. Затем добавили 200 мл воды, тщательно смешали, и смесь выдержали в течмше 4 часов при комнатной температ фе. Образовавшийся твердый осадок белого цвета отфильтровали, промыли водой и высушили на воздухе. Получе}щое твердое вещество растворили в ацетоне (100 мл) и раствор вьшарили досуха в вакууме (эту процедуру повторили 3 раза). Остаток кристаллизовали из смеси ацетона (100 мл) и воды (50 мл) и получили ацетиловый эфир фактора А (614 г) с т.пл. 100- 103°С. Приме р ы 5-9. Пропионшювый эфир Диктора А, полученный при реакции фактора А с ангидридом пропионовой кислоты в присутствии пиридина способом примера 5, имел т.пл. 96-98° С. Бутириловый эфир фактора А получили при реакции фактора А с ангидридом масляной кислоты в присутствии пиридина способом, описанным в примере 5; т.ш1. 79-81° С. Капроиловый эфир фактора А приготовили при реакции фактора А с ангидридом капроновой кислоты в присутствии пиридана способом, описанным в примере 5; т.пл. 16-167° С. Валердловый эфир фактора А получили при реакции фактора А с ангидридом вариановой кислоты в присутствии пиридина способом, описанным в примере 5; т.Ш1.173-175°С. П р и м е р 10. Приготовление натриевой соли фактора А. Фактор А (500г) растворили в ацетоне (50 мл). К этому раствору добавили воду (50 мл) и 5н. раствор гидроокиси натрия до рН 10,5-11. Полу генный раствор перемешивали 1 час, а затем экстрагировали этилацетатом. Экстракт вьшарнлн досуха в вакууме и остаток переосаднлн из раствора в смеси
39
ацетона и ъоаи, получили 378мг натриевой соли фактора А с Т.Ш1. 120-123° С.
Примеры 11-15. Бариевую соль фактора А орнготовили из фактора А (500 мг) и насыщенного раствора гидроокиси бария способом примера 10. Получили 369 мг бариевой соли фактора А с Т.ПЛ. 199-190° С.
Калиевую соль фактора А получили из фактора А (500 мг) и 5н. раствора гидроокиси калия способом примера 10: получили 363 мг калиевой соли фактора А; т.пл. 165-167°С.
Цезиевую соль фактора А приготовили из фактора А (500 мг) и 1и. раствора гидроокиси цезия способом примера 10 . получили 540 мг цезиевой соли фактора А; т.пл. 190-210°С.
Натриевую соль фактора В приготовили из фактора В и 5н. раствора гидроокиси натрия шособом примера 10.
Пример 16. Ферментация А - 28086 в встряхиваемой колбе с применением S. anreofaciens NRRL 8092.
Культуру Streptomyces aureofaciens NRRL 8092 приготовили и выдержали на косом агаре, имевшем следующий состав:
ИнгредиентыКоличество, г
Кг НРО42,0
MgSO4 7H2O0,25
NH4 МОз2,0
СаСОз2,5
FeSO4-7H2O0,001
МпСЬ - 7Н2О0,001
ZnS047H2O0,001
Глюкоза10,0
Агар20,0
Деионизированная водадо 1 л рН (самопроизвольное)
7,7.
Косой агар инокулировали Streptomyces aureofaciens NRRL 8092 и инкубировали при 30°С в течение примерно 7 дней. Созревшую культуру на агаре покрыли стерильной & 1чьей сывороткой и стерильной петлей сияли культуру для приготовления суспензии спор и мицелия. Полученную суспензию подаергали лиофилизации.
Один из полученных лиофильных шариков использовали для инокуляции 50 мл вегетативнс« среды, имевшей следуннций состав:
ИнгредиентыКоличество, г
Глюкоза20
Соевая мука15
Водный кукурузный настой 10 СаСОя2,0
Водопроводная водаДо 1 л,рН после
добавления МаОН
6,5.
Инокулированную вегетативную среду в 250 миллилитровой колбе Эрленмейера инкубировал при 30° С 48 часов на аппарате для взбалтывани вращающемся со скоростью 250 об/мин по ду диаметром 50,8 мм.
40
Описанную выщ инкубированную вегетативную среду ишользовали (0,5 мл 1%) для инокуляции 50 мл бродильной среды следующего состава: Ингре1шентыКоличество, г
Декстин топиока60,0
Казеин, гидролизованный энзимом 6,0
Энзиматическнй гидролизат казеина 2,0
СаСОз2,0
MgS047H2015
Черная тростниково - сахарная меласса15,0
Рафинированное соевое масло5,0
Водопроводная водадо 1 л, рЖсама. произвольное) 6,(
1)Декстрин Сталей N 11 фирмы А. Е. Сталей, Декатур, шт. Иллинойс
2)Амбер ШС, .Лаборатории Амбер, Джюно, - щт. Висконсин ,
3)NZ Амин А, фирмы Шеффилд Кемикал, Норвич, щт. Нью-Йорк
Пример 17. Ферментация в чане А - 28086 с применением S.ureofaciens NRRL 8092.
В данном случае применяли первоначально описанную в примере 16 процедуру ферментации А-28086. Для получения большего объема посевного материала Щмл инкубированной вегетативной среды использовали для инокуляции вегетативной среды второй стадии (400 мл), имевщей тот же состав. Среду второй стадии в 2 - литровой колбе Эрленмейера инкубировали при 30° С 24 часа во вращающемся аппарате для взбалтьшания при скорости 250 об/мин.
Инкубированную вегетативную среду второй стадии (800 мл) использовали для инокуляции 100л стерильной бродильной среды, имевшей следующий Состав:
ИнгредиентыКоличеслво. г/л
Q Декстрин тапиока60,0
Гидролизованный знзимом
6,0
казеин
Энзиматический гидролизат
казеина
2,0 2,0
СаСОз
0,5 г/л
MgSO4i-7H2O
Черная тростниково - сахарная
меласса 15,0
Рафинированное соевое масло5,0
Водопроводная водадо 1 л.
1)Декстрин Сталей № 11 фирмы А. Е. Сталей, Декатур, щт. Иллинойс.
2)Амбер Н С, Лаборатории Амбер, Джюно, шт. Висконсин.
3) NZ Амин А, фирмы Шеффилд Кемикал, Норвич, шт. Нью-Йорк.
После стерилизации в автоклаве (в течение 30 минут при температуре 121°С и давлении 1,05-1,4кг/см) среда имела рН 6,8 + 0,1-Ферментация протекала в течение 10-12 дней при температуре 28±
4J
± 1°С в 165 - литровом чане при аэрировании среды стерюгьным воздухом, подаваемым в количестве 0,4 объема воздуха на 1 объем кулъгурной среды в минуту. Среду перемешивали мешалками, вращающимися со скоростью 300 об/мин.
П р и м е р 18. AHTHtffloTHKM А - 28086 получили, как шисано в примере 17, но с применением среды для сбраживания в колбе и чане, имевшей следуншдий состав: ИнгредиентыКоличество, г/л
Декстрин тапиока30,0
Глюкоза15,0 Казеин, гидролизованный
энзимом 3,0 Энзиматический гидролизат
казеина1,0
Дрожжевой экстракт 2«5i
CaCOj2,0
MgSO47H2O1,0 Черная тростниково-сахарная
меласса15,0
Рафияйровлиное соевое масло5,0
Зодовроводная водадо 1 л.
1)Декстрин Сталей , А.Е.Сталей, Декатур,
шт. Иллинойс.
2)АмберН С Лаборатории Амбер, Джюно, шт. Висконсин.
3)NZ Амин А, Шеффилд Кемикал, Норвич, шт. Нью-Йорк.
После стерилизации в автоклаве, как описано q примере 17, среда имела рН 6,4.
Пример 19. Выделение комплекса антн& отика А - 28086, полученного с помощью S, aureofaciens NRRL 8092.
Цельный бродильный бульон (60л), полу%нный способом, описанным в примере 17, после добавле шя разбавленной соляной кислоты имел рН 3. Этот раствор профильтровали через фильтр (П1ФЛО Супер - цел, инфузорная земля, фирмы Джон - Манвилл Продактс корп.). Мицелярный остаток на фильтре экстрагировали 30 л метанола и к зкстракту добавили при перемешивании 1,56к1 бикарбоната натрия. Поаю отделения этого экстракта мицелярный остаток снова экстрагировали в вакууме для удаления метанола. Оставшийся водный раствор ( 7 л) подкислили разбавленной соляной кислотой до рН 7,5 и полученный раств дважды зкстрагировали этилацетатом (дважды по 7л). Экстракты объединили и концентрировали Р вакууме до получения маслообразного остатка, который растворили в 1500мл ацетона. К этому раствору добавили разбавленную соляную кислоту до рН 3 и перемешивали 1 час. Образовавшийся осадок отфильтровали, растворили в ацетоне (1500мл) и к раствору добавили 400мл воды. Полученный раствор вьщержали 16 часов для кристаллизации. Кристаллы отфильтровали, высушили в вакууме и получили 74 г кристаллического продукта, содержавшего факторы А и D и кристалпические примеси.
42
Сырой кристаллический п;)одук1 (40 i) pacinoили примерно в 250 мл бензола и pactBfjp проj cnuiH колонку с силикагелем (9x120 см; илккагель сорта 62 Грайс - Давидсона). Колонку люировали последовательно 40 л каждого нэ еле ующих растворителей:
1)Бензол
2)Бензол- зтилацетат (9:1)
3)Бензол - зтилацетат (4:1)
4)Бензол- этилацетат (7:3)
5)Бензол- этилацетат (1:1)
6)Этилацетат
7)Метанол.
Каждую фракцию проверяли, определяя активность в отношении Bacillus subtilis и хроматографировали в тогком слое для идентификации злюированных соединений А - 28086, элюировали смесью бензола и этилацетата (4:1). Фактор В злюировалн смесью бензола и этилацетата (7:3). Факторы А и D злюировали смесью бензола и зтнлацетата (7:3 и 1:1), фракции 119-156. Эти фракции объединили, вьшариш досуха и остаток растворили в 500 мл ацетона. К полученному раствору добавили 500 мл воды, подкислили его разбавленной соляной кислотой до рН 3 и перемешивали в течение 1 часа. Образовавшийся осадок отфильтровали и кристаллизовали из смеси ацетона (500мл) и воды (180мл). Кристаллы отфильтровали, высушили в вакууме и получили 20,1 г смеси ракторов А и D.
Пример 20. Разделение и очистка ИНДИЕЙ дуальных факторов А и D.
f Кристаллическую смесь факторов А и D, полученную, как описано в примере 18 (18,8 г), растворили в бензоле (50 мл). Раствор поместили в колонке силикагелЯ (7X100 см) (силикагель сорта 60 фирмы Мерк, тоньше 230 меш ASTM). Колонку злюировали при скорости потока 90 мл/час последовательно следующими растворителями:
1)12л бензола;
2)12л смеси бензола и этилацетата (9:1); 3) 12л смеси бензола и этилацетата (4:1) ;
4)32л смеси бензола и этилацетата (7:3);
5)Юл метанола.
После хроматографии в тонком слое (Целлюлоза Мерк, Дармштат на алюминиевой подложке) проводили биоавтографию с по мо1цью В. subtilis для регулирования процесса элюирования. Применили следующую систему растворителя: вода - метанол цетон (12:3:1), добавляя вначале гидроокись аммония до рН 10,5, а затем соляную кислоту до рН 7,6.
Фракции объемом от одного до двух литров отбирали, пока обнаруживали актщзность: затем собрали 200 - миллилитровыё фракции, содержавшие только фактор D, которые объеди1гили и выпарили в вакууме досуха. Остаток К1)исгаллизовали из смеси ацетона и воды. Кристаллы отлепили и высупшли в вакууме; получили 140 г кристалли ческого фактора D. Так же обработали фракция, содержавшие фактор D и следы фактора А, и получили дополнительно ISO мг кристаллического фактора D, содержавшегр небольшое количество фактора А. Фракции, содержавшие только фактор А, 5 ботали так же, получили 4,7 г кристаллическогс; фактора А. Пример21. Антибиотики А - 28086 получили в процессе примера 16, но с применением косой среды еледушцего состава:i о Ингредиенты1Соличес1во, г Мясной экстракт2,00 Декстрин20,00 Дрожжевой экстракт2,00 Энзиматический гидролизатts казеина4,00 CoClj ,02 Агар20,00 Деионизированвая водадо 1 лС помощью КОН установили рН7,0 и инокулированную косую среду инкубировали при 28° С примерно 7 дней. Пример 22. Антибиотики А - 28086 приготовили в процессе примера 17, но с применением среды , следующего состава: Количество, г/л Ингредиенты Декствин тапиока Ингредае Измельченная желтая кукуруза Соевая мука, экстрагированная растворителем, обрушенная, тонк помола, 50% белка %1вотш ш жир (говяжий топлен Сухая рыбная мука с растворимы веществами (60% белка) Р&створимые вещества кукурузы винно - водочного завода / Ь1капьцийфосфат пищевого сорт Карбонат кальция Витаминная CMeci (витамины А, D, Е, К, и В| 2, холии, ниащш, пентотеновая кислота, {жбофлавин, биотин с агентом, связывающим глюкозу) Смесь минералов, содержащихся в виде следов (представляющая сульфат магния, окись цинка, йодистый калий, сульфат железа и карбонат кальция) 2 - Амин - 4 - оксимасляная кислота (оксианалог метионина) Фактор А антибиотика А - 28086 Эти композиты смешали обьтвым способом, применяемым для смешения кормов. Цьшлята, которым скармливали этот корм, противостояли воздействию кокцидий и прибавляли в весе так же быстро, как цьшлята здоровые, получившие так же корм, но без антибиотика. Энзи aп{чecкий гвдролизованный казеин15,0 Тростниково - сахарфя меласса15,0 Карбонат кальция2,0 Сульфат аммония,о Сульфат магния0,5 Рафинированное соевое масло4,6 1) Декстрин Сталей N11, А.Е.Сталей, Декатур, игг.Иллинойс. 2) Амбер ЕНС лабораторин Амбер, Джюно, шт.Висконсин. П р и м е р 23. Антибиотики А - 28086 приготовили в процессе примера 21, но с применением промежуточной вегетативной среды второй стадии, имевшей следующий состав: Ингредиенты Количество, r/f Церелоэа 20,0 Водный кукурузньш настой (сырой вес) Соевая крупа Карбонат кальция Дрожжи Свекольная меласса П р и м е р 24. Модифицированный А - 28086 корм ДЛЯ лечения болезни цыплят, вызванной кокци днями. Сбалансированный высококачественный корм для цыплят, обеспечивающий быстрое прибавление в весе, приготовили по следующему рецепту: Количество го й) и Прямер25. Корм мясного скота с добавкой А - 28086. Сбалансированный с большим содержанием зерна корм для откармливаемого скота приготовили по следующему рецепту:
Иштйоденты Ji°кг
Тоикоизмельчанная кукуруза6,78617
Измельчеш1ый стерзвень почапса
кукурузы1090,7
Обезвоженная мука из люцерны, 17%
белкаS45,3
Мука из обрушенной сон,
экстрагированшя растворителем9,995690,0
Тростниковая меласса545
Мочевинао,65,4
Фактор А - 280866,00440,04
Дикальцийфосфат пищевой0,54,5
Карбонат кальция0,54,5
Хлористый натрий0,32,7
Смесь минералов в виде следов0,030,27
Смесь витаминов А и D20,070,63
Предварительная смесь
, витамина ,
Пропионат кальцияОД 51,36
1)Содержит в 1 фунте (0,453 кг) 2000000 ед. витамина А; 227200 ед витамина Оз и 385,7 г соевого корма с добавкой 1% ма
2)Сухие кукурузные зерна с растворителем, содержащим
о; а- токофериловый эфир уксусной кислоты в количестве 20000 Смешанный kbpM прессовали в форме таблеток. Средний дневной рацион - 6,8 кг для одного животного. Этот корм содержит примерно 300 мг фактора А на каждое животное. П р и м е р 26. Ациловьо эфир фактора D антбиотика А - 28086. Фактор О растворили в пиридане и к раствору добавида стехнометрическое ка;шчество уксусного ашидаи/щ. Полученный раствор тщательно перемеШЕ1ЛИ и выдержали в течение ночи при комнатной температуре. Затер добавили избыток воды, тщательно смещали я выдержали несколько часов при комнатной теьшервтуре. Образовавшийся осадок отфильтровали, промыли и высуишли. Полученное твердое вещество { створили в ацетоне и выпарили досуха в вакууме; получили а131етиловьш зфир фактора О.. Примеры 27-30. Пропионовьш эфир фактора О получили при реакции фактора D с ангид ждом прсягаоновой кислоты в присутствии .пирядака способом, описанным в примере 26. Бутнридовьй эфир фактора О приготовили при реакщга фактора D с ангидридом масляной кислоты в присутствии пиридит способом, описанным в примере 26.. J Каприловый зифир фактора О приготовили при реакции фактора D с ангидридом капроновой -.Ингредаенты
Молотая желтая кукуруза Мука из обрушенной соли, экстрагированная растворителем и тонкоизмельченная; 50% белка
Количество
453,5
50
282
31,09 кислоты в присутствии пиридина способом, описанным в примере 26. Валериловый эфир фактора D приготовили при реакции фактора D с ангидрвдом валериановой кислоты в присутствии пиридина способом, описанным в примере 26. П р и м е р 31. Получение натриевой соль фактора D. Фактор D растворили в ацетоне и к раствору добавили эквивалентное количество воды и 5н. раствор гидроокиси натрия в количестве , достаточном для установления рН 11. Полученный раствор перемешивали в течение примерно 1 часа, а затем экстрагировали этилацетатом. Экстракт выпарили в вакууме и получили натриевую соль фактора О. Примеры 32-34. Калиевую соль фактора D полущ|яи из фактора D и 5н. раствора гидроокиси калия способом примера 31. Бариевую соль фактора D получили из фактора D и насыщенного раствора гидроокиси бария способом примера 31. Цезиевую соль фактора D получили из фактора О и }н. раствора гидроокиси цезия способом примера 31. Пример 35. Корм для цьшлят, содержащий фактор О и пригодный для лечения кокцидиоза. Сбалансированный высококачественный корм, пригодный для быстрого увеличения веса цьшлят, приготовили по следующему рецепту: Количество %кг
47
, UKaBonojA жир (топленый говяжий) Сухая ры&шя мука с paciBopijMbiMH; 60% белка
йстаоримые вещества кукурузы, отхода огарто водочного производства
Дикальцийфосфат пшцевой Карбонат кальция Смесь витаминов (витамины А, О, Е, КиВ22,холин, шшцин, нантотеновая кислота, рибофлавин, биотин с агентом, связьтающим глюкозу) Смесь минералов, содержащихся в виде следов, 2 амин - 4 - оксичуисляная кислота (оксианалог метион Фактор D Эта компоненты смешали обычным способом. Цьашяп к laKOM рационе противостоят воздействшо кокцидий; вес их увеличивается так же, ,как вес цыплят не зараженных кокцидиями и волучашцих тот же корм, но без антибиотика. Ингредиенты Тонко измельченная кукуруза Измельченный стержень початка кукурузы Обезвоженная мука из люцерны; 17% белка Мука из обрушенной сои, зкстрагированная растворителем; 50% белка Тростниковая меласса Мочевина Фактор Дикальцийфосфат пищевой Карбонат кальция Хлористый натрий Смесь минералов в виде следов Смерь витаминов А и D «. Смесь витаминов Е Пропионат кальция IJ Содержит в 1 фунте (0,45 227200 ед. витамина Dj и 385,7 2) Сухое зерно с растворимы спирто-водочного завода, содер в 1 фунте.
Смешанный корм прессовали в форме таблеток. При среднем количестве корма, равном 6,8 кг в день, каждое животное получало примерно 300 мг фактора D ежедневноФормула изобретения
48
58,9
36,3 16,3 7,27
4,53
0,9 ч0.09
Культуру микроорганизма Streptomycesaureofaciens NRRL 5758/или Streptomycesaijreofaciens NRRL 8092 выращивают в аэробньис условиях на питательной среде, содержащей усвояемые источники углерода, азота и неорганических солей с последующим вьщелением из культуральной жидкости целевого продукта.
49
фракции, содержащие А,В и О факторы данного антибиотикаПриоритет по,признакам:
. 10.06.74 (заявка N 477954) по признаку п. I Streptomyces aureotaciens NRRL 5758 - и по аризна-. куп. 2-фактор А;
50
при экспертизе;
/ 9nf 9fnOfi 2Olf
Csi
§Р
Й
fe 3t §
§
P l§ 5 5tJ
I
«M
j
-j I
ч
evj
: 6«i
Ю
8|
§
%
fif f 3/}iJOCfi/
CM
§
JX /7f ffAfJ trcflf
it
I I
« «
N ( 5)
elO
Csi
/Vi ffn oj sAuocfi/
м
c:a
«5 «O O
if
Csl
-л8
Cs
Сэ NJ
S
4i
CM
« «K
«5 ЧУ
«
ts.
5s
«r
I
5- c.
irT
X
§
I
«i
«i
«5
fn
«N
/ f-/oj/o/Ji/oef/
s
«5
§
2
иг
«N
э
о
«5
ъ
сэ
oi
«и
ад
«5
К
О
ча
S
г
iv
I
I
ъ
I I
л
sa
vrj Csi
% s/ ivгfno(
Авторы
Даты
1977-10-15—Публикация
1975-06-09—Подача