I
Изо етевие относится к оргашчвской химии, в честности щ)едлвгается способ по пучения новых производных 1,2,4-триазола н их солей, которые могут найти прик енешсе в качестве фувгвцвдов.
Б литературе отшсана реакция замещения апкокси;шной грушш на аминогруппу в тех случаях, когда эфирная связь в достаточной мере активирована находящимися в ft -попожешга карбонильными, карбоксильными или нитрильными группами. Так j -метоксикетоны переводягся в fj -аминокетоща flj.
Известно, что 1-тритил-1,2,4-триазол обладает 4унгицидной активностью. Его действие на различные растения не всегда удовлет.ворительно.
Цепью изобретения является получения зао- вых производных 1,2,4-триаэола, обладающих улучшенными свойствами.
Г едлагаемый способ получения производных 1,2,4 триазола ойцей I
Ж
-Ж
1 j
Br -C-Y-Rj S,
де - фенил, незамещеняыв или замешенный галоидом, алкЕоюм с числом атомов 1-4, галоидалкипом с числом атомов углерода 1-4, витрогрутшой, аминогруппой, метоксилом или фенилом; R - водород, алкил с числом- атомов
углерода 1-4, фцнил; R - алкил с числом атомов углерода 1-4, циклоалкил с числом атомов углерода 5-6, февил, гаглоидфенилУ - группа -СО-, -С-, -С(ОН)2
NOH
или их солей заключается в том, нение обшвЛ формулы 2
ORi
RI-O-C-Y-R
R
где 9 , 3 имеют указанные
значения.
сС (С11 Кетали могут быть получены раакциам Реформатского ила Гриньяра, ведущим к аралКвлкето1 у, с последующими бромкрованием у соседнего к кетогругше атома углерода и реакцией образовавшегося дибромкетона с ал«коголятом фенопатом. Прйм4рами КИСЛОТ образующих солй с проваводЕЫмв 1,2,4-трйаэолаэ шяшогс1а галоген водородные КИСЛОТЫ, напргашра .хлор- и бромводородные КИСЛОТЫ, в особенности хлоркетоВ19Доро{ща;с Кислота, фосфорнаа кислота, монон бис{ункш1ональная карбоновая к юлота и гид рокСЕкарбоновые к: юлотыз например уксусная, мапеиноваа ангарная, фумаровая, вЕнная лимонная, сакшшловая, (сорбнновая, молочиаНэ 1,&-нафталн1здж:упьфоновая кислота. Синтез проводят, беря ни 1 моль соедЕ2шнвя общей 2 предпочтич льно око ло 1 моль 1,2,4 арйааопгидрохлорнда, Для выдеяешш соединеннй обшей формулы 1 ре акдионцую смесь переносят в прЕчем смась частично переходитврасгвор. Суспекзию нейтрализуют щелочью ипи . кар&онатом щелочного металла и экстрагируют органическим растворителем, трудно смешивающимся с водой, например метнленхлоридом, С ганическую фазу высушивают в растворитель отгоняют. Полученный твердый цли маслянястый остаток очищают перекрисгаплнза- шаей. Полученные предлагаемым способом соединения можно обычными методакз и привести в их соли. Пример, 0-Ш-С0 С(СН.5)
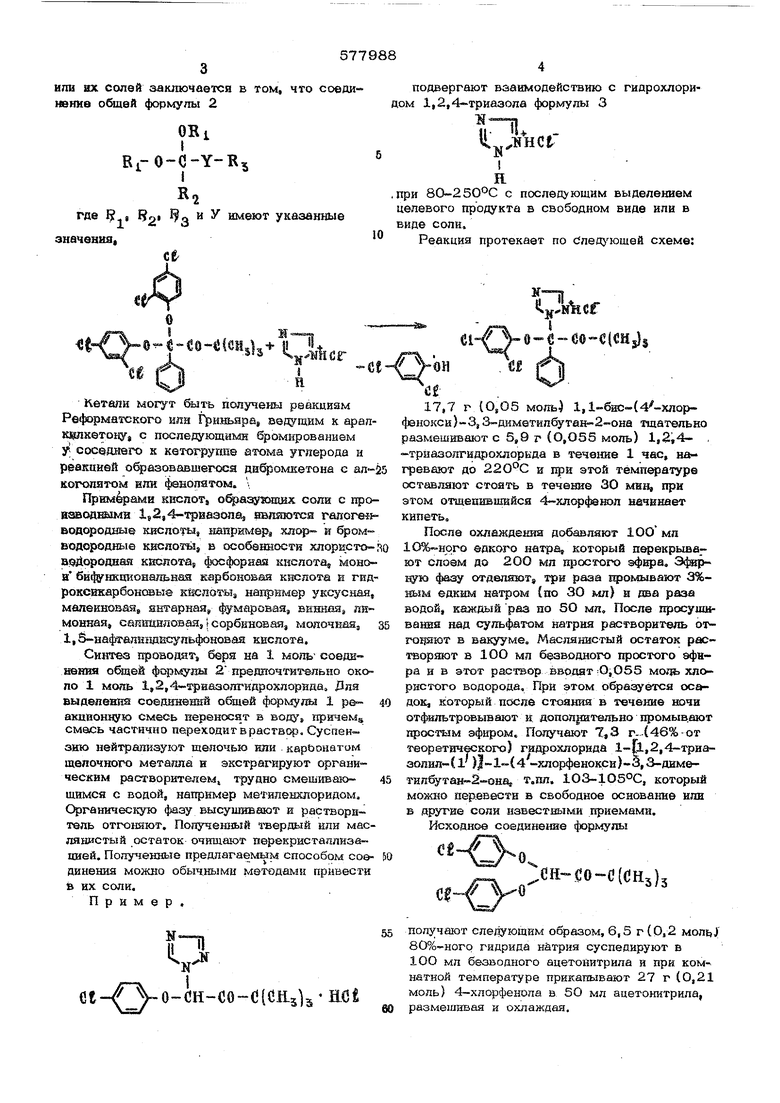
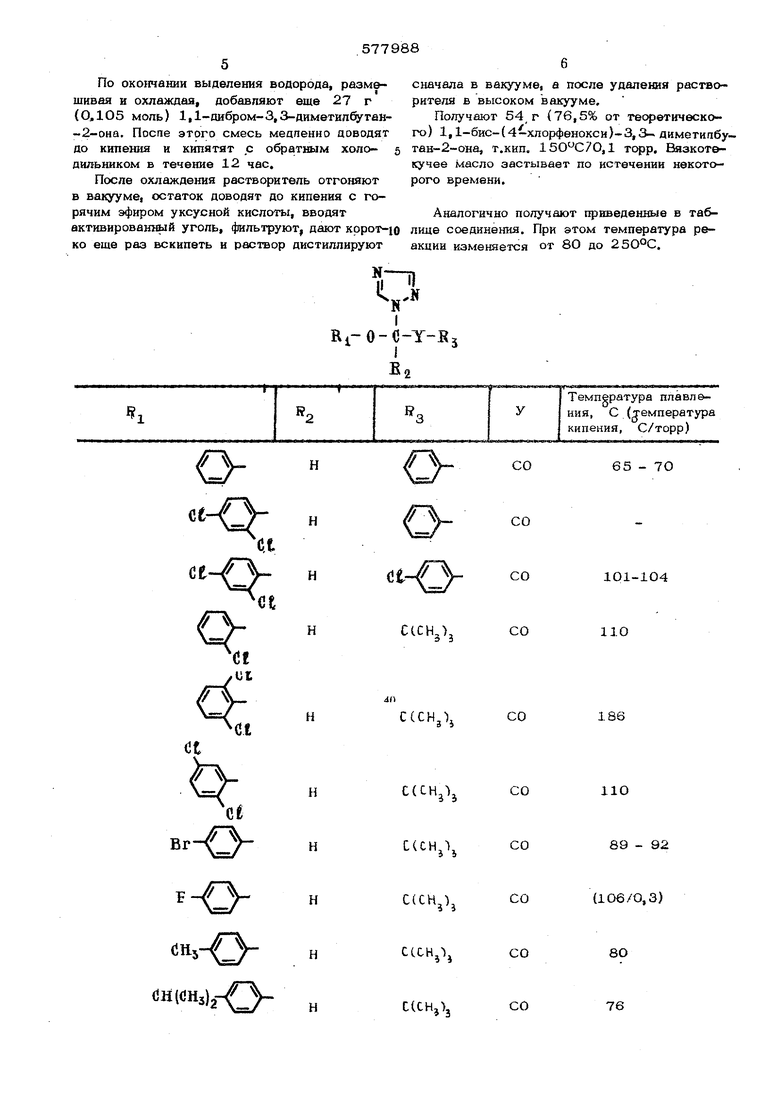
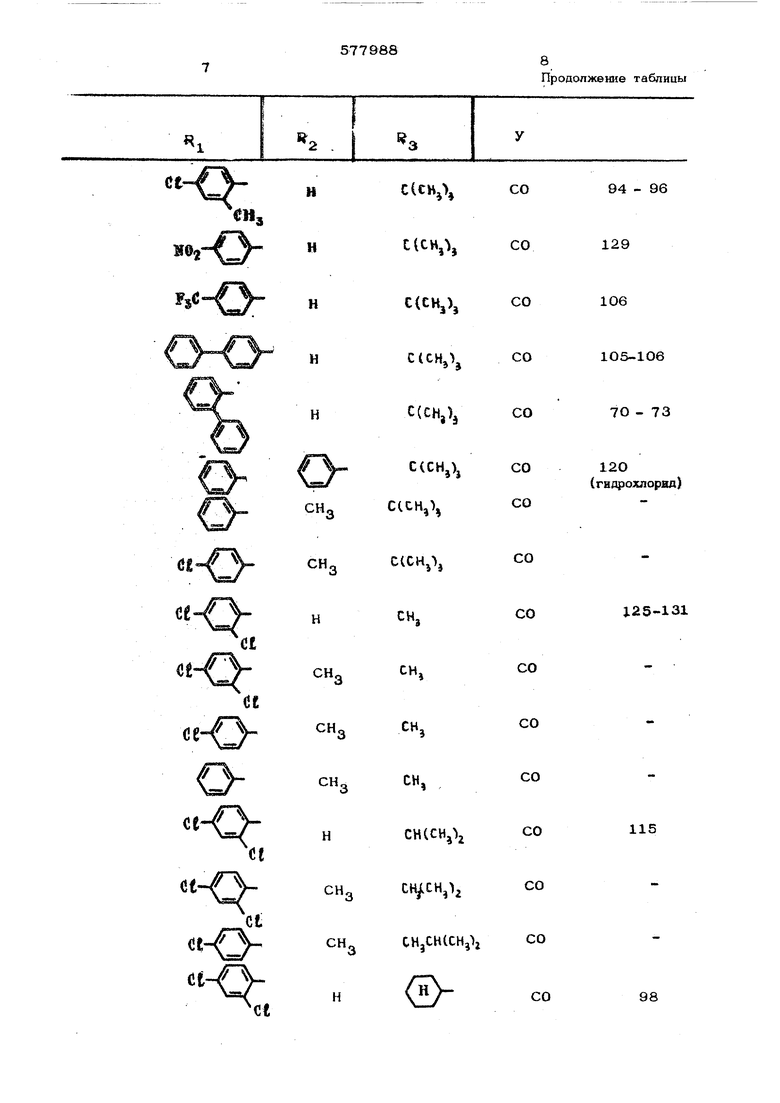
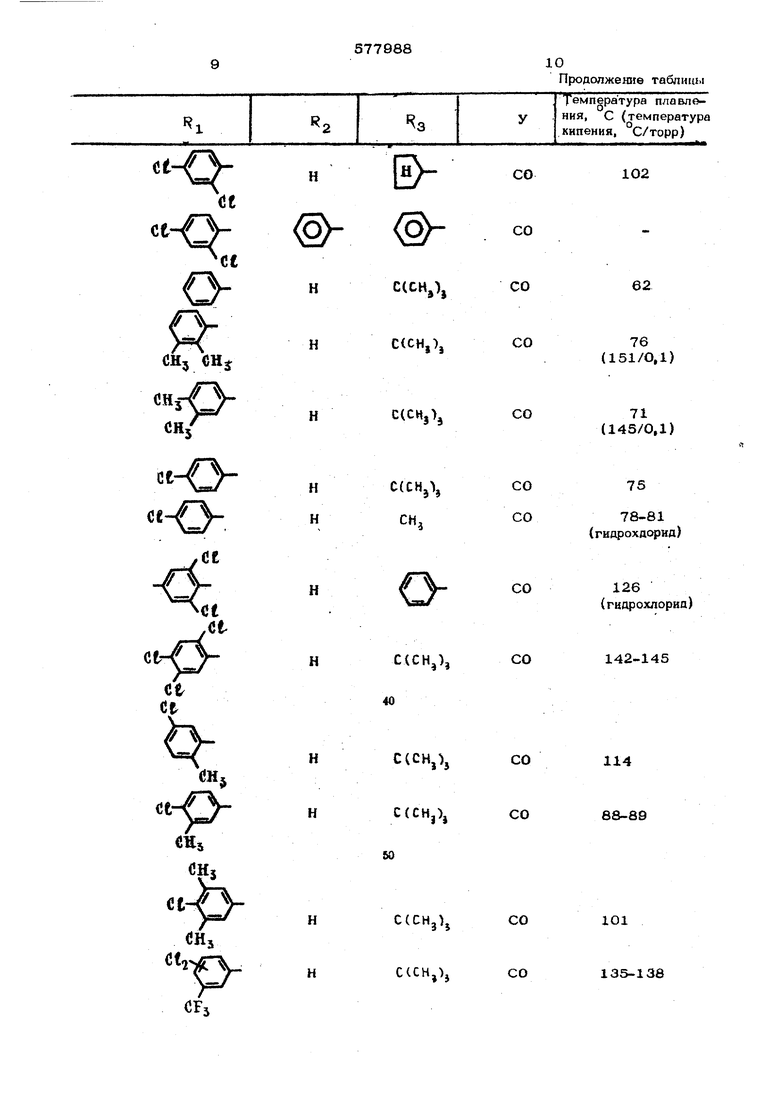
подвергают взаимодействию с гидрохлоридом 1,2,4 триазола формулы 3 S-n
4« HCt5К
R
,при 80-250°С с последующим выделением целевого продукта в свободном виде или в виде соли. Реакция протекает по След юшей схеме: o-e-co-cicMjls fil f 17,7 г (0,05 моЫ 1,1-бис-(4 хлор|енокси)-3,3-дд метилбутан 2-она тщательно азмешивают с 5,9 г (О,О55 моль) I,2t4- траазолгидрохлоркда в течение 1 час, наревают до и при этой температуре ставляют СТОИТЬ в течение 30 MHI при этом отщепнвшнйся Ф-хлорфакюл начинает ипеть. После охлаждения добавляют 1ОО мп едкого натр который перекрывают слоем до 200 мп простого эфнра. Эфирную фазу отделяют, три раза промывают 3%ным едкнм натром (по 30 мл) н два раза водой, каждый раз по 5О мл. После просушивания над сульфатом натрия растворитель отгощют в вакууме. Маслянистый остаток растворяют в 1ОО мл безводного простого эфнра и в этот раствор вводят-О.Обб мода хлористого водорода. При этом обра ётся осадок, который после СТОЯНИЙ в течение ночи отфильтровывают и допол|штельно промыв.ают прсютым эфиром. Получают 7,3 г--(46%-от теоретического) гйдрохлорида 1-Ц,2,4 триаэолил-Сг )(4 -хлорфенокси)-3,3-диметипбутан 2 она т.пл, 103-1О5°С, который можно иеревестн в свободное основатсе или в другие соли известными приемами. Исходное соедйнемне формулы 0. ,, „ . „.Сй-.со-а(снз)з получают следующим образом, 6,5 г (0,2 моль| 8О%-ного гидрида натрия суспедируют в 1ОО мл безводного ацетонитрила и при комнатной те лпературе прикапывают 27 г (0,21 моль) 4-хлорфенола в, 50 мл ацетонитрила, размешивая и охлаждая. По окончании выделения водорода, разм&шивая и охлаждая, добавляют еще 27 г
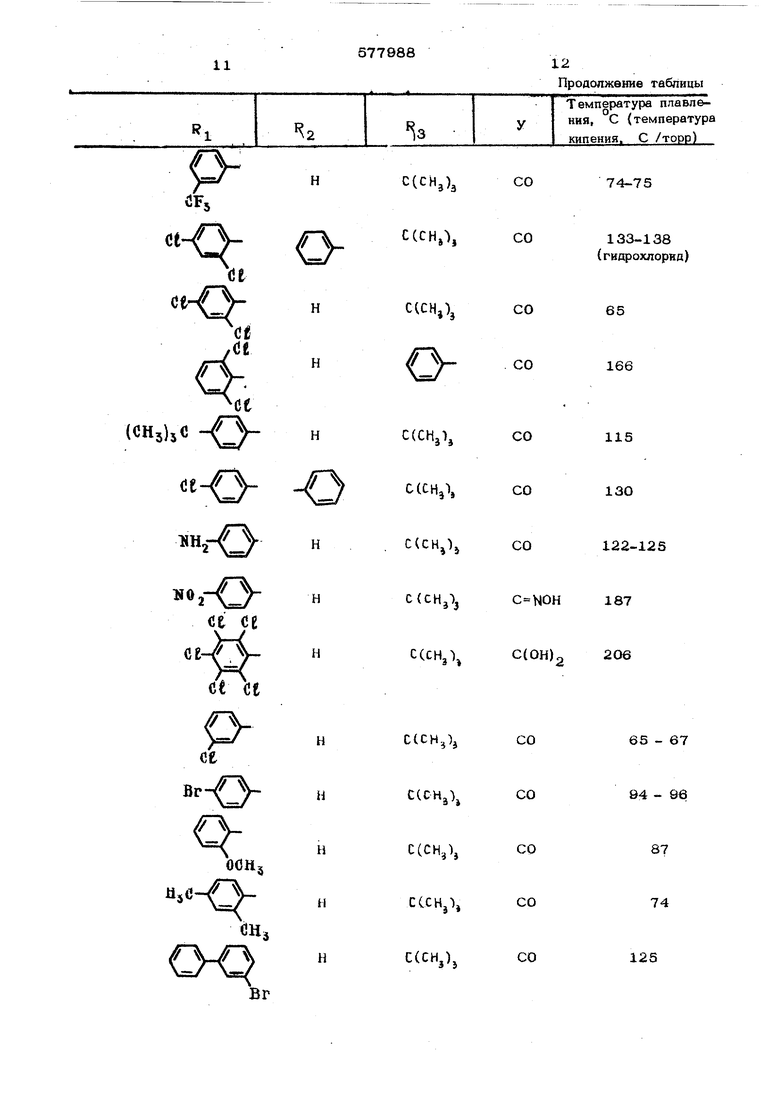
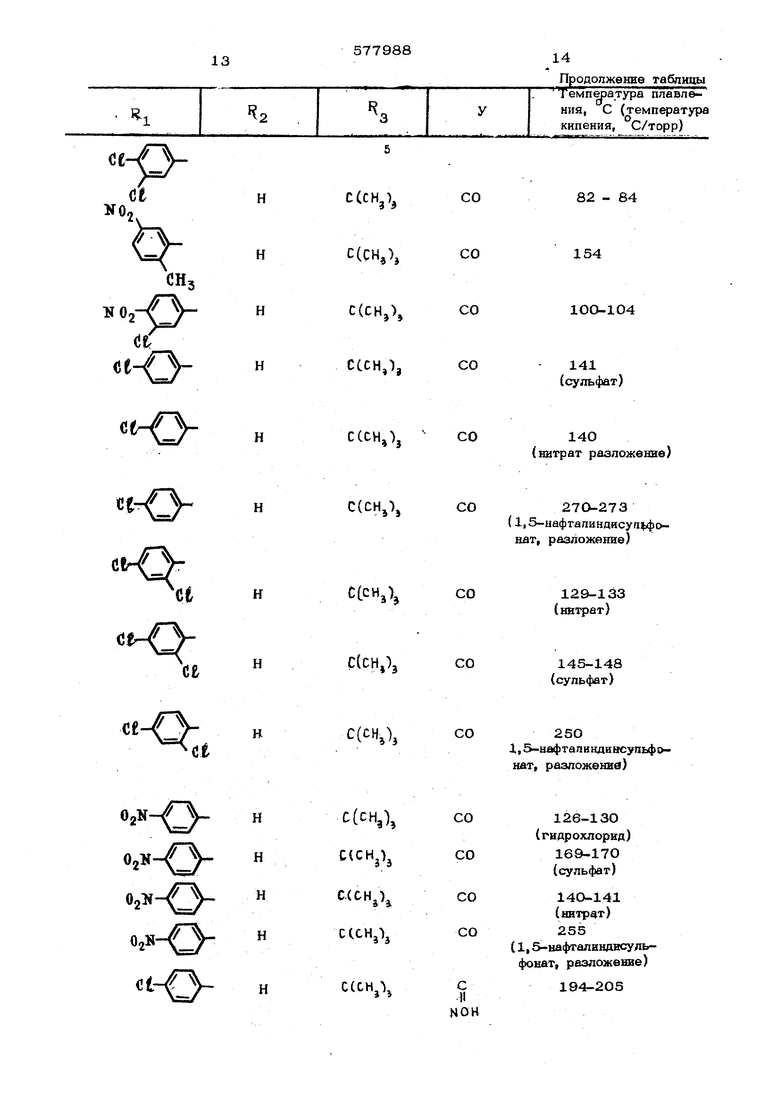
(0,105 моль) 1,1-дибром-3,3-диметилбуган-Получают 54 г (76,5% от теоретическо-2-она. Посгте этого смесь медленно доводятго) 1,1-6ис-(4-хлорфенокси)-3,3--диметипбудо кипения и кипятят с обратным холо- gтан-2-она, т.кип. ,1 торр, Вязкотедильником в течение 12 час.кучее масло застывает по истечении некотоПосле охлаждения растворитель отгоняютрого времени, в вакууме, остаток доводят до кипения с горячим эфиром уксусной кислоты, вводят Аналогично получают приведенные в табактивированный уголь, фильтруют, дают кррот-юлице соединения. При этом темп атура реко еще раз вскипеть и раствор дистиллируютакции изменяется от 8О до 25О°С.
RI-O-C-Y-B.
рителя в высоком вакууме.
|-Т1 li.,,N 1 сначала в вакууме, а после удаления раство

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 1,2,4-триазола или их солей | 1975 |
|
SU615857A3 |
| Способ получения производных простых арилфениловых эфиров или их кислотно-аддитивных солей,или их металлических комплексов | 1982 |
|
SU1148564A3 |
| Способ получения производных 1-карбонил-1-феноксифенил-2-азолилэтанола | 1983 |
|
SU1331427A3 |
| ЦИКЛИЧЕСКИЕ АЗОТСОДЕРЖАЩИЕ ПРОИЗВОДНЫЕ, СМЕСЬ ИХ ИЗОМЕРОВ, ОТДЕЛЬНЫЕ ИЗОМЕРЫ ИЛИ ИХ СОЛИ | 1994 |
|
RU2126002C1 |
| ГЕТЕРОЦИКЛИЧЕСКОЕ АМИДНОЕ СОЕДИНЕНИЕ | 2014 |
|
RU2681941C2 |
| МИКРОБИЦИДНОЕ СРЕДСТВО, СПОСОБ ПОЛУЧЕНИЯ МИКРОБИЦИДНОГО ПРЕПАРАТА И СПОСОБ БОРЬБЫ С МИКРОБАМИ | 1992 |
|
RU2095982C1 |
| ПРОИЗВОДНЫЕ ТРИАЗОЛО-(ПИРРОЛО-ТИЕНО- ИЛИ ФУРАНО-)-АЗЕПИНА, ОБЛАДАЮЩИЕ АНТИАЛЛЕРГИЧЕСКОЙ АКТИВНОСТЬЮ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНОЕ ДЛЯ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЕЕ ПОЛУЧЕНИЯ | 1993 |
|
RU2127737C1 |
| Способ получения производных -триазоло/1,5- / пиримидинов | 1969 |
|
SU511001A3 |
| Способ получения производных 1,2,4-триазолокарбамата или их кислотно-аддитивных солей | 1985 |
|
SU1436873A3 |
| N-Замещенные 3-алкилсульфанил-5-(1,2,4-триазол-1-илметил)-1,2,4-триазолы, способ их получения, фунгицидные и рострегуляторные композиции на их основе | 2017 |
|
RU2668212C1 |

н
н
се-/Л
н
со
65 - 70
со
со
101-1О4
Н
Н
С(
110
CCCHJ,со186
О 7
н
н
CCCHj-Jj
110
со
89 - 92
CCCHjlj
со
Б-/Л
Н
СПл-ГЛ
н
(}Н(ОНз),н
(106/0,3)
со
C(CH)j
CCCHj j
80
со
со
С(СН,)з
76
577988
Н
ct
8
Продолжение таблицы
98
СО
9
10 продолжение таблицы
ct-/
H
(je
1O2
CO
се-/Л
Ct
H
H
€H
H
H H
ce
H H
CO
62
CO
76
CO
C(CH,)j (151/0,1)
C( CO
71 (145/0,1)
75
(CHj,
CO
78-81 CO CH, (гидрохдорид)
126
CO (гндрохлорид)
СХСН,),CO142-145 HC(CH,)j (H, / CHj Ct C(CHj)j CCCH,) C(CH,)j 88-89 135-138
11
577988
12 Продолжение таблицы
Н
C(CHj)j
125
СО
13
577988
14
Продолжение таблицы
15 Формула взобретевия Спсюоб получения производных 1,2,4-три ааола обшей формулы К -О-С-У-ВЭ где Ц - фенил, незамещенный или аамешеаный галоидом, алкилом с числом атоме 1-4, галоидалкклом с числом атомо углерода l- нитрогруппой, аминогруппой метоюзилом или фенилом} - водород, алкил с чисзпом атомо углерода 1-4, фенил} алкил с числом атомов углерода 1-4, циклоалкил с числом атомов углерода 5-6, галоидфенил;У - группа -СО-, - -С(ОН)2-1
16 нли их солей, заключающийся в том, что единение общей формутш RI-O-C-Y-RS где R.,, Rp, Rg и У имеют указанные начения, подвергают воздействию с гидрохлоридом ,2,4-триазола формулы н при 8О-25О°С с последующим выделением цепкого продукта в свободном вида или в ввде соли. Источники информации, принятые во внимание при экспертизе: 1. Вейганд-Хильгетаг Методы эксперимента в огранической химии, М., Химия 1968, с. 498.
Авторы
Даты
1977-10-25—Публикация
1975-07-10—Подача