(54) СПОСОБ ПОЛУЧЕНИЯ ЦЕФАЛОСПОРИНОВЫХ СОЕДИНЕНИЙ ИЛИ ИХ СОЛЕЙ
Изобретение относится к способу попуче ния ио№1х цефалодпориновых соединений, имеющих широкий антимикробный спектр, Korojxjie могут найти применение как лекарственные препараты.
Известен Способ получения ацильных прОч. .Вэвовнътх цефалойпориновых кислот путем ацилнрования соответствующих 7--аминоцёфапоспориновых кислот 1.
Цепью изобретения является получение ношлх антибиотиков цефалоспоринового ряда, обладающих повышенным антимикробным спектром действия.
Предложен способ получения дефалоспориновых соединений формулы Т
ющ
)
о- т Ctt-s соон.
где R - 2-амино-2-фёнш1ацетил и 2-тиенилацетилгруппы;
1X - атом водорода или галоида,
или их солей, заключаквдийся в том, что 5 а1шлируют соединение формулы jl
НоХ
10
Х)(щСН.18
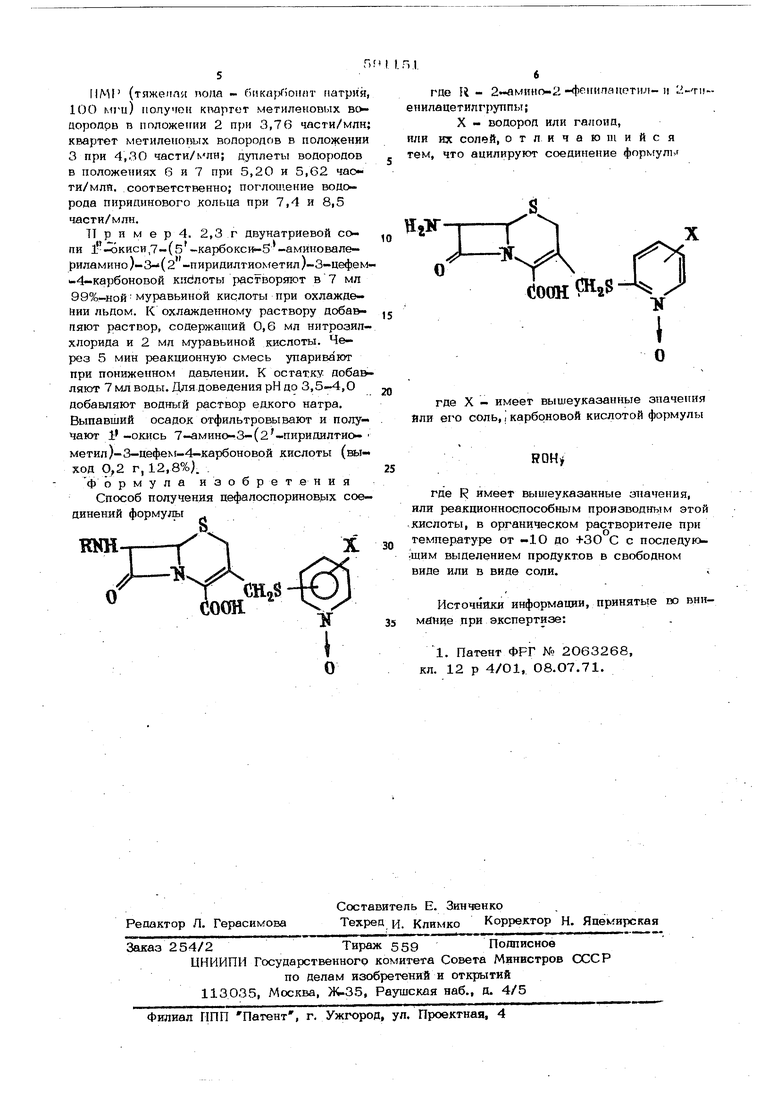
где X - имеет выщеуказанные значения, или его соль, карбоновой кислотой формулы
ROH ,Ш
где R имеет выиюуказанные значения, или реакционноспособным производным этой кислоты в органическом растворителе при температуре от -10 до +30 С с последующим выделением продуктов в свободном виде или в виде соли.
Если в реакциях ацилнроваиия в качес1 ве ашшируюшего реагента применяют свободную карбоновую кислоту, то лучше применять и соответствуюшие «онденсируюшие реагенты, к ним относятся N,N -дпзамешенные карбодиимиды, напримерN,N -дицикло1-ексилкарбодиимид и т.п..; азолидные соединения, напримерH,N карбонилимидазол, N,N тионилдиимидазол и т.п.; и такие дегидратируюшие реагенты, как N -этокси- карбонил-2--этокс -1,2-дигидрохинолин, хлорокись фосфора, алкоксиацетилен и т.п. Эта реакция, как правило, проводится в растворителе. Растворителем может служить обычный растворитель или civecb растворител.ей. К таким растворителям относится вода, ацетон, тетрагидрофуран, диоксан, ацетрнитрил, хлороформ, дихлорметап, дих(лорэтилен,пиридин, диметиланилин, диметил- формамид, диметилацетамид, диметилсульфок- сид и т.п. Реакцию обычно ведут при охлаждении или при комнатной температуре.
Пример. 1,84 части N -трет-бутоксикарбонил-D-фенилглицина и 1,08 части триэтиламииа добавляют к 2О мл сухого татрагидрофурана. Смесь охлаждают до -6 С К охлаждаемой от -6 до -10 С смеси по каплям добавляют 1,06 г по объему изобу тилхлоркарбоната. По окончании добавления смесь нагревают до комнатной температуры и перемешивает в течение 30 мин. Выпа&ший хлоргидрат триэтиламина отфильтровывают. Полученный раствор смешанного анги дрида кислоты добав-пяют к смеси 1,77 г I -окиси 7-а.м1гао-3-(2-пиридилтиометнл)-З-цефем-4-карбоновой кислоты и 200 мл диметилацетамида. Смесь перемешивают 2 час при комнатной температуре. Димети- лацетамид отгоняют при пониженном давлении. К остатку добавляют смесь 24 мл три(} торуксусной кислоты и 6 мл анизола. Этой смеси дают реагировать 5 минут при комнатной температуре, а затем ее упаривают при пониженном давлении. Концентрированный раствор обрабатывают ионообменной смолой (Амберлит. и- сушат ,вымораживанием с получением 0,83 части 1 -окиси 7-(D-2-амино-2 -({)енилацетамидо)-3-(2 -пирицилтиометил)-3-цефем-4-карбоновой кислоты .(выход 32,4% ).-{асть этого продукта очищают, растворив его в водном растворе бикарбоната натрия и пропустив раствор через KOHOHjcy, заполненную нолистирол - ной смолой (Амберлит ХАД-Ц ) с получением eio натриевой соли.
В11числено для С ,ИдМ,О,5„Мв1/2 II О ,%: С 5О,08; и 4,00,- k 11,12.
Найдено,:.:.: С 5О,13; II 4,37; N 11,03.
Ультрафиолетовый спектр поглощения (водо); при 236 ммк ( 289ОО) и 263 ммк (I 16100).
ПМР (тяжелая вода, 100 мгц) дал KBfii тет метиленового водорода в положении 2 при 3,49 части/млн. квартет метипенового водорода в положении 2 при 3,49 части/млн квартет метиленового водорода в положении 3 при 4,40 части/млн и дуплеты водородов в положениях 6 и 7 при 5,14 и 5,48 части/млн, соответственно.
Пример 2.3,48г l-oкиcи7-aминo-3-(2 пиридилтиометил)-3-Ц.ефам-4-карбоновой кислоты суспендируют в 60 мл диметилацетамида. К суспензии добавляют при nepeMeujHBaHHH 2 г 2-тиенилацетилхлорида и перемешивают в течение 3 час. Нерасрворикшге вещества отфильтровывают, диметилаиетамид отгоняют при пониженном давлении, к остатку добавляют воду. Выпавший осадок фильтруют и промывают, хлороформом с получением 2,5 г 1 -окиси 7-(2-тиенилацетамидо)-3-(2 -пиридилтиометил)-3-цефем-4-карбоновой кислоты (выход 52%).
В. ПМР спектре (тяжелый диметилсульфоксид, 100 мгц) продукт дал квартет ме тиленовых водородов в положении 2 при 3,6О части/млн; синглет метиленовых водородов 3,73 части/млн; синглет метиленовых водородов тиенильной группы, при 5,07 части/млн; дуплет водорода в положении 7 при 5,62 части/млн,
П р и м ё р 3. 3 г 1 -окиси-7-(5карбокси-5--трет-бутоксикарбониламинова. лериламидо)- . (2 -пиридилтиометил)-3-цефем-4-карбоновой кислоты, которая поч лучена при обработке 7-(5-карбокси-5-. -тре т-бутоксикарбонила мино вал ерилам и до )-. цефалоспораната натрия, и натриевую сЪль 2-меркаптопиридин-1-окиси добавляют к 100: мл дихлорметапа. К этой смеси добавляют 5. мл пиридина и- 10 мл триметипхлорсилана и перемешивают в течетгае 10 мин при комнатной температуре. Реакционную смесь охлаждают до -1О С и в нее добаЕ ляют 1О мл пиридина: и 7 г пятихлористо-. го фосфора и перемешивают в течение 2 О мин с образованием ими.дгалоида. Далее реакционную смесь еще раз охлаждают до
-20 с.и добавляют в нее 125 мл метанола для получения имшюэфира.Полученную таким смесь нагревают до комнатной температуры и добавляют 20 мл 25Xiного водного, раствора муравьиной кислоты, далее, добавляют триэтиламин для доведения рП среды до 3i5-r4,0. Выпавший осадок отфнльтровыкают и получают 1 -окись 7-амино-З-(2 -анридилгпомспш)-3-цефем« -4-карбонопой кислоты (выход 0,4 г,
19,7%). ; .
, В ультрафНопотовом спектре поглощения (0,в°л-ный 1юдш;,1й растгор бикарбоната Гнатрия): при 236 ммк ( I 21300) и при 264,5 ммк ( 1380О), IMP (тяжепля пода - патрия, 100 мги) полутон Kiioprer метиленопых воаоропрв п ппложечни 2 при 3,76 части/млн; квартет метилеиш ых вопородов в положении 3 при 4,30 части/млн; дуппетъ водородов в положениях 6 и 7 при 5,20 и 5,62 части/мля. соответственно; поглощение водорода пиридинового кольца при 7,4 и 8,5 части/млн, IT р и м е р 4. 2,3 г двунатриевой сопи 1 -6киси,7(5-карбокси-5 -аминовалериламино)-3-(2 -пиридилтиометил)-3-цефеК1 -4-кау:боновой кпелоты pacTBopsnor в 7 мл 9Э%-ной муравьиной кислоты при охлаждении льдом. К охлажденному раствору добавпяют раствор, содержащий 0,6 мл нитрозилхлорида и 2 мл муравьиной кислоты. Через 5 мин реакционную смесь упаривают при пониженном давлении. К остатку добавляют 7 мл воды. Для доведения рН до 3,5-4,0 добавляют водный раство.р едкого натра. Выпавший осадок отфильтровывают и получают 1 -окись 7-амино-3-(2-пиридилтие - метил )-3-цефем-4-карбоновой кислоты (выход Of 2 г, 12,8%). . формула изобретения Способ получения нефалоспориновых соединений формутаг Д соон. где R - 2-амииг -2-ф ля тил-и L.-ri -енилацетипгруппы;X - водород или галоид, или их солей, отличающийся тем, что ацилируют соединение формуль dooH 2 где X - имеет вышеуказанные значения или его соль, I карбрновой кислотой формулы где R имеет вышеуказанные значения, или реакционноспособным производшэ1м этой кислоты, в органическом растворителе при температуре от -1О до +30°С с последуюим выделением продуктов в свободном виде или в виде соли. Источники информации, принятые во вниMdHi e при экспертизе: 1. Патент ФРГ № 2О63268, кл. 12 р 4/01, 08.07.71.

| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ЦЕФАЛОСПОРИНА | 1971 |
|
SU425401A3 |
| Способ получения производных цефалоспорина | 1981 |
|
SU1087076A3 |
| Способ получения 3-йодметилцефалоспоринов | 1981 |
|
SU1069627A3 |
| Способ получения производных цефалоспорина или их легко гидролизуемых сложных эфиров или их солей с щелочными металлами | 1981 |
|
SU1194279A3 |
| Способ получения цефалоспоринов или их солей | 1974 |
|
SU676166A3 |
| Способ получения 7-ациламидо-7метокса-3-р-3-цефем-4-карбоновой кислоты | 1972 |
|
SU454742A3 |
| Способ получения 7-метоксицефалоспори-HOB или иХ СОлЕй | 1976 |
|
SU799668A3 |
| Способ получения производных цефалоспорина | 1982 |
|
SU1119607A3 |
| Способ получения сложных эфиров 3-цефем-3-сульфоната или их солей | 1974 |
|
SU576946A3 |
| Способ получения производных 7-аминоцефалоспорановой кислоты | 1971 |
|
SU640664A3 |


Авторы
Даты
1978-01-30—Публикация
1972-11-23—Подача