-триазин, 3-хлор-5|6-бис- (4-.пропиленил}-,2,4-триаэин, З-хлор-5,6-еис-(4-изопропил енил)-1,2,4-триазин, З-хлор-5,6-бис- (4--метоксифенил) -1,2,4 -триазин, З-хлор-5,б-6ис(4-этоксиенил)-,2,4-триаэин, 3 хлор-5,6бис-(4-пропоксифенил)-1,2,4-триазин, З-хлор-5,б-бис(4-изопроПоксифенил)-1,2,4-триазин, 6- 4-6ромфенил)-3-хлоЕх-5- (4-фторфенил) -1,2,4 триазин, З-хлор- т (.4- хлорфенил) -6- (4 ггропилфенил)-1,2,4-триазин, S(4-бромфенил) -З-хлор-6- С4-изопропоксифенил) -4,2,4-триазин, 3-хлор 6 -.(4-9Тилфенил) -5-{4-метилфенил)-1, гИ-триазин, З-хлор-5-{4-изопропокоифенил)-ё-(4 метилфенил)-1,2,4-триази, 3-хлор-5- (4-э.токсифенил) -б- (4-мвт6ксифенил) -1,2,4-триазин,
Предцрчтнтельны соединения формулы I, в которой RI и Кг.- алкоксйл. с 1-3 -aTOMajviH углерода пре1шущёственно метоксил
Исходнне, 3.-океи-5,.б-диариЛ 1,2,4-триазины могут бнть пЬлученн кондеН сацией соотйетствуюадегс ди бен зоила с семикарбазидом
Необходимые дибаизоилы получают окислением соответствунндйк бензойно сульфатом меди в пиридине.
Пример 1, Получение.; 3-хлор-5,6-бис- (4-мвтоксифвнйл);-1,.2,4-трИазина. . . .,. -, . - , :, , J
540 г (2 моль) диайизоила ,4,4-ди метоксибенэйла/- 223-fc ) - соля-; нокислого семикарбазйда, 180 г (2,2 моль) ацетата натрия и 3j-5 л уксусной кислоты кипятят io. обратным холодильником в. теч1енив ночи. Охлажденную реакционную смесь выливают в 5 л зводы. .Выпавший твердый -продукт ©тделяют филbTpOBaHUeMir промывSK)T водой и перекристаллйзОвЫвают из уксусной кислоты. Получают 434 г..3-окси -5,6-бис- (4-метоксиф.енйл) -1,2 |4-триазина, т.пл. 272-27.. .
Вычислено, % С 66,01; Н 4,89 .N. 13.58.. .
С.,Н„М,0,. : : ,:/:.
Найдено, %: С 65,92;:Н 5,04 N13,66.
10 г 3-окси-5,6-бис-(4-метоксифенил)-1,2,4-триазина в 50 мл хлороки. си фосфора кипятят с обратнша холодильником в течение 1,5 ч.. Охлажденную смесь выливают в измельченный : лед и полученную, смесь экстрагируют эфиром. Экстракт последовательно промывают 2%-ной гидроокисью натрия и водой до нейтральной реакции промывных вод; Эфирный экстракт сушат безводным сульфатом натрия и упаривают. Остаток вновь растворяют в эфире, фильтруют, и после упа.ривания фильтрата получают 9.,О Г 3-хлор-5,6-бис-(4-метоксифенил),4-триазина, т.пл. 130-132 С.
Вычислено, %: С 62,30j Н 4,31 се10,82; N 12,82. C Hi-vOeNjOaНайдено, %: С 62,50; Н 4,487 се 10,53; N 12,99.
Пример 2. Получение 3-хлор-5,6-бис-(4-фторфенил)-1,2,4-триазина..
Смесь 23,3 г 4,4 дифторбензила, 12,1 г солянокислого семикарбазйда,. 8,8 г ацетата натрия и 200, мл уксусной кислоты кипятят с обратным холодильником в течение ночи. Реакционную смесь разбавляют 200 мл воды. Твердый осадок отделяют фильтрованием ,-перекристаллиэовывают из 90%-ногЬ (по объему) этанола и -оолучают 13,6 г 5,6-бис-(4-фторфенил) -З-окси-1,2,4-триаэина, т.пл. 263-266°С. Вычислено, %: С 63,16,- Н 3,18; N1-4.73. .
,№0.
найдено,-%: С Ь3,37; Н 3,35; H 14,52.
. Смесь 7,1 г 5,6-бис-{4-фторфенил1
-3-окри-1;,2,4-триазина и 50 мл хлорокиси фосфора кипятят с обратным холодильником в течение 2 ч. Реакционный раствор выливают в воду и полученную смесь экстрагируют эфиром.
эфирный экстракт промываютводой и сушат безводным сульфатом натрия. Эфир отгоняют в , твердый остаток перекристаллизовывают из . .втилйцетата и получают 2,1 г З-хлор-г -5,6-бис- (4-фторфенил} -1,2,4-триази- на, т.пл. 185-192 с.
П р и м ер 3. Получение 3-хлор-5,6-ёис-(4гхлорфенил) -1,2,4-триазина.,
Смесь 55,8 г 4,4-дихлорбензила, 24,5 солянокислого семикарбазйда, 18,1 г ацетата натрия и400 мл уксусной кислоты кипятят с обратном холодильником в течение ночи. Реакционную смесь разбавляют 300 мл воды.
Твердый осадок отделяют фильтрованием. Твердое вещество растворяют в этаноле и полученный раствор охлаждают. Выпавшие кристаллы отделяют фильтрованием.
Фильтрат концентрируют досуха в вакууме и твердый остаток три раза перекристаллизовываю.т из этанола, получая 4,7 г 5.,6-бис-(4-хлорфенил)-3- ,. -окси-1,2,4-триазина, т.пл. 237-240 С Вычислено, .%: С 56,63 Н 2,85
Г 13,21.
Найдено, %s С 56,49; Н 2,80; N12,94 Смесь 1 г 5,6-бис-(4-хлорфенил)-3-окси-1,2,4-триазина и 10 мл хлорокиси фосфора кипятят с. обратным холодильником до тех пор, пока реакционная смесь не начнет темнеть. Реакционную смесь концентрируют досуха в вакууме. Оставшееся масло растворяют в эфире. При охлаждении эфирного pacf вора выпадает твердый осадок. Получают
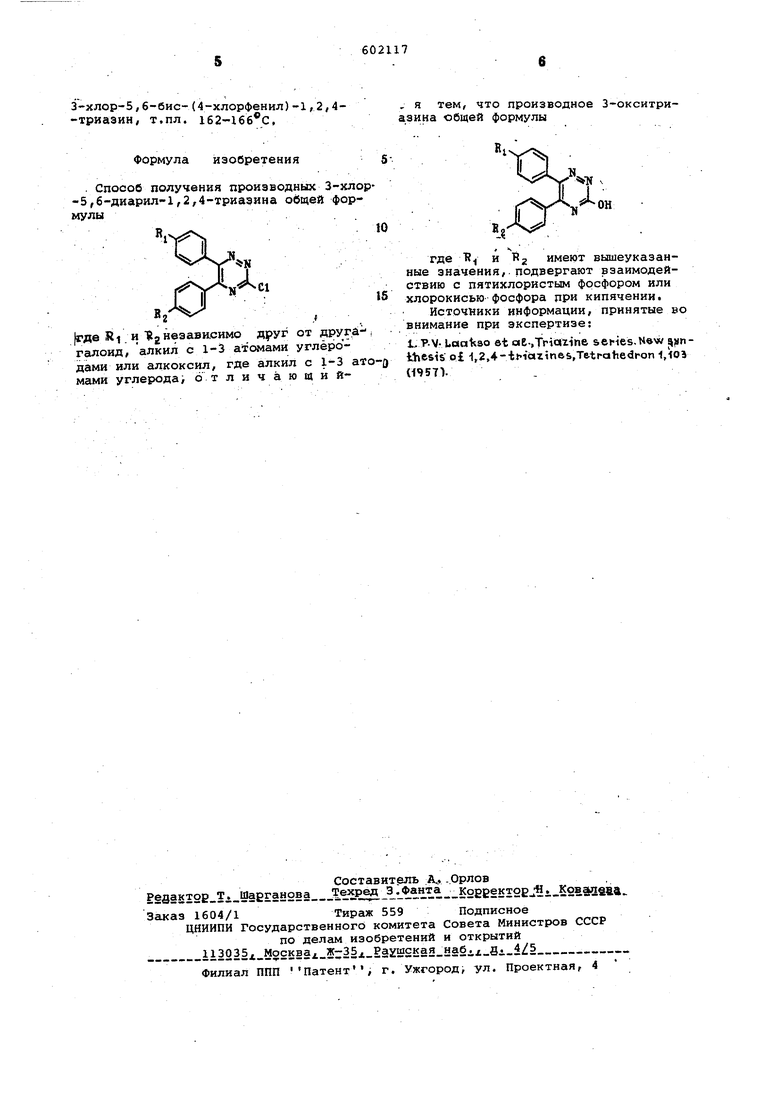
З-хлор-5,6-бис-(4-хлорфенил)-1,2,4-триаэин, т.пл. 1б2-16б с, Формула изобретения Способ получения производных 3-хлор-5,б-диарил-1,2,4-триаэина общей формулы. где RI.H RjHeaaBKCHMO друг от друга-. галоид/ алкил с 1-3 атомами углёродами или алкоксил, где алкил с 1-3 атомами углерода; 6 т л и ч а ю щ и й, я тем, что производное 3-окситриаэина общей формулы где К| и Kj имеют вышеуказанные значения,, подвергают взаимодействию с пятихлористым фосфором или хлорокисью фосфора при кипячении. Источники информации, принятые во внимание при экспертизе: 1, -V- et dt-.Trioizine seHes.New jjnthesisol 1,2,4-iMazine&,Tetraliei3ron «/roi H957V

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных 5,6-диарил-1,2,4-триазина и их солей | 1976 |
|
SU598561A3 |
| Способ получения @ -арил-4- @ 4,5-дигидро-3,5-диоксо-1,2,4-триазин-2-(3Н)-ил @ -бензолацетонитрилов | 1985 |
|
SU1443799A3 |
| ГЕТЕРОПОЛИЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ (ВАРИАНТЫ), ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ И СПОСОБ ЛЕЧЕНИЯ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С МЕТАБОТРОПНЫМИ ГЛУТАМАТНЫМИ РЕЦЕПТОРАМИ | 2000 |
|
RU2296127C9 |
| КОНДЕНСИРОВАННЫЕ ТРИАЗОЛАМИНЫ В КАЧЕСТВЕ МОДУЛЯТОРОВ Р2Х7 | 2010 |
|
RU2533122C2 |
| Способ получения производных 5,6,7,8-тетрагидропиридо-(4",3:4,5)-тиено-(2,3-д)-пиримидина | 1969 |
|
SU504492A3 |
| ДИФЕНИЛЬНЫЕ ГЕТЕРОЦИКЛИЧЕСКИЕ СОЕДИНЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ И СПОСОБ ЛЕЧЕНИЯ | 1997 |
|
RU2175319C2 |
| Способ получения производных 3-азабицикло (3,1,0)-гексана или их солей, рацематов или оптически-активных антиподов | 1977 |
|
SU786891A3 |
| Способ получения производныхиМидАзОлА | 1978 |
|
SU803858A3 |
| Способ получения 2-замещенных 1,4-бензодиазепинов | 1976 |
|
SU1126209A3 |
| Способ получения производных меркаптоимидазола или их кислотно-аддитивных солей | 1979 |
|
SU1259962A3 |


Авторы
Даты
1978-04-05—Публикация
1976-03-17—Подача