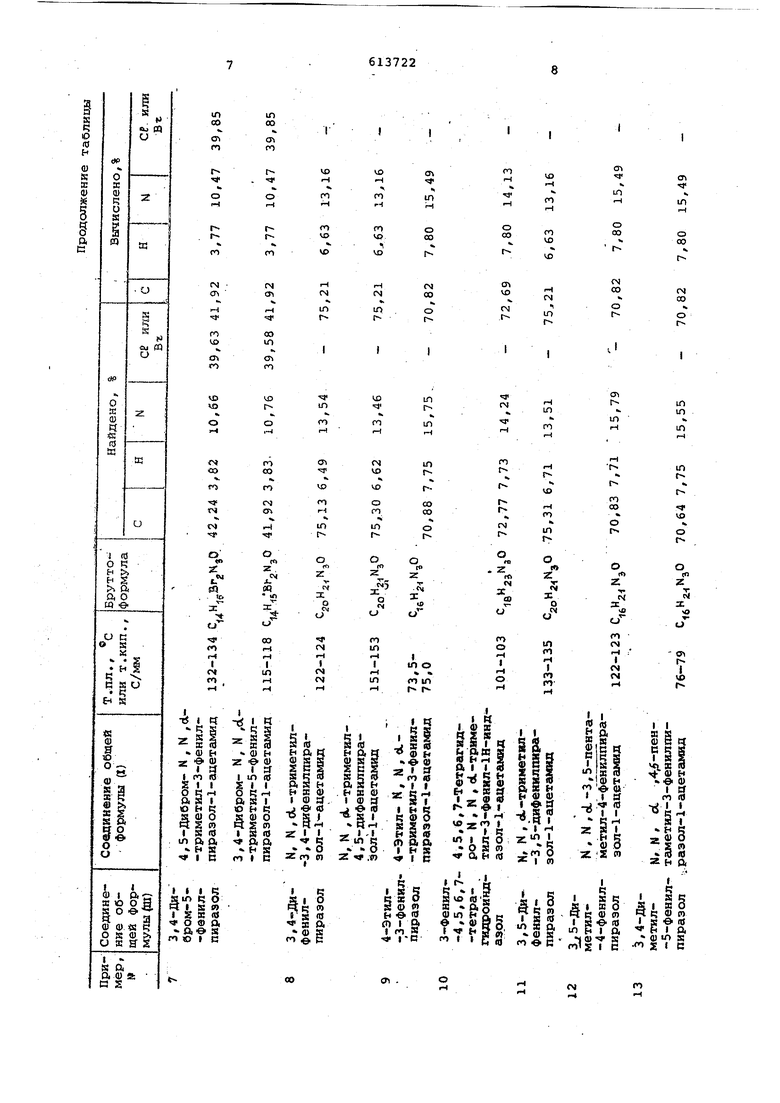
Изобретение относится к спосб получени новых замещенных пиразоло общей формулы .Кг Ri-e-c-u/ .К - водород. галоген, алкил.с атомами углерода, галогенгшкил атомами углерода или фенил; В - водород И.ПИ метил; ЕЗ - водород, ёшкил с 1-8 атома ми углерода, фенил или ,бензил; В - водород или алкил с 1-6 ат мамя углерода или . 3 морфолин, пирролидин или пиперидин; АН В - алкил с 1-6 атомами углеро да, фенил, гёшоген, циан, нитрогруп па или трифторметил, кроме того, В и R, вместе обозначают кольцо с 5-7 атомами углерода; Z - rovrtna формулы -Хп , TJ-lCfl или З где X - галоген, нитрогруппа, алкил га 1огенсшкил или алкоксигруппа с 1-3 атомами углерода; П - О,1 или 2, или их кислотно-аддитивных солей с сильными кислотами, обладающих биологически активными свойствами. в литературе известны пиразолы, заманенные углеводородаи и, обладающие биологической активностью, которые получают взаимодействием пиразолов с галогензамещенным углеводородом l. Цель изобретения - синтез новых замещенных пиразолов общей формулы (I), которые могут найти применение в сельском хозяйстве. Предлагаемый способ получения замещенных пиразолов, основанный на известной в органической химии реакции, заключается в том, что 2-галогеналканамид о(аей формулы R -C-C- « R, Y где Y - галоген; К, B,B,jHR, имеют указ-анные значения, подвергают взаимодействию с пиразолом общей формулы -U-: гце А, В и Z имеют yxiaaaHHbie значения в присутствии основания при 0-200°С. В качестве основания используют такие, как гидрид натрия, метоксид натрия, этоксид натрия, карбонат натрия, карбонат калия и другие. Реакцию проводят в присутствии растворителя такого, как бенэбл, эфир, тетрагидрофуран (ТГФ), метанол, этанол, ацетон, димётилформамид и другие. П р и м е р 1 .N / N , oL , 4-тетраметил-З-фенилпйразол-1-ацетамйд и N, N , оС , 4-тетраметил-5-фенилпиразол-1-ацетамид. К раствору натриевой соли 4-метил -3-фенилпиразола, полученной добавле нием 3,0 .г (0,071 моль) гидрида натрия в масле (57%) к 10,5 г (0,066 моль) 4-метил-З-фенилпираэола в 100 мл ТГФ, добавляют 10,0 г (0,075 моль)N ,N -диметил-2-хлорпропионамида. Через 18 ч раствор упаривают, остаток экстрагируют хлороформом и водой. Остаток, полученный пос ле выпаривания хлороформной фазы, хр матографируют на силикагеле, применяя в качестве элюента смесь бензолэтил ацетат, и получают 17,7 г первого целевого продукта, который после 2-кратной перекристаллизации из циклоГексана выделяется в виде тонких игл, т.пл. 74,5-76 , . , ЯМР: (СБСЕз) ( : 1,63 (d, 3, CHjCH), 2,20 ( s , 3, ArCHj), 2,92 ( 8 , 3, N-CH,), 3,02 ( s , 3, N-СНз), 5,43 ( Я 1/ CHjCH), 7,30-7,5a ( m, 4 At-H) , 7,56-7,80 (m, 2, ) . Найдено,%: С 70,08; Н 7,46; N16,62 C.ffH, W,0 . Вычислено,%: С 70,00)i Н 7,44; N 16,33. При продолжении элюирования колонны получают 2, второго целевого продукта, который после перекристаллизации из смеси бензол-скеллизольв В, а затем из этилацетата выделяется в аналитически чистом виде, т .пл. 88-90°С.. , ЯМР (CBCEj) ( : 1,67 (d , 3, СН,СН), 1,97 ( а, 3, АУСН), 2,57 (в., 3, N -СНд), 2,83 (б , 3, N -СН-), 5,02 ( «Vf 1 СН,СН) и 7,15-7,55 ( tr , 6, AfH) . Найдено,% С 70,13; Н 7,51, N16,49. Вычислено,%: С 70,00, Н 7,44 N16,33. Пример 2. N, N,ol ,4-тетраметил-3-фенилпиразол-1-ацетамид. Смесь 3,65 г (0,023 моль) 4-метил-3-фенилпиразола, 3,78 г (0,027 моль) N , М.-диметил-2-хлорпропионамида и 4,4 г. (0,032 моль) безводного карбоната натрия 6 ч нагревают, размешивая при 130 С, смесь охлаждают и кристесллйзуют из 50%-ного водного метанола, получая 4, 5 целевого продукта в виде больших брусков, т.пл. 87-89с. В таблице 1 приведены соединения общей формулы (I), полученные аналогично примеру 1 из соотвегствуювдих пиразолов общей формулы (i ).
Oi
(П 1Л
VO
ъ
го
чсо









| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 1замещенных 3,4,5-трибромпиразолов | 1973 |
|
SU625605A3 |
| Способ получения ациламинопроизводных гетероциклических соединений | 1976 |
|
SU648094A3 |
| Гербицидный состав | 1975 |
|
SU581838A3 |
| Способ получения производных @ -фенилпиразола | 1983 |
|
SU1309909A3 |
| Способ получения ациламинозамещенных гетероциклов | 1977 |
|
SU654168A3 |
| СПОСОБ ПОЛУЧЕНИЯ N-ФЕНИЛПИРАЗОЛОВ | 1987 |
|
RU2035452C1 |
| ПРОИЗВОДНЫЕ N-ФЕНИЛПИРАЗОЛА | 1991 |
|
RU2087470C1 |
| Бис-четвертичные соли пиразола в качестве активаторов спектральной сенсибилизации бромйодсеребряных фотографических эмульсий для черно-белых и цветных фотоматериалов | 1990 |
|
SU1747441A1 |
| Способ получения бензил-2,2-диметокси ацетамидов | 1976 |
|
SU663299A3 |
| Способ получения - 4-/2-(пиразол-1-КАРбОНАМид)-эТил/-бЕНзОлСульфОНил-МОчЕВиН | 1978 |
|
SU816398A3 |

01
го
00
ш
со
о
1Л
40
о
91
л
о
-
в
I гu00
го 1Л
г о
ъ Г)
оо г
%
го «л
N
о
о
ОЧ
о
00
ы
s с; н н ж ф
и
X I
а о -
Н А I I н 5 ((SO
IfS
|
«т
, н S а S ж я ч
I X 0) с о П I «1 I л
.л (N
&Л. «C5SS
я я S 5
I 9 Ш с О го I о I л 15 Пример 28. Аналогично примеру 1, заменяя 2-хлор- N, N,-диметилпропионамрш 2-хлор- N, N -диэтилпропионамидом, а 4-метил-З-фенилпира эолом 4-метил-З-фенилпиразол, 4-хлор- N , N-диэтил- оС-метил-3-фенилпираэол-1-ацетамид, т.кип. 191 192°С/О, 74 мм рт.ст. Найдено, % С 62,50; Н 6,74, N 13,48; Се 11,58 с бН оСеНзО Вычислено,%: С 62,84; Н 6,59; N13,74; Ct-ll,59 и 4-хлор- N , N-диэтил- о--метил-5-фенилпиразол-1-ацетамид, т.пл. 85-87°С. Найдено,%: С 62,92; Н 6,71; N 13,62; се 1.1,58 CifiHsoCI N30 Вычислено,: С 62,84; Н 6,5; N13,74; се 11,59 П р Н м с р 29. Аналогично приме ру If заменяя 2-клор Н , N -димет.илпропионамид 2 хлор- N, N-диматилбутирамидом, получают d этил-М , N,4 Тримет ил 3 -фенил пираэ ол-1 - ацетамид т.пл. 86-88°С, Найдено,%: С 70,91; Н 7,93; N15,73 С,,,Н2, N,0 Вычислено,S: С 70,82 Н 7,80; N15.1 49 и ci зтил N, N , 4-триметил-5-фенилпнразол-1-ацетам1д, т.пл. 88-90°С. Найдено, %:: С 70,83; П 7,82; N15,56 С,5Н;,„НзО Вычислено,%1 С 70,82; Н 7,80; N15,49. Пример 30, о(. Этил- N, N,4 -триметил 3-фенилпиразол т-ацетамид К перемешиваемому раствору 632 г (4,0 моль) 4-метил-З-фенилпиразола в .1,0 л ТГФ при за 10 мин добавля ют 216 г (4,0 моль) порошкового метоксида натрия, поддерживая температу ру ниже 30°С путем охлаждения извне в 30 мин по каплям добавляют 911 г (4,7 моль) 2-6ром- N, N-димети бутираыида, раствор размешивают еще 30 мин при комнатной температуре, за тем удаляют ТГФ при пониженном давле нии. Остаточное масло распределяют между хлороформом и водой. Хлороформ ный слей выпаривают,остаточное масл перекристсшлизовывают из смеси бензо скеллизольв В,: получая 722 г,целевог соединения, т.пл. 85,5-87,5 С. Упариванием полученного при кристаллизации маточного раствора получа ют, 365 г масла, содержащего дополнительный продукт. Пример 31. Аналогично приме ру 1, но заменяя 4-метил-З-фенилпир зол 3-(2-тиенил)-пиразолом, получают N , N, оС-триметил-3-(2-тиенил)-пиразол, т.пл. 95-97°С. Найдено,%: С 57,52, Н 5,98; N16,76; 513,17 C,jH,5 N305 Вычислено,%; С 57,80; Н 6,06; 16,85; 5 12,85 и N, N ,оС-триметил5-(2-тиенил)-пиразол-1-ацетамид, .пл. 80-82с. Найдено,%: С 58,10; Н5,95; N16,87; 313,05 С«Н.5,05 Вычислено,: С 57,80; Н 6,06; N16,85; 312,85 Пример 32. Аналогично примеу 1, заменяя 4-метил-З-фенилпиразол -метил-З-(2-тиенил)-пиразолом, полуают N,N ,oL,4-тетраметил-З-(2-тиенил)пиразол-1-ацетамид, т.пл. 100-102 с. Найдено,%: С 59,09; Н 6,52; N15,86; eil,99 C,,H,,N,OS Вычислено,%: С 59,29; Н 6,51; N15,96; 512,17 и N, N ,oL ,4-тетраетил-5- (2-тиенил) -пиразол-1-ацетамид .пл. 77-80 С. Найдено,%: С 59,02; Н 6,27; Г)115,87; 512,29 С.3 Н.,7 Вычислено,%: С 59,29; Н 6,51; N15,96; 912,17 Пример 33. Аналогично примеУ 1, заменяя 4-метил-З-фенилпиразол -метил-З-(2-тиенил)-пиразолом, а 2хлор- N, N-диметилпропионамид 2-бромN, N-диметилбутирамидом, получают сА-этил- N , N , 4-тримётил-З- (2-тиенил) иразол-1-ацетамид, т.пл. 83-85°С. Найдено,%: С 60,61; Н 6, N15,14; 311,49 С 4Н дНз05 Вычислено,%: С 60,62; Н 6,90; N15,15; 511,56 и oL-этил- N, N,4триметил-5-(2-тиенил)-пиразол-1ацетамид, т.кип. 170°С/0,7 мм рт.ст. Найдено,%: С 60,31; Н 6,97; N15,07; Sll,23 )3° Вычислено,%: С 60,62; Н 6,90; N15,15; S 11,56 Пример 34. Аналогично примеу 1, заменяя 4-метил-З-фенилпираэол -метил-З-(5-хлор-2-тиенил)-пиразолом олучают. N, N , ci- , 4-тетраметил-З-(5хлор-2-тиенил)-плразол-1-ацетамид, .пл. 111,5-114с. Найдено,%: С 52,44; Н 5,59; N14,19; се 11,68; S 10,85 СЕ N305 Вычислено,%: С 52,43; Н 5,42; 14,11; се 11,91; S 10,77 Пример 35. Аналогично примеу 1, заменяя 4-метил-3-фенилпиразол -метил-З-(2-тиенил)-пиразолом, полуают N , N , 4-триметил-с.-пропил-3-(2тиенил) -пира:зол-1-ацетамид, т . пл. 5-87,5с. Найдено,%: С 61,70; Н 7,40; Ц 14,40; S 11,05 , NjOS Вычислено,%:С 61,82; Н 7,26; N14,42; ,11,00 Пример 36. Диалогично при ру 1, заменяя ;3-метил-4-фенилпираз 3-{2-фурил)-4-метилпиразолом, полу чают 3-.(2-фурил)-N / N , сС ,4-тетрам тилпиразол-1-ацетамид, т.пл. ЭЗ-ЭБ Найдено,%: С 63,17; Н 7,13; N17,07 вычислено,%: С 63,14; Н 6,93; N16,99 Пример 37, Аналогично при ру 1, заменяя 4 метил-3-фенилпираз 3-( 2-фурил) -4- метшширазолом, полу ют с -этил-3-(2-фурил)- N, N ,4-три метилпиразол-1-ацетамид, т.пл, 115 117°С. Найдено,%: с 64,46; Н 7,26; М15,89 Ci4 oN3C2 Вычислено,%: С 64,34; Н 7 3 N 16,08 Пример 38. Аналогично при меру 1, заменяя 4-метил-З-фенилпир зол 3-(2-фурил)-4-метилпиразолом, лучают 3-(2-фурил}- N, N,4-тримети -et-пропилпиразол-1-ацетамид, т.пл 107-109°С. Найдено,%: С 65,61; Н 7,78; N15,21 Вычислено,%: с 65,43; Н 7,69; N15,26 Пример 39. Аналогично при ру 1, заменяя 2 хлор- N, N,2,2-TeT раметилпропионамидом 2-хлор- N, Nметилпропионамид, получают N, 4-пeнтaмeтил-5-фeнилпиpaзoл-l-пpoп aмид, т.пл. 59-60с. Найдено,%5 С 71,61; Н 8,31; N14,65 «23 3° вычислено,%; С 71,54; Н 8,12; N14,73 и N, N , oL, oL, 4-пентаметил-фенилпиразол-1-пропионамид, т.кип ,03 мм рт.ст. Найдено,: С 71,43; Н 8,45; N14,79 C,H.,5NjO С 71,54; Н 8,12; Вычислено,% N14,73 Пример 40. Аналогично примеру 1, заменяя 4-метил-З-фенилпиразол З-(о-нитроФенил)-пиразолом, получают Nr N , oL-тpимeтил-3-(O-нитpoфeнил)-пиpaзoл-l-aцeтaмид в виде КО ричневой жидкости. Пример 41. Аналогично приме ру 1, заменяя 4-метил-З-фенилпиразол З-(о-хлорфенил)-пиразолом, а 2-хлор-N, N-диметилпропионамид 2-бром-Nj N-диметилбутирамидом, получают З-(о-хлорфенил) - С1.-ЭТИЛ- N, М-диметилпиразол-1-ацетамид, т.пл. 38,5-40 ,Найдено,%: С 61,99; Н 6,22; Ni5,38; се 12,31 . 218 вычислено,%: С 61,74; Н 6,22; N14,40; се 12,15 Пример 42. Аналогично примеру 1, заменяя 4-метил-З-фенилпиразол 3-(О-толил)-пиразолом, а 2-хлор-М,Кдиметилпропионамид 2-бром- N,N -диметилбутирамидом,. получают оС -этил- N,N -диметил-3-(o-тoлил)-пиpaзoл-l-aцeтaмид, т.пл. 48-51 С. Найдено,%: С 70,66; Н 7,74; N15,32 . С16 На, Мэ О С 70,82; Н 7,80; Вычислено,%; N15,49 Пример 43. Аналогично примеру 1, заменяя 4-метил-З-фенилпиразол З-(о-хлорфенил)-4-метилпиразолом, а 2-хлор- N, N-диметилпропионамид 2-бром- N,N -диметилбутирамидом, получают З-(о-хлорфенил) - ci-этлл N, N,4-триметилпиразол-1-ацетамид, т.кип. 180°С/О,15 мм рт.ст. Найдено,%: С 62,69; Н 6,81; N13,73; се 13,52 C H oCeNjO Вычислено,%: С 62,84; Н 6,59; 13,74; се 11,59 Пример 44. Аналогично примеру 1, заменяя 2-хлор- N, N-диметилпропионамид 2 ,5-дибром- N , N -диметилвалерамидом, получают оС-(3-бромпропил)- N, Nе4 триметил-3-фенилпиразол-1-ацетамид в виде жидкости. Пример 45, Аналогично примеру 1, заменяя 2-хлор- N,N -диметилпропионамид 2,6-дибром- N, N-диметилкапроамидом, получают сС -(4-бромбутил) - N , N , 4-тpимeтил-3-фeнилпиpaзoл-1-ацетамид в виде жидкости. Пример 46. Аналогично примеру 1, заменяя 4-метил-З-фенилпиразол 4-метил-З-(о-толиЛ)-пиразолом, а 2-хлор- N , М -диметилпропионамид 2-бром- N, N-диметилбутирамидом, получают dL-этил-N , N , 4-триметил-3-(0-толил)-пиразол-1-ацетамид, т.кип. 155157°С/0,05 мм.рт.ст. Найдено,%: С 7i,18; Н 8,27; N14,65 . С 71,55; Н 8,12; Вычислено,% N14,72 Пример 47. Аналогично примеу 1, заменяя 2-хлор-N ,N-диметилпропионамид 2-бром-4-хлор-Н , N-диметилбутирамидом, получают с1-(2-хлорэтил)-N, N,4-триметил-З-фенилпиразол-1-ацатамид в виде жидкости. Пример 48. Аналогично примеру 1, заменяя 2-хлор- N,N -диметилпропионамид -й -бром-..1, М-диметил-1-циклогексанацетамидом, получают ot -циклогексил- N, N ,4-тpимeтил-3-фeнилпиpaзoл-l-aцeтaмид, т.пл. 102,5104,. Найдено,%: С 73,70;.Н 8,44; N12,69 Вычислено,: С 73,81; Н 8,36; N12,91 Пример 49. Аналогично прим ру 1, за 1еияя 2-хлор N , N -диметилпропионамид оС -бром- N, М-диметил-1 -гликлогексанацетамидом, а 4-метил-З -фенилпираэол 3-фенилпиразоном полу чают оС -циклогэксил- N, N-диметил-З-фенилпираэол-1-ацетамид, т.пл, 87,. Найдено,%: С 73,36; Н 8,08; N13,39 С,, н Вычислено, %; С 73,28; II 8,09; N13,49 П р и м е р 50. Аналогично приме ру 1, заменяя 2-хлор- N , N-диметилпpoпиoнa 1ил 2-бром- Ц, N-диметилкап роамидом, получают ct -бутил- N , N , 4 -триметил-3--фенилпиразол, т.кип. , i MI-5 рт .ст. . Найдено,%:е 71,76; Н 8,30; N13,89 C,eH,NjO ВЕ-лчислено, %: С 72,20; Н 8,42; N14,04 Пример 51. Аналогично прим ру 1, но заменяя 2-хлор- N, N-диме тилпропионамид 3-хлор- N, М-диметил пропионамидом, получают N, Н ,4-триметил-3-фенилпиразол-1-пропионамид, т.пл. 60-63°С. Найдено,;: С 70,01; Н 7,45; N16,52.. C-isHi NaO. Вычислено,%: С 70,00; Н 7,44; N16,33 Пример 52. Аналогично приме ру 1, ко заменяя 4--метил-3-ФенилЬир зол 3-(С -этоксифенил)-пиразолом, по лучают 3-(о-этоксифенил) - N, N,oi. ,4 -тетраметилпиразол-1-ацетамид, т.пл, 96-97,5°С. Найдено,%: С.67,74; П 7,66; N13,71 С.;7Н2, вычислено,%: С 67,75; Н 7,69; N13,94. Пример 53. Аналогично прим ру 1, заменяя 4-метил-З-фёнилпиразо 4-йод-З-фенилпиразолом, получают 4-йод- N, N,d-тpимeтил-3-фeнилпиpaз -l-aцeтaмид, т.пл. 108-111 С. Найдено,%: С 45,93; Н 4,92; N11,02; J 34,51 C 4H gЗNэO Вычислено,%: С 45,54; Н 4,37; 11,38; I 34,37. Пример 54. Аналогично прим ру 1, заменяя 4-метил-З-фенилпиразо З-метил-5-фенилпиразолом, а 2-хлор-М, N -диметилпропионамид 2-бром-N/ N -диметилбутирамидом, получают d-этил- N, N , 5-триметил-З- фенилпир зол-1-ацетамид, т.пл, 117-119,5 С.. Найдено,%: С 70,61; Н 7,57; N15,64; , NgO Вычислено,%: С 70,82; Н 7,80; N15,49 Пример 55. Аналогично примеру Ij заменяя 4-метил-З-фенилпиразол 3-(0-фторфенил)-пиразолом, 3-(О-фторфенил)-4-метилпиразолом; 3-{о-бромфенил)-4-метилпиразолом; 3-(О-трифторметилфенил)-пиразолом; 3-(о-трифторметилфенил)-4-метилпиразолом и 3-(6-этилфенил)-пиразолом, получают соответственно N , N , oL -триметил-3-(о-фторфенил)-пиразол-1-ацетамид; N , N ,7.4-тетраметил-3-(о-фторфенил)|-пиразол-1-ацетамид; М , N , oL ,4-тетра етил-3- { о -бромфенил) -пиразол-l-aueilмид; N, t f cL -триметил-3- ( о -трифтор етилфенил) -пиразол-1-ацетамид;. N , N ,л,4-тетраметил-3- ( о трифторметилфеил)-пиразол-1-ацетамид и 3-(этилфеил)- N, N,оС-триметилпиразол-1-ацетмид, Пример 56. Аналогично примеу 1, заменяя 4-метил-З-фенилпиразбл 5-нитро-З-фенилпиразолом, получают N , N ,oL , 4-тетрамети л-5-нитро-3-фенилпиразол-1-ацетамид, т.пл. 141-143 С Найдено,%: с 59,62; Н 6,02; 1 18,53. -16 Вычислено,: С 59,59; Н 6,00; N18,53 Формула изобретения 1. Способ получения замещенных пиаз олов формулы BjC-C-lT л-0где 1 - водород, галоген, алкил с 1-6 атомами углерода, галогеналкил с 1-6 атомами углерода или фенил; R - водород или метил; Kj - водород, алкил с 1-8 атомами углерода, фенил или бензил ; ЕЗ - водород или алкил с 1-6 атомами углерода или морфолин, пирролидин или пиперидин; А ч Б - алкил с 1-6 атомами углерода, фенил галоген, циан, нитрогруппа или трифторметил, кроме того. В;; и БЗ вместе обозначают кольцо с 5-7 атомами углерода; , Z - группа формулы или О SО где X - галоген, нитрогруппа, алкил, галогеналкил или алкоксигруппа с 1-3 атомами углерода; «-.0,1 или 2, 21 отличающий с я тем, чГто -галогеналканамид общей формулы «.-U--W л RS где - галоген; В , R, B,j и ВJ имеют указанные чения, подвергают взаимодействию пиразолом общей формулы 61372222 2-Н I - где А, В или.2 имеют указанные зна5чения, в присутствии основания при 0-200С. Источники информации, принятые во зна-внимание при экспертизе: 1. Патент Великобритании W 1298642, jOкл. С 2 С, 06.12.72.
Авторы
Даты
1978-06-30—Публикация
1975-11-14—Подача