(54) СПОСОБ ПОЛУЧЕНИЯ у -АМИДОВ НУКЛЕОЗИД-5 -ТРИФОСФАТОВ


| название | год | авторы | номер документа |
|---|---|---|---|
| Иммобилизованные на полимерной матрице @ и @ -амидные производные нуклеозид-51-ди или трифосфатов в качестве сорбентов для афинной хроматографии и способ их получения | 1980 |
|
SU977463A1 |
| Способ получения меченых тритием нуклеозид-5-триофосфатов | 1973 |
|
SU462467A1 |
| Способ определения аденозинтрифосфата | 1986 |
|
SU1439508A1 |
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ 5'-ТРИФОСФАТОВ ПРИРОДНЫХ И МОДИФИЦИРОВАННЫХ ДЕЗОКСИРИБО- И РИБООЛИГОНУКЛЕОТИДОВ | 2007 |
|
RU2348643C1 |
| Спин-меченые производные олигорибонуклеотидов как спиновые зонды для исследования механизма действия ферментов и способ их получения | 1977 |
|
SU659573A1 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 2'-ДЕЗОКСИ-2'-ФТОРРИБОНУКЛЕОЗИДОВ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫХ СОЛЕЙ | 1990 |
|
RU2043361C1 |
| Способ получения меченного тритием гуанизин-5-триофосфата | 1973 |
|
SU461622A1 |
| АНАЛОГИ ПРИРОДНЫХ ДЕЗОКСИРИБОНУКЛЕОЗИДТРИФОСФАТОВ И РИБОНУКЛЕОЗИДТРИФОСФАТОВ, СОДЕРЖАЩИЕ РЕПОРТЁРНЫЕ ФЛУОРЕСЦЕНТНЫЕ ГРУППЫ, ДЛЯ ИСПОЛЬЗОВАНИЯ В АНАЛИТИЧЕСКОЙ БИООРГАНИЧЕСКОЙ ХИМИИ | 2014 |
|
RU2582198C1 |
| Способ выделения и очистки внеклеточной гуанилрибонуклеазы ТRIсноDеRма наRZIаNUм | 1986 |
|
SU1392093A1 |
| Способ получения реагента для иммунохимического анализа | 1980 |
|
SU1067443A1 |

Предлагается способ получения новых соединений, которые могут найти применение в биологической химии и фармацевтической промышленности.
Нукпеозид-5 -трифосфаты обычно применяются в качестве промежуточных веществ в синтезе различных лекарственных препаратов и витаминов |11.
Предлагаемые -амиды нуклеозид-5-трифосфаты обладают повышенной реакционной способностью.
Способ получения Jf -амидов нуклеозид-З-трифосфатов заключается в том, что нуклеозид-5- трифосфат обрабатывают 15-20-кратным избытком водорастворимого карбодиимида в водной среде при рН 5,0-6,0 и температуре 10-15 С с последующей обработкой амином алифатического или ароматического ряда или азидом.
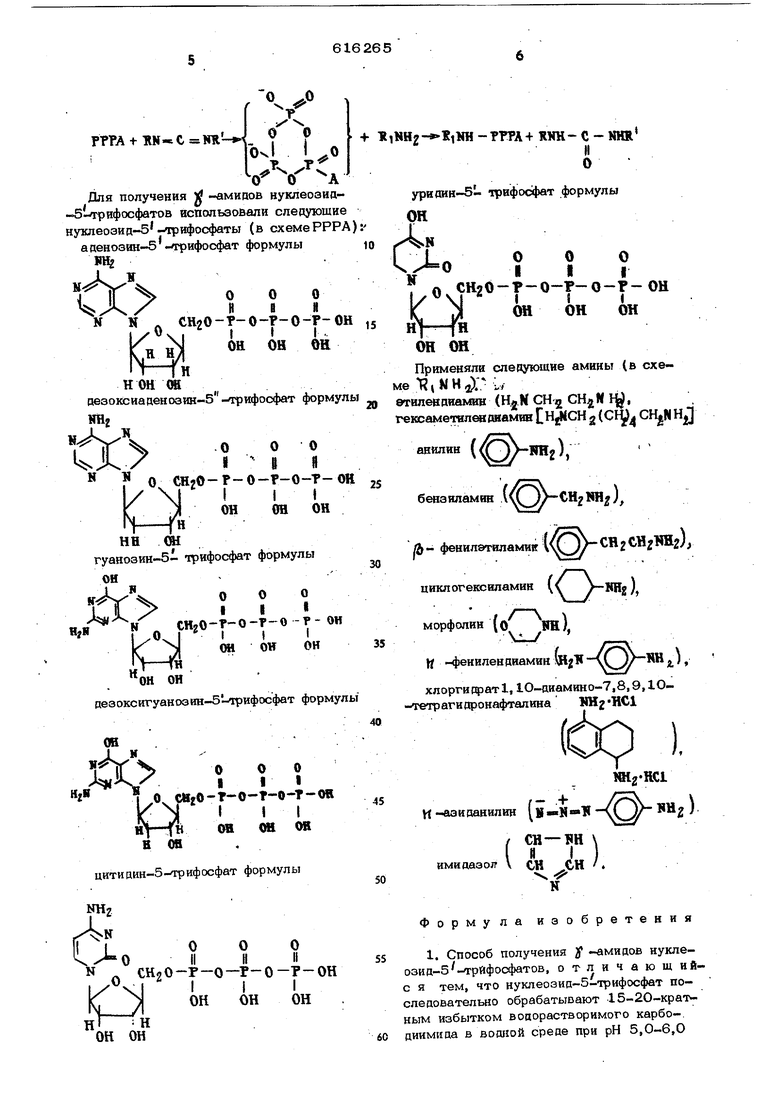
В качестве аминов алифатического или ароматического ряда или азидов обычно используют этилендиамип, гексаметилендиамин, анилин, бензпламин, ( (Ь -фенилэтиламин, циклогоксиламин, морфолин,
М -фенилёндиамин, хлоргидрат 1,10-диамино-7,8,9, Ю-тетрагиоронафталина, И -азиданилин, имидазол. Выход у -аминов нуклеозид-5 -трифосфатов составляет 85-9О%.
Пример. Получение Jf -анилида аденозин-5 трифосфата.
Реакцию водорастворимого карбо- диимида с аденозин-5 -трифосфатом (АТФ) проводят в термостатированной кювете с погруженными в нее стеклянным и каломелы1ым электродами для измерения рН среды с помощью потенциометра ЛПУ-01. Реакционная смесь содержит 45 мкмоль АТФ, 38О мг водорастворимого карбодиимида, объем реакционной смеси 15 мл, температура 11 С. рН 5,6 поддерживают при непрерывном подтитровывании 0,5 н. соляной кислотой, контролируя рН с помошью потенциометра ЛПУ-01. Через 30 мин добавляют 0,5мл анилина.
Реакционную смесь наносят на колонку (V ЮО мл) с диэтиламнноэтилцел- люлооой (ДЭАЭ-целлюлозоП) в бикарбонатной форме н хроматографируют в линейном грагасенте концентрации триэтиламмонийбикарбонатного буфера (рН7,5 Концентрация буфера в смесителе 0,01М в резервуаре - 0,3 М. Объем смесителя и резервуара по 1 л. Скорость элюирования 30 мл/час, объем фракций 12 мл. Фракции пика, соответствующие продукту, собирают и упаривают на ротационном испарителе при 30 С, Полученный продукт анализируют мето дом хроматографии на бумаге, проведением кислотного гинролиаа, снятием УФ-чзпектров и спектров ЯМР ( R). П р и м е р 2. Получение -бензиламида гуанозин-5 -трифосфата. Реакцию водорастворимого карбоаиими да с гуанозин-5-трифосфатом (ГТФ) про водят в термостатированной кювете с погруженными в нее стеклянным и каломель ным электродами для измерения рН среды с помощью потенциометра ЛПУ-01. Реакционная смесь содержит 45 мкмоль ГТФ, 38О мг водорастворимого карбодиимида, объем реакционной смеси 15 мл, температура 11 С, рН 5,6 поддерживают при непрерывном поотитровывании 0,5 в. соляной кислотой, контролируя рН с помощыо потенциометра ЛПУ-01. Через 30 мин добавляют 5 ммоль (0,5 мл) бензиламина. Реакционную смесь наносят на колонку ( Y 100 мл) с ДЭАЭ-целлюлозой в бикарбонатной форме и хроматографируют в линейном градиенте концентрации три©т1У1аммонийбикарбонатного буфера (рН 7,5). Концентрация буфера в смесителе 0,01 М, в резервуаре 0,3 М, Объем смесителя и резервуара по I л. Скорость элюирования 30 мл/час, объем фракций 1.2 мл. Фракции пика, соответствующие продукту, собирают и упаривают на ротационном испарителе при 30 С. Полученный продукт анализируют методом хроматографии на бумаге, проведением кислотного гидролиза, снятием УФ-спектров и спектров ЯМР ( Р). П р и м е р 3. Получение -амида аденозин-5 -трифосфата 1. Реакцию водорастворимого карбодиими да с аденозин-5 - трифосфатом проводятв термостатированной кювете с погруженными в нее стеклянным и каломельным электродами для измерения рН среды с помощью потенциометра ЛПУ-01. Реакционная смесь содержит 45 мкмоль АТФ, . 380 мг водорастворимого карбодиимида, объем реакционной смеси 15 мл, тем, пература , рН 5,6 поддерживают при непрорывном подт1ггр01и,1вании 0,5 и. СОЛЯНОЙ кислотой, контролируя рН с помошью потенциометра ЛПУ-01, Через 30 мин добавляют 5 ммоль (1,17 г) основания 1,10-диамино-7,8,9, 10-тетрагидронафталина. Реакционную смесь наносят на колонку ( V 100 мл) с ДЭАЭ-целлюлозой в бикарбонатной форме и хроматографируют в линейном градиенте концентрации триэтиламмонийбикарбонатного буфера (рН7,5), Концентрация буфера в смесителе 0,01 М, резервуара 0,ЗМ. Объем смесителя и резервуара по 1 л. Скорость элюирования 30 Nm/4ac, объем фракции t2 мл. Фракции пика, соответствующие продукту, собирают и упаривают на ротационном испарителе при 30 С. Полученный продукт анализируют методом хроматографии на бумаге, проведением кислотного гидролиза, снятием УФ-спектров. П р и м е р 4. Получение Jf - (П-азидо)анилида аденозин-5 -трифосфата). Реакцию водорастворимого карбодиимида с аденозин-5 -трифосфатом проводят в термостатированной кювете с погруженными в нее стеклянным и каломельным электродами для измерения рН среды с помощыо потенциометра ЛПУ-01. Реакционная смесь содержит 45 мкмоль АТФ, 380мг водорастворимого карбодиимида, объем реакционной смеси 15 мл, температура 11 С. рН 5,6 поддерживают при непрерывном подтитровывании 0,5 н. соляной кислотой, контролируя рН с помощью потенциометра ЛПУ-01, Через 30 мин добавляют 5 ммоль (0,67 г) г/-аз и Данилин а. Реакционную смесь наносят на колонку (V 1ОО мл) с ДЭАЭ-целлюлозой в бикарбонатной форме и хроматографируют в линейном градиенте концентрации триэтиламмонийбикарбонатного буфера (рН 7,5) Концентрация буфера в смесителе 0,О1М, в резервуаре 0,3 М. Объем смесителя и резервуара по I л. Скорость элюирова- ния 30 мл/час, объем фракций 12 мл. Фракции пика, соответствующие продукту, собирают и упариаают на ротационном испарителе при 30 С. Полученный продукт анагпюируют методом хроматографии на бумаге, rifJOBcдением кислотного гидропиаа, снятием УФ-спект1:)ов. К-еакцня идет по слеауюмоЛ схеме: V 0 0 t HH-iC Nll- -i H U Для получения j -амипов нуклеоаид -5-огрифосфатов использовали следующи нуклеоэид-б -трнфосфаты (в схеме РРР аденозин-5 -трифосфат формулы 000 Н I я СН20-Р-0- -0-Р-О I I I. ОЕ 08 OU НОН 08 дезоксиаденозин-5 -1трифосфат форму Щ 00 о v / II о CHjO-P-O-f-O-T-O I II он он он гуанозин-5- тркфосфат формулы ОН lf V000 « « СНгО-Т О-Т-0 ОИ N : I II И ОН СИ он он ОИ дезоксигуанозин-5-трифосфат формул
000
I II
ijO - т-о-Т-0-т - OR
III
it он оа OR
цити аин-5 -тр иф осфат фор мул ы
000
IIНII
p-o-р-о-р-он он он он
СИ-НН
и I )
сн сн л
V.
Н
Формула изобретения

Авторы
Даты
1978-07-25—Публикация
1974-04-22—Подача