1
Изобретение относится к усовершенст вованному способу попучения сложных . эфиров замещенных 1-фенил-2,2,2-три- гапогенэтанопов общей формулы
W
СХз
где R - апкил Cj , алкоксил С.- С, циклогексил, фенил или фенил, замещенный хлором или сульфонипом, бензил, дихлорфеноксигруппа;
X - галогену
Y -галоген, метил, метоксигруппа
П SO-2,
которые могут быть использованы в ка честве инсектицидов.
Известен способ получения сложных эфиров 1-фени7 -2,2,2-тригалогенэтанола взаимодействием галогензамещенных бензолов с тригалогенацетальдегидом в присутствии катализатора ФридепяКрафтса, например хлористого алюминия, хлористого железа, трифторида бора или
концентрированной серной кислоты, в среде органического растворителя.
Полученный карбинол выделяют и зтерифицируют ангищзидом или хлоридом кислоты при 8О С в присутствии каталитических количеств .концентрированной кислоты, например серной fll.
Однако такой способ многостадийный и выход продукта низок, .
С цетЕЬю упрощения процесса и по- выщения выхода целевых продуктов предлагается способ получения сложных эфиров общей формулы f I) путем взаимодействия замещенного бензола общей формулы
где и tt имеют указанные значения, с галогенированным альдегидом общей формулы
XjCC( Оч)
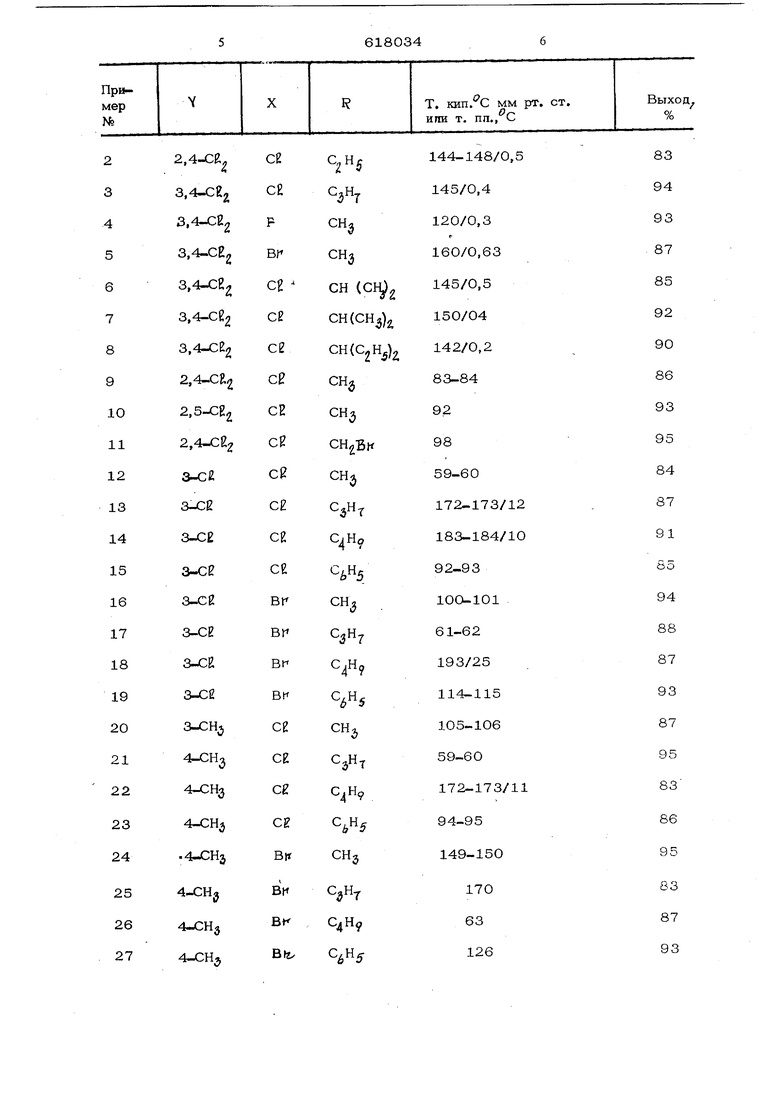
где X имеет указанные значения, в среде органического растворителя в присутствии хлористого алюминия в качестве катализ тора при мольном соотношении соединение формулы {II ); соединение формулы (111); катализатор 1-2:1:1. Полученную при этом реакционную массу, содержащую алкоголятный Комплекс общей формулы непосредственно этерифицируют галогенангидридом кислоты общей формулы )2: где 1 имеет указанные значения{ Z -галоген, или соответствующим ангищэидом. Процесс ведут при температуре от -10 до+аб С. Выход целевого продукта 83-95%. В качестве растворителей применяют такие органические растворители, которы инертны в отнощении применяемого катализатора, например алифатические и ароматические углеводороды, . Исходные соединения формулы (II ) взятые в избытке, могут также служить растворителем. Реакционную смесь по окончании реакции выливают на лед и целевой продукт экстрагируют органическими растворителями. При использовании в качестве катализатора хлористого алюминия получают сточную воду, которую из-за содержания алюминиевых солей нельзя выпускать в канализацию без предварительной переработки. Однако можно обойтись без образования сточной воды, если к реакцион ной смеси добавлять по каплям свежеприготовленный насьпценны и водный раство сульфата натрия. Образующийся при этом твердый осадок из основного галогенида алюминия И N0(2604 10 отсасываю Этот осадок содержит всю предварительно примененную для растворения сульфата натрия воду, связанную в виде крис таллизационной воды. Целевой продукт выделяют из органической фазы. Преимущество такой переработки заключается в том, что сточной воды не образуется И образукяциеся алюминиевые, соли попучают в твердом виде. Другой вариант переработки заключается в том, что после добавки по кагьлям галогенидангищ)ида кислоты (или ангигфида кислоты) всю смесь подают в суспензию Wa SO/lO Н20 в среде инертного растворителя. В этом случае также образуется твердый осадок из основного галогенида алюминия и сульфата натрия, который отсасьюают. Целевой продукт выделяют из органической фазы. Предложенный способ позволяет получать сложные эфиры 1-фенил-2,2,2тригалогенэтанола с высоким выходом и в одну стадию, что упрощает процесс. Проведение процесса без выделения алкоголятного комплекса, например из хлорида алюминия и фенилтригалогенэтанола, возможно вследствие устойчивости его при данных условиях реакции. Установлено, что известную реакцию карбинола с ангидридом или хлоргидридом кислоты, протекающую обычно при повышенной температуре, можно проводить при низкой температуре. Пример 1. К 500 мл (4,4 моль) 0-дихлорбензола (избыток служит в качестве растворителя) при размешивании добавляют 134 г (1 моль) хлорида алюминия, охлаждают до ОС и при 0-5 С по каплям добавляют 147,5 г (1 моль) безводного хлораля, смесь выдерживают 6 ч при 0-5 С и затем при 0-8 С по каплям добавляют 78 г (1 моль) ацетиткхлорида или 102 г (1 моль) ацетанги{ьрида. По/ ченный раствор порциями напивают в суспензию 322 г (1 моль) NcXgSp 10 НлО в о-дихлорбензоле, поддерживая температуру при 20 С за счет охлаждения. Выпавшие соли фильт«руют, промьтают два раза 300 мл одихлорбензола и растворитель отгоняют при 100 С в ротационном выпарном аппарате. Остаток смешивают с 100 мл изопропанола. Образукхциеся при ОС кристаллы отсасьгеают, промьюают небольшим количеством изопропанола и сушат в вакуум-экстракторе. Получают ЗО9 г (92%) 1-.(3,4-дихлорфенил)-2,2,2трихлорэтанолацетата, т. пл. 85-86 С. В таблице приведены соединения общей формулы ( I ) полученные аналогичным образом.
Продолжение таблицы Пример 53. К TOO мп (4,4 мопь о-дихлорбензопа (избыток одновременно служит растворителем) добавляют при раз мешивании 134 г (1 моль) хлористого алюминия. Охлаждают до О С и при температуре от-10 прибавляют по каплям 147,5 г (1 моль) безводного хлорапя. В течение 7 ч выдерживают от 1О до - 5 С, затем прибавляют по каплям 78 г (1 моль) хлористого аце- тила или 102 г (1 моль) ацетангид- рида при 15-20 С, выдерживают 30 мин и выливают на 200 г льда. Органическую фазу отделяют, а водную экстрагируют с 100 млО-дихлорбензола. Соединенные органические фазы сушат над сульфатом натрия в ротационном испарителе под вакуумом и при 100 С удаляют растворитель. Остаток смешивают с 100 мл изопропанола и выкристаллизовывают при О С. Кристаллы отсасывают, промьтают холодным изопропанолом и сущдт в вакуум- эксикаторе. Получают 302 г (90,5%) 1-(3,4-дихлорфен 1л)-2,2,2-трихлорэтанол ацетата, т. пл. 84-8бС. Пример. 54. К 500 мл (4,4 моль) о-дихлорбензола (избыток одновременно служит растворителем добавляют при размешивании 134 г (1 моль) хлористого алюминия, охлаждают до О С и прибавляют по каплям при 5-10 С 147,5 г(1мол безводного хлораля, затем выдерживают 4 ч при 5-10С, прибавляют по каплям 78 г (1 моль) хлористого ацетила или 102 г (1 моль) ацетангидрида при тем- пературе от -10 до -5 С, выдерживают 60 мин и выливают на 200 г льда. Органическую фазу отделяют, а водную экстрагируют 100 мл о-дихлорбензола.Соединенные органические фазы сушат над сульфатом натрия и удаляют растворитель в испарителе при 100 С. Остаток смешивают с 100 мл изопропанола и выкристал лизовывают. Кристаллы отсасывают, промывают холодным изопропанолом и сушат в вакуум-эксикаторе. Получают 306 г (91,4%) 1-( 3,4-дихлорфенил)-2,252-трихлорэтанолацетата, т. пл. 85-86°С. Пример 55. К 500мл(4,4моль D-дихлорбензола (избыток одновременно служит растворителем) добавляют при раз мешивании 134 г (1 моль) хлористого алюминия и по каплям при 20-25 С 147, (1 моль) безводного хлораля, выдерживают 2,5 ч при 20-25 С и прибавляют по каплям 7 8 г (1 моль) хлористого ацетила или 102 г (1 моль) ацетангидрида при 20-2 , выдерживают 20 мин и пеерабатывают аналогично npraviepy 5, Полуают 312 г (93,2%) 1-(3,4-дихлорфенил)2,2,2- рихлорэтанолацетата, т, пл. , Формула изобретения Способ получения сложных эфиров замещенных 1-фенип-2,2,2-тригалогенэтанолов общей формулы CH-O-COB(I) где R - алкил С| CH2Br ;,CH2C. апкоксил С|- Сд, циклогексил, фенил или фенип,замещенньй хлором или сульфонипом, бензил, дихпорфеноксигруппа; X - галоген; V - галоген, метил, метоксигруппа; tl 0-2, путем взаимодействия замещенного бензола общей формулы где Y и IY имеют указанные значения, с галогенированным альдегидом общей формулы х,,сс(о)н (Л|) где X имеет указанные значения, в среде органического растворителя в присутствии хлористого алюминия в качестве катализатора с последующей этерификацией полученного продукта галогенангидридом или ангидридом кислоты, о т л и ч а ю- щ и и с я тем, что, с целью повышения выхода и упрощения процесса, последний ведут при мольном соотношении замещенный бензол: галогенированный альдегид: катализатор 1-2:1:1 и полученную при этом реакционную массу, содержащую алкоголятный комплекс общей формулы СН-0-А1-С1 СХзС1 непосредственно этерифицируют галогенангидридом кислоты обшей формулы RC(0)2:7
1161803412
где R имеет указанные значения;Источники информации, приня1Ъ1е во
Z галоген,внимание при экспертизе:
ипи соответствующим ангидридом и процесс ведут при температуре от-1О до1. Выложенная заявка ФРГ . 5 №2110056, кп, 45 g 9/30, 1973.






Авторы
Даты
1978-07-30—Публикация
1976-09-10—Подача