Изобретение относится к усовершенс вованному способу получения гапоиданги ридов супьфаминовой кислоты, которые находят применение как иcxoшiыe вещес ва дня получения средств защиты растений, красителей и фармацевтических пре паратов. Известен способ получения гапоидангидридов сульфаминовой кислоты общей формулы :к-:5г-$02Т н где R - алифатический или циклоалифатический радикал Y-галоид, с применением галоидирующего агента и с последующим выделением целевого продукта, заключающийся в том, что галоидированию подвергают сульфаминовую кислоту общей формулы ,н: I н где J имеет вышеуказанное значение, или ее соль, а в качестве гапоиди- рующего агента используют галоицангидрид сернистой, фосфорной, фосфористой, угопь- ной или щавелевой кислоты. Процесс проводят в присутствии катализатора, в качестве которого используют амиды М,Ы-дизамещенной карбоновой кислоты или третичные амины. Выход целевого продукта при использовании галоидангидрида угольной кислоты составляет 33-44,5% l. Недостатком данного способа является невысокий выход целевого продукта Целью изобретения является повышение выхода целевого продукта. Поставленная цель достигается способом получения гапоидангидридов сульфаминовой кислоты общей формулы I где R - Сд -апкил и пи Qцикпоалкип, незамещенные или замещенные атомами хпора или брома или С алкилом} X - хлор или бром взаимодействием сульфаминовой кислоты общей формулы К Ki- -so3ii t н где R - имеет вьппеуказанное значение, или ее соли с галоидангидридом угольной кислоты в присутствии катализатора, заключающийся в том, что в качестве катализатора используют дихлорметиленаммонийхлорид общей формулы Д или хлорангидрид карбаминовой кислоты общей формулы W II r-ti-(li где R и R,oдинaкoвыe или различные С - С„- алкил или С - С -хлоралкил, ил вместе с атомом азота образуют 5-или 6-членный гетероцикл, который может содержать еще один атом азота или кислорода, причем алкилы и гетероцикл могут быть замещены С - апкилом или Q - Сх- алкоксилом. Процесс предпочтительно проводят при 20.100°С. При этом следует отметить, что цел вые галоидангидриды сульфаминовой кис лоты могут быть получены также, исхо из изоциаиата общей формулы )1 где I - как указано выше, который подвергают взаимодействию с серной ки лотой, и полученную соответствующую сульфаминовую кислоту или ее соль с металлом подвергают взаимодействию с галоидангидридом угольной кислоты в присутствии предлагаемого катализатора Наиболее экономично и безвредно дл окружающей среды использование в качестве галоидангидрида угольной кислоты фосгена, так как в качестве отходящего газа в этом случае наряду с хлористым водородом образуется только двуокись углерода. Хлорангидрид карбаминовой кислоты формулы IV после проведения процесса выделяют путем дистилляции и при желании ре цирку лиру ют. Исходные вещества формулы li применяют в виде сульфаминовых кислот, свободных от серной кислоты, или их сульфаминовых солей с металлом. Предпочтительными солями с металлом являются соли со щелочными или щелочноземельными металлами, такими, как магний, кальций, литий, калий и натрий. Исходные вещества формулы Д берут в стехиометрическом количестве, но предпочтительно используют 1,1-2 моль галоидангидрида кислоты на 1 моль вещества формулы Д. Пригодными галоидангидридами кислоты являются дибромид угольной кислоты и особенно фосген. Процесс, как правило, проводят при 2О-1ОО С, в частности при 60-10О°С, без давления или под давлением, по непрерывной или периодической схеме. В качестве катализатора используют предпочтите льно дихлорметиленаммонийхлорид формулы Ш или хлорангидрид карбаминовой кислоты формулы IV. В общем используют 1О-ЗО вес. %у предпочтительно 15-25 вес %,катализатора формулы Ш по отношению к веществу формулы I и 5-30 вес.%, предпочтительно 10-20 вес.%,катализатора формулы IV если его используют только как катализатор. Но так как его можно рекуперировать, он может одновременно служить реакционной средой, причем в этом случае используют 30-5ОО вес.%, предпочтительно 200-300 вес.%, хлоран гидрида карбаминовой кислоты формулы IV по oi ношению к веществу формулы Ц. Вместо катализатора формулы IV могут быть использованы образующие эти катализаторы амины, например диметиламин, так как они в условиях реакции в присутствии фосгена превращаются в хлорангидриды карбаминовой кислоты формулы IV, например хлорангидрид диметил- карбаминовой кислоты. Катализаторы формулы JU могут быть получены например, путем хлорирования N -замещенных тиокарбамоилхлоридов, таких как М,М-диметилтиокарбамоилхлориды или соответствующие дитиурамы, или путем взаимодействия замещенных сложных эфиров дитиокарбаминовой кислоты с тионилхлоридом. Используют предпочтительно дихлорметилендиметипаммонийхпорид, дихпорметилендиэтипаммонийхпорид, дихлорметипен-ди-н-пропиламмонийхлорид, дихлор метилендиизопропиламмонийхлорид, дихлорметипен-ди-н-бутиламмонийхлорид, дихпорметилен-ди-втор-бутиламмонийхлорид, дихлорметилендиизобутипаммонийхлорид, дихлсрметилен-био- ( i-хлор этил)-аммонийхлорид, дихлорметиленметилэтиламмонийхпорид, дихлорметиленметилпропиламмонийхлорид, дихпорметиленпирролидинийхлорид, дихлорметиленпиперидинийхлорид, дихлорметиленморфолинийхлорид. Можно использовать также следук щие катализаторы формулы IJI, а также их смеси:ди-{трет-бутил)-, ди-(пентил)-, ди-(пентил)-(2)-, ди-(пентил)-( 3)-, ди-(н-гексил)-,, ди-(н-гептил)-, ди-( н-октил)-, ди-(2-этилгексил)-, ди-(2,2,6-триметил-н-пёнтил)-, ди-( 2-этилпентил)ди-( 3-этилпентил)-, ди-( 2,3-диметил-н-бутил)-, ди-( 2,2-диметил-н-бутил)-, ди-(2-метилпентил) -, ди-( 3-метиллентил) -, ди-( 2,2,4- риметилпентил)-, ди-(2--метилгептил)- ди-(З-метилгептил)- ди-(4-ме ТИЛГеПТИл)-, ДИ-( 3-ЭТИЛГеКСИл)-, ДИ-(2,2-диметилгексил)-, ди-( 2,3-диметилгексил) ди-( 2,4-диметилгексил)-, ди-( 2,5-диметилгексил)-, ди-( 3,3-диметилгексил)-, ди..(3,4-диметилгексил)-, ди-(2-метил-3-этилпентил j-, ди-( 3-метил-З-этилпентил ди-(2,2,3-триметилпентил)-, ди-{2,2,4-триметилпентил)-, ди-( 2,3,3-триметилпентил)-, ди-( 2,3,4-триметилпентил)-, ди-( 2,2,3,3-тетраметилбутил)-, метилизопропил-, метил-н-бутил-, метилизобутилметил-втор-бутил, метил-трет-бутил,метилпентилдихлорметиленаммонийхлориды, соответствующие замещенные у атома углерода в положении 2 или и) -положении кждого алкила атомом хлора диалкилдихлорметиленаммонийхлориды; оксазиридино-, азетидино2-азетино- Д-пирролино-, А -пирролино-, пирроло-, имидазоло-, имидазолидино-,3-имидазолино-, 2Н-1,2-оксазино-,пипера- ЗИНО-, 1Н-азепинодихлорметиленаммонийXлориды. В качестве катализаторов формулы IV используют предпочтительно ангидриды димети лкарбаминовой диэти лкарбаминовой, ди-н-пропилкарбаминовой, диизопропилкар- баминовой, ди-41-бутилкарбаминовой,диизоб тилкарбаминовой, ди-втор-бутилкарбамино- вой, ди-н-пентилкарбаминовой, пирролидинокарбаминовой, морфолинокарбаминовой, пипе ридинокарбаминовой, метилэтилкарбаминовой, метилпропилкарбаминовой, метилбутил- карбаминовой, этилпропилкарбаминовой, ме- илхлорметилкарбаминовой и бисхлормеилкарбаминовой кислоты. Можно применять и следующие катализаторы формулы IJ, а также их смеси: хлорангидрид ди-(трет-бутил)-,ди-(пентил)-(2)-,ди-(пентил)-(3)-,ди-(н-гек- сил)-,ди-(н-гептил)-,ди-{н-октил)-, ди2-этилгексил)-, ди-( 2,2,6-триметил-нпентил)-,ди (2-этилпентил)-, ди-( 3-этилпентил)-, ди-( 2,3-диметил-н-бутил)-, ди-( 2-метилпентип)-,ди-( 2,2-диметил-н-бутил)-, ди-(2-мeтил-пeнтил)-,ди-(3-мeтилпeн- ти л)-, ди- (2,2,4-тримети лпентил)-, ди-(2-метилгептил)-,ди-(3-метилгептил)-, ди-(4-метипгептил)-,ди-(3-этилгексип)-, ди-(2,2-диметилгексил)-, ди- (2,3-ди мети л-гексил)-,ди-( 2,4-диметилгексил)-, ди-( 2,5-диметипгексил-, ди-( 3,3-диметилгексил)-,ди-(3,4-димeтилгeкcил)-,ди-(2-мeтип-3-этилпeнтил)-,ди-(3-мeтил-3-этилпeнтип)-,ди-(2,2,3-триметилпентил)-, ди-(2,3,3-триметилпентил)-,ди-(2,3,4- -триметилпентил)-,ди-(2,2,3,3-тетраметилбутил)-,метипизопропил-,метилизобуТИЛ-, метил-втор-бутил-, метил-трет-бу метилпентилкарбаминовой кисйоты: ,г., ..o„т«н т« V соответствующие замещенные у атома углерода в положении 2 или Ш-положении каждого алкила атомом хлора хлорангид- риды диалкилкарбаминовой кислоты} хлоразе тидино-, 2ангидрид оксазиридино-, 2 3 -азетино-, Д -пирролино-, Д пирролино-, пирроло-, имидазоло-, имидазолидино-,3-имидазолино-, 2Н-1,2-оксазино-, пипераЗИНО-, 1Н-азепинокарбаминовой кислоты. Целесообразно использовать целевой продукт формулы IB качестве растворителя, но можно применять и инертный органический растворитель. В качестве растворителя пригодны, например, хлорированные алифатические углеводороды, такие как метиленхлорид, хлороформ, тетрахлоруглерод, 1,1- и 1,2-дихлорэтан, 1,1,1- JJ.. 1,1,2 -трихлорэтан, 1,1,2,2- и 1,1,х,-2-тетрахлорэтан, н-пропилхлорид, н-бутилхлорид, втор-бутилхлорид, изобутилхлорид, 1,4-дибромбутан, 1,10дибромдекан; хлорированные ароматические углеводороды, такие,как хлорбензол, бромбензол, йодбензол, орто-, мета-дихлорбензол, орто-, мета-дибромбензол, орто-, мета-, пара-хлортолуол, 1,2,4- трихлорбензол, нитроугеводороды, такие, как нитробензол,нитрометан, нитроэтан, орто-, мета, пара-хлорнитробензол; нитрилы, такие, как бензонитрил, мета-хлорбензрнитрил, алифатические и циклоалифатические углеводороды, такие, как гексан, петролейный эфир, циклогексан, пёнтан, гептан или соответствующие смеси. Обычно применяют растворитепь в копи- честве 0-600 вес.%, лучше 50-600вес,% по отношению к исходному веществу фор мупы Я . Выгодно также использовать катализатор формулы W как растворитель, в случае необходимости в смеси с указан ными растворителями и/и пи целевыми продуктами формулы I . Реакцию проводят следующим образом Смесь исходных веществ, катализатор и растворитель выдерживают 3-16 ч при температуре реакции. Катализатор в раст ворителе можно насьпцать фосгеном и затем добавлять соответствующую сульфаминовую кислоту. Можно также сульфаминовую кислоту в смеси с катализатором вводить в растворитель и затем добавлять фосген. Целевой продукт отделяю от реакционной смеси путем фракционной дистилляции. В большинстве случаев из смеси необходимо удапять только раство- ритель и катализатор,так как остающийся целевой продукт и без дистилляции является достаточно чистым для дальнейшей переработки в другие продукты. В качестве исходного вещества формулы ill может быть использована реакционная смесь, полученная при синтезе этого вещества, без его выделения из смеси В качестве исходной смеси применяют предпочтительно смесь, которую получают при взаимодействии изоцианата с безводной серной кислотой при температуре минимум 25 С Б инертном растворителе, например в указанном выше растворителе Предпочитают следующий метод работы. При интенсивном перемешивании одновременно, но раздельно подают изоцианат и растворитель, а также серную киспоту, соответственно смесь серной кислоты и растворителя, в предварительно введенный растворитель. Добавление ведут в течение 1О-55 мин при 25-5О С, реакци проводят по меньшей мере при 50 С. В качестве растворителя используют указанные выше растворители. Затем добавляьют катализатор и в случае необходимости растворитель и выдерживают 3-16 ч при 6О-100 С, предпочтительно при 80-100°С. Отличительным признаком способа является использование в качестве ката- 6 28 лизатора дихлорметиленаммонийхлорида формулы 1|1 или хлорангидридкарбаминовой кислоты формулы у и проведение процесса предпочтительно при 20-100 С. Приведенные в примерах части являются весовыми частями. Пример 1. 69,5 ч. изопропилсульфаминовой кислоты и 15 ч.х дихлорметилендиметиламмонийхлорида при суспендируют в 370 ч. 1,2-дихлорэтана и путем введения фосгена нагревают до 83 С. При размещивании вводят 200 ч. фосгена в течение 12 ч. После удаления избыточного фосгена и растворителя остаток дистиллируют в вакууме, получая 55,2 ч. (70% хлорангидрида изоцропилсульфаминовой кислоты, т. нп. 66-69°С/0,01 мм рт.ст.; П 1,4548. П р и м е р 2. Через два ввода подают 42,5 ч. изопропилизоцианата и 49,5 ч. олеума (1 вес.% SO) в течение 2О мин одновременно при размешивании и 2535 С в 280 ч. 1,2-дихлорэтана. Реак- донную смесь в течение 15 мин при 83 С размешивают до окончания выделения газа и затем, добавляя фосген, смешивают с 15 ч. дихлорметилендиметиламмонийхлорида. В течение 12 ч при 83 С вводят 260 ч. фосгена. После удапения растворителя и избыточного фосгена путем дистилляции остатка в вакууме получают 54,3 ч. (69%) хлорангидрида изопропилсульфаминовой кислоты, т. кип. 65-75°С/0,1 мм рт. ст.; (,4550. Пример 3. 15ч дихлорметилен- диметиламмонийхлорида суспендированного в 54О ч. 1,2-дихлорэтана, при и размешивании насьлцают 40 ч,, фосгена. Затем прибавляют 89,6 ч. циклогексилсупьфаминовой кис поты и, размешивая, при 83 С в течение 15 ч добавляют еще 550 ч. фосгена. После удаления избыточного фосгена и растворителя в вакууме путем дистилляции остатка получают 67,2 ч, (68%) хлорангидрида циклогексилсульфаминовой кислоты, т. кип. 100- 114°О/0,01 мм рт.ст.; т. пл. 43-47°С Примеры 4-6. Проводят опыт, как в примере 2, и получают целевые продукты, перечисленные в табл. 1.
1
оГ
ю
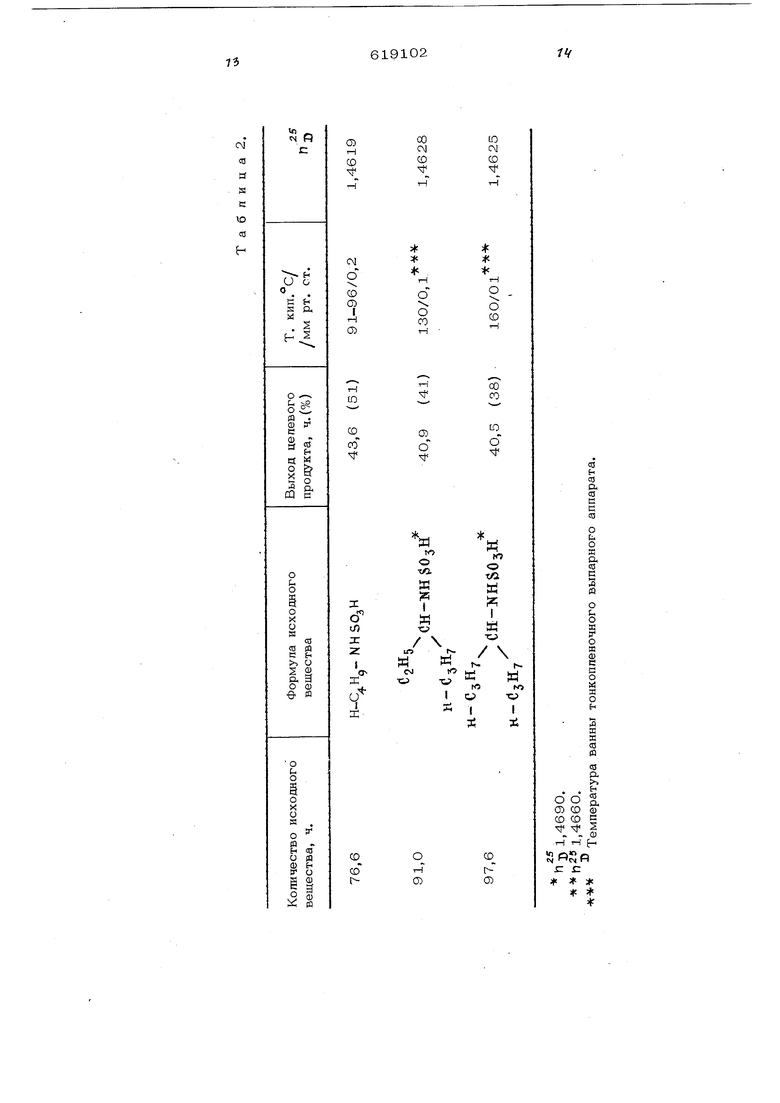
ю ю Пример. В раствор 15 ч-хлор ангидрида диметитткарбаминовой киспогы в 310 ч. 1,2-дихаорэтана при 2О°С вво дят ЗО ч. фосгена до насыщения. Затем добавтшют 69,5 ч-изопропилсульфаминовой кислоты, нагревают до , размешивая, в течение 11 ч добавляют 200 ч. фосгена. Образовавшийся прозрачный раствор сгущают в ротационном испарителе и остаток дистиллируют на насадочной колонне. Получают 55,2 ч. (70%) хлорангидрида изопропилсульфами новой кислоты, т. кип. 68-72 С/0,004 мм рт. CT.J h 1,4540. Примере. В суспензию 69,5 ч. изопропилсульфаминовой кислоты в 310ч 1,2-дихлорэтана при комнатной температуре и размешивании добавляют 54 ч. хлорангидрида диметилкарбаминовой кислоты, нагревают до 83 Сив течение 13 ч смешивают с 25О ч. фосгена. После сгущения в ротационном испарителе путем дистилляции остатка получают 49,6 ч. (63%) хлорангидрида изопропил сульфаминовой кислоты, т. кип. 67-72 С/ /0,04 мм. рт. ст. П р и м е р 9. 4ерез два ввода подают 42,5 ч. изопропилизоцианата и 49,5 ч, олеума (1 вес.% SO) в течени 20 мин одновременно при размешивании В 28О ч. 1,2-дихлорэтлна. Реакционную смесь размешивают 15 мин при до окончания выделения газа и затем путем введения фосгена смешивают с 15 ч. хлорангидрида диметилкарбаминовой кислоты. В течение 13 ч подают 270 ч. фосгена при 83 С. После удаления paci ворителя и диметилкарбамоилхлорида путем дистилляции получают 52,6 ч. (67%) хлорангидрида изопропилсульфаминовой кислоты, т. пл. 64-69 С/ 0,01 мм рт. ст.; ,4521. П р, и м е р 10. Раствор 15 ч. хлорангидрида диметилкарбаминовой кислоты в 310 ч. 1,2-дихлорэтана при 25С насыщают 30 ч.фосгена и затем добавляют 89,5 ч. циклогексилсульфаминовой кислоты. Продолжая добавлять фосген, реакционную смесь нагревают до 83С. В течение 13 ч добавляют 330 ч, фосгена. После удаления растворителя и хлорангидрида диметилкарбаминовой кислоты остаток дистиллируют в вакууме, получая 57 ч. (58%) хлорангидрида ЦИК логекси лсу льфаминовой кис лоты, т. кип. 1О8-127 С/0,1 мм рт. ст. т. пл. 42-44 С. П р и мер ы 11-13. Согласно примеру 10 получают приведенные в табл. 2 соединения.






| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения галоидангидридов сульфаминовой кислоты | 1976 |
|
SU689618A3 |
| Способ получения галоидангидридов сульфаминовой кислоты | 1972 |
|
SU462332A3 |
| Способ получения о-сульфаминобензойных кислот | 1972 |
|
SU450401A3 |
| Способ получения 2,2-двуокисей-2,1,3-бензотиадиазин-4-она | 1972 |
|
SU509233A3 |
| Способ получения изоцианатов | 1973 |
|
SU479284A3 |
| Способ получения тетразамещенных мочевины | 1972 |
|
SU472500A3 |
| Способ получения 5-меркапто-1,2,3-триазолов | 1979 |
|
SU961559A3 |
| Способ получения галогенангидридов сульфаминовой кислоты | 1979 |
|
SU1015822A3 |
| ПРОИЗВОДНЫЕ НУКЛЕОЗИДОВ ПИРИМИДИНА ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ И СПОСОБ ИХ ПОЛУЧЕНИЯ | 1992 |
|
RU2085557C1 |
| Способ одновременного получения 1,3-дизамещенных мочевин и 1,2-диолов | 1978 |
|
SU856379A3 |


Авторы
Даты
1978-08-05—Публикация
1976-03-17—Подача