охлаждают реакционную смесь до 0°С и отфильтровывают выпавший гидрохлорид указанного соединения, который сушат в эксикаторе и (Перекристаллизовывают из метанола; т. пл. 250-260°С (разложение).
Пример 2. 2-метил-1,3,4,9&-тетрагН|Дро-2Яиндено- 1,2,-с -пиридин.
Раствор 5 г 2-метил-1,2,3,4,4а,9Ь-1гек1сагидро5Я-и.ндено- 1,2-с -|нирид1Ин-5-ола и 15 г иафталин-1,5-дисульфокислоты в 50 м.л воды нагревают до кипения С обратным холодильником в течение 1,5 час. Затем испаряют реакционную смесь в -в-акууме досуха И кристаллизуют остаток дважды из этанола. «с-(2-метил-1,3,4,96-тетрагидро-2Я - индеНО- 1,2-е -пиридин) нафталин-,5-дисульфонат плаъится с разложением при 275-280° С.
Пример 3. 2-бензил-1,3,4,9Ь-1гексагадро5Я-индено- 1,2-с -пиридин.
1:0 г 2-|бензил-1,2,3,4,4а,9&-.гвксагидро-5Я-индено- 1,2-с -пи1ридин-5-ола нагревают до кипения с обратным холодильником в смеси 15 м,л концентрированной соляной кислоты и 35 мл воды .в течение 20 мин. При охлаждении реакционной смеси кристаллизуют гидрохлорид указанного соед инения, который отфильтровывают и Перекристаллизовывают сначала из воды, затем из этанола. При разогревании ири 165°С он окрашивается постененно в зеленый цвет и плавится с разложением При 215-225° С.
Пример 4. 1,3,4,9&-те-11рагидро-2Я-индено 1,2-е --пиридин.
10,0 г 1,2,3,4,4а,9&-1гексатидро-5Я-инден10 1,2-е -1пиридин-5-ол-гидрохлорида нагревают с 40 мл 2 «. соляной кислоты ири обратном Потаке цо кииения. Затем охлаждают реакционную смесь до 0° С -и отфильтровывают выпавший тидрохлорид указанного соединения, которое сушат в вакууме и иеракристаллизовывают из метанола, т. пл. С (ipasложение).
П р и м ер 5. 7-хлор-2-метил-1,3,4,9&-тетрагидро-2Я-1ИНД1ено- 1,2-е -пиридин.
10 г 7-хлор-2-метнл-1,2,3,4,4а,9й-тексагидро5Я-.индено- 1,2-е -1пиридин-5-ола нагревают со смесью 20 мл концентрированной соляной кислоты и 40 мл воды 20 мин с обратным потоком до кипения. Затем реакционную Маосу охлаждают, испаряют в вакууме и иоглощают остающуюся пену ацетоном, причем 1К1ристаллизуется гидрохлорид указанного соединения; т. ПЛ. 256-258° С (разложение) юосле Кристаллизации из йзопропанола.
Примере. 2,7-диметил-1,3,4,9&-тетрагидро2Я-И1нденю- 1,2-е -пиридин.
10 г 2,7-диметил-1,2,3,4,4а,9Ь-текса1ГИДро-5Яиндено- 1,2-е -пиридин-5-ола нагревают с 100 мл соляной кислоты с Обратным (Потоком до кипения В течение 20 мин. Затем июпаряют реакционную смесь в вакууме, добавляют 25 мл этанола и испаряют еше раз. Получаюшийся в Остатке гидрохлоркд указанного соединения Перекристаллизовывают из этанола/ эфира и затем из этанола. При нагревании
он, начиная с 195° С, постепенно окрашивается в зеленый цвет и плавится с разложением при 250-255° С.
Пример 7. 2-н-пропил-1,3,4,96-тетратидро2Я-нндено- 1,2-е -пиридин.
8,0 г 2-н-пропил-1,2,3,4,4а,9Ь-гексагидро-5Яиндено- 1,2-е -|ПИридин-5-ола нагревают с 80 лгл 2 н. СОЛЯНОЙ кислоты 20 мин с обратным потоком до кипения. Цри охлаждевии смеси кристаллизуется гидрохлорид указанного соединения, который отфильтровывают и лерекристаллизовывают из 2 н. соляной -кислоты, т. Пл. 261-264°С (разложение). Пр.имер 8. 2-алкил-1,3,4,9Ь-тетрагидро-2ЯИНдено- 1,2-е -пиридин.
10 г 2-алкил-1,2,3,4,4а,9Ь-гексагидро-5Я-индена- 1,2-е -1пиридин-5-Ола нагревают с 100 мл 2 Н. соляной кислоты 20 мин с обратным потоком до кипения. ПоСле охлаждения смеои отфильтровывают выпавший гвдрохлорид указанного Соединения и Перекристаллизовывают из 2 н. соляной кислоты, т. 1ПЛ. 260-265° С (разЛОжение). Пр.имер 9. 2-(,2-фенилэтил)-1,3,4,9&-тетрагидро-2Я-индено- 1,2-е -пиридин.
10 г 2-(2-фенилэтил)-1,2,3,4,4а,9&-гек1сагидро5Я-индено- 1,2-е -пиридин-5-ола нагревают со смесью 30 мл конщентрированной |СОЛЯной кислоты и 70 мл воды 20 мин с Обратным потоком до кипения. Выпадающий уже во время нагревания гидрохлорид указанного соединения отфильтровывают после охлаждения смеси и Перекристаллизовывают из метанола; т. пл. 240-242°С (разложение).
Пример 10. 7- бром-2-метил-1,3,4,96-тетрагИ|Дро-2Я-индено- 1,2-е -ширидин.
4,8 г 7-1бро.м-2-метил-1,2,3,4,4а,9&-гексагидро5Я-И1ндено- 1,(Иридин-5-ола н-атревают со смесью 14 мл концентрированной соляной кислоты и 28 мл ВОДЫ 50 мин с обратным потоком до 1ки1пения. Затем реакционную Маосу охлаждают, испаряют в вакууме и поглощают остаток этанолом, причем кристаллизуется .гидрохЛОрид указанного соединения, т. пл.
251-255°С (разложение).
Пример 11. 2-этил-1,3,4,9&-тетрагидро-2Яиндено- 1,2-е -(Пиридин.
10 г 2-этил-1,2,3,4,4а,9Ь-гексатидро-5Я-индено- 1,2-е -пиридин-5-ола нагревают с обратным потоком до кипения с 100 мл 2 н. соляной кислоты в течение 20 мин. Выпадающий При охлаждении реакционной смеси гидрохлорид указанного соединения отфильтровывают и Перекристаллизовывают из 2 1Н. соляной кислоты;
т. |пл. 27.3°С (разложение).
При м ер 12. 2-нзопрапил-1,3,4,9&-тетрагидро-2Я-индено- 1,2-е -пиридин.
10 г 2-из.алро(пил-1,:2,3,4,4а,9Ь-гаксагидро5Я-индено- |1,2-е -пиридин-5-ола нагревают до
кипения с обратным шотаком с 100 мл 2 н. соляной кислоты в течение 20 мин. При охлаждении реакционной смеси выпадающий гидрохлорид указанного соединения отфильтровывают и Перекристаллизовывают .из 2 н. соляной
кислоты; т. пл. 260-265°С (разложение).
Пример 13. 2-(2-1Пропинил)-1,3,4.9&-тст,рагидро-2Я-индено- 1,2-с -пири,ди.н.
10 г 2-(2-П:ро1пин.ил)-1,2,3,4,4а,9&-.ге1Ксагиаро5Я-индено- 1,2-с -1пириди1Н-5-ола налревают до кипения с 100 Л1Л 2 н. соляной кислоты 20 мин с обратным ПОтокОМ. |При охлаждении реакционной смеси выпадающий гидрохлорид указанного соединения отфильтровывают и перекристаллизовывают из воды; т. пл. 235-. (разложение).
Пример 14. А. ( + )-2 - метил - 1,3,4,9Ьтетрагидро-2// - индено- 1,2-с -пиридин - гидрохлорид.
10 г (-)-2-метил-1,2,3,4,4а,9Ь-гексагидро5Я-индено- 1,2-с -пиридин-5-ола, т. пл. 135- 136°С из ацетона; ,5° (, метанол), нагревают до кипения с 50 }лл 3 н. соляной кислоты в течение 15 лин с обратным потоком. Затем охлаждают реакционную смесь до 0° С и отфильтровывают выпавший осадок, который перекристаллизовывают из 15 мл 2 п. соляной кислоты и сушат в вакууме при 80° С. (4-)-2-метил-1,3,4,9&-тетрагидро-2Я-индено- 1,2-с -пиридин-гидрохлорид плавится с разложением при 250-255° С; а 43б +253° С (,0, метанол).
Б. (-)-2-метил-1,3,4,9Ь - тет,рагидро-2Я-.индено- 1,2-с -таиридин-гидрохлорид.
Поступают, как аписано выше, БО употребляют вкачестве-исходного продукта ( + )-2-метил-1,2Д4,4а,9&-ГаксаГИдро-5Я - видено- 1,2-6- пириди«-5-ол, т. 1ПЛ. 135-136°С (из ацетона); а f +97° (с : 1,0, метанол). Полученный (-)-2-метил-1,3,4,9&-тетрагид|ро-2Я - индено 1,2-с -пиридин-гидрохлорид плавится с разложением .при 250-255° С; ./ -253° (с 1,0, метанол).
Пример 15. 2-(2-|бут,инил)-1,3,4,9Ь-тетрагидро-2Я-:индено- 1,2-с -1Пиридин.
10 г 2-(2-бутинил)-1,2,3,4,4а,96-1гекса1гидро5Я-ивдено- 1,2-с -пиридин-5-ола «агревают до кипения ;В 100 мл 2 .н. соляной кислоты В течение 20 мин с обратным холодильником. Далее ма|ссу оставляют охлаждаться и отфильтровывают. Остаток 1перекристалли.зовывают из 2 н. соляной кислоты. Полученный при этом гидрохлорид указанного соединения плавится При 210-215°С (разложение).
Пример 16. 2-(2-метилаллил)-1,3,4,96-тетрагидро-2Я-индено- 1,(пириди,н.
Поступают, .как в примере 1:5, но применяют в качестве исходного продукта 2-(2-меТ|Илаллил)-1,2,3,4,4а,9 |-геКоагидро - 5Я-индено- 1,2с -пиридин-5-ол. Полученный при этом гидрохлорид указанного соединения плавится при 210°С (разложение).
Пр.и.мер 17. 2-(г/ анс-2-бутенил)-1,3,4,9Ьтетрагидро-2Я-индено- :1,2-е -пиридин.
Поступают, как в примере 15, но в качестве 1СХОДНОГО соединения применяют 2-(гранс-2бутенил) - 1,2,3,4,4а,9Ь - 1гек сагидро-5Я-индено 1,2-с -пириа,ин-5-Ол. Полученный три этом гидрохлорид указалного соединения пла.вится при 225-227° С (разложение).
П р и м ер 18. 2-(3,3-диметилаллил)-1,3,4,96тет|рагидро-2Я-иидено- 1,2-с -пиридин.
К раствору 10 г 2-(3,3-диметилалл:ил)1,2,3,4,4а,96-гексагидро-5Я - индено- 1,2-с -ПИридин-5-ола в 100 мл хлорофор.ма приливают 5,7 мл тиОНИлхлорида и нагревают до киления в течение 30 мин с обратным холодильником. Реакционную .массу после этого п.ол,ностью испаряют. Остаток затем нагревают до 75° С
в течение 10 мин с 20 мл ъады, дают ему охладиться, отфильтровывают полученный при этом продукт и перекристаллизовывают из этанола. ГидрОХлорид указанного соединения плавиться (при 230-236°С (разложение).
Пример 19. 2-(3-бутинил)-1,3,4,9Ь-тетрагидро-2Я-индено- 1,2-с -пиридин.
10 г 2-(З-бутинил)-1,2,3,4,4а,96-тексагидро5Я-индено- 1,2-с -1пиридин-5-ола нагревают до кипения в 200 мл 2 п. соляной кислоты .в течение 20 мин с обратным холодильником. После этого реакционную массу оставляют охлаждаться и отфильтровывают. Остаток перекристаллизовывают из 2 ,н. соляной кислоты. Полученный этом т.идрохлорид указанного
соединения плавится три 235-237° С (разложение) .
Пример 20. А. (-)-7-хлор-2-метил1,3,4,9Ь-тетрагидро - 2Я - и.няено- 1,2-с чпиридин-гидрохлорид.
8 г ( + )-7-хлор-2-метил-1,2,3,4,4а,96-гексагидро-5Я-индено- 1,2-с -1пиридин-5-ола, т. пл. 158-160°С из ацетона; aj g+144,9° (с 1,0, метанол), нагревают до кипения с40лгл 5 н. соляной кислоты в течение 40 мин с о братным холодильником. После этого истаряют в вакууме, испаряют окОНчательно спиртом и перекристаллизовывают остаток дважды из изопрапанола, содержащего 5% осонцентрированной соляной кислоты. (-)-7-хло.р-2-метил1,3,4,9Ь-тетрагидро-2Я - индено- 1,2-с -пиридин-гидрохлорид плавится при 255-260° С (разложение); ,0° С (с 1,0, метанол).
Б. ( + )-7-.хлор-2-метил - 1,3,4,9Ь-тетраг.идро2Я-индено- 1,2-с -пнридин-1ГИДрохлорид.
Поступают, как указано .вы:ше, но применяют в качестве исходного продукта (-)-7-хлор2-метил-1,2,3,4,4а,9; .. гексагидро - 5Я-инд9Н0 1,2-с -пиридин-5-ол, т. 1ПЛ. 158-160°Сиза1цетона; -144,9° (с 1,0, метанол). Полученный ( +) -7-хло.р-2-метил-1,3,4,9Ь-тетраГИдро-2Я-индено- 1,2-с -пиридин-5-ол плавится при 255-260°С (разложение); а +173,0°
(с 1,0, метанол).
Предмет изобретения
Способ получения кислотно-аддитивных солей производных ИндеНОпири.диНа обш,ей формулы
/,
N-R,
65
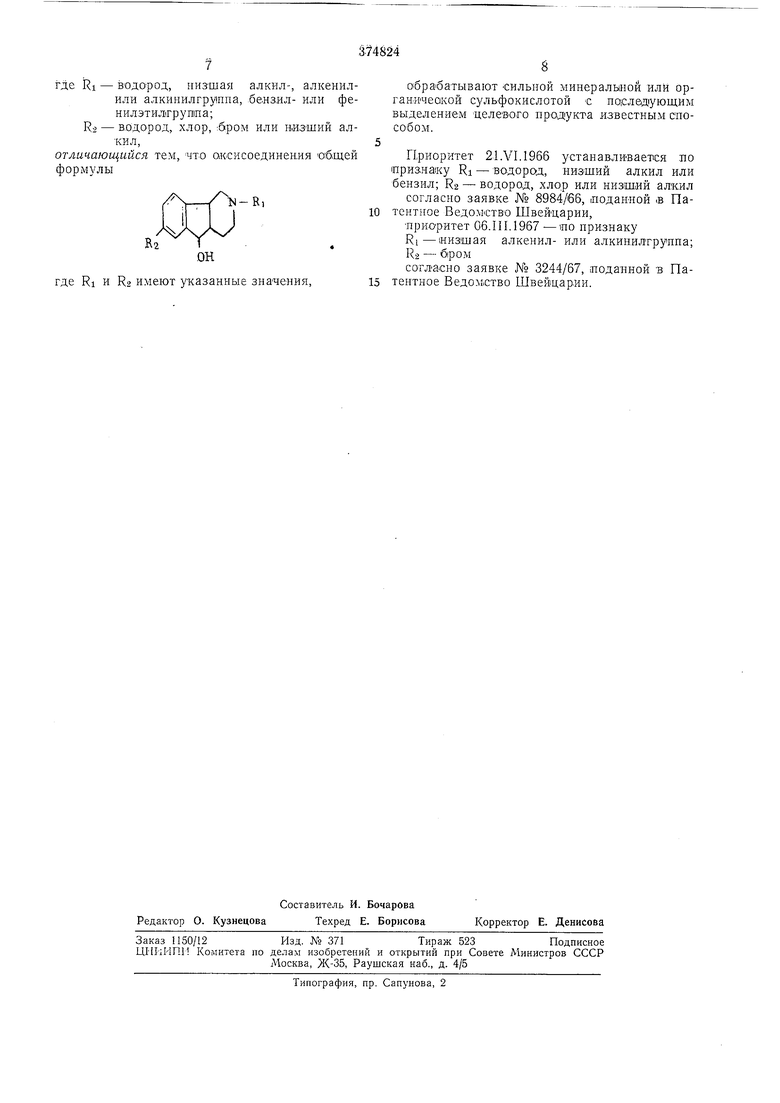
где Ri - водород, низшая алкил-, алкенилили алкинилгруипа, бенаил- или фенилэтил1груп1па;
R-2 - в,одород, хлор, :5ром или низший алкил,
отличающийся тем, что аксисоединения «бщей
формулы
где RI и Re имеют указанные значения.
обрабатывают сильной минеральной или органичеакой сульфокислотой € норледующим выделением щелевого продукта известным способом.
Приоритет 2:1.VI.1966 устанавливается ло орианаку Ri - водорад, низший алкил или бенаил; Ra - водород, хлор или низший алкил
согласно заявке № 8984/66, поданной .в Патентное Ведомство Швейцарии,
приоритет 06.III.1967 -ino признаку
RI-(низшая алкенил- или алкннилгруппа;
Ra - бром
согласно заявке № 3244/67, поданной в Патентное Ведомство Швейцарии.


| название | год | авторы | номер документа |
|---|---|---|---|
| СПОСОБ ПОЛУЧЕНИЯ СОЛЕЙ ИНДЕНОПИРИДИНА | 1972 |
|
SU432717A3 |
| Способ получения производных индено-пиридина | 1970 |
|
SU437284A1 |
| СПОСОБ ПОЛУЧЕНИЯ КИСЛОТНЫХ СОЛЕЙ ИНДЕНОПИРИДИНОВ1Изобретение относится к области получения новых кислотных солей инденопиридинов, об- ладаюидих высокой фитологической активностью.Известны инденопиридины и их кислотные соли общей формулы (I), содержащие в положении «5» заместитель и полученные реакцией дегидратации соответствующих 5-окси- соединений.-CH-CH-CCH^VR^ Кз Riсогде RI — водород, низший алкил, С1, Вг илиF; R2—CN, —COORs; —CON (^R. R»' | 1973 |
|
SU383293A1 |
| Способ получения кислотных солей инденопиридинов | 1970 |
|
SU517256A3 |
| Способ получения производных пиперидина или их солей | 1975 |
|
SU634665A3 |
| ПРОИЗВОДНЫЕ АЗЕТИДИНА И ПИРРОЛИДИНА | 1998 |
|
RU2198873C2 |
| Способ получения производныхизОХиНОлиНА или иХ СОлЕй | 1978 |
|
SU852172A3 |
| СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНБ1Х 9,10-ДИГИДРО-4Н- -БЕНЗО-[4,5]-ЦИКЛОГЕПТА-[1,2-б]-ТИОФЕНА | 1968 |
|
SU231414A1 |
| ПОЛИЦИКЛИЧЕСКИЕ ТИАЗОЛИДИН-2-ИЛИДЕНОВЫЕ АМИНЫ, СОДЕРЖАЩИЕ ИХ ЛЕКАРСТВЕННЫЕ СРЕДСТВА И СПОСОБ ПОЛУЧЕНИЯ ЛЕКАРСТВЕННОГО СРЕДСТВА | 1999 |
|
RU2236405C2 |
| Способ получения 9 -метилстероидов | 1971 |
|
SU488405A3 |


Авторы
Даты
1973-01-01—Публикация