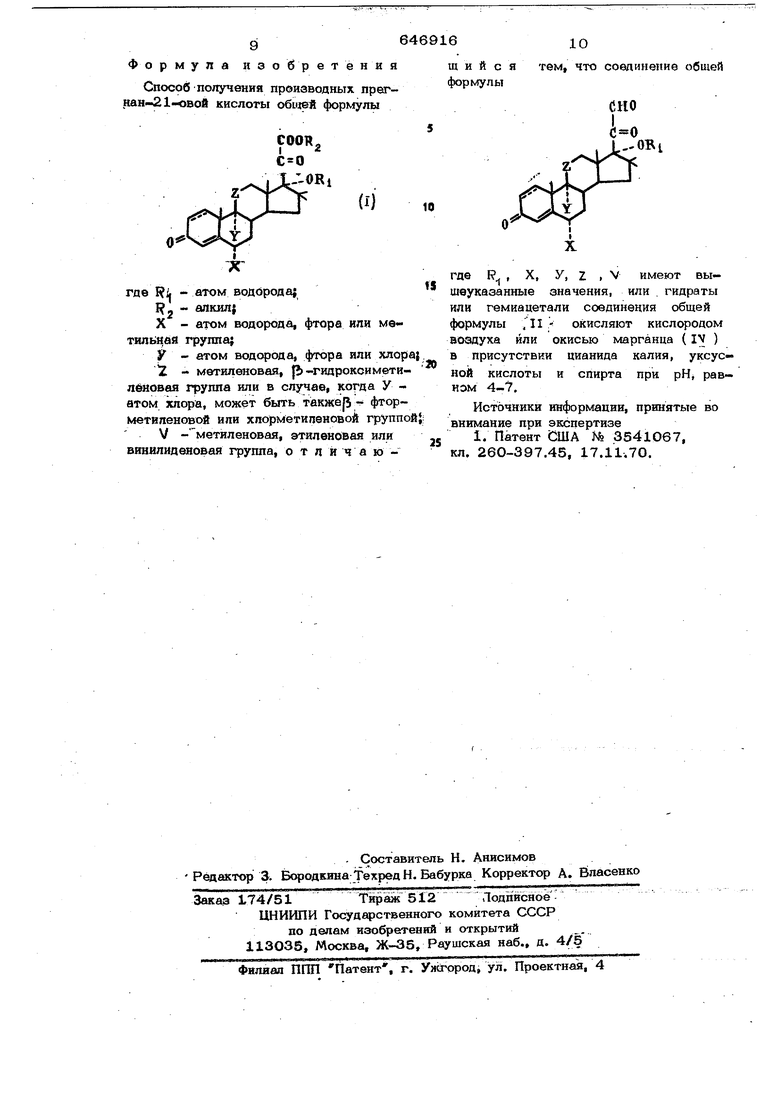
364 Способ согласно взобретеняю заключается в том, что соединение обш формулы/«НО Ц. . .: - -: ..: где , X, У, 1 .V имеют вышеукааанные диачения, или гидраты или геми« «йетапи соедияевия обшей формулы ;1 ШжЫ1ааот йисйсчиэйрм воавуха или окисью марГёвша ((V У в 1фйсутст«ии иианида калия, уксусной кислоты и спирта рН, равном 4-7, Целевые продукты выделяют из вяокноД смеси известным способом. И к« вй в ей1фт6в 1 ЬнЕф1Кич1Мб 1Ш Й1 ер44й1ае i фатическке или шклоалифатйчёские спир рбпаиол, г ссаиол, ЕШклогёксанол, изоЛ|р и1иловый спирт, бутиловый спирт, бутен 2-нс1Л, пентанол,: бшзиловый или ок ГИЛОВЫЙ СП1фТ. Предвочтителыю првменаот О,О11О, аще 0,1-1,0 моль диаинаа калия иа 1 моль соединения обшей формулы 1Реакцию проводят таким , что к реакционной смеси прибавляют дополнительное количество кислоты, кроме тоt4 К1апячества, которое необходимо для нейтрвйязадия аианвда. В качестве 1 ислоты ис оользуки, например, минеральйыб кислоты, aпpимep серную, фосфорную или соляную сульфокислотЫ например п-толуолсульфокислоту, или карбоновые кислоты,напри м - 0гравьиную или уксусну1б. PeaкшIЮ проводят йреопочтительно в присутствии биполярных апротоняых растворителей, таких, кшс диметилформамид, Мгметйладетамид, дяметвяацетамнд, ц-метилпнрролидон, диметилсульфоксид, сульфолан, диметилсультон. гексаметилтриамид фосфорной кислоты или ацетонитрил. В качестве растворителя предпочтнтельно используют 2-200 мл (на 1 г ; соединения обшей формулы ).. смеси 5-50% низшего спирта и 5О-9В% биполярного апротонного растворителя. Реакцию предпочтительно осуществляют в интервале температур от О до50Рс. Продолжительность ее определяется температурой реакции и составом реагентов: 16 при использовании кислорода воздуха 5-120 мин, а активной окиси марганца (W ) - 1-ЗО мин. Пример 1. 2,8 г 11|5 ,17ot -дигидрсйсси-3,20-диоксо-1,4-прегнадиен-21-аля растворяют в 90 мл метиленхлорида и 50 мл метанола и обрабатывают 3 мл концентрированной уксуснс кислоты и 700 мг цианида калия. Реакционную смесь п емешивают 15 мин при комнатной температуре, а затем раз0ввляют метилш1хпоридом и промывают водой. Органический слой высушивают над сульфатом натрия и выпаривают. Остаток хроматографируют на силикагеле, перекристаллизовывают из смеси ацетонгекса я и получают 433 мг метилового Эфира 11 fb ,17рС -дипирокси-3,2О-диоксо-1,4-прегн |Диен-21 овой кислоты. Т.1Ш. 215,. П р и м е р 2. 2,5 г 9ot-фтор-Ир 17о6-дигидрокси-3,2О-диоксо-16-клетил-1,4-прегнааиен-21-аля растворяют в 10О мЛ мгетанола, раствор обрабатывают 2,5 мл концентрированной уксусной кислоты и 400 мг цианида калия и перемешивают 25 мин при комнатной температуре при Пропускании воздуха через реакЕЙонНую смесь. Затем реакционную ,ассу разбавл1ают метиленхлоридом, промывают водой, высушифают сульфатом натрия и концентрируют в вакууме. Неочищенный продукт пропускают через хроматографнЧескую колонку, заполненную сйликагелем, и перекрнсталлизовывают из смеси ацетон-гексан, получая 719 мг метилового эфира 9о6-фтор-11 Ь Д7ct-дигвдpoкcн-3,20-диoкco-16-метил-1,4-прегнадиен-21-овой кислоты, т.пл. 191,. Пример 3,2,5 г 9рС-фтор 11|Ь .i7ct-flИГвдpoкcи-3,2O-диoкco-16с(.-метил-1,4-прегнадиен-21-аля растворяют в 10О мл бутанола, раствор обрабатывают 2,5 мл уксусной кислоты « 400 мг цианида калия и перемешива„,. 30 мин при комнатной температуре. Раствор раэбавлякп- метиленхлоридом, промывают водой, высушивают над сульфатомнатрия и отгоняют растворитель вакууме. Неочищенный продукт лропус ,р хроматографическую колонку, заполненную силикагелТм, и после nepi кристаллизации ,иа смеси адетон-гексан получа 67 мг бутилового эфира 9о6н}«ор-11&,17о6-дигвдрокси-3,20-диоксо-16с -иетил-1,4-прегнадиен-21-овоЙ кислоты, т.пл. 172,. Пример 4. 5,О г 11 (Ъ,17с6 -дигидрокси-3,20-диоксо-4-прегнен-21-аля обрабатывают в условиях примера 2. Неочшценный продукт пропускают через хроматографнческую колонку, перекристалпизовывают из смеси ацетон-г&ксан и получают 825 мг метилового эфира 11|Ь, 17 pt-Д игид роксн-3,2 О.ю кco-4-пpeгнeн.-21-oвoй кислоты, Т.ПЛ. 216,, Пример S. В условиях примера 1 обрабатывают 750 мг 111 ,, 21-тригидрокси-16-метилеи-1,4-прегнадиен-3,2О-диона и получают после перекристаллизации из смеси эфир-днизопро пиловый эфир 210 мг метилового эфира 11 (5,17о(,-дигидрокси-3,20-дион- 16-метипен- ,4-лрегнадиен-.21 -овой кнблоты, Т.ПЛ, 179С. Пример 6. В условиях примера 1 из 5,0 г 9с -фтор-11р,17оС,21-три. гидрокси-4- регнея-3,2О-диона получают после перекристаллизация из смеси адетон-гексая 688 мг метилового эфира 9о6-фтор-11 )Ь , 17ot-дигид кжcи-3,20-диoкco-4-пpeГнeн-21-)вoй кислоты, Т.Ш1. 228,3С, П р и м е р 7. 1,О г11/,17с6-ди гвдрокси-3, 2О-Д иоксо-6 об-метил-1,4- -прегиадиен-21-аля растворяют в 25 мл безводного ацетонитрила в атмосфере азота. Раствор обрабатывают 8 мл абсолютного этаиола, 1,6 мл концеитрированной уксусной кислоты, 2 г активной окиси марганца (IV) и 350 мг циш1ида калия. Смесь перемешивают 4 мин при ком натной температуре и затем отфильтровы вают двуокись марганца. Фильтрат разбавляют хлороформом, промывают водой, высушивают над сульфатом натрия и концентрируют в бакууме. Остаток хроматографируют на силикагеле и после перекристаллизации из смеси эфир-гексан получают 490 мг этилового эфира lip), 17aL -д игкдрокси-3,2 0-диоксо-6о6 -метил -1,4-прегнадиен-21-овой кислоты, т.пл 205,. Пример 8. 1,5 г 11р,17с -аигидрокс11-3,2О-диоксо-6с6-метил-1,4 -прегнадиен-21-аля в атмосфере азота растворяют в 1О мл безводного метанола и 35 мл диметилформамидау к раствору прибавляют 2,5 мл концентрированной уксусной кислоты, 3 г активной окиси MapriaHua {IV) и 530 мг цианида калия. Смесь .перемешивают 4 мин при комнатной температуре. Действующую об работку я . хроматографирование проводят по примеру 7. Получают 415 мг метило 64 вого эфира 11Р,17с -диГидрокси-3, иоксо-6 с1-метил-1,4-прегнадиен-21-овой кислоты: т.пл. 152,4°С. ; Пример 9. 1,3 г 11(),17оС-дигидрокси-3,20-аиоксо-6о6-метил-1,4-прегнадиен-21-аля .в 25 мл сульфолана подвергают взаимодействию с 8 мл пропилового спирта, 1,6 мл уксусной кислоты, 2г окиси марганца {IV) и 350 г цианида калия в условиях 7. После перекристаллязаш1и из смеси эфир-ацетон получают 1225 мг пропнлового эфира 11 , 1 ioL -дигвдрокси-3,20-диокco-6oL -метил-1,4-пр€Гнадиён-21-овой кислоты, т.пл. 20О,. Пример 10. 1,О г 11|Ь,17сС-дйгидрокси-3,2О-дкоксо-6о --метил-1,4-прегнадиен-21-аля в 25 мл N -метилпирролидона обрабатывают 6 мл бутанола, 1 мл уксусной кислоты, 2 г окиси марганца (IV) и 350 мг цванида калия в условиях примера 7. После перекристаллизации из смеси эфир-гексан получают 487 мг бутиловйго эфира 111%, 17о6-дигид рокси-3,20-лиоксо-6 1-метил-1,4-прегнадиен-21-овой кислоты, т;пл. 189,1С. Пример 11. К раствору 1,0 г 11 1%, 17ot -дйгидроксит, 20-д иоксо-16-метилен-1,4-прегнадиен-21-аля в 25 мл ацетонитрила и 8 мл бутанола прибавляют 1,6 мл концентрированной уксусной кислоты, 2 г активной окиси марганца (IV) и 350 мг цианида калия и переме шивают при комнатной температуре 5 мин. Затем отфильтровывшот двуокись марганца, фильтрат разбавляют хлороформом н промывают водой.. Органический слой вы- t сушивают сульфатом натрия и отгоняют растворитель. Остаток (1,05 г) хроматографируют на сюшкагеле, вымывают 45-5О%-ным paci BopOM уксусноэтнлового эфира в гексане. После перекристаллизации из смеси эфир-аяизопропиловый эфир получают бутилсдаый 11/4,17оС-дигиДроксн-3,2О-диоксо-16-ме илён- , -1,4-прегнаднен-21-овой кислоты, т.пл. 178,. Пример 12. В условиях примера 10, за исключением того, что вместо бутанола применяют пропанол, из i,Or lljb ,ltcC Н1игидрокси-3,20-диоксо-16-метш1ен-1,4-лрегнадиен-21-аля получают 286 мг пропилового эфира 11(5, 17оС-Дигидрокси-3,20-аиоксо-16-метилен-1,4-прегнадиен-21 -овой кислоты, т.пл. 166,4°С. (из смеси эфир-диизопропиловый эфир). Пример 13. К раствору 1,0 г lip ,1 ТоК-дигидрокси-3,20-диоксо-16-мвтилен-1,4-прегнааиен-21-аля в 8 мл этанола, и 25 мл гексаметилфосфортриамида, прибавляют 1,6- мл концентрированной уксусной кислоты, 2 г окиси мар ганца ()V) и 35О мг цианнца калия,перемешивают 1О мин при комнатной температуре. Продукт выделяют по примеру Ю и очнщшот хроматографически с поспШутотеА перекристаллизацией из смеси адетон-гексан. Получают 400 мг эти лового эфира 11 р, 17с6 -дигидрокси-3, 2О-Д иоксо-16-метил ен-1,4 -прети ад иен-21-овой кнслоты, т.пл, . Пример 14, К раствору 1,7 г 11 fb , 17cL -дигндрокси-3,20-диоксо-16-метилен-1,4-прегнадиен-21-аля в 12м метанояа н 35 мл диметилсульфоксида прнбавляхуг 2,4 мл уксусной кислоты, 4,5 г окиси марганца (IV) и 530 мг цианида калия н перемешивают 3 мин при комнатной температуре. Продукт реакции выделяют согласно примеру 10, .очищают хроматографически в перёкрнсталлизаяией из смеси эфир-дийзопропило вый эфир получают 49О мг метилового эфира 11,17о6 -д игидрокси-3, 2О-диокСО-16-метилен-1,4-прегнадиен-21-ОБой кислоты, т,пл, 181,. Пример 15, Аналогично примеру 7, но применяя метанол вместо этанола, получают метиловый эфир боС-фто -11 р ,17ot-днгидрокси-3,20-диоксо-16сС-метил-1,4-щ)егнадиен-21-овой кислотыут,пл, 182,6 С, Пример 16, Так же, каз в при мере 7, получают этиловый эфир - feet -фтор-11 ,17о --дигидрокси-3,20-диоксо-16 -метил-1,4-прегнадиен-21-0&ОЙ кислоты с т.пл, 14О,5 С. )( Пример 17, Аналогично примеру 7, применяя пропанол вместо этанола получают пропиловый эфир боС-фтор-11 fb, 17с(.-д игидрокси-3,2 0-д ирксо-16сС-метил-1,4-прегнадиен-21-овой кислоты, т.пл, 134,4 С, Пример 18, Аналогично примеру 7, но используя бутанол вместо этанола, получают бутиловый эфир бс -фтор V-11 р ,.-ангидрокси-3,20-дноксо-16 сз(.-метил-1,4-прегнадйен-21-овой кислоты,. т,пл, 169,6РС. Пример 19, Так же, как в при мере 7, получают этиловый эфир 6 6-фтор-11|6,17оС-дигидрокси-3,20-диоксо-1,4-прегнадиен-21-овой кислоты, т.пл. 238,5°С. Пример 20, Аналогично приме-, ру 7, применяя бутанол вместо этанола, получают бутиловый эфир боС-фтор-Ц, 17сС-д игид рокси-3,20-ДИОКСО-1,4-прегнадиен-21-овой кислоты, т.пл. 193,. Пример 21. Аналогично примеру 7 получают этиловый эфир 9с -фтор-11 (5 ,170С-ДИГидрокси-3,2О-дирксо- , -16 оС-метип-1,4-прегнадиен-1-овой кислоты, т.пл. 184,2 С. Пример 22. Согласно примеру 7Jиспользуя изопропиловый спирт вместо этанола, получают изопропиловый эфир 9 а6-фтор-11 p,17o6-flигвдpoкcи-3,2O диoкco-l 6 оС-метил-1,4-прегнадиен-21 -овой кислоты, т.пл. 174,7С. Пример 23, Аналогично примеру 7, применяя амиловый спирт вместо этанола, получают амиловый эфир 9о6-фтор-11 j3 ,17с|С-дигидрокси-3,20-диоксо-16ot -метил-1,4-прегнадиен-21-овой кислоты, т.пл. 165,5°С. Пример 24. Согласно примеру 7 получают этиловый эфир 11 ji , 17о6 -ди- гвдрокси-3,20-гДноксо-1,4-прегнадиен-21 овой кислоты, т.пл. 225,. Пример 25. 1,0 г llft-гвдрокси-17СС-бутирилокси-3,2O-aиoкco-4-пpeгнeн-21-aля растворяют в 5 мл абсолютного метанола и 30 мл аиетонитрила в атмосфере азота. К раствору прибавляют 1,6 мл конпвентрйрованной уксусной кислоты, 2 г марганца (V) и 350 мг цианистого калия и выдерживают реакционную смесь 8 мин при комнатной температуре. Отфильтровывают двуокись марганца, фильтрат разбавляют хлороформом, промывают водой и высушивают над сульфатом натрия. После отгонки растворителя получают 1,25 г масла, которое хроматографируют на силикагеле. Вымывают 4О-45%-ным раствором уксусной кнслоты и перекрнсталлизовывают из смеси эфир - петролейный эфир. Получают 360 мг метилового эфира 11 ft -гидрокси-17оС-бутирилокси-3,20-диоксо-4-прегнен-21 -овой кислоты, т.пл. 197,. g6 Формула изобретения Способ получения производных претнвн -21«овой кислоты ободей формулы где . - атом водорода; Ef- алкил; X - атом водорода, фтора или метяпщ&й группа; У - атом водорода, фтора или хлора - метиленовая, fb-гидроксиметилёмовая группа или в случав, когда У атом хлора, может быть такжер -т фторметиленовой или хлорметипеновой группо V - метиленовая, этиленовая или виннлиденовая группа, отличаю 610 щ и и с я тем, что соединение обшей формулы -г г X. У, Z где R имеют вы- шеуказанные значения, или гидраты или гемиацетали соединеция общей формулы ,11 окисляют кислородом воздуха или окисью марганца ( IV ) в присутствии цианида калия, уксусной кислоты и спирта при pHj равкэм 4-7. Источники информации, принятые во внимание при экспертизе 1. Патент США № 3541067, кл. 260-397.45, 17.11,70.



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных прегнановой кислоты | 1973 |
|
SU524523A3 |
| Способ получения производных прегнановой кислоты | 1974 |
|
SU622411A3 |
| Способ получения производных прегнановой кислоты | 1975 |
|
SU609472A3 |
| Способ получения производных прегнановой кислоты | 1972 |
|
SU686623A3 |
| Способ получения производных прегнановой кислоты | 1975 |
|
SU615863A3 |
| Способ получения производных 6 -фтор-16 ,18-диметил1,4-прегнадиен-3,20-диона | 1971 |
|
SU504493A4 |
| Способ получения кортикоидов или их солей | 1978 |
|
SU668611A3 |
| Способ получения производных 6 -фтор-16 ,18-диметил-1,4прегнадиен-3,20-диона | 1971 |
|
SU468409A3 |
| Способ получения производных 9-фторпреднизолона | 1978 |
|
SU862829A3 |
| Способ получения кортикоид -21- СульфОпРОпиОНАТОВ или иХ СОлЕй | 1979 |
|
SU818489A3 |


Авторы
Даты
1979-02-05—Публикация
1974-12-20—Подача