Изобретение относится к спос получения новых производных аде которые могут найти применение честве исходных продуктов в син коферментов. Известна реакция алкилирован меркаптидов галоидпроизводными роциклических соединений 1. . Предлагается способ получени изводных аденина общей формулы V$(tH,) (1 Н Н НИ A-HO(,Hj- -C t-tЯНИН он о н н н I I I II II I ) I -с- C-t- с- СНгО -г- OF-о СИ,- t-t-C- С-И г ч окон I л 1 -о--о М - ион щелочного металла; п 1 или 2. Способ заключается в тсял, что соединение общей формулы Лух где А имеет вышеуказанные значенияj X - галоид, подвергают взаимодействию с соединением общей формулым® |«1иО„((ш), где М и п имеют вышеуказанные значения , в полярном апротонном растворителе при комнатной температуре. В качестве апротонного полярного растворителя могут быть использованы гексаметилфосфотриамид, диметилаульфоксид, диметилформамид. Пример 1. Получение 8-(2-карбоксиэтилтио)аденозина. В раствор 380 мг (1,1 ммоль) 8-бромаденозина в 5 мл безводного гексаметилфосфотриамида вносят при перемешивании при комнатной температуре (в атмосфере азота) 683 мг (4,2 ммоль) динатриевой соли 3-ме 36 каптопропионовой кислоты (полученной обработкой при комнатной температуре меркаптокислоты стехиометрическим количеством гидрида натрия в безводном тетрагидрофуране и последующей отгонкой растворителя в вакууме). После перемешивания в течение 16 ч при комнатной температуре смесь фильтруют, к фильтрату приливают 15 мл воды и несколько раз экстрагируют хлороформом до удаления гексаме тилфосфотриамида. Водный раствор доводят разбавленной соляной кислотой до рН 8,5, хроматографируют на смоле Доуэкс-1 (НСОО), элюируя градиентом муравьиной кислоты в воде. Фракции с fixoKc -282 им объединяют и сушат вымораживанием. Получают 327 мг 8-(2 -карбоксиэтилтио)аденозина. Соединение оказывается чистым по данным тонкослойной хроматографии (силикагель с флуоресцентным индикатором; элюентг изопропанол - вода - 32%-ный едкий аммоний в объемном соотношении 7:2:1; проявление пятна под УФ-лучами при 254 нм; Rf 0,56) и высоковольтажного электрофореза (ватманская бумага ЗММ Их х57 см; электролит - 0,02 М раствор ацетата аммония, рН 5,0, потенциал 5000 В в-течение. 40 мин; проявление пятна в УФ-свете при 254 нм; мобильность соединения в сторону анода, чт находится в согласии с наличием карбоксильной группы, между тем как аденозин мигрирует в сторону катода) УФ-спектр в 0,1 М растворе едкого натра обнаруживает пик поглощения при 282 нм, между тем.как 8-бромаденозин - при 263 нм. ЯМР-спектр в NaOH. показывает в дополнение к сигналам аденозина (за исключением сигналов протона в положении 8) сигналы протонов боковой цепиг 2,88(5(2 Н, t; СЕ„СОО) и 3,86 (2 Н, t, СНр). Масс-спектр также подтверждает структуру (м/е 239, 221, , 167). Пример 2. Получение никотиноиламид-8-(2-карбоксиэтилтио)-адено зиндинуклеотида. В раствор 118 мг (160 мкмоль) никотиноиламид-8--бромадениндинуклеот да в 2 мл безводного диметилсульфоксида вносят при. перемешивании при комнатной температуре в условиях защиты от влаги в атмосфере азота 98,4 мг (656 мкмоль) динатриевой соли 3-меркаптопропионовой кислоты (по лученной описанньэм в примере 1 способом) . После перемешивания в течение 16 при комнатной температуре смесь отфильтровывают и к фильтрату приливают 10 объемов ацетона. Полученный осадок отфуговывают, промывают ацето ном, сушат в вакууме к растворяют, в 15мл 0,1 М раствора соляной кислоты. Раствор доводят разбавленным раствором соды (едким натром) до рН 7,5, хроматографируют на смоле Дауэкс-1 (НСОО), элюируя градиентом муравьиной кислоты в воде. Хроматографические фракции с X ДДО1КС 276,5 нм объединяют, сушат вымораживанием (лиофильная сушка) и получают 90 мг никотиноиламид-8(2-карбоксиэтилтио)-аденозиндинуклеотида. Вещество оказывается чистым по данным то.нкослойной хроматографии (силикагель с флуоресцентным индикатором; элюент: изомасляная кислота вода - 32% аммиаком в объемном соот|ношении 66:33:1,7; проявление пятна УФ-лампой при А 254 им; Rf 0,31) и высоковольтажного электрофоре.за (ватманская бумага 31-Ш 11x57 см; электролит - 0,02 М раствор ацетата агфюния, рН 5,0, потенциал 5000 В в течение 30 мин; проявление пятна под УФ-лампой при 254 нм; подвижность соединения в сторону анода 5оль;ше, чем у НАД в соответствии с наличием карбоксильной группы).. УФ-спектр в растворе пирофосфатного буфера, рН 8,7, обнаруживает пик при 276,5 нм, который при ферментативном восстановлении спиртовой дегидрогеназой иэ дрожжей., переходит к 282 нм с появлением нового пика при 340 нм, характерного длявосстановленного ядра нигкотиноиламида. ЯМР-спектр в показывает в дополнение к сигналам НАД (за исключением сигналов протона у углерода в положении 8 аденинового ядра) сигналы, характерные для протонов боковой цепи: 2,88с (2Н, t; СЧ„СОО) и 3,86 (2Н, t; CHg). Масс-спектр также находится в согласии с указанной структурой (м/е 221, 192, 1.67) . Пример 3, Получение никотиноиламид-8- (2-карбоксиэтйлтио) -адениндинуклеотидфосфата. В раствор 50 мг (57,6 мкмоль) никотиноила.мид-8-бромадениндинуклеотидфосфата в 1 мл безводного диметилсульфоксида вносят при перемешивании при комнатной температуре в условиях защиты от влаги в атмосфере азота 36 мг (240 мкмоль) динатриевой соли З-меркаптопропионовой кислоты (полученной описанным в примере 1 способом) . После перемешивания в течение 16ч при комнатной температуре смесь отфильтровывают и .к фильтрату приливают 10 объемов ацетона. Полученный осадок отфуговывают, промывают ацетоном, сушат в вакууме и растворяют в 10 мл О,1 М раствора соляной кислоты. Раствор доводят разбавленным раствором едкого натра до рН 7,5 и хроматографируют на смоле Даузкс-1 (С ) , элюируя градиентом хлористого кальция в воде, имеющим рН 3 благодаря добавлению с(ляной кислоты, Хроматографическиё фракции, содержащие целевой продукт объединяют, упаривают до небольшого объема и обессоливают фильтрацией через Сефадекс- G-10, элюируя вещество водой.
Строение никотиноиламида-8-(2-карбоксиэтилтио)-адениндинуклеотид
ЛНг
VY$№)COOV
Y н н нн III где A-HOCHj-C-t-t-C-t-d-C-t-CHjO-pV I; - Пи-t-d-C-t ОНОН: I ч IpJОН ОН
фосфата устанавливают аналогично описанному в примере 2 для соответствующего производного НАД (для ферментативного восстановления используется дегидрогеназа глюкоза-6-фосфата).
Формула изобретения
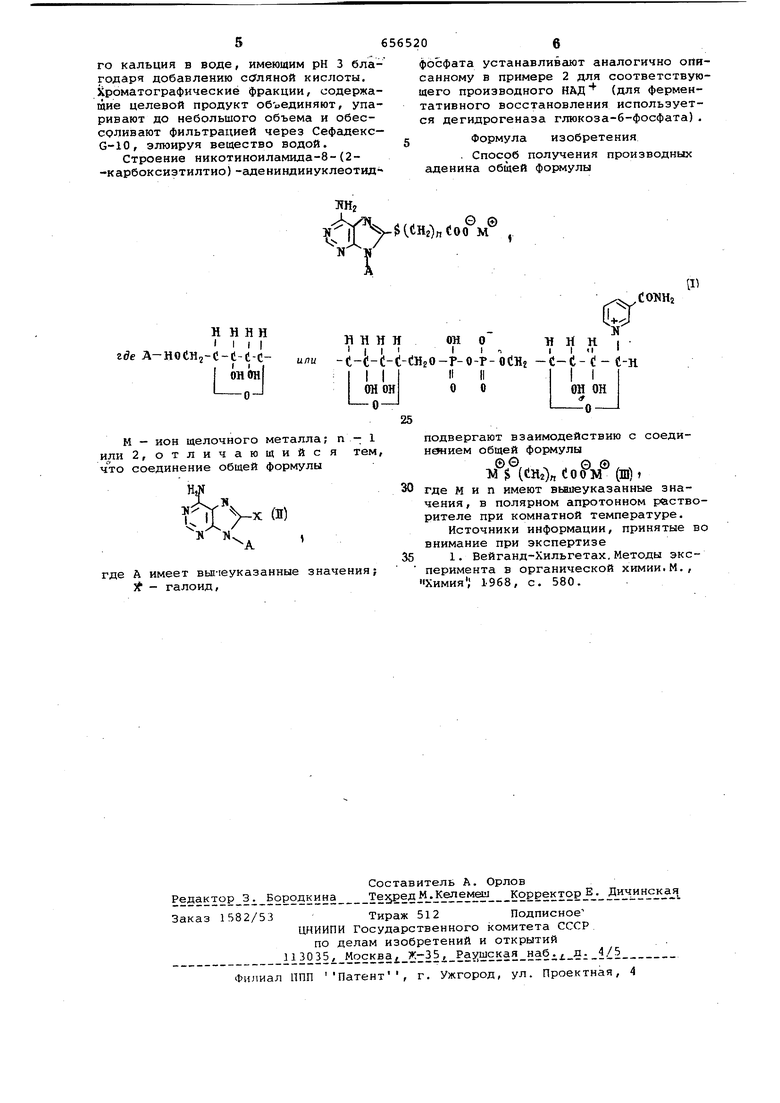
. Способ получения производных аденина общей формулы Н Н Н Н I I I II 0 I -r-flCHz -c-C-d- с-н 11I I 0он он Iо
М - ион щелочного металла; п -; 1 или 2, отличающийс я тем, что соединение общей формулы
где А имеет вшчеуказанные значения; 5 - галоид.
подвергают взаимодействию с соединежием общей формулы
3®$(«1Нг)„( (Ш) где М и п имеют вьниеуказанные значения , в полярном апротонном растворителе при комнатной температуре.
Источники информации, принятые во внимание при экспертизе
1. Вейганд-Хильгетах.Методы эксперимента в органической химии.М., Химия; 1968, с. 580.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения макромолекулярных производных аденина | 1977 |
|
SU704455A3 |
| Способ получения макромолекулярных производных аденина | 1975 |
|
SU691095A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГАММА-АМИДОВ ГЛУТАМОВОЙ КИСЛОТЫ | 1999 |
|
RU2395490C2 |
| Способ получения дегидропенициллинов | 1978 |
|
SU721004A3 |
| СПОСОБ ПОЛУЧЕНИЯ (2,8-H) АДЕНОЗИНА | 1980 |
|
SU892902A1 |
| Способ получения замещенных производных пенем-3-карбоновой кислоты или их сложных эфиров или их солей с щелочными металлами | 1983 |
|
SU1299512A3 |
| Способ получения факторов 1,2,3,4,5 тейхомицина @ и их солей | 1983 |
|
SU1318170A3 |
| АГЕНТЫ ДЛЯ КРОВЯНОГО ДЕПО ДЛЯ ДИАГНОСТИКИ С ПОМОЩЬЮ ЯДЕРНОГО МАГНИТНОГО РЕЗОНАНСА | 1999 |
|
RU2250765C2 |
| Способ получения [8-(6-аминогексил)-амино]-аденозин-5-дифосфата | 1980 |
|
SU883056A1 |
| Способ получения монофосфата нуклеозида | 1972 |
|
SU470114A3 |


Авторы
Даты
1979-04-05—Публикация
1976-07-15—Подача