(54) 4-АМИНО-4 -ДИФЕНИЛСУЛЬФОНАММОНИЕВАЯ СОЛЬ
6-МЕТИЛ-2,4-ДИОКСО-1,2,3,4-ТЕТРАГИДРОПИРИМИДИНА, И ПРОТИВОСУДОРОЖНОЙ АКТИВНОСТЬЮ
ОБЛАДАЮЩАЯ ПРОТИВОЛЕПРОЗНОЙ -дифенилсульфонаммониевой соли 6-метил-2,4-дирксо-1,2,3,4-тетрагидропиримидина . Пример 3. Смесь 2,48 г (0,01 моль) 4,4-диамикодифенилсульфона 1,26 г (0,01 моль) 6-метилурацила нагревают на масляной бане при в течение 10 мин, периодически взбалтывается, По охлаждении получаю кристаллы 4-амино-4 -дифенилсульфонамМониевой соли 6-метилурацила (выход количественный). I В эксперименте на мышах-самцах весом 18-22 г и крысах-самцах 180200 г изучены противосудорожные и психотропные свойства 4-амино-4 -дифенилсульфонаммониевой соли 6-метил-2,4-ДИОКСО-1,2,3,4-тетрагидропир мидина. Изучено влияние вещества на действие судорожных агентов, максимального электрошока (50мА, 0,2 сек, 50 ГЦ для мышей и 150мА, 0,2 сек, 50 ГЦ для крыс), коразола 110,мг/кг подкожно или 1%-ный раствор внутривенно, стрихнина (1,4 мг/кг),никотин (7, мг/кг), ареколина (25 мг/кг), на активность эпилептического очага, созданного аппликацией пенициллина на сенсемоторную кору головного мозга крыс (50 ед. в 0,001 мл) через вживленную канюлю, запись ЭЭГ через , вживленные в кору и гипокамп. Сравнение проводили с эталон ными противосудорожными фенобарбиталом и бензоналом. Изучено также влияние препарата н поведение животных и эффекты взаимодействия со стимуляторами и блокаторами медиаторных структур мозга: фенамином (6 мг/кг), апоморфином (10 мг/кг), Л-ДОФА (300 мг/кг), ареколином (25 мг/кг), резерпином (2,5 мг/кг). В случае обнаружения положительного против.осудорожного эффекта вычисляли средние эффективные дозы ЭД50 (по методу Литчфильда и Уилькоксона, 1949) . Обнаружено, что препарат обладает выраженной противосудорожной актив. ностью. Особенно четко она проявляет ся в тестах с электросудорожным припадком, В других тестах препарат эффективно защищает животных от тоническоЙ фазы припадка. По широте тера певтического действия он значительно превосходит эталонные противосудорож ные препараты. Прёпйрат повышс1ет пороговую дозу коразола на 30-60%, а при введении его животньм в дозе 110-80 мг/кг тонико-экстензорная фаза не развивается совершенно. При изучении пеницил линового эпилептического очага оказа лось , что препарат не предупреждает развитие очага, но ослабляет его ак тивность, уменьшая количество припа ков и межприступных разрядов на ЭЭГ на 40-60%. В этом он уступает дейст ВИЮ диазепама и фенобарбитала, которые в дозе 3 и 10 мг/кг соответственно полностью подавляют активность эпилептического очага. Исследуемый препарат не влияет на гиперкенез, вызванный холиномиметиками никотином и ареколином. В противоположность противосудорожным типа фенобарбитала, бензонала препарат не оказывает седативного действия на животных, не вызывает нарушения координации движений и мышечного расслабления. В больших дозах (45.0-500 мг/кг) он дает возбуждающий эффект, усиливает двигательную активность животных. В дозах, проявляющих противосудорожную активность, препарат потенцирует действие снотворных, продлевает стереотепию, вызванную фенамином, апоморфином,Л-ДОФА, ослабляет птоз и гипотермию, вызванную резерпином. Это сближает его с группой актидепресантов. Таким образом, действие предлагаемого препарата обеспечивает сочетание своеобразных противосудорожных и психотропных свойств, поэтому применение его в клинике для лечения больных эпилепсией с эффективными нарушениями перспективно. Противолепрозная активность проверялась набелых мышах, зараженных, микобактериями, взятыми от больного лепрой человека (штамм 166). Эти комплексы испытывают на 40 мышах., зараженных в пах и в ламку подкожно микобактериями штамма 166, выделенного от больных. ЖивотнЕлх лечат 4-амино-4 -дифенилсульфонаммониевой солью 6-метил-2,4-диоксо-1,2,3,4-тетрагидропиримидина перорально, начиная со дня заражения. В каждой серии по 20 мышей. В качестве контроля берут две группы мышей по 20 мышей в каждой, зараженных одновременно с опытными мышами тем же штаммом микобактерий, той же дозой подкожно в лапку и в пах. Контрольных мышей содержат в одинаковых условиях с опытными, но не получают каких-либо препаратов. В контрольной группе животных, зараженных в пах, к концу третьего месяца заражения в месте инокуляции сформировались подкожные лепромы размером 0,5 X 1 см, животных, зараженных подкожно в лапку, появилась эритематозностькожи и припухлость. При бактериоскопическом исследовании органов поражения животных обеих контрольных групп выявлено громадное количество микобактерий. В группе животньк, получавших исследуемый препарат, развитие лепром и поражение лап ни в однсм случае не наблюдалось. При бактериоскопическом исследовании ткани.из мест инокуляции в некоторых полях зрения отмечались единичные микобактерии, представляющие собой, по-видимому, остатки инокулированного материала. Результаты экспериментов показали что 4-амино-4 -дифенилсульфонаммониевая соль 6-метил-2,4-диоксо-1,2,3,4тетрагидропиримидина полностью задерживает размножение введенных микобактерии и развитие у мьвией клинических и бактериоскопических проявлений инфекционного процесса. Полученные данные позволяют рекомендовать его для клинического испытания. Острую токсичность определяют на белых мьадах-самцах весом 18-20 г и на наркотизированных кошках при введении препарата внутрь (зондом в желудок) в виде 10 и 20% водной взвеси
Токсичность 4-амино-4 -дифенилсульфонакмониевой соли 6-меТил-2,4-ДИОКСО-1,2,3,4-тетрагидропиримидина и ДЦС при введении внутрь белым мышам. Мышам препарат вводят в дозах 500j 1000, 2000, 3000, 4000, 5000 мг/кг. Каждую дозу испытывают на 10 животных, наблюдение проводят в течение 5 суток. Установлено, что через 20-25 мин после введения препарата мыпГам у всех животных отмечается легкое, постепенно усиливающееся возбуждение, через 90-120 мин мыши начинают метаться по клетке из стороны в сторону, вскакивать на задние лапки, координация движений нарушается, животные были возбуждены и на следующие сутки; на третьи сутки животные постепенно успокаиваются. Результаты исследований острой токсичнрсти препаратЪв на мышах приведены в табл. 1 ( рассчитывают по Литчфилду и Уилькоксону) . Таблица 1

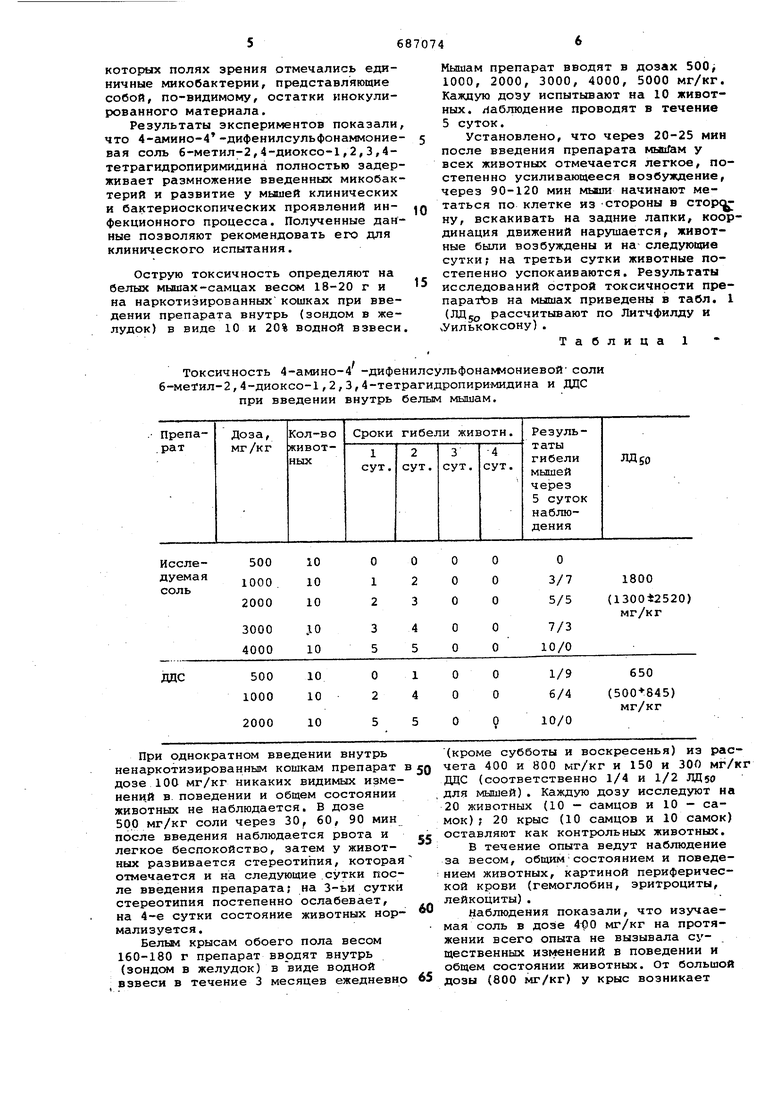


При однократном введении внутрь ненаркотизированным кошке м препарат дозе 100 мг/кг никаких видимых измененцй в. поведении и общем состоянии животных не наблюдается. В дозе 500 мг/кг соли через 30, 60, 90 мин после введения наблюдается рвота и легкое беспокойство, затем у животных развивается стереотипия, которая отмечается и на следующие сутки после введения препарата; на 3-ьи сутки стереотипия постепенно ослабевает, на 4-е сутки состояние животных нормализуется. Белым крысам обоего пола весом 160-180 г препарат вводят внутрь (зондс 1 в желудок) в виде водной взвеси в течение 3 месяцев ежедневн (кроме субботы и воскресенья) из расчета 400 и 800 мг/кг и 150 и 300 мг/кг ДЦС (соответственно 1/4 и 1/2 ЛД50 для мышей). Каждую дозу исследуют на 20 животных (10 - самцов и 10 - самок) ; 20 крыс (10 самцов и 10 самок) оставляют как контрольных животных. В течение опыта ведут наблюдение за весом, общимсостоянием и поведением животных, картиной периферической крови (гемоглобин, эритроциты, лейкоциты). Наблюдения показали, что изучаемая соль в дозе 4i30 мг/кг на протяжении всего опыта не вызывала существенных изменений в поведении и общем состоянии животных. От большой дозы (800 мг/кг) у крыс возникает
цианоз слизистых и кожного покрова лапок. На .3-Я день введения одна самка пала, на 4-й день пали еще 3 самки, после 8-го и 9-го дня введения препарата пало 5 самцов, на вскрытии обнаружили резкое увеличение надпочечников, кахексия. На 10Влияние изучаемой
Влияние соли и ДЦС на картину периферической крови Каквидно из данных табл. 2 живот ные, 11олучавшие соль вдозе 500 мг/к по привесу существенно не«отличаются от контрольных. Привес контрольных животных отличается от привеса крыссамок, получавших ДЦС в дозах 150 и 300 мг/кг. Эти животные отстают в весе от контрольных более, чем в 3 раза. Картина периферической крови при введении препаратов существенно не изменилась только У самок, получавших ДЦС: наблюдается небольшая тенденция к гипохромной анемии.
12-й день введения препарата животные этой группы стали более подвижными, состояние их постепенно улучшилось и в дальнейшем их поведение существенно не отличалось от поведения 5 контрольных животных (см. табл. 2 и 3) .
Таблица 2 соли и ДЦС на привес крыс.
Таблица После.окончания введения препаратов животные были забиты путем декапитации, часть сразу, часть через 2 недели. При микроскопическом исследовании крыс, получавших внутрь в течение трех месяцев соль э дозе 800 мг/кг и диаминодифенилсульфон в дозе 300 мг/кг, каких-либо изменений не обнаружено. При микроскопическом исследовании срезов головного мозга, гипофиза, легких, сердца, почек, желудка, селеэенки, костного моэг.а, гонад, надпочечников, окрашенных гематоксилинэозином, патологических изменений не обнаружено. В печени животных обеих групп йыявлены дистрофические изменения, -наиболее выраженные у животных, получавших диаминодифенилсульфон.
Таким образом, проведенные испытания показывают, что 4-амино-4 -дифенилсульфонаммониевая соль -б-метил-2,4-ДИОКСО-1,2,3,4-тетрагидрспиримидина значительно (в 5-7 раз) менее токсична, чем диаминодифенилсульфон при хроническом введении в эквито сических дозах, токсические язвления (уменьшение веса и патоморфологические изменения в печени) более выражены у животных, получавших ДЦС.
Формула изобретения . 4-АМИНО-4-дифенилсульфонаммониевая соль 6-метил-2,4-диоксо-1,2,3,4-тетрагидропиримидина :.
обладанлцая прЬтиволепрозной и противосудорожной активностью.
Источники информации, принятые во внимание при экспертизе
1,Машковский М.Д. Лекарственные средства. М., Медицина , 1977,
ч. 2, стр. 277.

Авторы
Даты
1979-09-25—Публикация
1978-01-06—Подача