Изобретение относится к новым произодным класса нуклеиновых кислот, общей ормулы:
Э)$UU
NH,7 t
Н
f
он
о « -О-К
0
о
I
К-сн, 1
Р-О-Т,
ила
в
I
ОН
обладающих противовирусной активностью.
В современной медицине известны ингибиторы вирусов, а именно производные . 2-ангидро-1-()-арабииофуранозил)-цитозина, обладающие вирицидной и цитоксической активностью. Данных о том, что упомянутые производные обладают ингибирующей активностью в отношений вирусов герпеса и адено. не имеется.
Известны также производные 2,2 -цик- лоцитидина формулы
$$$W
где , Н или НзРОз.
или Н2РОг.
или ОН, . СНз. или Hal, обладающие противоопухолевой и противовирусной активностью. Данных об активности в отношении вирусов герпеса и адено не имеется.
Целью изобретения является расширение ассортимента противовирусных препаратов, проявляющих ингибирующее действие в отношении вирусов герпеса и адено.
Поставленная цепь достигается путем синтеза производных дицитидин-5-пирофосфата, основанного на известной реакции конденсации нуклеозид-5-монофосфата в присутствии дициклогексилкарбодиимида.
Настоящий способ получения производных дицитидин-5-пирофосфата заключается в том. что безводный О ,2 ииклоцитидин-5-монофосфат или безводная пиридиниевая соль 2 3 N-триацетил а.раб и нофу ран ози л цитозин-5-монофосфат подвергаются конденсации а пиридине в присутствии дициклогексилкарбодиимида с последующим выделением целевого продукта путем обработки реакционной смеси
эфиром, водой, и хроматографическим разелением на колонке с ДЕАЕ-целлюлозой. П р и м е р 1. Р Р -ди{0,2 -циклоцитиин-5)-пирофосфат,
К навеске О ,2 -циклоцитидин-5-монофосфата (0,2 г., 0,65 ммоль), высушенной париванием с пиридином (3x20 мл), приливают 4 мл безводного пиридина, 5 мл иметилформамида и прибавляют дициклогексилкарбодиимид 0,9 г (4,3 ммоль). Реакционную смесь выдерживают 10 сут при комнатной температуре и выливают в эфир 0,5 л). Эфир декантируют. К остатку припивают 5 мл воды и экстрагируют эфиром. Водный слой отделяют и наносят на колонку с
ДЕАЕ-целлюлозой ДЕ-32 (АсО-, 1,6x45 см),
элюируют водой. Получают 0,075 г (39%) Р,
Р -ди(0 -, 2 -циклоцитидин-5 пирофосфата,
Т.пл.227°С(сразл,), Rf 0,19.
УФ: ЯНаО (нм) (к-10): 232 (14,7), 263
(16,4)..
П р и м е р 2. Р .Р -дЦарабинофуранозилцитозин-5)-пирофосфат. Пиридиниевую соль 2 3 Ы-триацетиларабинофуранозил цитозин-5-монофосфата 0,53 г (1 ммоль) высушивают упариванием с пиридином (3x20 мл), растворяют в 10 мл безводного пиридина, прибавляют 1,2 г (5.8 ммоль) дициклогексилкарбодиимида и оставляют на 10 дней при комнатной температуре. К реакционной смеси приливают 20мл воды, экстрагируют эфиром, «водный рйствор упаривают. Для удаления ацетильных групп остаток обрабатывают водным аммиаком (25% , 72
ч при 20°С). Упаривают, наносят на колонку
с ДЕАЕ-сефадексом А-25 (НСОз, 1.8x30 см)
и хроматогафируют в линейном градиенте
концентрации триэтиламмонийбикарбоната (1л 0.05 М - 1 л 0.2 М ТЕАБ). Водный раствор упаривают с пиридином и пропускают через колонку с ионообменной смолой Дауэкса 50x12 (Н -форма). Получают 0.26 г (83%) (араб1/1нофуранозилцитозин-5 )-пирофосфата. Т.пл, 208°С (с разл.). Rf0.12
УФ: Я Н20(нм)( 275(17.5). Антигерпетическое действие производных дицитидин-5-пирофосфата оценивалось по снижению цитопатогенной активности вируса, репродуцированного в присутствии соединений в культуре ткани фибробластов куриных эморионов (ФЭК). Активность отношении аденовируса 3 типа также оценивалась по снижению цитопатогенной ,эктивности вируса, репродуцированного в культуре ткани пассируемых кожно-мышечных клеток эмбриона человек.ч в присутствии соединений.
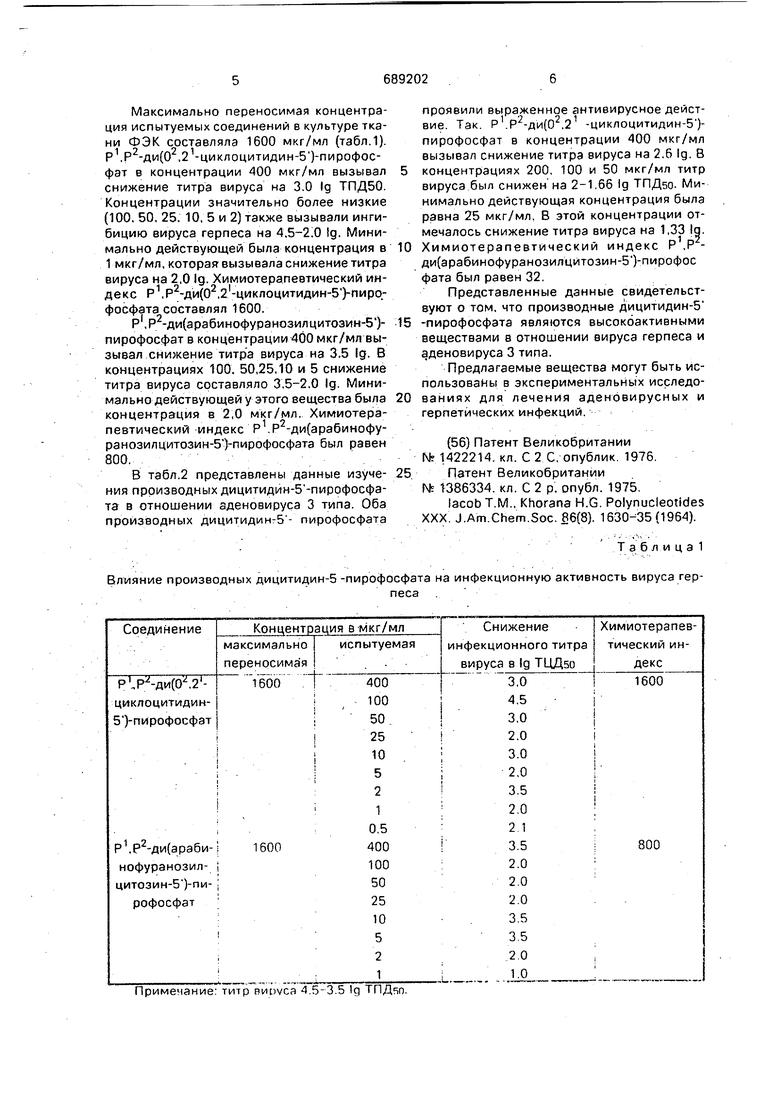
Максимально переносимая концентрация испытуемых соединений в культуре ткани ФЭК составляла 1600 мкг/мл (табл.1). (0,2 -циклоцитидин-5)-пирофосфат в концентрации 400 мкг/мл вызывал снижение титра вируса на 3.0 Ig ТПД50. Концентрации значительно более низкие (100. 50, 25. 10, 5 и 2) также вызывали ингибицию вируса герпеса на 4.5-2;0 tg. Минимально действующей была концентрация в 1 мкг/мл, которая вызывала снижение титра вируса на 2.0 Ig. Химиотерапевтический индекс (0.2-циклоцитидин-5)-пирофосфата составлял 1600.
Р ,Р -ди(арабинофуранозилцитоэин-5)пирофосфат в концентрации400 мкг/мл вызьгеал снижение титра вируса на 3.5 Ig. В концентрациях 100. 50,25,10 и 5 снижение титра вируса составляло 3.5-2.0 Ig. Минимально действующей у этого вещества была концентрация в 2,0 мкг/мл. Химиотерапевтический индекс (арабинофуранозилцитозин-5)-пирофосфата был равен 800.
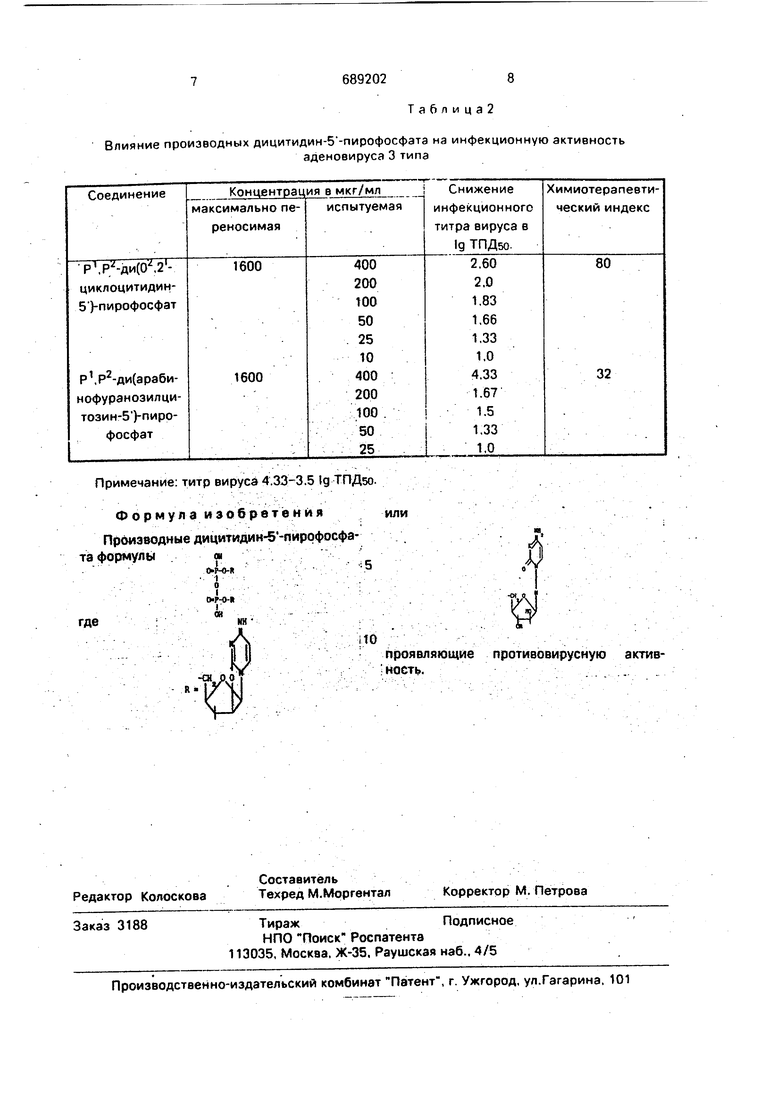
В табл.2 представлены данные изучения производных дицитидин-5-пирофосфатэ в отношении аденовируса 3 типа. Оба производных дицитидинтБ- пирофосфата
Влияние производных дицитидин-5 -пирофосфата на инфекционную активность вируса герпроявили выраженное антивирусное действие. Так. Р .Р -ди(0.2 -циклоцитидин-5)пирофосфат в концентрации 400 мкг/мл вызывал снижение титра вируса на 2.6 Ig. 8 концентрациях 200. 100 и 50 мкг/мл титр вируса был снижен на 2-1.66 Ig ТПДзо. Минимально действующая концентрация была равна 25 мкг/мл, В этой концентрации отмечалось снижение титра вируса на 1.33 |q. Химиотерапевтический индекс Р .Р ди(арабинофуранозилцИтозин-5)-пирофос фата был равен 32.
Представленные данные свидетельствуют о том. что производные дицитидин-5 -пирофосфата являются высокоактивными веществами а отношении вируса герпеса и аденовируса 3 типа.
Предлагаемые вещества могут быть использованы в экспериментальных исследованиях для лечения аденовирусных и герпетических инфекций.
(56) Патент Великобритании Nf1422214.кл.С 2 С. опублик. 1976.
Патент Великобритании Ne 1386334. кл. С 2 р. опубл. 1975.
1зсоЬ Т.М.. Khorana H.G. Polynucleotides XXX. J.Am.Chem.Soc. 86(8). (1964).
Т а б ли ц а 1 песа . 
| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения симметричных пирофосфатов | 1980 |
|
SU888502A1 |
| Производные 3-(2-метил-4-тиазолил)- или 3-(5-этоксикарбонил-2-фурил) хромонов, обладающие противовирусной активностью | 1986 |
|
SU1415716A1 |
| ЛУПАНОВЫЕ А-СЕКОТРИТЕРПЕНОИДЫ, ПРОЯВЛЯЮЩИЕ ПРОТИВОВИРУСНУЮ АКТИВНОСТЬ | 2011 |
|
RU2470003C1 |
| 2-О-Сульфонаты метил 5-О-бензил-3-фтор-3-дезокси-Д-арабинозы в качестве промежуточных продуктов в синтезе биологически активных 3 @ -фтор-3 @ -дезоксирибонуклеозидов | 1987 |
|
SU1521739A1 |
| СПОСОБ ПОЛУЧЕНИЯ ДЕЗОКСИНУКЛЕОЗИД-5'-ТРИФОСФАТОВ | 1994 |
|
RU2080325C1 |
| L-НУКЛЕОЗИДЫ, ОБЛАДАЮЩИЕ АНТИ-HBV ИЛИ АНТИ-EBV АКТИВНОСТЬЮ, СПОСОБ ИНГИБИРОВАНИЯ HBV ИЛИ EBV ИНФЕКЦИИ | 1995 |
|
RU2171809C2 |
| 1-О-Ацетил-2,5-ди-О-бензоил-3-фтор-3-дезокси-Д-рибофураноза в качестве промежуточного продукта в синтезе биологически активных 3 @ -фтор-3 @ -дезоксирибонуклеозидов | 1987 |
|
SU1507764A1 |
| ВЕЩЕСТВО, ОБЛАДАЮЩЕЕ ПРОТИВОГЕРПЕСНЫМ ДЕЙСТВИЕМ | 1990 |
|
RU2032674C1 |
| ДИМЕРНОЕ ПРОИЗВОДНОЕ НЕТРОПСИНА-15-ЛИЗ-БИС-НЕТРОПСИН- И КОМБИНАЦИИ НА ЕГО ОСНОВЕ, ОБЛАДАЮЩИЕ АНТИГЕРПЕТИЧЕСКОЙ АКТИВНОСТЬЮ | 2004 |
|
RU2265610C1 |
| Новые пиримидиновые ингибиторы репликации аденовируса человека | 2016 |
|
RU2628456C1 |

Примечание: титр вируса 4.5-3.5 Ig ТПДяп.
Влияние производных дицитидин-5-пирофосфата на инфекционную активность
аденовируса 3 типа
Та6лица2
Примечание: титр вируса 4.33-3.5 Ig ТГТДзо.
Формул а изобретенияили
Производные дицитидин-5-пирофосфата формулы
где
мипроявляющие
противовирусную активi HOCTI.
Авторы
Даты
1993-10-30—Публикация
1978-07-10—Подача