где X - водород, 3-метокси, 3,5-дибром6 - метил - 3-.изопропил « группа -СН СН-СН СН-;
R водород, фенил, «-тол,ил, «афтил, оксиметил;
Y водород, метил, этил, бензил, я-тол;ил, л-хлорфевил.
Однако недостаточная чистота оптически активного соединения (невысокая величина удельного вращения хризантемовой ашслоты, полученной гидролизом алкилхризаитемата) вызывает необходимость дальнейшего усовершенствования данного способа.
Цель изобретения - повышение качества целевого продукта - оптически активного алкилхризантемата.
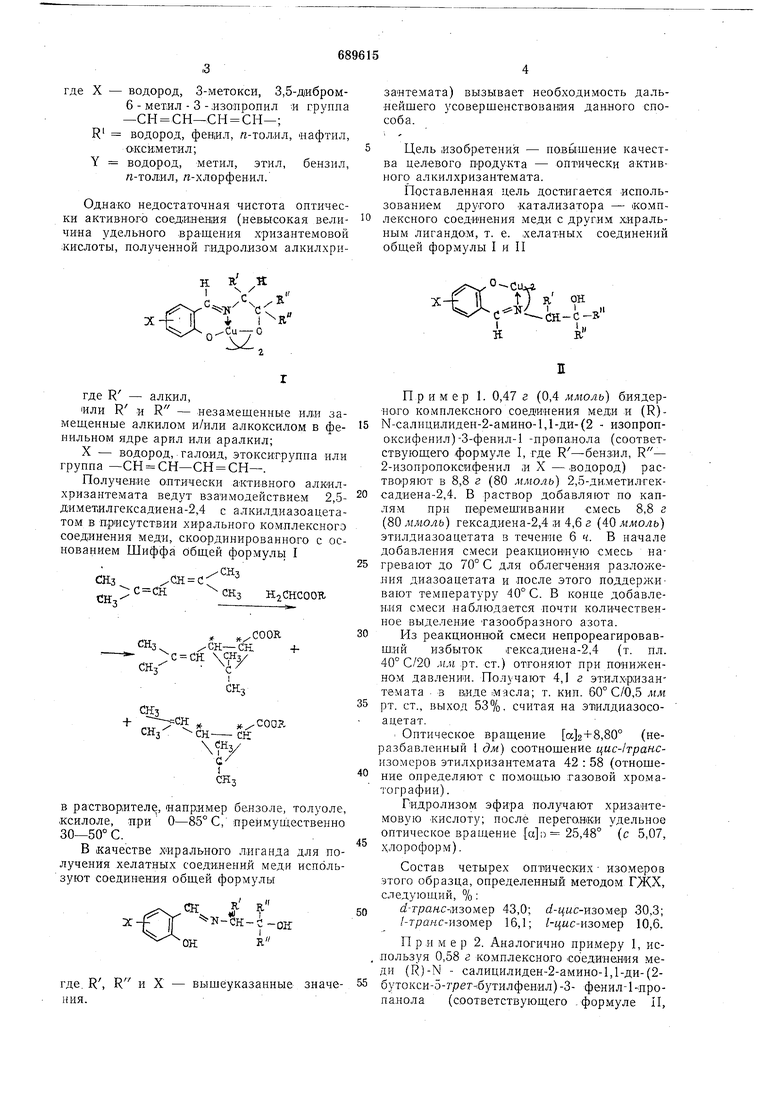
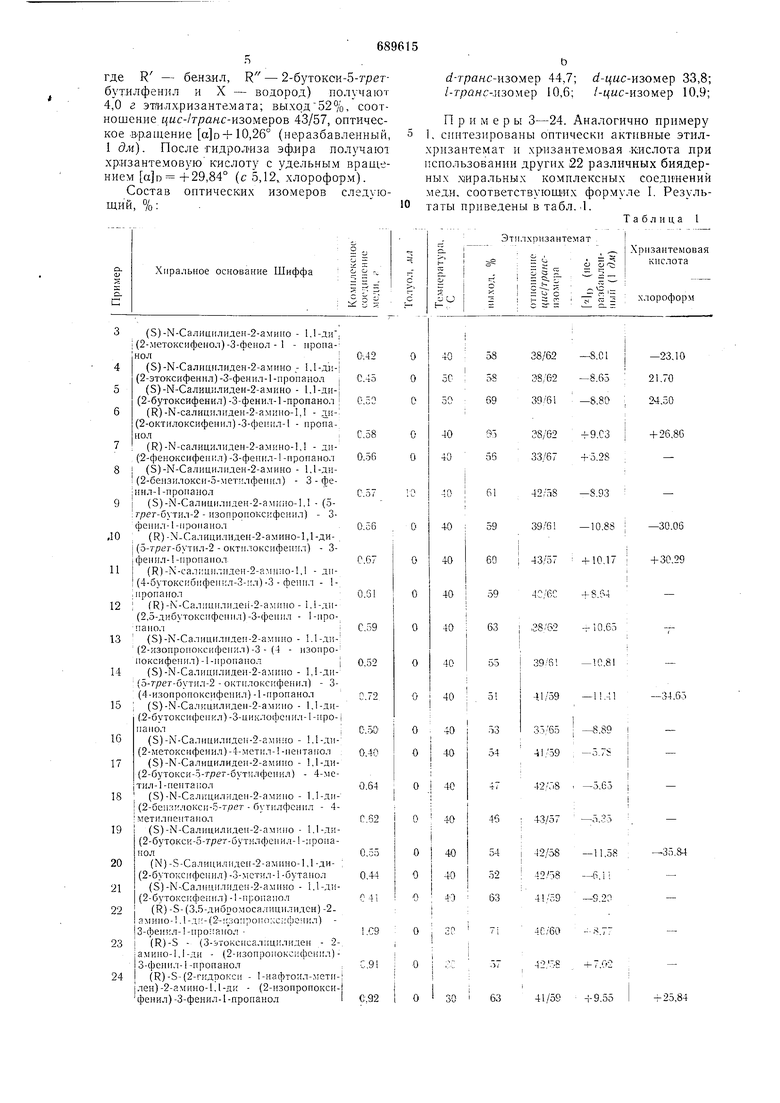
Поставленная цель достигается использованием другого катализатора - комплексного соединения меди с другим х;иральным лигандом, т. е. .хелатных соединений общей формулы I и II
ff я L L скгде R - алкил,
или R и R - незамещенные или замещенные алкилом и/или алкоксилом в фенильном ядре арил или аралкил;
X - водород, галоид, этоксигруппа или группа -СН СН-СН СН-.
Получение оптически активного алкилхризантемата ведут взаимодействием 2,5диметилгексадиена-2,4 с алкилдиазоацетатом в присутствии хирального комплексного соединения меди, скоординированного с основанием Шиффа общей формуль I
СНз/СН
;С HjCHCOOBсн.
COOR
«-х/СН-СК,
сн снз/
с
СН-,
/.соог.
ск
в растворителе, например бензоле, толуоле, ксилоле, при О-85° С, преимущественно 30-50° С.
В качестве хирального лиганда для получения хелатных соединений меди используют соединения общей формулы
сн f
N- H-i-oH R
где. R, R и X - вышеуказанные значения.
Пример 1. 0,47 г (0,4 ммолъ биядерно,го комплексного соединения меди и (R)Н-салицилиден-2-амино-1,1-ди-(2 - изопропоксифенил)-3-фенил-1 -пропанола (соответствующего формуле I, где R-бензил, 2-изопропоксифенил и X - водород) растворяют в 8,8 г (80 льиолб) 2,5-ди,метилгексадиена-2,4. В раствор добавляют по каплям при перемешивании смесь 8,8 г (80 мжоль гексадиена-2,4 и 4,6 г (40 лшоль) этилдиазоацетата в течение б ч. В начале добавления смеси реакииониую смесь нагревают до 70° С для облегчения разложения диазоацетата и после этого поддерживают темнературу 40° С. В конце добавления смеси наблюдается почти количественное выделение газообразного азота.
Из реакционной смеси непрореагировавший избыток |Гексадиена-2,4 (т. пл. 40° С/20 лш рт. ст.) отгоняют при пониженном давлении. Получают 4,1 г этилхризан темата в виде :масла; т. кип. 60° С/0,5 лш рт. ст., выход 53%. считая на эт1илдиазосоацетат.
Оптическое вращение ,80° (неразбавленный 1 дм,} соотнощение цис-1трансизомеров этилхризантемата 42 : 58 (отношение определяют с помощью газовой хроматографии).
Гидролизом эфира получают хризантемовую кислоту; после перегонки удельное оптическое вращение ) 25,48° (с 5,07, .хлороформ).
Состав четырех оптических- изомеров этого образца, определенный методом ГЖХ, следующий, %:
й -г/ аяс-изомер 43,0; с/-г ыс-изомер 30,3;
/-т/зш-гс-изомер 16,1; /-1{мс-изомер 10,6.
П р и м е р 2. Аналогично примеру 1, ис. пользуя 0,58 г комплексного соединения меди (R)-N - салицилиден-2-амино-1,1-ди-(2бутокси-5-г/ ег-1бутилфенил)-3- фенил-1-лропанола (соответствующего , формуле И,
где R - бензил, R - 2-бутокои-5-гретбутилфенил и X - водород) получают 4,0 г эт/илхризантемата; выход52%, соотношение 1{ис-/г/ анс-изомеров 43/57, оптическое .Вр.ап1ение +10,26° (неразбавленный, 1 дм). После гидролиза эфлра получают хризантемовую кислоту с удельным вращением -f 29,84° (с 5,12,. хлороформ).
Состав оптических изомеров следующий, %:
й -гранс-изомер 44,7; d-цыс-изомер 33,8; /-гронс-лзомер 10,6; /-цис-изомер 10,9;
П р и меры 3-24. Аналогично примеру 1, сннтезированы оптически активные этилхризантемат и хрнзантемовая .кислота ири использовании других 22 различных биядерных х|иральных комплексных соединений меди, соответствующих формуле I. Результаты приведены в табл. Л.
Таблица 1

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения оптически активных алкилхризантемата | 1976 |
|
SU719491A3 |
| Способ рацемизации оптически активных галогенангидридов 2,2-диметил-3 /1-алкенил/-циклопропан-1-карбоновых кислот | 1974 |
|
SU722479A3 |
| ОПТИЧЕСКИ АКТИВНЫЕ СОЕДИНЕНИЯ БИСОКСАЗОЛИНА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ПРИМЕНЕНИЕ | 2004 |
|
RU2326874C2 |
| ИНСЕКТИЦИД | 1973 |
|
SU398018A1 |
| Способ получения (+) или (-) производных триазолилового спирта | 1981 |
|
SU1582987A3 |
| Инсектицидная композиция | 1975 |
|
SU572171A3 |
| РОСТРЕГУЛИРУЮЩАЯ КОМПОЗИЦИЯ | 1989 |
|
RU2017423C1 |
| Способ получения 2,2-диметил-3-(2'-метил)-1-пропенил-1,3-трансциклопропан-1-карбоновой кислоты и ее алкиловых эфиров | 1973 |
|
SU929007A3 |
| БИСЦИКЛОПЕНТАДИЕНИЛДИЕНОВЫЕ КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ, СПОСОБ ПОЛИМЕРИЗАЦИИ ОЛЕФИНОВ | 1995 |
|
RU2135508C1 |
| Инсектицидная композиция | 1973 |
|
SU664529A3 |


Авторы
Даты
1979-09-30—Публикация
1974-02-13—Подача