1
Изобретение относится к химическим средствам защиты растений, а именно к инсектоакарицидонематоцидным средствам на основе производных бискарбамоилсульфида,
Известно использование несимметричных Ы-замещенных бискарба -;оилсульфидных соединений в качестве инсектицидов 1,
Прототипом изобретения является инсектицидное средство, действующим началом которого является бис-(3,4-диметилфенил-Ы-метилкарбамоил)-сульфид 2,
Однако известные соединения недостаточно активны при низких концентрациях .
Целью изобретения является изыскание новых инсектоакарицидонематоцидных средств, -обладающих высокой биологической активностью.
Это достигается использованием инсектоакарицидонематоцидного средства, активным веществом которого является производное бискарбамоилсульфида формулы
R-O-CO-NR-S-NR-OCOR i (О
где R и R - метил,
R-( - нафтил, диметилфенил, грут:мегде Rj - водород,
R,,
тил, Н метилтио, 2-метилтиоизопропил или группа , где радикал А вместе с атомом углерода образуют 1,4--дитиан, 3,5 , 5-триметилтиазолидиь: .-4-ОН
R2 - пропарги.п, 2 ,2-Д метил-2 , 3 дигкрробензофуран, нафтил, иэопропилфенил, трет.бутилфенил, нитрофенил, 5,6,7,8-тетрагидронафтил, мет;,.лтио 3-метилфенил, 4-метоксикарбокила.-.шно-3-изопропилфенил, триметилфенил, 2,4-дикитро-6-втор,бутилфенил, Ы,Ы-диметиламинофенил, 4-формила.мино-3-метилфенил, 4- (2 , 7-цис )-октадиенилфенил, 2-хлор-4-изопропилфенил, нонилфенил, додецилфени.п, дифеНИЛ, 2-метокси-4-аллилфенил, феноксифенил, 1, 4-дитиоланфенил, 1,4-диоксоланфенил, трет.бутоксифенил, пропаргилоксифенил, 1,3,5-трити&н или группа-N c; , где Кэ - водород, метил, метилтио, R4. - фенилкарбонил, 2-метилтиоизопропил, этоксикарбонил, цианоэтилтио, диметилкарбамоил, или группа -H-CJ f. где радикал А вместе с атомом углерода образуют 1,4-дитиан, 1 , 3 , 5-тритиан. Содержание активного вещества в средстве .от 0,5 до 95 вес,%, осталь ное добавка. Предлагаемые соединения получают по схеме акц,ептор он т о FC-N-S-N-cr U OH -SS i ai i - -K OCN-S-N-CF , 9 акцептор О U Т1 О R,OC-N-S-N-CF -R,OHJ ii l U OC-N-5-N-CO где R, R , R , R2 имеют вышеуказанные значения. Пример 1, Получение N- 2-метилтио-2-метилпропиональдегид-О- (Ы-метилкарбс 1ил) -оксим метилтиоацетальдегид-0-(N-метилкарбомоил -оксим -сульфида. А, В полипропиленовый реакционны аппарат, вводят 80 г (4,0 моль) фто ристого водорода в 1800 мл толуола охлаждают до температуры -40°С, по каплям и с перемешиванием добавляют 228 г (4,0 моль) метилиэоцианата в течение 20 мин. Затем реакционную смесь нагревают до и выдержива.ю при этой температуре в течение 1 ч Затем добавляют 206 г (2 моль)свеж перегнанной двуххлористой ляют в нее 246 г (4,4 моль) пириди при температуре от -20 до п°с.Пос ле перемешивания в течение 2 ч при -10°С и в течение 16 ч при комнатной температуре реакционную смесь разбавляют 500 мл воды. Далее TQлуольный слой промывают 3 порциями по 500 мл воды, высушивают и перегоняют с получением 244 г (66%) бл -(К-метил-Ы-фторкарбомиламино)-сульфида, т. кип. 55-57°С/ /0,25 мм рт.ст., т. пл. 40-41°С. Найдено,%: С 26,19; Н 3,20; N 14,79 C H FgNjOg Вычислено,%: С 26,09; Н 3,28; N 15,21. В. В раствор 0,714 г 1-метилтио ацетальдоксима и 1,36 г бис-(N-меЗаместители в формуле I R
Н -SCH Н СН,
СНз СН5
99-101
сн,
164-165
сн
170-171
сн. ил-Ы-фторкарбомиламино)-сульфида 15 мл диоксана по каплям добавлят 0,687 г триэтиламина. После выержки раствора в течение 20 ч его разбавляют водой и экстрагируют этилацетатом. Органический экстракт промывают водой, сушат сульфатом магния и концентрируют в вакууме с получением 1,0 г 1-метилтиоацетальдегид-О- N-метил-N-(N-метил-N-фторформиламиносульфенил)-карбамоил -оксима, который кристаллизуют из смеси изопропилового эфира с Этилацетатом, т.пл. 102-104С. Найдено,%: С 31,67; Н 4,69; N 15,34 Вычислено,%: С 31,22; Н 4,49; N 15,60. С. В раствор 2,69 г 1-метилтиоацетальдегид-О- N-мeтил-N-(N-фторформиламиносульфенил)-карбамоил -оксима и 1,3 г 2-метилтио-2-метилпропионалкоксима в 50 мл диоксана при перемешивании добавляют постепенно 1,01 г триэтиламина. По истечении 48 ч выдержки реакционную смесь разбавляют водой и экстрагируют этилацетатом. Экстракт промывают водой, сушат и концентрируют Полученный продукт N- 2-метилтио-2-метилпропиональдегид-0- (Ы-мети;-1карбомоил)-оксшд -N-1-метилтиоацетальдегид-0-(N-метилкарбомоил)-оксимсульфид, кристаллизуют из изопропилового эфира. Получают 1,87 г сухого вещества, т пл, 99-101С. найдено,% С 37,68; Н 5,72; N 14,51 C iH25LN40 S Вьлчислено,%: С 37,68; Н. 5,80; N 14,65. В табл. 1 приведены температуры плавления соединений формулы Г, Таблица 1
Заместители в формуле 1 -снг-€ сн 0 S НзС-С ЫSCHjснз$-с-сн кCH3-C NSCH3CH3-C Nсн1СНз)г
Ш(СНз)г
-14:- C-CHi NCCHgCH S
I j CH,
CH3-C NSCH3
NOz
СНз-С Ы- N C-COC2H5
SCHj
SCHj
CH3-C N I
ix
ЗСНз
CH5-C NSCH3
SCH3
Про,:1;сгг1.жение тдб.п, ).
fl
R
Т , ш-j . С
II
СНт
CH
CH,
11 9 - J 2 0
CH.
СИ. 96-96,8 141-144 масло 88-90 108-110
Продолжение табл. 1

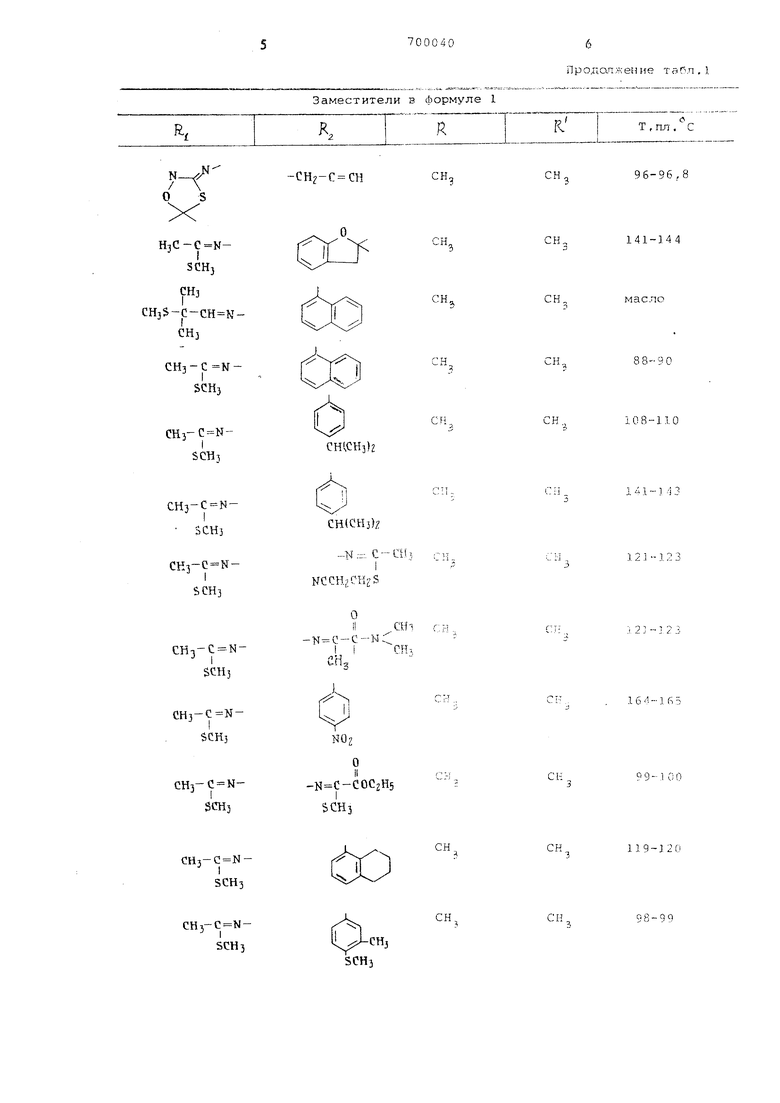




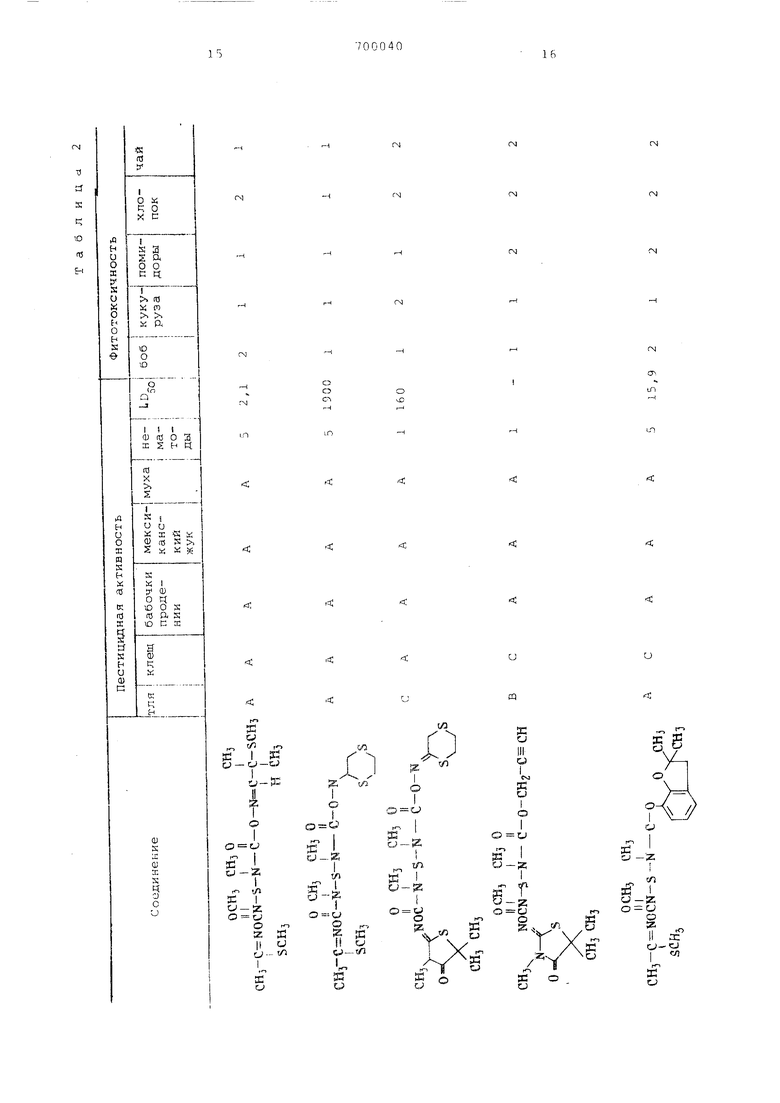

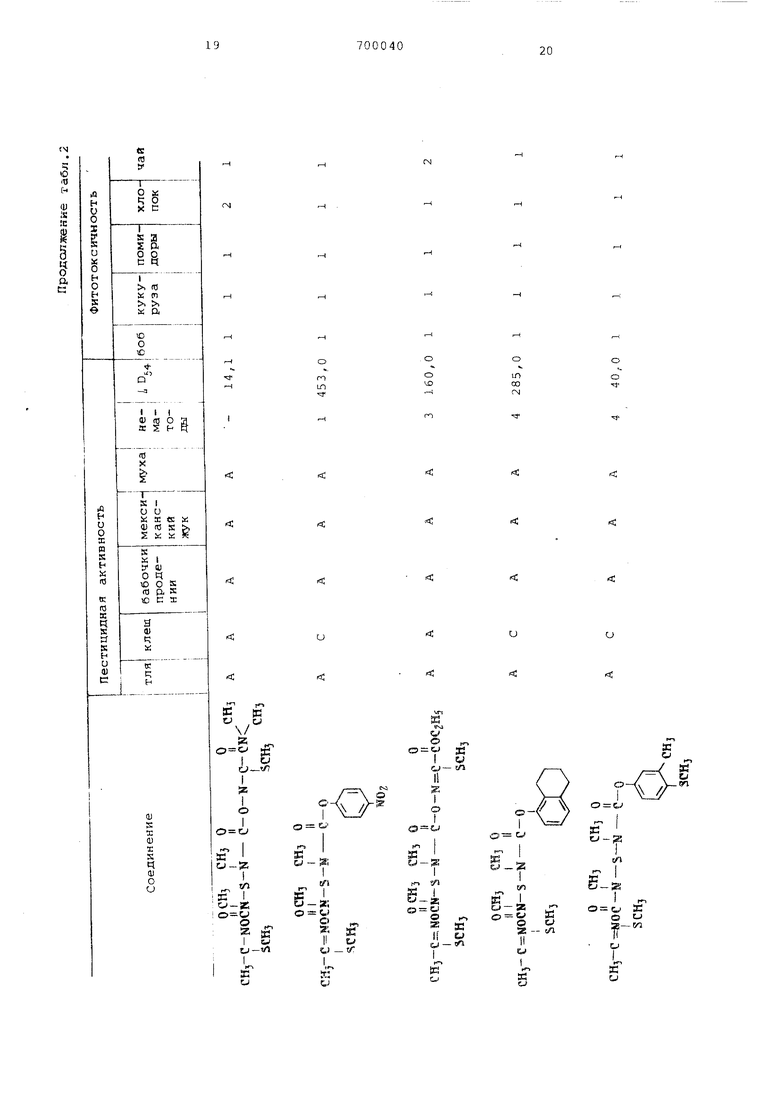
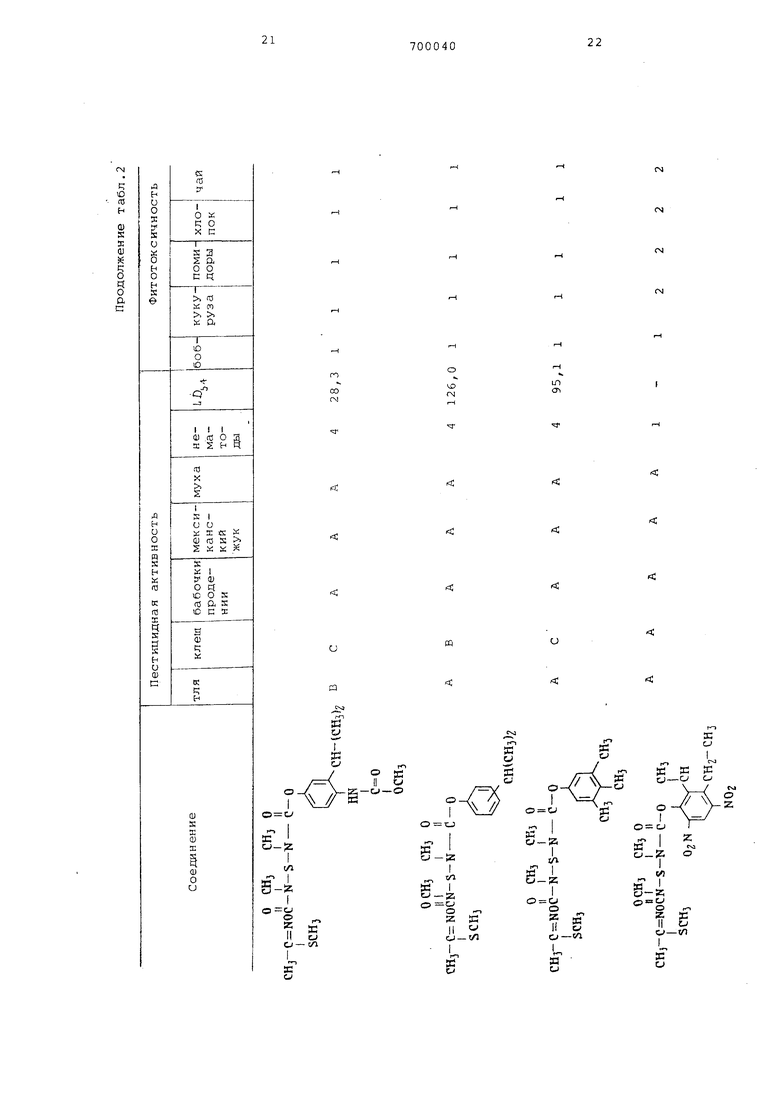





| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения -замещенного бис- КАРбАМОилСульфидА | 1977 |
|
SU799655A3 |
| Способ получения N-замещенного бис-карбамоилсульфида | 1977 |
|
SU895285A3 |
| Способ получения карбаматсульфенилкарбамоилфторидных соединений | 1978 |
|
SU944501A3 |
| ИНСЕКТОАКАРИЦИД | 1973 |
|
SU391768A1 |
| СИНЕРГИЧЕСКАЯ ДОБАВКА ПРИ ПРИГОТОВЛЕНИИ ИНСЕКТО-АКАРИЦИДНОГО ПРЕПАРАТА12 | 1972 |
|
SU346828A1 |
| СПОСОБ БОРЬБЫ С ВРЕДНЫМИ НАСЕКОМЫМИ И КЛЕЩАМИ | 1966 |
|
SU225109A1 |
| Способ получения производных -зАМЕщЕННыХ биС-КАРбАМОил-СульфидНыХ СОЕдиНЕНий | 1977 |
|
SU799656A3 |
| Способ борьбы с насекомыми | 1973 |
|
SU668563A3 |
| ПРОИЗВОДНЫЕ 1-АРИЛПИРРОЛОВ, ИНСЕКТОАКАРИЦИДОНЕМАТОЦИДНАЯ КОМПОЗИЦИЯ И СПОСОБ БОРЬБЫ С НАСЕКОМЫМИ | 1991 |
|
RU2092479C1 |
| Инсектоакарицидонематоцидная композиция | 1975 |
|
SU747399A3 |

СН1СНз)2
снгс сн
-сь
S чо
Продол же н и е т абл . 1
Ьыса; ра/хэнны;
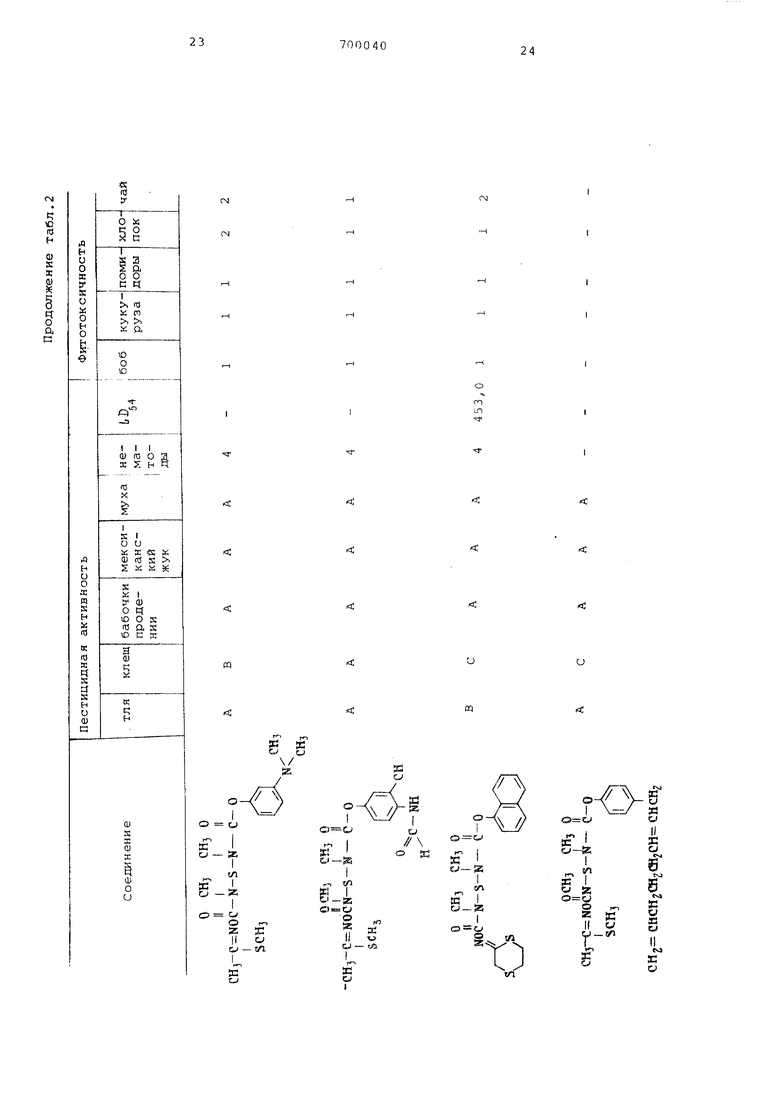
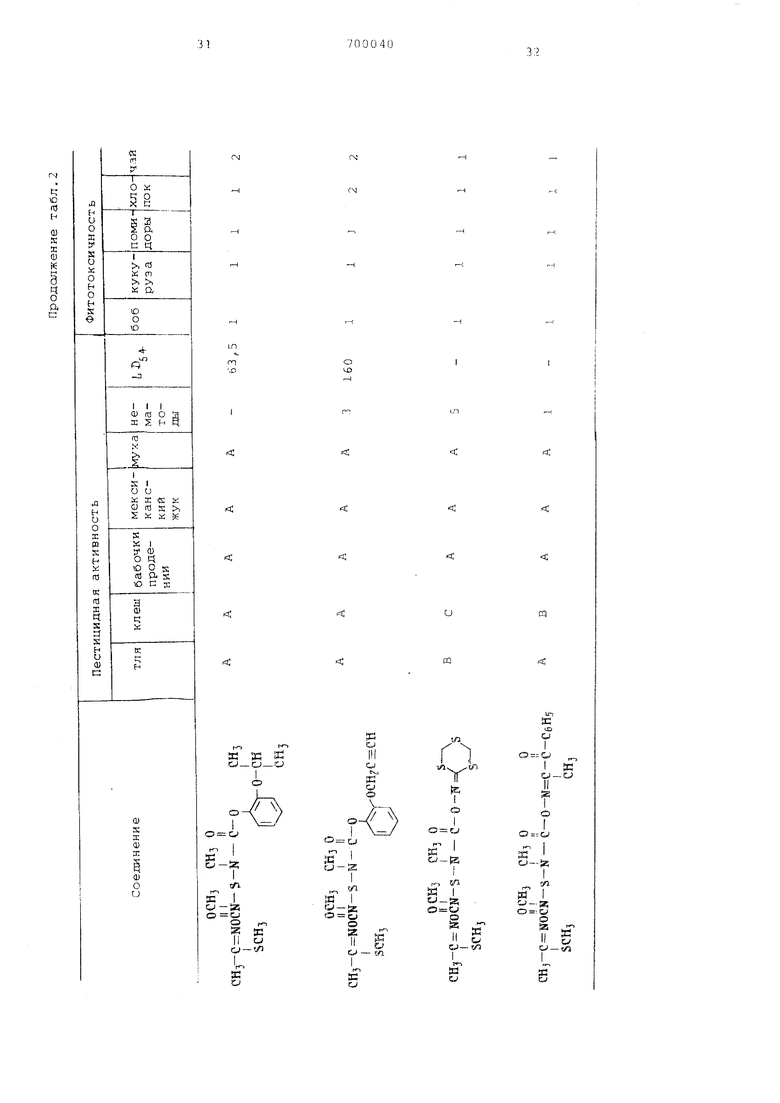
nOMI-OTOi MOrO t:Oi 80 ± 5°F (26,67 ±2,78°С) и относительной влажности 0 ±5%. Композиции испытываемых соединений готовят разбавлением исходных суспензий водой, получают суспензии которые содержат 500 ч. испытываемо го соединения на млн вес.ч. готовой композиции. Находящиеся в горшках растения боба стандартной высоты и возраста опрыскивают 100-110 мл ком тозиции испытываемого соединения.ил смесью вода-ацетон-эмульгатор, кото рая не содержит испытываемых соедин ний, используют распылительную наса ку Де Вильбисса, опрыскивают под да лением 0,6031 кг/см в течение 25 с до стенании жидкости. После сушки спаренные листья отделяют друг от др га и каждый из листьев помещают в чашку Петри (9 см); снабженную прокладкой из влажной фильтровальной бумаги. В каждую из чашек сажают по 5 личинок и чашки закрывают. Личинки выдерживают при 80 i5°F {26,67± ±2,77°С) в течение 3 дней. Затем подсчитывают количество погибших личино Пример 5.Испытания на мухах. В качестве подопытных насекомых используют комнатную муху Musca dom&stica U в возрасте взрослых особей от 4 до 6 дней, выращенную в условиях при температуре и влажноети 80 ± 5°F(26,67 t 2,77°С) и 5015%. Мух индивидуально иммобилизуют, самцов и самок и помещают в клетку, которая снабжена стандартной пищевой сеткой приблизительно 127 мм в диаметре, перевернутой над поверхностью покрытой оберточной бумагой. Композиции с iиспытываемыми соединениями готовят разбавлением исходной суспензии 10%-ным (по весу) раствором сахара, получают суспензию, которая содержит 500 ч испытываемого соединения на млн вес.ч. готовой композиции. По 10 композиции испытываемого соединения наносят а ватный тампон сечением 6,45 см . Эту приманку вводят и устанавливают в центре бумаги под пищевой сеткой перед допуском к ней испытуемых мух. Находящиеся Б клетке мухи имеют свободный доступ к приманке для питания в течение 24 ч при 80l5°F (26,67 ± 2,77°С) и относительной влажности50 Приме р6. Испытания на клещах В качестве подопытных животных используют взрослые особи клещика двупятнистого Tetran chus urticackocti и насекомых на личиночно стадии раз вития, выращенных на растениях боба Tenderg-hun при 80±5°F (26,67±77°С и относительной влажности 50±5%. За раженные листья помещают на первичные листья двух растений боба высотой 15,24-20,32 см, которые выращивают в глиняном горшке размером 63,5мм 150-200 клещей переносят с отрезанных листьев на свежие растения в течение 24 ч. Находящиеся в горшках растения опрыскивают 100-110 мл при готовленной композиции испытываемого соединения или смесью вода-ацетонэмульгатор, которая не содержит испытываемого соединения. Используют распылительную насадку де Вильбисса, опрыскивают под давлением 2,81 кг/см в течение 25 сек до стекания жидкости. После опрыскивания растения выдерживают при 80±5°F(26,67 t2,77°С) и относительной влажности 50±5% в течение 6 дней, после чего производят подсчет гибели насекомых по степени их подвижности. Затем огуречные ростки извлекают из горшков и с их корней удаляют почву, что позволяет визуально определить число наростов. Результаты проведенных испытаний приведены в табл. 2. Пестицидную активность соединений в указанной дозировке в отношении тли, клещей, бабочки продении, мексиканского жука и ксяинатной мухи выражают следующим образом: А - поражение 70%; В - поражение от 50 до 70%; С - поражение менее чем 50%. Определение активности против нематод эффективность воздействия оценивают следующим образом: 1 - очень большое число наростов, равное числу наростов у необработанных растений; 2 - умеренное число наростов; 3- незначительное число наростов; 4- небольшое число наростов; 5 отсутствие наростов, полное уничтожение нематод. Пример 7. Испытания на фитотоксичность. Готовят растворы аналогично вы- ше описанной методике, концентрация испытываемых соединений составляет 2 500 ч испытываемого соединения на млн вес.ч. готовой композиции. Растения опрыскивают, обработанные и контрольные растени выдерживают в течение 1 ч для просушивания истьев, затем помещают в оранжерею. Через 10 Дней определяют степень овреждения листьев. 1 - отсутствие заметного поврежения; 5 - гибель растения; 2,3 и 4- ромежуточные степени повреждения, онкретная величина которых зависит т числа поврежденных участков и тепени повреждения листьев. Пример 8. Испытания на токичность. Некоторые из соединений испытыват для определения их пероральной оксичности в отношении млекопитаюих животных по обычным методикам. Испытания проводили на крысах. езультаты испытаний выражают в иллиграммах на килограмм живого веа (LBj-o). В табл. 2 пpивcдeнl:J реультаты испытаний.
TS
и s к, ю
re
н
о сз
ел
-
1Л
и
CJ
О VD
ГVD (N Гч
VO
С
;
и
о
ю
:
t)
з: о
-vl
S
I
г
с
J
о
S
CJ О1
г
0 11
00
CN
;
и
и
1Л (T.
) OJ
;
о
ю
И у
да с
Т g
-CJ -о
W
и
и
о cj
1Л
i
I
о
К с
Z
и
СУ - 1/1
в
и
5
я
CJ
II К u
с I
-i
ъ
- f
ГчЗ 3S I
5
y И
f-4
ic и
2
g
i
u )sr)
rII
E
a
и
ю
и
и йг
«Г
5-i
о, л
к V S
LJ
В
Ч
а::
C.i - tS/
ЭТ
I
tJ - К
г
C5 t
W
О
е
2 IE;
S, | а
в
с t- - «п
Ь -sn
0Wс;
R D It) H
0)
к a:
t;
о
§
га
о
1Л
о
и
и
0 CJ
CJ-1Л
%:
CJ
CJ
t; ю ПЗ
н ш
X
я
0)
i
ч о U
с
и;
0 и
B-i
.-r
J
о
И
щ
п
о о
I к
Y U -U
II
te
f о
i
о I
- I
S к
tJ0-S;
I
i
rl bl
СП
I
a I tj-a
CJ-Й
g
f «
к
п g
IIи
II CJ CJ-1ЭТ
CJ -аа
о- Л
I
И о
В табл. 3 приведены результаты испытаний на биолсгическую активность предлагаемых соединений формулы I, где R R CHj и известных соединений.
Летальная доза выражена в мг/кг. В табл. 3 приведены результаты испытаний на биологическую активность
(Предлагаемые)
сн.
I
си,5С-9-Nз-V
з сн.
NS-1
H C-C-NSCHj
(Известные)
СИCHaSC-с N- ОН,, S-C-C--M- л
ill 3 I , ч Формула изобретения Инсектоакарицидонематоцидное сре ство , содержащее производные бискар бамоилсульфида как активное вещество и добавку, выбранную из группы носитель, растворитель, .диспергатор эмульгатор, отличающееся тем, что, с целью усиления ,инсектоакарицидонематоцидной активности она содержит в качестве производног бискарбамоилсульфида соединение общей формулы R-O-CO-NR-S-NR-OCOR, где R и R - метил; R - нафтил, диметилфенил, группа -N-Cvp, 3 водород, метил, R .-метилтио, 2-метилтиоизопропил, ил группа , где радикал А вместе с атомом углерода образуют 1,4-дитиан, 3,5,5-триметилтиазолидин-4-ОН пропаргил, 2 ,2-диметил-2 , 3-дигидробензофуран, нафтил, изопропилфенил, трет.бутилфенил, нитрофенил, 5,6,7,8-тетрагидронафтил, метил тио-3-метилфенил, 4-метоксикарбониламино-3-изопропилфенил, триметилфенил, 2,4-динитро-6-втор.бутилфенил, N,N-диметиламинофенил, 4-формиламино-3-метилфенил, 4-(2,7-цис)-октадиенилфенил, 2-хлор-4-изопропилфвни
предлагаемых соединений Формулы 1 где R R CHj и известных, соединений. Летальная фаза выражена в мг/кг.
Таким образом предлагаемые соединения обладают хорошей активностью .
Таблица 3
50
2,1
19
50
1,1
/D
7500
10}
не испыт. конилф2иил, додедилфенил, дифенил, 2-метокси- 4- алл; Лфенил , феноксифенил, 1 , 4 дктиоланфеннл ; 1 4-дкоксоланфе НИЛ, трет.бутоксифенил, пропаргилокгде Rj -водород/ метил, л 1 - феннлкарбонил, 2-метилтиоизопрспил, этоксикарбонил, циакоэтилтис, диметилкарбамоил, или группа - N - Cj , где радикал А вместе с атомом углерода образуют 1,4-дитиан, 1,3 5 тритиан, в количестве от 0,5 до 95 вес.%, остальное добавка, Приоритет по признакам: 01.12.75 при R и R - метил; R - группа -N -Сч , где Rj-водород, метил, R4 метилтио, 2-метилтиоизопропил или группа - N - CJX , где радикал А вместе с атомом углерода образуют 1,4-дитиан, 3,5,5-триметилтиазолидин-4-ОН;R пропаргил, 2,2-Диметил-2,3-дигидробензофуран, нафтил, изопропилфенил, трет.бутилфенил, нитрофенил, 5,6,7,8-тетрагидронафтил, метил тио-3 -мет илфенил, 4-методе емка рбониламино-3-изопропилфенил, триметилФенил ,. 2 , 4-динитро-6-втор.бутил1;:сНИЛ, Ы,Ы-диметиламинофеяи.п, 4-фор-ммламино-3-метилфенил, 4-формиламино-3-метилфенил, 4- ( 2 , 7-цис ) -окта-диенилфенил;
Кз водород, метил, метилтио
или группа - N - с
где R А -2-меТшизопропил , этоксикйрбонилр цианоэтилтио, диметилкарбамоил или группа - N СJV , где радикал А вместе с атомом углерода образуют 1.3.5-трн тиан.
04„11,76 при R - нафтил, диметилфенил; R 2. 2-хлор-4-изопропилфенил, нонилфенил, додецилфенил, дифенил, 2-метокси-4-аллилфенил, феноксифенил, 1 , 4-дитиоланфенил, 1,4-диоксоланфенил трет,бутоксифенил,
пропаргилоксифенил или группа р
-N-cCn с где Кд - фенилкарбонил.
АИсточники информации, принятые во внимание при экспертизе
1,Патент США № 3920830,
кл. 424-300, опублик. 18Л1Л5.
2,Патент США № 3794733,
кл. 424.300, опублик. 1974 (прототип) .
Авторы
Даты
1979-11-25—Публикация
1976-12-01—Подача