Смесь 50 г (0,188 моль) бис (1,-метилсульфонилокси)-бензола и: 1 л метанола нагревают до до тех пор, пока раствор не станет гомогенным, затем охлаждают до , добавляют по каплям, перемешивая раствор гидроокиси калия, 24,7 г (0,03 моль в 100 мл 10%-ного водного метанола при температуре . После перемешивания при комнатной температуре около 4 дней образуется обильное количество осадка (калий метилсульфонат) .и его удаляют фильтрацией.
Фильтрат концентрируют в вакууме с получением смеси масла и твердого вещества. Осадок помещают в 500 мл воды, экстрагируют один раз 200 мл толуола для удаления нейтральных прдуктов, и затем подкисляют до рН менее 1 50 мл концентрированной соляной кислоты, после чего образуется осадок 3-(метилсульфонилокси)фенола Осадок отфильтровывают, промывают вдой и сушат на воздухе, получая 15,8 г (45%) продукта, т,пл, 78-80° , Фильтрат экстрагируют 3 раза по 100 мл порциями метиленхлорида. Экстракты объединяют, сушат над сульфатом натрия и концентрируют в вакуум получая дополнительно 11,5 г (33%) 3-(метилсульфонилокси)фенола, т.пл. 77-80°С.
Аналогично примеру А получают слдующие соединения:
Т.пл.С
Соединение
4-(Метилсульфонилокси J 75-76 фенол
2-(Метилсульфонилокси )фенол
105/0,1 мм 4- (н-Бутилсульфонилокси)фенол 155/0,2 мм 3- (ХлорметилсульфонилЬкси)фенол 64,8-67,0 4-(Этилсульфонилокси)фенол Масло
2,4-Дихлор-5-(метилсульфонилокси )фенол
136,5-137,5 2,5-Дихлор-4-(метилсульфонилокси )фенол 123,8-130,9 3-(3 -Хлорпропилсульфонилокси)фенол Масло 4-(Бензилсульфонилокси)фенол 75,5-76,,5 3-(Вензилсульфонилокси)фенол 89-90 4-(п-Толилсульфонилокси)фенол 94-95,5 4-(4 -Хлорбензилсульфонилокси)фенол 99-101 4-(о-Толилсульфонилокси)фенол 155/0,12 мм 3-(4 -Нитробензилсульфонилокси)фенол 126-128,5 3-(4 -Фторбензилсульфонилокси)фенол 78,5-79,5 4-(4 -Бромбензилсульфонилокси)фенол 105-107,9 3-(2 -Нитробен илсульфонилокси)фенол Масло
3-(Метилсульфонилокси) -5-Метилфенол
Масло 3-(3 -Нитробензилсульфонилокси)фенол
Масло 3-(2 4 -Диметилбензилсульфонилокси)
79,5-81,0
фенол
3 (Изопропилсульфонилокси)фенол-
Пример Б, Получение 3-(3 , 4 -дихлорбензилсульфонилокси)-фенола
Смесь 200 мл 48%-ного водного раствора бромистоводородной кислоты и 18,8 г (0,056 моль) 3-(3 ,4 -дихлорбензилсульфонилокси)анизола перемешивают с обратным холодильником в течение 7 дней при температуре . Раствор охлаждают до 0-10°С и подщелачивают до рН 12 300 мл 30%-ной гидроокиси натрия. Щелочной раствор экстрагируют 200 мл бензола для удаления нейтральных продуктов и затем подкисляют до рН менее 1 10 мл концентрированной соляной кислоты. Водный раствор экстрагируют три раза 150 4Л порциями хлороформа. Хлороформные экстракты объединяют, сушат над сульфатом натрия и концентрируют в вакууме, получая 5,9 г (33%) 3-(3 ,4 -дихлорбензилсульфонилокси) фенола в виде кристаллического твердого вещества; т.пл. 107-109 , 5С .
Пример 1. Получение 0-этил-0- 4-(метилсульфонилокси)фенил -5-н-пропилтиофосфата (соединение 1).
В раствор 3,5 г (0,019 моль) п-(метилсульфонилокси)-фенола в 150 м безводного ацетонитрила добавляют порциями 0,81 г (0,02 моль) гидрида натрия (57% в минезральном масле) при температуре 5°С. Реакционную смесь перемешивают до тех пор, пока не прекратится выделение водорода, и затем добавляют по каплям, перемешивая при температуре 5°С и в течение 10 мин 3,75 г (0,019 моль) хлорида 0-этил-5-н-пропилтиофосфата. Смесь перемешивают два дня при комнатной температуре, фильтруют для удаления хлорида натрия и минерального масла и концентрируют в вакууме, получая 6,1 г (93%) продукта в виде желтого масла.
Пример 2. Получение 0-этил-0- (метилсульфонилокси)фенил}-S-H-пропилтиофосфата (соединение 2).
Дисперсию гидрида натрия - 0,90 г (0,0376 моль) в 20 мл ацетонитрила добавляют порциями к перемешиваемому раствору 7,08 г (0,0376 моль) 2-(метилсульфонилокси) -фенола в 100 мл ацетонитрила при комнатной температуре. Смесь перемешивают до тех пор, пока не прекратится выделение газа, ,и затем добавляют по каплям при комнатной температуре 7,62 г (0,0367 моль) хлорида и-этил-5-н-пропилтиофосфата. Смесь перемешивают в течение ночи, затем концентрируют в
вакууме. Осадок извлекают 100 мл бензола, один раз промывают водой, суша над сульфатом натрия и концентрируют в вакууме, получая целевой продукт в виде масла. Масло очищают хроматографией на силикагеле, используя в качестве элюента смесь бутилацетата и гептана, получая 7,0 г (52%) целевого продукта в виде бледно-желтого масла.
Пример 3. Получение О-этил-0- 3-(метилсульфонилокси)фенил -S-н-пропилтиофосфата (соединение 4)
Дисперсию гидрида натрия - 0,74 г (0,03 моль) в 20 мл ацетонитрила добавляют порциями в перемешиваемый раствор 5,3 г (0,028 моль) 3-(метилсульфонилокси) -фенила в 100 мл ацетонитрила при комнатной температуре. Смесь перемешивают до тех пор, пока не прекратится выделение газа, затем добавляют по каплям при комнатной температуре 5,7 г (0,028 моль) хлорида 0-этил-5-н-пропилтиофосфата. Смесь перемешивают в течение ночи и затем концентрируют в вакууме. Осадок извлекают 100 мл бензола, промывают один раз водой, сушат над сульфатом натрия и концентрируют в вакууме, получая 8,1 г (91%) целевого продукта в виде масла. Масло очищают хроматографией, как описано в примере 2 .
ЯМР (СОСе}),сГ:г 0,97 (ЗН, t, CHj) 1,42 (ЗН, t, СНз), 1,75 (2Н, т, CHjCH CH), 2,92 (2Н, т, ЗСН} ) 3,10 (ЗН, S, SOjj, СНз). 4-35 (2Н, т, OCHjiCH), 7,1-7,6 (4Н, m, ароматический) .
Пример 4. Получение 0-этил-0- {3-(метилсульфонилокси)фенил -S-изобутилтиофосфата (соединение 6).
Раствор 4,09 г (0,022 моль) 3-(метилсульфонилокси)-фенола в 30 мл ацетонитрила добавляют по каплям в перемешиваемую суспензию 0,57 г (0,024 моль) гидрида натрия в 120 мл ацетонитрила при 22-26°С. Раствор нагревают до до тех пор, пока не прекратится выделение газа, и затем по каплям добавляют 5,1 г (0,024 моль) хлорида 0-этил-5-изобутилтиофосфата. Смесь перемешивают в течение ночи, затем фильтруют для удаления хлорида натрия. Фильтрат концентрируют в вакууме. Осадок извлекают 100 мл толуола, промывают дважды порциями по 100 мл воды, сушат над сульфатом натрия, фильтруют через 10 г силикагеля и концентрируют в вакууме, получая 4,1 г (51%) целевого продукта в виде бледно-желтого масла.
ЯМР (CDCgj } ,(f 1,02 6Н, d, СН(СНз)гЗ , 1,43 (ЗН, t, ), 1.92 IH, m, SCH2CH(CHj)j3 , 2,88
CHi
(2H, m, SCH CH ), 3,18 (3H, S,
CHj
SOjCHi), 4,35 (2H, m, ), 6,957,60 (iiH, m, ароматич.). Пример 5. Получение 0-этил-0- З-(метилсульфонилокси)фенил}-S-втор- бутилтиофосфата (соединение 8) Это соединение получают и очищают согласно описанному в примере 4.
5,1 г (0,024 моль) хлорида 0-этйл-S-втор-бутилтиофосфата используют в качестве фосфорилирующегоагента, получая 4,1 г (51%) целевого продукта в виде желтого масла.
ЯМР (СОСез),б 0,92 (ЗН, т,
СН-СН), 1,15-1,90 .8Н, т, 5СН(СНз.)г, и OCHjCHi, cf 3,12 (ЗН, S, ЗОгСНз), 3,40 LIH, m, SCH (СИ j) ,. 4,30 (2Н, m, OCHjCH), 7,10-7,60 CfH, m, ароматический).
Пример 6. Получение О- З-(хлорметилсульфонилокси)фенил -0-этил-S-н-пропилтиофосфата (соединение 9) .
Раствор 4,0 г (0,018 моль) 3-(хлорметилсульфонилокси)-фенола в 50 мл ацетонитрила добавляют по каплям в 0,47 г (0,020 моль) гидрида натрия в 150 мл толуола. Смесь перемешивают до тех пор, пока больше не
прекратится выделение водорода, и затем добавляют по каплям 4,01 г (0,020 моль) хлорида 0-этил-5-н-пропилтиофосфата.
Раствор перемешивают в течение ночи при комнатной температуре и затем фильтруют для удаления хлорида натрия. Фильтрат промывают и концентрируют , как описано в примере 4, получая 4,1 г (53%) сырого целевого продукта, который далее очищают хроматографически и получают чистый продукт.
ЯМР (СОСЕз). cf-0,98 (ЗН, t,CHj), 1,42 (ЗН, t, CHj) , 1,61 (2Н, m, SCHaCHgCHj), 2,90 (2Н, m, SCHgCH CH,),
4,30 (2H, m, ), 4,80 Т2Н, S, ), 7,05-7,55 (4H, ароматич.).
Пример 7. Получение О- 3-(метилсульфонилокси)-фенил -0-метил-S-н-пропилтиофосфата (соединение 12);
Это соединение получают и очищают согласно описанному в примере 4, используя 4,42 г (0,024 моль) 3-{метилсульфонилокси) -фенола, 0,62 г . (0,026 моль) гидрида натрия и 4,87 г (0,026 моль) хлорида 0-метил-5-н-пропилтиофосфата. При этом получают 3,9 г (49%) целевого продукта в виде светло-зеленого масла.
ЯМР ( ) ,93 (ЗН, t,CHjCHj), 1,69 (2Н, т, SCH CHjCHj), 2,85 (2Н,
т, ), 3,82 (ЗН, d, OCHj), 6,95-7,50 (4Н, ароматич.).
Пример 8. Получение 0-этил-0- 4-(метилсульфонилокси)-фенил -S-н-пропилдитиофосфата (соединение 13) .
Это соединение получают и очищают согласно описанному в примере 4, используя 2,54 г (0,0135 моль) 4-(метилсульфонилокси)-фенола, 0,35 г (0,015 моль) гидрида натрия и 3,3 г (0,015 моль) хлорида 0-этил-5-н--пропилтиофосфата. При этом получают 2,4 г (48%) целевого продукта в виде зеленого масла, после хроматогрс1фии.
ЯМР (СОСГ. ), f 0,98 (ЗН, t,: СН, СНд), 1,37 ГЗН, t, ОСНгСН), 1,70 . (2Н, т, SCH CHgCH), 2,83 (2Н, т, SCH2,CH2), 3,10 (ЗН, S, SOjCHj), 4,20 (2Н, т, ), 7,12 (4Н, S, ароматич.).
П р и м е р 9. Получение (бензилсульфонилокси)фенил -0 этил--S-н-пропилтиофосфата (соединение 16
К раствору 7,5 г (0,03 моль) п- (бенэилсульфонилокси)-фенола в 40 м безводного ацетонитрила добавляют диперсию 0,95 г (0,03 моль.) гидрида натрия (без минерального масла) в 20 мл ацетонитрила при температуре 25-4-0°С. Затем добавляют по каплям 6,4 г (0,03 моль) хлорида О-этил-S-н-пропилтиофосфата и полученную смесь выдерживают при температуре 45°С около 18 ч, после чего ее фильтруют в вакууме для удаления хлорида натрия. Фильтрат разбавляют 100 мл бензола и 50 мл гексана и промывают трижды водой. Органическую фазу сушат над сульфатом натрия, фильтруют через слой силикагеля и концентрируют в вакууме. Получают 9,2 г (73%) целевого продукта в виде бледно-желтого масла. Масло далее очищают на силикагеле хроматографией с использованием в качестве растворителя смеси бутилацетата и гептана.
Пример 10. Получение О- З-(бензилсульфонилокси)фенил -0-этил-S-н-пропилтиофосфата (соединение 17
Гидрид натрия, 0,64 г (9,027 моль в 20 мл ацетонитрила, добавляют порциями в перемешиваемый раствор 6,3 г (0,025 моль) 3-(бензилсульфонилокси)-фенола в 50 мл ацетонитрила при комнатной температуре 30-40°С. Смесь нагревают до 6ОС, выдерживают при этой температуре до тех пор, noKci не прекратится выделение водорода, за тем охлаждают до ЗО-С, добавляют по каплям при температуре 30-4О С хлорид 0-этил-5-н-пропилтиофосфата - б ,, 3 г (О, 026 моль). Смесь перемешиЕ1ают в течение ночи при температуре ЗО-С, затем фильтруют через короткую колонку силикагеля и фильтрат концентрируют в вакууме. Получают 10 г (96%) целевого продукта в виде темно-янTcipHoro масла. Масло далее очищается с помощью хроматографии, как описано в примере 9. Получают 6,0 г чистого продукта в виде бледно-желтого масла
Пример 11. Получение 0-. 4-(4-метилбензилсульфонилокси)
фенилЗ-S-н-пропилтиофосфата (соединение 18).
Это соединение получают и очищают согласно описанному в примере 10, используя 7,2 г (0,027 моль) 4-(4-метилбензилсульфонилокси)-фенола. Получают 11,5 г (98%) сырого целевого продукта в виде желтого масла и 7,0 г (60%) чистого целевого продукта в виде бледно-желтого масла после хроматографии.
Пример 12, Получение 0-этил-0- 4-(о-толилсульфонилокси)-фенил -S-н-пропилтиофосфата (соединение 20
Дисперсию гидрида натрия - 0,61 г (0,025 моль) в 20 лл ацетонитриладобавляют порциями в раствор 6,2 г (0,02 моль) 4-(о-толилфенилокси)-фенола в 100 мл ацетонитрила. Смесь перемешивают до тех пор, пока не прекратится выделение водорода. Затем добавляют по каплям при комнатной температуре хлорид 0-этил-5-н-пропилтиофосфата, 4,7 г (0,023 моль). Раствор перемешивают при комнаткой температуре около 2 дней, фильтруют для удаления хлорида натрия и концентрируют в вакууме. Получают 10,2 г (10,2%) целевого продукта в виде коричневого масла, которое далее очищают с помощью хроматографии, как описано в примере 9.
ЯМР (CDCt,, ) , d 0,95 (ЗН, t , СН, 1,37 (СН, t, СН) , 1,68 (2Н, m
t, СН) , 1,68 ), 2,88 (2Н, SCH,
CHg СН
СН, СН„СН, )
m
(2H/m, OCHoCHj), 4, , 4,2«
(2Н, S, m, ОСНоСН
R 5 , 6,98-7,50 (9Н, apoмaтич.. СН.
Пример 13. Получение ( З ,4 -дихлорбензилсульфонилокси) фенил -О-этил-S-н-пропилтиофосфата (соединение 21).
Суспензию 0,44 г (0,018 моль) гид рида натрия в 30 мл ацетонитрила добавляют порциями в перемешиваемый раствор 5,3 г (0,017 моль) 3-(3 , 4 -дихлорбензилсульфонилокси) фенола в 120 мл ацетонитрила при комнатной температуре. Когда прекратится выделение газа, добавляют по каплям 3,34 г (0,016 моль) хлорида 0-этил-5-н-пропилтиофосфата. Смесь перемешивают при комнатной температуре около 2 дней, фильтруют для удаления хлорида натрия и концентрируют в вакууме. Получают 7,3 г (91%) целевого продукта в виде желтого масла. Часть масла (4,0 г) далее очищают хроматографией, как описано в примере 9, получая 1,7 г чистого продукта.
Пример 14. Получение 0-этил-0- 3-(3 -нитробензолсульфонилокси) фенил -S-н-пропилтиофосфата (соединение 26) .
Раствор 5,1 г (0,017 моль) 3-(3 -нитробензилсульфонилокси)фенола в 30 мл ацетонитрила добавляют по каплям в перемешиваемую суспензию 0,46 (0,019 моль) гидрида натрия в 120 мл ацетонитрила при температуре 21-26°С Смесь нагревают до 45°С и вьщерживаю до тех пор, пока не прекратится выде ление газа. Затем добавляют по кап лям при температуре Зб-37°С 3,86 г (0,019 моль) хлорида 0-этил-5-н-про пилтиофосфата в 30 мл ацетонитрила. Смесь перемешивают в течение ночи при комнатной температуре и фильтруют для удаления хлорида натрия. Фильтрат концентрируют в вакууме. П лучают 7,3 г (91%) продукта в виде темного масла, которое далее очищаю как описано в примере 9, получая 1,-8 г чистого целевого продукта. ЯМР (CDCEj ) , cf 0,95 (ЗН, t, CHjCH), 1,38 (ЗН, t, OCHnCHj), 1,6 (2H, m, CH,j CHoCHj) , 2,82 (2H, m, SCHjCH), 4,28 (2H, m, ), 6,8-8,8 (8Н, m, ароматич.). Пример 15. Получение (бензилсульфонилокси)-фенил -0-метил-5-н-пропилтиофосфата (соединение 28) . Это соединение получают и очищаю согласно описанному в примере 14, и пользуя 3,7 г (0,015 моль) 4-(бензи сульфонилокси) -фенола , 0,39 г (0,016 моль) гидрида натрия и 3,09 (0,016 моль) хлорида 0-метил-5-н-пропилтиофосфата. Получают 5,01 г (83%) целевого продукта в виде темного масла. Часть масла далее очищают с помощью хроматографии, как описано в примере 9. Получают продукт в виде светло-желтого масла. ЯМР (СОСЕз ), (f 0,95 (ЗН, t, CH2.CHj), 1,61 (2Н, m, SCH CHnCHj), 2,85 (2Н, m, ), 3,88 (ЗН, d, OCHj), 7,00 (k, myароматич.), 7,67 (5Н, m, ароматич.). Аналогично получают следующие сое динения: 0-этил-О- З-(метилсульфонилокси) фенил -S-H-бутилтиофосфата (соединение 10) . Выход 40%; ЯМР (СОСЦ ), ( - 0,98 (ЗН, t, СНзСН), 1,50 (ЗН, t, ) , 1,25-2,10 CiH, m, ,СНз) , 3,07 (2Н, M, SCH.CH 4,35 (2Н, m, ), 7,10-7,60 CtH, m, ароматич.). О- 4-(этилсульфонилокси)фенил -О-этил-S-н-пропилтиофосфата (соединение 11) . Выход 49%; ЯМР (CDCe), d 0,98 (ЗН, t, ), 1,20-1,98 (SH, m, SCHjCHgCHj, OCHjCHj, SOjCH CHj), 2,90 (2H, m, ), 3,18 (2H, q, SOj., ), 4,30 (2H, m, OCHgCH,) 7,17 (4H, S, ароматич.). 0-этил-О- з-(метилсульфонилокси)-5-метилфенил -S-н-пропилтиофосфат (соединение 14). Выход 96%; ЯМР ( ) , cf г 0,98 (ЗН, t, СНз), 1,43 (ЗН, t, GCHgCHj) 1,71 (2Н, m, SCH-jCHgCHj) , 2,35 (ЗИ, S, CHg), 2,85 (2Н, т, ), 4,27 (2Н, т, OCHjjCHj), 7,03 (ЗН, т, ароматич . ) . (3 -хлорпропилсульфонилокси) фенил -0-этил-5-н-пропилтиофосфат (соединение 15). Выход 19%; ЯМР (COCe.,),rf г 0,98 (ЗН, t, ), 1,40 (ЗН, t.OCHjCHj), 1,72 (2Н, т, SCHjCHjCH,), 2,50 (2Н, п, so.CH CHjCHjjCe), 2,90 (2Н, т, SCHjCHg), 3,48 (2Н, t, SOjiCHjCHj -) , 3,70 (2Н, t, СЕСНлСНр-), 4,30 (2Н, т, ), 7,05-7,60 (4Н, т, ароматич . ) . 0-этил-О- 3-(4 -фторбензилсульфонилокси)фенил -S-изобутилтиофосфата (соединение 23). Выход 100%; ЯМР (CDCEj), ( . 0,99 (6Н, d, CH/CHjt) , 1,41 (ЗН, осилен,), 1,87 2Н, т, CH2CH(CHj)2 , 2,78 (2Н, d из d, СН2СН ), 4,30 (2Н, т. OCHjCH), 6,72-7,48 (6Н, m, ароматич.), 7,85 (2Н, пп, ароматич.). О- 4- (4 -бромбензилсульфонилокси) фенил -0-этил-5-втор-бутилтиофосфата (соединение 24). Выход 97%; ЯМР (Сосе, ), сГ 0,95 (ЗН, т, CHj), 1,20-1,85 8Н, т, SCH(CH3,)CHjCH3 и ОСН2;СНз1 , 3,36 , т, CH2(CHj)CH2 , 4,30 (2Н, т, OCHj , СН.1,), 7,15 (4Н, т, ароматич.), 7,73 CtH , S , ароматич.) . 0-этил-О- з-(2 -нитробензилсульфонилокси)фенил -S-изобутилтиофосфат (соединение 25). Выход 70%; ЯМР (СОСЕ ), сГ - 0,99 (6Н, d, -СН(СН;)2 ) , 1,41 (ЗН, t, OCHjCHj), 1,89 )Н, m, СН, СИ (СН )2 , 2,77 2Н, d из d SCH CHTCH,) , 4,30 (2Н, m, GCH CHjCHj), 7,12 CiH, ffl, ароматич.), 7,88 , m, ароматич. ) . 0-этил-О- з-(2 ,4 -диметилбензилсульфонилокси)фенил -S-н-пропилтиофосфат (соединение 27). Выход 94%; ЯМР (СОСЕ ) , f 0,95 (ЗН, t, CHjCH,), 1,40 (ЗН, t, ОСН СН), 1,68 (2Н, Шг 5СН2СН2СНз), 2,39 (ЗН, 5СНз), 2,71 (ЗН, SCHj), 2,90 (2Н, т, SCH2CH2), 4,30 (2Н, т, GCHjCHj), 6,70-7,9 (7Н, т, аромагич.Г. В табл. 1 приведен элементарньй анализ полученных соединений. Формы применения препаратов обычные. Первоначальную оценку биологической активности производят на клещах, насекомых и нематодах, приведенных в табл. 2. Раствор, содержащий600 ррт испытуемого соединения, получают путем растворения испытуемого соединения в растворе (ацетон:метанол-1:1) добавлением поверхностно-активного вещества и затем воды с получением еледующей системы: ацетон : метанол i водный раствор ПАВ 10 ; 10 . 80 , Смесь алкиларилполиэфирового спирта (коммерческое название - заводская марка Tri ton Х-155) и модифицированной фта,|-1евОй глицериналкидной смолы (коммерlecKoe название - заводская маркг1 Triton В-1956) в соотношении 1:1 испОГьзуют: в качестве поверхностноактивного вещества.
Для испытания предлагаемой комло,:ии,ии на клещах зараженные бобовые листья Phaseolus limeanus, содержащие около 50 клещей, а при испытания на зеленом персиковом клеще листья или часть их, зараженные broceoif В г а S 5 i са о i е г асез i tа 1 са ) , содержаигие около 50 клещей, помещают под 1 -рышку в чашки Петри на влажные куски хлопка. Затем литья опрыскивают IcnHiyeMbiM раствором, используя ротагп1О1П- ьй иршдалощийся стол, вгзвдерживаю околс 24 ч, после чего определяют процент гибели HaceKONMx;
Для испытания на бобовом жуке и южном черве отдельные бобовые листья помещают на куски влажной фидп-ТрсзалМой бумаги в чашки Петри, опрыскиэаго ifaK описано вшле, и дают нм высохнуть, В одну 4aiJiKy Петри помещают 30 личинок мексикаЕгского бобового , л дру-гую - 30 ли-чинок южного червя, Чаш-Л/г залсрывают и вьщерживают 48 ч , затем опоеделяют процент гибели нас(гксмых.
,Для испытания композиции на семенном долгоносике и домашней .мухе используют стакан емкостью 1 пинта (0,56 л) с решеткой на крышке. В с:тагсл.11 помещают пищу для долгоносика (.яблоко) и д,омашней мухи (сладкая вода), {шпытуеглыми насекомьэди служат j,0 взрослглк семенных долгоносиков я 20 взрослых домашних мух. Стаканы, содерлсащие насекомых, опрыскивают, 1- спользуя вращающийся стол. Процент гибели долгоносика определяют через 40. ч после обработки. При испытании домашней мухи: процент падения определяют через 1 ч после обработки, процент гибели - через 24 ч.
Для испытания предлагаемой компоэ.яции на клещах Hci дно пластмассовые чашек Петри помещают куски фильтровальной бумаги и образгивают испытуемым соединением. После высыхания фильтровальной бумаги небольшое количество воды пипеткой добавляют в ка)К,:а;ую чашку для сохранения влажное;ти. Затем чашки заполняют 50 л.нчин-ками звездчатого клеща и закрывают плотно прилегающими пластмассовыми кршлками. После выдерживания около 24 ч определяют процент гибели нас€;комых,
В случае испытания предлагаемой композиции на навозных мухах стеклянные колбы емкостью 0,5 пинты с кусками фильтровальной бумаги на дне каждой колбы заполняют 20-1.0-3-5-дневными самцами и самками этой мухи. Используют сито, решетчатые крышки для удерживания мух. Мух в колбе опрескивают испытуемым соединением на вращающемся столе и выдерживают при 26, и 55% относительной влажности Через 1 ч наблюдают падение (КД) и через 24 ч - гибель насекоглых. Результаты регистрируют, как число павших или погибших мух от общего количества.
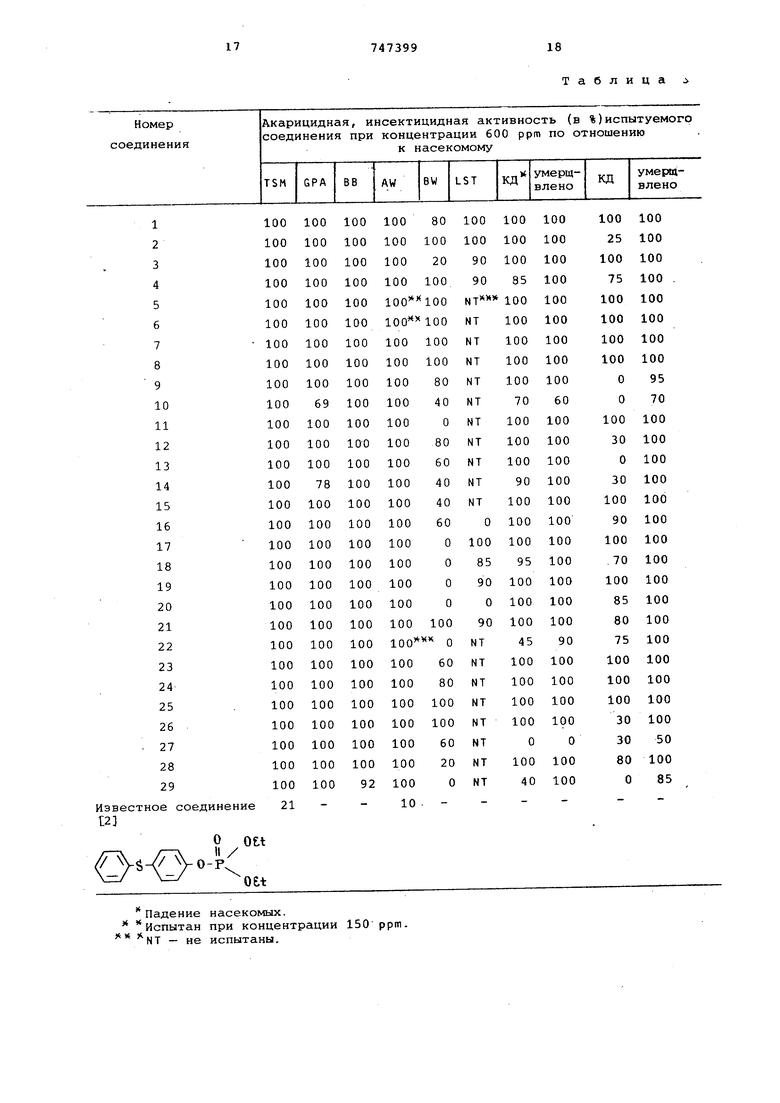
В табл, 3 приведены результаты этих биологических испытаний,
Овицидные (0) и лаврицидные (L) испытания. Для испытаний предлагаемой композиции на клещах, включая яйца и личинки двухпятнистого клеща, часть бобовых листьев, содержащих около 100 тиц, помещают на влажный кусок хлопка в чашку Петри и опрыс1сивают на вращающемся столе испытуеМЕЛМ раствором в количестве 150 ррт, вытверживают их в течение б дней и исследуют под микроскопом. Невылупившиеся яйца и мертвые и живые личинки подсчитывают и определяют овицидную и лазрицидную активность.
Для испр ятания южного зернового корневого червя (Oiabrotica undecimpunetata liowardi) и личинки, два слоя по 4,5 см фильтровальной бумаги помещают в небольшие чашки Петри, опрыскивают на вращающемся столе 600 ррп1 раствора испытуемого соединения и сушат на воздухе. Около 100 яиц в 1 МП воды пипеткой помещают на фильтровальную бумагу, чашки закрывают и вьщерживают в течение б дней, после чего проверяют под микроскопом Определяют процент гибели яиц и личинок .
В случае испытания предлагаемой композиции на личингсах москита приблизительно 20 .итук 3-дневных желтых лихорадочных москита (Aedes aegypti) помещают в чашки, содержащие 100 рдл воды, предварительно обработг нные раствором испытуемого соединения так, чтобы получить концентрацию 1 ррт. Через 24 дня определяют процент гибели личинок,
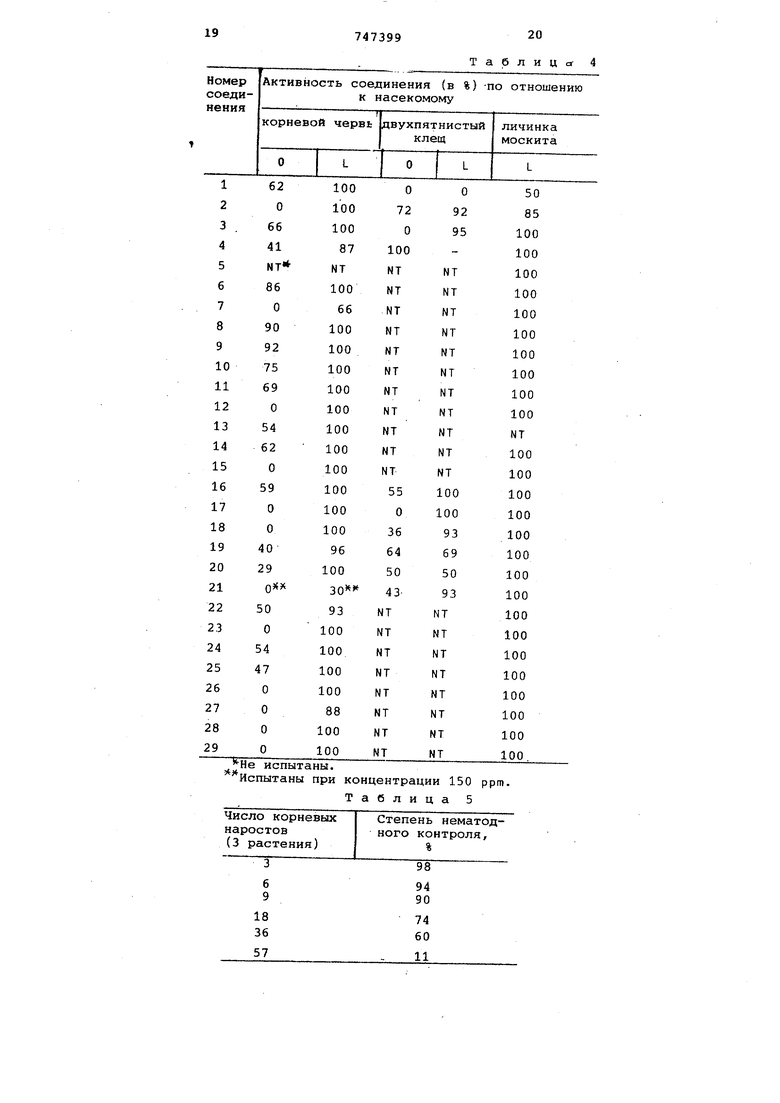
В табл. 4 приведены результаты испытаний ,
Нематоцидные испытания,
Для испытания на нематоцидную активность почву равномерно смешивают с размоченными корнями томата, обильно запутаннЕлми корнеплодной нематодой 10 мл раствора испытуемого соединения добавляют к 200 .мл перемешанной почвы в стакане емкостью 16 унций с получением объемной концентрации около 30 ррт. Стакан встряхивают для перемешивания, немедленно открывают и выдерживают на воздухе 24 ч. Почву помеща.ют в горшок, после чего высевают 3 семя огурца. По прошествии 23 дней растение удаляют из почвы и корневую систему проверяют на присутствие узлов. Используемый инокулят (посевная культура) продуцирует около 200 наростов на трех корневых сиетемах растений, находящихся в одном горшке. Если на корнях растений обнаруживают более 25 наростов, то считают, что никакого контроля или подавления нематод не достигается (отсутствие контроля) и это коррелирует с менее чем 70% нематодного контроля.
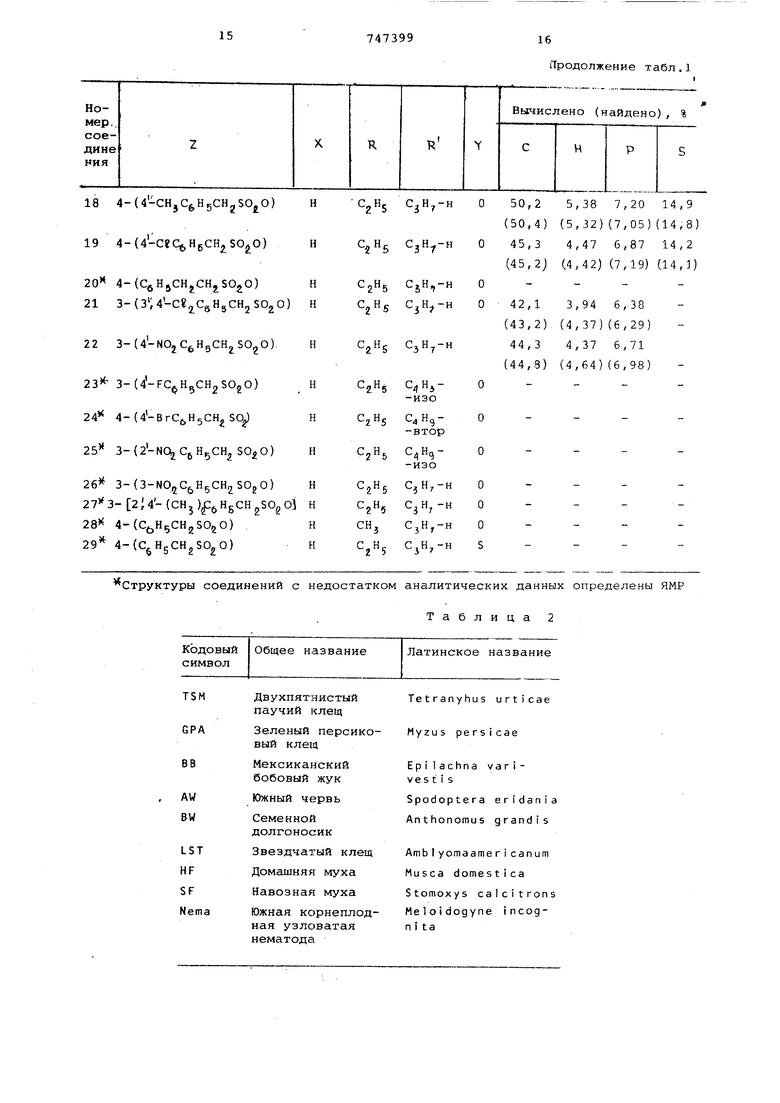
Стандартная кривая, построенная для случая с несколько меньшей плотностью инокулята, может быть использована для пересчета данных о числе корневых наростов,, выраженную в процентах степень и нематодного контроля.
Результаты испытаний представлены в табл. 6.
Таким образом, предложенная инсектоакарицидонематоцидная композиция обладает высокой активностью.
.Таблица 1





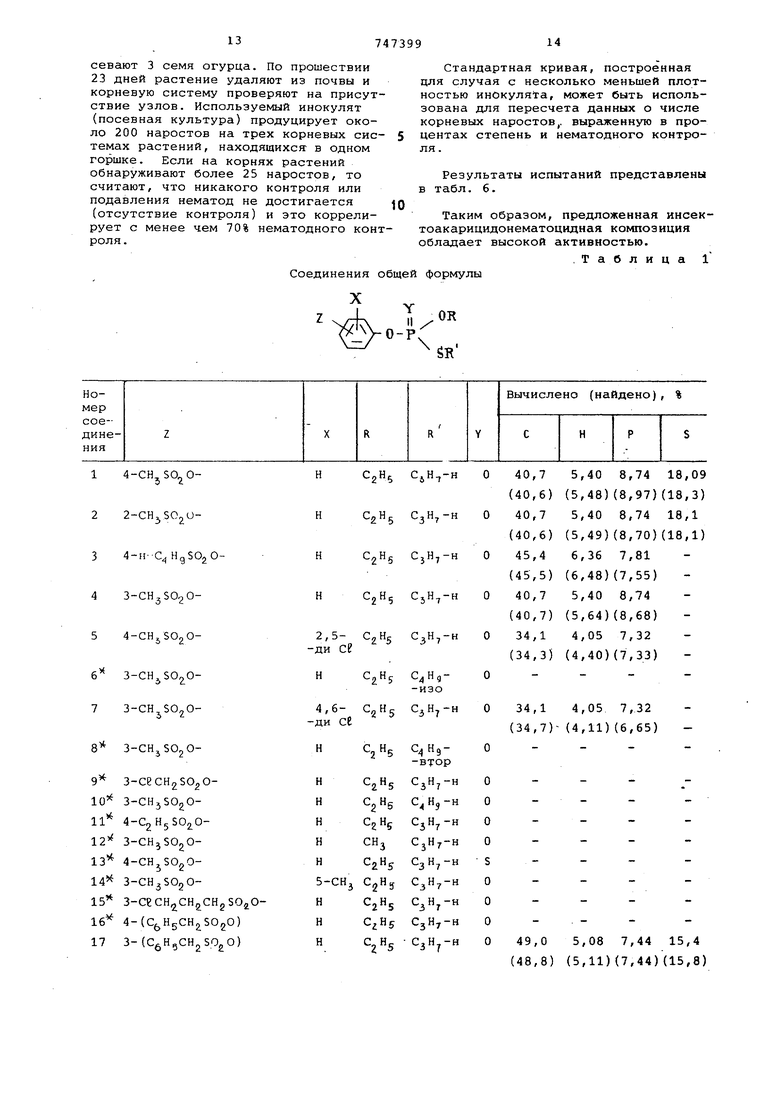


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения цефалоспоринов или их солей | 1974 |
|
SU676166A3 |
| Способ получения производных имидазола или их солей, или их комплексов с солями металлов | 1977 |
|
SU730298A3 |
| Способ получения дихлортиолфосфатов | 1976 |
|
SU718012A3 |
| ПРОИЗВОДНЫЕ S- β -ТИОАКРИЛАМИДОВ И КОМПОЗИЦИЯ ДЛЯ ПРЕДОТВРАЩЕНИЯ ИЛИ ИНГИБИРОВАНИЯ РОСТА БАКТЕРИЙ | 1990 |
|
RU2024226C1 |
| Способ получения неионных борановых смол | 1977 |
|
SU707524A3 |
| Способ получения четвертичных аминоалкилтиолов | 1985 |
|
SU1442072A3 |
| Способ получения 4,5-диарил-2-нитроимидазолов | 1979 |
|
SU940647A3 |
| Способ борьбы с нежелательной растительностью | 1988 |
|
SU1836021A3 |
| Способ получения производных пиперидина | 1989 |
|
SU1836346A3 |
| Способ получения замещенных мочевин | 1976 |
|
SU659090A3 |

(48,8) (5,11)(7,44)(15,8) 184-(4-CHjC6H5CHgSOjO)Н 194-(4-CeCg,,0)Н (CgH,jCHj,CHjS020)Н 213-(3;4-С«2,СбНдСН25020)Н 22 3-(4-N02C HgCH,S020)HCgHg
нематодс1
Продолжение табл.1 CgHs CnHt 50.25,38 7,20 14,9 50,4)(5,32) (7,05) (14,8) 45.34,47 6,87 14,2 (45,2j(4,42) (7,19) (14,1) 0--CiH|i H 0 42,1 3,94 6,38 (43.2)(4,37) (6,29) 44,3 4,37 6,71 (44.3)(4,64) (6,98)
Падение насекомых.
Испытан при концентрации 150 ррт.
).
NT - не испытаны.
Таблица
19
20
747399
Т а б л и ц cr
Известное соединение
1 /ОСаНб 0-Р
OCiHs
Таблица b
30
23
7473 9
Формула изобре-5:енйя
Инсектоакарицидонематоцидная композиция, содержащая действующее начало на основе замещенных фениловых эфиров фосфорных кислот и добавку, выбранную из группы: носитель, разбавитель , наполнитель, о т л и ч а гоад а я с я тем, что, с целью усиления инсектоакарицидонематоцидной активности, она содержит в качестве замещенного фенилового эфира фосфорной кислоты соединение общей формулы
J. OR
«-k
К
где R - С-, -Сз-алкил;: R - С,-Сд-алкил;
24
кислород или сера; хлор или метил; О, 1 или 2;;
,)-алкил, хлорметил, хлорпропил, бензил, фенильна.я группа формулы
Хл7
где X - нитро, хлор, бром, фтор, метил;
т - О , 1 или 2 , в количестве 0,000001 - 99 вес.%.
Источники информации, принятые во вниг.инне при экспертизе
кл. 45 е 9/36, опублик. 09.03.61.
кл. 260-461, опублик, 03.07.62 (прототип) ,
Авторы
Даты
1980-07-23—Публикация
1975-10-30—Подача