(54) РОДЕНТИЦИДНЫЙ СОСТАВ




| название | год | авторы | номер документа |
|---|---|---|---|
| Родентицидный состав | 1977 |
|
SU689598A3 |
| Способ получения производных дифениламина | 1976 |
|
SU679128A3 |
| Способ получения дифениламинов | 1976 |
|
SU626688A3 |
| Способ получения производных дифениламина | 1976 |
|
SU628811A3 |
| Способ получения производных дифениламина или их солей | 1981 |
|
SU984402A3 |
| Способ получения 3-третбутил6-метил-5-нитросалициланилида | 1972 |
|
SU508179A3 |
| Способ получения алканоиланилида или его аммониевых солей | 1986 |
|
SU1528343A3 |
| Способ получения карбоксанилидов или их аммониевых солей | 1986 |
|
SU1561822A3 |
| 3,5-ДИНИТРО-2-(АРИЛАМИНО)-N-(4-НИТРОАРИЛ)БЕНЗАМИДЫ, ОБЛАДАЮЩИЕ РОДЕНТИЦИДНОЙ АКТИВНОСТЬЮ | 2011 |
|
RU2528419C2 |
| Способ получения производных -(2,2-дифторалканоил)-0-фенилендиамина | 1976 |
|
SU645554A3 |

- . . Изобретение относится к родентицидам, используемлм для снижения популяции крыс и мышей, .. Известный родентицидный состав, содержащий, п-хлсрфенил-2-ацетил- .,. -1 3-индандибя и пищевой наполнитель, малоэффективен при длительно применении. Отмечается -Непоедание . грызунами корма с родентицидом.: Целью изоб зетения является увеличение эффективности действия сос тава, ;. . Поставленная цель достигается тем, что в -качестве Действующего начала используют соединение дифен амина общей формулы где один из R и R - нитрогруппа, а другой -. триЛторметил или нитрогруппа ; . , R .- водород, метил, этил или про пил, при условии, что когда один и IR -или R трифторметил, то R водород; R - триЛ.торметил, то кажR,.R И дый из R и R хЛор, бром или ФТОР, или R трифторметйл, а R, R;, - водород когда R - триЛторметил, то R галоген, водород, циано- и нитроТруппа, Метил или трифторметил; независимо друг. от., друга.: каждый изхлор, бром, фтор, метил, трифторметил, нитрогруппа или водонезависимо друг от друга каждый из R .и R - хлор, бром, фтор, метил, трифторметнл Й.ПИ водород при условии, что R,, R и R - водород, причем не означает фтор, метил или водород; когда водород, не более двух из R , R , RH водород; не более двух из R,R,,R и R трифторметил; когда один и только один из R,R,R и R трифторметил, то два или три из R,R и R- - хлор, или бром, , не более одного из В-, И, R или Е метил, то два или три из В , В и R - хлор, бром или фтор; В и R - ИНТне более одного из рогруппа; не более одного из R,R , R, R и R - метил, за исключением того, что каждый из R и R может обозна чать когда S или в ,- нитрогруппа, R - хлор, бром или нитрогруппа.; когда R.. и В - нитрогруппа, а R -водород, то R - галоген, водоро циано-.- нитрогруппа или трифторметил, независимо друг от друга каждый из R и R - .бром, хлор, фтор, водород или нитpoгpyппa R и R Независимо друг от друга хлор, бром, фтор, трифторметил или ёод;ород: . : ; .. . . . ,„.,. , при условии, что не более двух и , R и - водород, за R R и R исгключением того,что водород, когда R -тпифтормети не более одного из R , R и R нитрогруппа; « , л. s когда два из R , R R, К и R водород, то они не располо)кены рядо дауг-ь другом; , ... когда- R или R - нитрогруппа, и R не обозначают то ни В, ни В водород; К не обозначает цйано-, нитрогруппу или трифторметил, когда R или R - трифторметил;. когда R® не обозначает водород, Гб. независимо друг от друга R , R R5, s и к - хлор., бром, фтор или воДброд при условии, что не более дву;х из S, -R, R , R и R - водо род и два таких атома водорода не расположены рядом друг.с другом; при условий, что в выпгеуказ анны соединениях, ., ,. .. . когда один из R , R , R , R и R - фтор, то два или три из R, R и R - хлор или бром; / и при условии, что в вышеуказан ных соединениях,, .. когда R,R,R,R или R .- трифтор метил,то ни один 63 R,R ,R,R и R не обозначает фтор или; метил в количестве 0,00051 0,2% от веса пищевого наполнителя. .. , Соединения, используемые в практике f легко синтезировать из фенилгалогенида, замещенного на три. нитрогруппы или две нитрогруппы и трифторметил, и соответствуювдм образо замещенного анилина известными мето далда в присутствий акцептора кислоты,., например неорганического основа ния, третичного амина или избытка.. гфЫлежУтбчного соединения анилина, в среде диметилформамида (ДМФА) при , - с использованием гидрида натрия. : ;, Наилучшим способом.получения три 4)торметилзамещенных анилинов являет ся синтез карбокейзамещенных анилийов С последующим Фторированием кар боксигрупп четнрехЛтористой серой. Фторированные соединения анилина получают из фторбората диазо.ния с последующим разло.ением диазониевой соли при нагревании. Кроме того, атомы Лтора можно ввести в . бензольное кольцо с помощ.ью элементарного Фтора при 6чёнь ййзких температурах. В некоторыхслучаях в качестве исходных соединений удобно использовать айилины, не галогенированные или галогёйированные неполностью, как требуется для целевого соединения. Их обрабатывают фенилгалогенидом, а .для окЬнча:тельнсэго галогенирования применяют , например, элементарный галоген в уксусной кислоте или хлористом метилене, , Иодирование лучше всего протекает в присутствии однохлористрго иода. Для получения 4-замещенных соеди нений перед галогенированием необходимо блокировать положение 4, например, с помощью сульфокислотных групп, так как они легко вводятся и легко удаляются. Очень часто двухстадийный процесс удобен для получения N-алкрловых соединений. В таких случаях N-алкиланилин взаимодействует с тринитрофенилгалогенидом с образованием Ц-алкилдифениламина, не галогенированного или гало- генированного неполностью. И наоборот, иногда.удобно получить сначала . дифениламин, а затем провести алкилирование его с помощ,ью такого реагента, как диалкилсульЛат или алкилгалогенид. Ниже приведены примеры типичных методов, с йбйбщьк)которых могут быть синтезированы любые из предлагаемых соединений, П р.и м е р 1. 2,4,6-Трихлор-2 ,4 ,б -тринитродифениламин (соединение № 1) . 3 г гидрида йатрия суспендируют в 50 мл сухого ДМФА и охлаждают до -10°С. При проведении следующих операций тумпературу поддерживают достоянной. В течение 15 мин добавляют раствор 2, 4,6-.трйхлоранилина в 75 мл сухого ДМФА, перемешивают 45 мин,-в течение 20 мин вводят раствор 12,6 г хлористого пикрила в 75 МП ДМФА, перемешивают 90 мин (температура повышается до ) , смешивают со льдом и водную сусп.ензию Подкисляют разбавленной соляной кислотой. Осадок отфильтровывают . и перекристаллйзовывают из этанола. Получают .10,8 г целевого продукта, т.пл. 17б-177 с, индентифицированного с помощью ЯМР- и ИК - спектроскопии а также данных элементарного микроанализа, С З5.,37; Н 1,24; Вычислено,%; N 13,75; О 23,55; С1 26,10.
Найдено, %: С 35, 16; Н 1,36; N 13,72; О 21,52; С1 26,34.
Аналогично получены.: 2,6-Динитро-З , 4, 5-трис-(трифторметил) -дифениламин (соединение № 2), т.шт. 150°С, выход 35%.
3,5-Бис-(трифторметил)-2 ,.4,б -тринитродифениламин (соединение т.пл.,1ВОг1В1 с, выход82%.. ..
2, 3,4,5,б-Пентахлор-2 ,4 ,6 т . -тринитродифениламин. (соединение 4) т.пл. . 234с, выход. 95.%.
-2,6-Динитро-2 , 3 ,4 г 5 ,6 -лентхлор-4-трифторметилдифениламин (соединение №.5), т.пл, 2бз-205с, выход 56%...
2, 4,5-Трихлор-2, 4, б-тринитро-дифениламин (соединение № 6), т.пл. 198-200с, выход 40.%. .
3,4,5-Трихлор-2,4,б-тринитродифениламин (соединение №7), т.пл..201-203 С, выход 61%.. ..
2,3,4,5,6 -Пентафтор-2, 4 , 6 -тринитродифениламин (соединение № 8), т.пл.. 117-119С, выход 24%.
2, 4-,Цинитро-2 ,4 ,6 -трихлор-б-т гйфторметилдифениламин .(соединение № 9), т.пл. 106-108°С, выход 26
2, б-Дихлрр-2 , 4J4, б -тетранитродифениламин (соединение 10), т.пл.. 157-159°С, выход 63%.
2,4,б-Трибром-2,4-Динитро-6-трифторметилдиФениламин (соединение 11), т.пл. 153-155°С, выход 60%.
2,3,5,6-Тетрахлор-2 ,4,6-тринитродифениламин ,т.пл.192,5-193, выход 58%.. .
2,4,6-Трибром-2 ,4 ,6-тринитродифениламин (соединение №12), т.пл.. 220-221° С, выход 52%...
2,3,5f6-Тетрафтор-2,4,б -тринитродифениламин, т.пл. 113-115 С, выход 25.%..
2,3,4,5,б-Пентахлор-2 ,4 -динитро-б -трифторметилдиЛениламин, т.пл.. 172-172,5°С, выход 65%.
2,4-Дихлор-2,4,6,6 -тетранитродифениламин (соединение 13), т.пл. 187-189°С, выход 37%.
2, 4-Динитро-4., б -биоЧтрифторметил)-дифениламин, т.пл., выход 16%..,
2,5-Дихлор-2 ,4-динитро-6 -трифторметилдифениламин, т.пл. 133134С, выход 45%..
2,6-Лихлор-2 , 4 -динитро-6 -три-фторметилдифёниламин, т,пл.9 3-9 , выход 3 5 %. «
2,4,б-Трифтор-2 ,4 -динитро-б-трифторметилдкфениламин (соединение № 14.), т.пл.104-1р5 С, выход 10%
2,4-Дихлор-2, 4-динитро-6 -трифторметилдифени.памин (соединение 15 т.пл. 99 5-10lc, выход. )0%
2,3,5,6 Тетрахлор-2 ,4 -динитро-6 -трифторметилдифениламин, т.пл. 172-173°С, выход.70%.
2,б-Дибром-2,4-динитро-4,б -бисЧтрифторметил)-дифениламин, 5 т.пл.125,5-127с, выход 8%.
4-Хлор-2 , 4 -динитро-6- -трифтор-метилдифениламин, т.пл.104-105°С, выход 50%.
2,б-Дибром-2. ,4 -динитро-б -три 0 Фторметилфениламин,т.пл.127-128 С, выход 30% , .
3,4-Дихлор--2 , 4 -динитро-6 -трифторметилдифениламин ,т.пл.111-112 С выход 3% ..
. 4-Циано-2 , 4.-динитро-6 -трифтор метилдифениламин, т.пл. 199-200°С, выход 8%. .
4-Бром.-2 , 4 -динитро-6 -трифторметилдифениламин ,т.пл.118-119°с, выход 2010 4-ЙОД-2;4 динитро-б-трифторметилдифениламин, т.пл . 138-139 с выход 10% . .
2,4-Дибром-2,4-динитро-б-трифторметилдифениламин, т.пл. 124,55 126С, выход 17%2,4-Дифтор-2 , 4-динитро-б |-трифторметилдифени.памин, т,пл. 89,590°С., выход 25% ..
2,5-Дифтор-2 ,4 -динитро-б -три0 фторметилдифениламин, т.пл. 100i01°C, выход 32%.
.3, 5-Дихлор-2 , 4 -динитро-б -три фторметилдифениламин, т.пл. 136-. , выход ЮГ. .. ..
5 2,4-Динитро-З ,5,6 -трис-(трифторметил)-дифениламин, т.пл. 136137°С, выход 15% ...
2,3, 4,5,б-Пентафтор-2, б -динитро-4-трифторметилдифениламин, т.пл. 0 120-120,5°С, выход 75%.
П р и м е р 2. 2, 4,6-Трифтор-Н-метил-2 ,4,б -тринитродифениламин (соединение I 16).
3 г гидрида натрия в виде 0%с ной дисперсии в масле смешивают с 50 мл.сухого ДМФА в атмосфере азота и охлаждают до , В течение процесса температуру поддерживают примерно постоянной. Затем в течение р. 16 мин добавляют раствор 10 г N-ме тиланилина в 50 мл ДМФА, перемеши.вают 1,5 ч в течение следующих 25 мин добавля от раствор 23,1 г. хлористого пикрила в 75 мл ДМФА, перемешивают и дают нагреться до комнатной температуры в течение ночи.
Затем смесь перемешивают с болы1П1М объемом измельченного., льда, .подкисляют соляной кислотой, на следующий день фильтруют; осадок пёрекристатши0 зовывают из денатурированного этанола и получают 10,2 г М-метил-2, 4, б -тринитродифениламияа, т.пл. 104-105 С.
2,3 г полученного соединения суспендируют в 30 -мл уксусной кислг.Г.., 5 насытают газгобразным хлором пт-и перемешивании и комнатной темйератур Через 3 ч непрерывного перемешивания в течение которого медленно добавляю хЛор, смешивают с водой, отфильтровы вают осадок, фильтрат перемешийают b сульфатам магния и активировайным углем, фильтруют и выпаривают досуха. Остаток растворяют в смёси дяЭти лового и петролейного эфиров, фильтруют, выпаривают, перекристалдизовывайт остаток и полу-чают 0,48 г.. це левого соединения, т.пл, 178-179,Ь. Вычислено,%: С HI,67 N С1 25,23. С 37:, 24 Н 1,87 . Найдено,%: N 13,42; С1 24,99. 3. -2,4-Дибром-б- . При м е р -хпор-К-метил-2 ,4,6 -тринитродифениламин .(соединение 17) J .--, 1,3 г промежуточного. сЬё)с(йнёния, полученного в примере 2, суспёндируют в 10 мл Уксусной кислоты и в течение 2 ч перемешивают при комнатHoW температуре с 1 мл элементарного брома. Смешивают с водОй, фильтруют осадок растворяют в 20 мд уксусной кислоты, немного нагревают и насыщайт хлором. После пе ремешйвания в течение 1,5 ч с пер1И.одическим дОбавлеЧ нием небольших количеств хлора светло-желтый осадок отфильтровывают.Получают 0,ii2 г целевЬгЪ продукта, т.пл.199-200 С. С 50,59 Н 1,38 Вычислено,%: N 10,98 С1 6,95. НайДёно,%: С 30,74 Н 1,51 N 10,75 С1 6,99. Подобным образом синтезированы: 2,4,6-Трихлор-Н-этил-2,4 ,6 -трийитрЬдйфёниламин {сЬёДййенйё 18), т.пл.138-140°С/ выход 60%. Вычислено,%: С 38,60 Н 2,08 N 12,86 О 24,42 С1 22,04. Найдено,%: С 38,90 Н 2,03; N 13,10 О 24,71 , С1 21,94. 2,4-Дибром-6-хлор-2,4-динитро-6-трифторметилди4енйламин,т.пл.129, 130с, выход 50% - ; 2,6-Дихлор-4-йод-2 , 4,б -tJ:;rйнйтpoдафёнилaмйн, т.пл.202-2Р4С, выход 12% 2, б-Дихлор-4-циано-2 , 4, 6 -тринитродифениламйн, т.Пл.216- 218с, выход 4% Т2 ,4-Дихлор-6-метил-2 , 4 гдинйтро-6-трифтОрметилдифениламин, т.пл. 143-144 C, выход 1% . У . .2,4,6-Трихлор-3,5 -диметил-2 , 4 -динитро-6-трифторметилдифениламин, т.Ш1.156-159 С, выход 42%:., , , 4-Бром-2,6-дихлор-2 ,4-динйтро-6-трифторметилдифениламин, т.пл. 115-115,5°С, выход 8%.
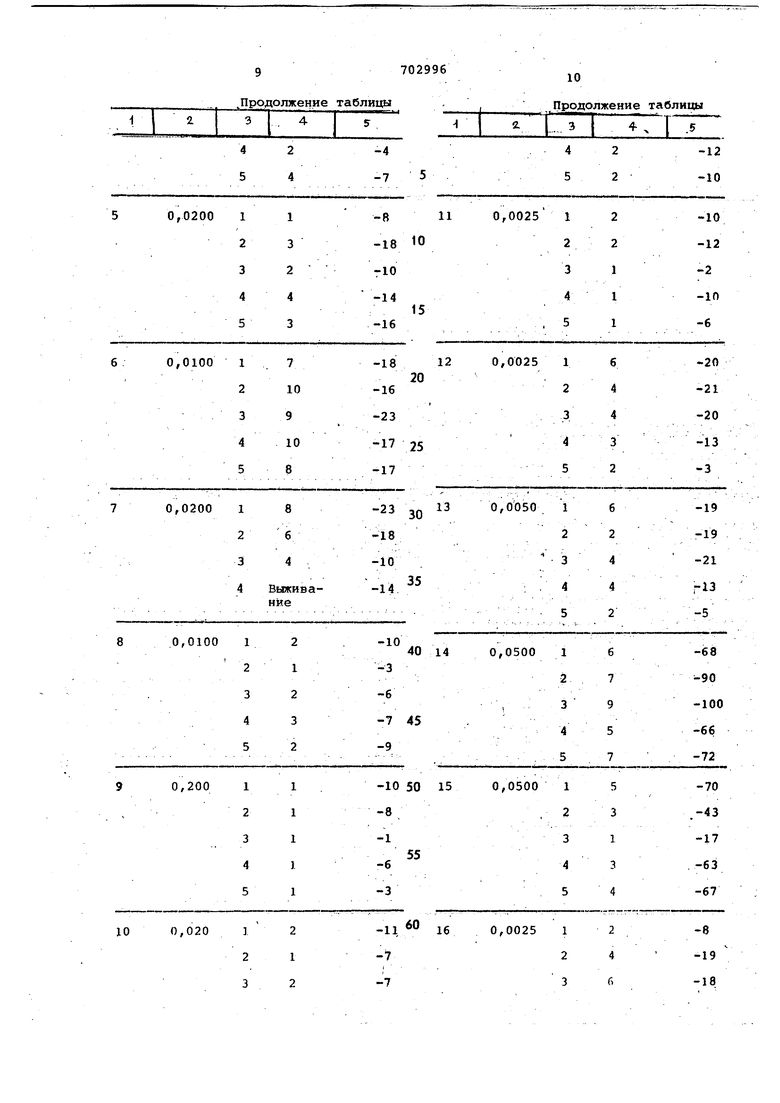
Испытуемые соединения .вают - с ТПйщевым наполнителем на основе хлебных злаков и скармливают мужским особям белыхкрыс. В таблице приведены концентрация испытуемых соединений в пищевом наполнителе, количество дней с начала принятйя состава до гибели крыс, SsivieHeHHe веса каждой крысы в течение 10-дневного эксперимента. В одних опытах используют молодые особи весом 50-60 г, в других - более старые Bei-ом примерно 250 г. Изменьние йеса контрольных крыс колеблется в широких пределах от опыта к опыту вследствие различного возраста и размера . Однако сггучаях привес, с контрольных крыс в ходе эксперимента составляет 4060 г на животное. Т э блица.,
9702996
Продолжение таблицы
10 Продолжение -таблицы 0,0030 0,0025 -86 20 Предлагаемые соединения эффектив ны при очень низких концентрациях, но убивают крыс не сразу. Как все хорошие родентициды, они обладают определенным периодом индукции. Соединения эффективны при -борьбе ;.с крысами и мышами следующих видов; Mus.musculus, Peromyscus leukopus Rattus norvegicus, Neditoma unerea, R rattus rattus, Microtus pennsyl- Vi niciis, R.r . frugivorus. Соответствующий подбор концентрации дей ствующего начала в составе обеспечи ет снижение популяции крыс или мыше Либо в результате немедленного отра ления,либо в результате хроническог отравления после многократного приНятия состава, содержащего родентицид.. Замедленное летальное действие предлагаемых соединений являегся; отличительной чертой при использований их в качестве родентицидов, В день крыса поглощает примерно 5-50 г пищи, мышь примерно 1-5 г в 5ШвЙсШой 1й о возраста, размера и состояния здоровья. Можно установить число животных в колонии и обеспечить места их обитания соответствующими количествами родентицидного со тава или других композиций, содержащих эффективное количество активного соединения в расчете на каждое животное. Родентицидные составы можно испол збва ь в виде порошков, или подмешивать в воду или в корм.Предпочтител 5 д .ные концентрации fleflcTE-rotnero начала в питьевой воде или порошках обеспечивают родентицидный эффект после двух или более принятий состава, Пигпевой наполнитель может представЛять собой любое съедобное вещество, поскольку крысы и мыши всеядны. Эти вещества не растворяются в воде. Их измельчают до очень небольшого размера частиц и суспендируют -в загустителях Скарбоксиметилделлюлоза, поливинилпирролидон, желатин, альгинаты), поверхностно-активных веществах (лецитин, полиоксицетилированные алкилфенолы, алкилсульфаты, нафталинсульфонаты, алкилбензолсульфонаты, и полиоксиэтилированные эфиры сорбината). В некоторых случаях можно использовать силиконовые пенсгасители, гликоли, сорбиталь и сахара, играющие роль сусдендирую1пих агентов. В родентицидные- составы могут быть включены различные добавки и ароматические вещества, например одоранты, половые гормоны, пахучие вещества, что помогает отвлечь грызунов от запаха приманки., Формула изобретения Родентицидный состав, содержащий ищевой наполн.итель и действующее ачало, о т л и ча ю щ и и с я ем, что, с целью увеличения эффекивности его действия, в качестве ействующего начала он содержит соединение дифениламина общей форму где один из R и R - нитрогруппа, а другой-трифторметил или нитрогруппа;Н - водород,метил, этил 1лй пропил при условии, что когда один из R или R -трифторметил, то R - водород . . когда R - трифторметил, то каждый и хлор, бром из:кЗ, , R, R или фтор, или К и R - трифторметил, а R, R, R - водород; когда R - трифторметил, то R галоген, воДброд, циано-, нитрогруппа, метил или трифторметил; независимо друг от друга каждый из и R хлор, бром, фтор, метил, трифторметил, нитрогруппа или водород; независимо друг от друга каждый из R и R - хлор, бром, фтор, метил, трифторметил или водород при условии, что R, R , R - водород, причем R не означает фтор, метил или водород;когда R - водород, не более двух из R, к, R и R - водород; не более двух из R, трифторметил; когда один и только один из R, R ., R и R - триЛторметил, то два или три из R, R и Rj - хлор или бром, не более одного из RjR, R, R и R - метил, тодва или три из R, R и R . итр jcj); не более одного из R и нитроrpj nna, не более одного из R,R, R R ь и R метил,за исключением того, что каждый из R и R мoжeт означать метил;кoi дa R или R - иитрогруппа, R - хлор, бром или нитрогруппа; ког да R или R - нитрогруппа, а R водород, то R - галоген, водород, ци ано-, нитрогруппа или трифторметил, независимо друг от друга каждый из R и R бром, хлор, фтор, водород или нитрогруппа; R независимо друг от друга хлор, бром, фтор, трилторметил или водород при условии, что Не более дв из R, R, R, R и R - водород, за исключением того, что R , R - когда R и R трифторметил-, не бояее одного из и R - нитрогруппа; , э л ч А когда два из R ,R,R, R и водород, то они не расположены рядом друг С другом; кргда R - нитрогруппа, то R, ни R или R не обозначают вони доррд; R не обозначает, циано-, нитрргрупг пу или трифторм -тил, когда R - трифторметил; когда К не обозначает вюдЬрод, то; независимо друг от друга R,R,R, R и R - хлор, бром, фтор или водород при ,условии, что не более двух водород и два таких атсма водорода не расположены рядом друг с другом; при условии, что в вышеуказанных соединениях. , R И R.коЬда один из R R фтор, то два или три из R , хлор или бром, и йрй условиИ, что R не обозначает фтор или метил. в количестве 0,00051-0,2% от веса пищевого наполнителя.

Авторы
Даты
1979-12-05—Публикация
1976-09-24—Подача