Изобретение относится к способу получения новых производных тиенотриазолодиазепина, обладакицих ценными фармакологическими свойствами.. Цель изобретения - расширение арЬемалд средств воздействия на живой сфганизм. Основанный на известной реакции Мйми ования производных спирта { предлагаемый способ получения проиэвсздных тиенотриазолодиазепина об|цей формуJ& L ir-AlK- « lf. 1 Haiv $ if-Cf С К где R и Rj - водород или С.-С4-а.лк RJ - водород, галоид или нитрорадикал; Alk - С -С -алкилен; Наб - галоид, или их солей, заключается в том, что сложный эфир метансульфоновой или га л оид водородной кислоты и спирта общей формулы КО-А1К-С Hai Л. где Alk, Hal и Rj имеют вышеуказанные значения, подвергают взаимодействию с амином общей фо ялулы где R. и RJ имеют вышеприведенные значения, с последующим выделением целевого продукта в свободном состоянии или в виде соли. Галоид Наб обычно представляет собой брсм, хлор, фтор и йод, пред-, почтительно хлор, а R j , если он галоид - хлор и фтор. Реакцию обычно проводят в присутствии Инертного органического растворителя, например диметилформамида, метанола или зтанола, при 0-100°С, .предпочтительно при . Целевые соединения можно пере. ьзс7:к в фармацевтически приемлемые еоли путем обработки неорганическиг-ли или органическими кислотами тз.кирди как соляная,.бромистоводородная, азотная, серная, фосфорная, винная, л1- - онная,. малеиноваЯр аскорбиновая, муравьиная,.уксусная, янтарная, метак-; беизо и п-толуолсульфоновая. Исходные спирты можно получить, например, циклизацией- соединения обглей формулы KO--AlK:-- -HNR НН И. fТГ где Hal, Alk, и Rj имеют указанные зиачениЯр при нагревании {20-300°С) бел1 растворителя или в присутствии инертного органического растворителя, В присутствии инертного оргаг- И аского растворителя циклизацию ведугт при бО-ХвО с, в частности при жемйературе дефлегмации реш ционнсй Огласиf, в отсутствие растворителя - при 200--2бОС, В качестве инертного органического растворителя можно ис пользовать углеводороды (толуол, кс ,jio«) , галоидированные углеводороды, . (лорбеизол) f эфиры (тетрагидрофуран I;KGKC&K, дг-шетиловый и диэтиловый ,/мэтилеигликоля, амиды (триамид -е сааметклфосфориой кис лоты j диме.;: лфор-ламид) , днметилсульфоксид, сп У {i-ievtnon, этенол, 1-пропанол, 2-,--пропанол г 1-бутаыол, 2 5утакол, циклогексанол) ., Продолжительность .р акции зависит от температуры и наличия растсюрителя, обычно реакция гфодолкается от нескольких минут до .В ч;., ггредпочтительно несколько минут при работе без растворителя и 1-24 ч при использовании растворите ля П р и р 1. 0,75 г 2-хлор 4 (о-хлорфенил) -бН-тиено Ь 2-f -сиг Триазоло- 4 f3-а 1,4 диазепин-9--мзтанола растворяют в 25 мл абсолютного хлороформа и прибавляют Of г триэтиламина и 0,6 г метансульфохлорида, перемешивают 2,5 ч при 25°С, промывают два раза водой к два раза насыщенньам раствором хлорида натрия, сушат.над сульфатом натрия и упаривают, получая 635 мг (70%) маслянистого сложного эфира метансульфокислоты и 2-хлор-4-(о-хлорфенил)-бН-тиено- 3,2-f -симм-триазоло- 4 ,3-а 1,4 Диазепин-.9-метанола, который растворяют в 10 мл диметилформамида и прибавляют по каплям при 0-5°С к раствору J МП жидкого аммиака в 5 мл диметил формамида. Перемешивают 2 ч при комнатной температуре, обрабатывают насыщенным раствором хлорида натрия и хлористым метиленсм. Органическую фазу сушат и упаривают, остаток перекристаллиэоаывают из этанола и получают 315 мг (60%) 9-аминометил 2-хлор 4-(о-хлорфенил)-бН-тиено- 3,2 fJ-симм-триаэоло- 4,3-а 1,4 -лиазепина, т. пл. 190-192С. Исходное вещество можно получить следующим образом. 1,1 г 7-ХЛОР-5-(о-хлорфенил)-1,3-дигидро-2Н-тиено-(2,3-е 1,4 -диазепин-2-тиона нагревают с обратным холодильниксяи вместе с 1,5 г гидразида гликолевой кислоты в абсолютном бутаноле в течение 8 ч, отгоняют растворитель и остаток перекристаллизовывают из этилацетата с обработкой активированным углем. Получают 2-ХЛОР-4- (о-хлорфенил)-бН-тиено- 3,2-f -симм-триазоло 4 , 3-а ,4 -диаэепин-9-метанол, т. пл, 219-221°С. Аналогично с выходом 40% получают 2-хлор-9-диметиламинометил-4-(о-нитрофенил)-бН-тиено- 3,2-f -cшvIM-тpиaзoлo- 4 , 3-а 1,4 -диазе- пин, т. пл. 234-236°С. Пример 2.0,5г сложного эфира метансульфокислоты и 2-хлор-4-(о-хлорфенил5-бП-тиено- 3,2 f Симм-триазоло- 4,3-а 1,4 -диазепин-9-метанола растворяют в 10 мл диметилформамида, выливают в тугоплавкую трубку, охлаждают до 0°С, вводят 0,5 г аммиака,расплавляют и нагревают 10 мин до . После охлаждения трубку открывают,реакционную смесь обрабатывают насыщенным раствором хлорида натрия и хлористым метил1эном.Органическую фазу сушат и упйривают, остаток перекристаллизовывают из этанола и получают 9-аминометил-2-хлор-4-(о-хлорфенил)-бН-тиено-ГЗ ,2-f -симм- триазоло- 4 ,3-а --и,4 -диазепин, т. пл. 190-192С. Пример 3.0,7г 2-ХЛОР-9-хлорметил-4(о-хлорфенил)-бН-тиено- 3,2-f -симм-триазоло- 4 ,3-а 1,4 - -диазепина растворяют в 5 мл диметилформамида, охлаждают до 0°С, прибавляют 1 мл жидкого аммиака в 5 мл тетрападрофурана и выдерживают в течение недели при 0°С. Смесь обрабатывают насыщенным раствором хлорида натрия и хлористым метиленом. Органическую фазу сушат, упаривают, остаток перекристаллизовывают три раза из этанола и получают 9- аминомеТИЛ-2-ХЛОР-4-(о-хлорфенил)-бН-тиено- 3,2-f -симм-триазоло- 4 ,3та 1 ,4 циазепин, т. пл. 19t)-192uc. Пример 4. О,5 г 2-ХЛОР-9-хлорметил-4-(о-хлорметил)-бН-тиено-(3,2-f -симм-триазоло- 4,3-а 1,4 -диазепина растворяют в 5 мл диметилформамида, прибавляют 1 мл жидкого аммиака в 5 мл диметилформамида, ра плавляют в тугоплавкой трубке и нагревают 2 ч до 100°с. После охлавд ния трубку открывают, содержимое тру ки обрабатывают насыщенньаи раствором хлорида натрия и хлористым метиленом. Органическую фазу сушат и упари вают, .остаток перекристаллизовывают три раэа из этанола и получают 9-ш..к нс 4етил-2-хлор-4- (о-хлорфенил) -бН--тиено- (3,2-f - :имм-триазоло- 4 ,3-а -f 1/4 -диаэепин, т. пл. 190-192С. Выход целевого продукта в примерах 2-4 достигает 20-30%. Используемый в примерах 3 и 4 исходный материал можно получить сле дующим образов. 1,О г 2-ХЛОР-4-(о-хлорфенил)-бН-тиено-(3,2-f 1 -симм-триазоло-{4,3-а 11,4 -диазепин-9-метанола растворяют в 10 мл хлороформа, прибавляют 3 мл тионилхлорида и нагревают 10 ч с обратным холодильником, упаривают в вакууме, остаток растворяют в хлористом метилене, встряхивают несколь ко раз с насыщенным раствором бикарбоната натрия и органическую фазу упаривают. Кристаллический остаток перекристаллизовывают из этилацетата. Получают 2-хлор-9-хлори1етил-4 (о-хлорфенил)-бН-тиено- 3,.1М -триазоло-14,3-а 1 ,4 -диазепин, Формула изобретения Способ получения производных тиенотриазолодиазепина общей формулы ЗГ А1К-С К «2 HaU S ,N-c тт Н, d (К где R и RJ - водород или .-алкил; .. Rj - водород, галоид или нитрорадиНае - галоид, или их солей,отличающийся тем, что СЛОЖНЫЙ эфир метансульфо;новой ИЛИ галоидводородной КИСЛОТЫ к спирта общей формулы НО А1К-С № IT н, где Alk, Hal и Rj имеют вышеуказанные значения, подвергают взаимодействию с алшном общей где Ал и Ел кмешт Бьаиепркведенные значения, с послед лоп1:.1м выделением целезого продхкта з свободном состоянии или 3 виде соли. Источники информации, принятые во внимание при экспертизе 1, U-Llmanus. Jncyklopadie der technischen Chemie, 3, Band 3, S-. 452-456, 1553.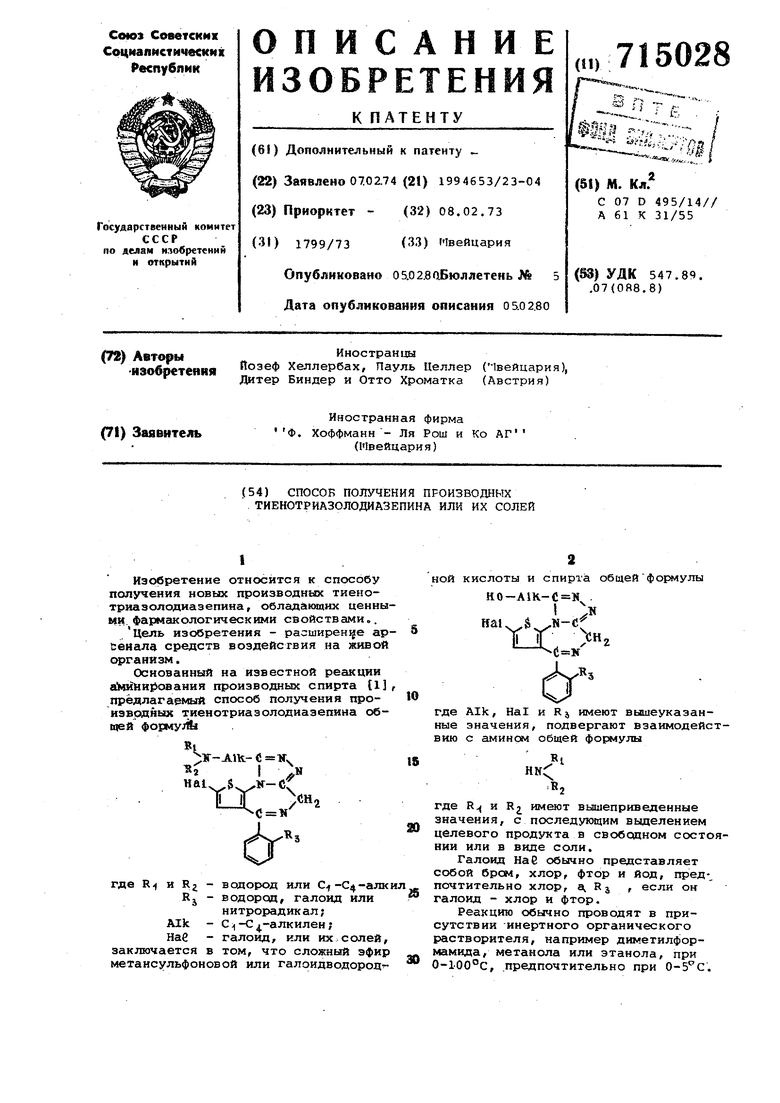




Авторы
Даты
1980-02-05—Публикация
1974-02-07—Подача