(54) СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИДА ОПТИЧЕСКИ АКТИВНЫХ ДАУНОСАМИНИЛПРОИЗВОДИЫХ АНТРАЦИКЛИНОНОВ
3 9.
HHRi,
i5i 2i-v; l i. .-, .---..-;,-.I OH (2)
0 OH
ООНз
.
8HR U)
HjC
NHR/, (3
Иг 0 OH
l l
IIII
Иг О он I
о
NHR
ОНч
724087
(4)
НзС
где RI является водородом;
Rj и Ra одинаковые и означают водород, метил, хлор
или Rj и RS оба являются водородом и RI представляет собой метил, метокси, хлор или RI и RS оба означают водород и Rj представляет собой метокси;
R4 - водород или трифторацетил, заключающийся в том, что оптически активный антрациклинон общих формул 5, 6, 7 и 8
COCHj ОН
В
Hi
RZ о он он
(67ll,9R)
Rg 0 OH OH
(7,7R,9S)
Rj 0 OH.
V2 0 OH OH
(8,7,9)
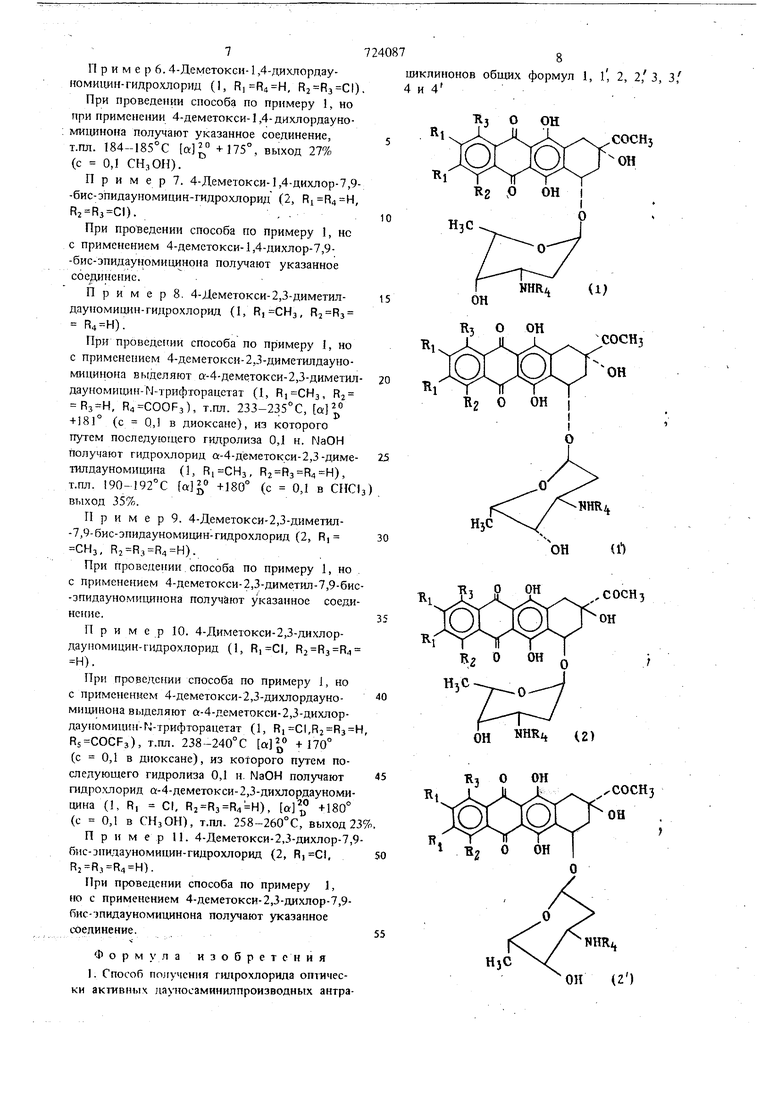
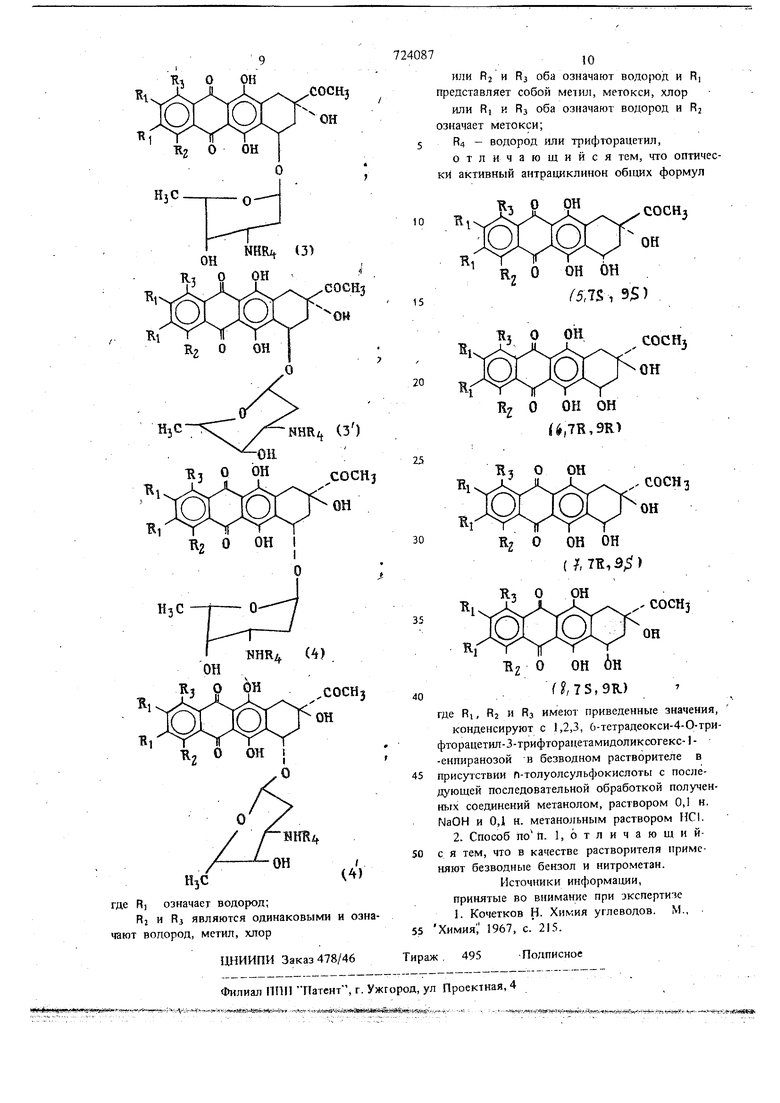
где RI , Rj и Ra имеют указанные значения, конденсируют с 1, 2, 3, 6 теградеокси-4-0-1рифторацетил-3-1риф|орацетамидоликсогекс-1-екпиранозой в безводном растворителе в присутствии n-толуолсульфокисдоты с последующей последЪвательной обработкой полученных соединений метанолом, раствором 0,1н. NaOH и ОДнметанольным раствором НС1. В качестве растворителя обычно применяют безводные бензол или нитрометан. Целевой продукт выделяют известными приемами. Приводимые далее примеры не оУраничивают объема изобретения. Ссылка на дауномици ноны относится к антрациклинонам, которые имеют такую же конфигурацию, что и естественный дауномицинон (7S ; 9S), и ссылка на 7,9-бис-эпидауномициноны - к антрациклинонам с 7R : 9R конфигурацией. Продукты получаемые в примерах, являются новыми соединениями за исключением самого антрациклинона. Пример 1. а-(-)-Дауносаминил-4-диметоксидауномицинон 4-диметоксидауномицин) -гидрохлорид(1, RS R4-H) и |3-(-)-да носаминил-4-демето ксидауномицинон (р-4-диметоксидауномицин)-гидрохлорид (1, ).. Kir 4-деметоксидауномицинона в 200 мл бензола добавляют 3 г 1,2,3,6-тетрадеокси-4-Отрифторацетил-3-трифторацетамидог L-ликсогекс-1-енпиранозы и 30 мг п-толуолсульфокис лоты. Раствор в темноте нагревают 8 ч с обратной флегмой. Добавляют 0,1 мл пиридина и раствор упаривают в вакууме. Остаток погл щают хлороформом и, промывают водой и 5%-ным rJaHCOj. Растворитель упаривают в вакууме, остаток растворяют в 350 мл метанола и оставляют стоять на ночь при комнатной температуре. После отгон ки растворителя остаток хроматографируют на 20 г силикагеля, причем сначала элюируют хлороформом и затем смесью хлороформ: ацетон (19:1); при этом получают 0,6 г о-(-)-дауносаминил-4-деметоксидауномицинон-Г 1-трифторацетат(1, R, H,R4 COCF3), т.Ш1. 155158° С, а -1-200° (с 0,1 в диоксане), и 0,30 г 0-(-)-дауносаминил-4-деметоксидауномицинон-М-грифторацетата (1, ,R4 СОСРз), т.пл. 148-150°С а +100° (с 0,Г в диоксане). Соединение формулы 1 (R,, R4 СОСРз) растворяют в 40 мл 0,1 н. NaOH и 30 мин вьщерживают при комнатной температуре. Раствор с помощью HCI доводят до рН 8 и экстрагируют хлороформом. После отгонки растворителя получают остаток, который поглощают небольщйм количеством смеси хлороформ/метанол, добавляют 0,1 н. метанольный раствор HCI до рН 4,5, после чего добавляют достаточное количество этилового эфира для осаждения гидрохлорида о- (-) -дауносаминш -4-деметокси дауномидинона(4-деметоксидауномицин) (l, ), 0,35 г, т.пл. 183-185 +210° (с 0,1 в СПзОН). Из соединения 1 (R,, R4 СОСРз) аналогичным образом получают гидрохлорид -(-)-дауносаминил-4-деметоксидауномицинон ((3-4-деметоксидауномицин) (2, R,), а +124° (с 0,1 в этаноле). П р и м е р 2 а:-(-)-Дауносаминил-4-деметокси-7,9-бис-эпидауномицинон (а-7,9-бис-эпи-4-деметоксидауномицин) - гидрохлорид (2, ) и/3-{-)-дауносаминил-4-деметокси-7,9-бис-дауномицинон (/3-7,9-бисэпи-4-деметоксидауномицин)-гидрохлорид (2, R,). Путем конденсирования 4-деметокси-7,9-бис-эпи-дауномицинона с 1,2,3,6-тетрадеокси-4-0-трифторацетил-З-трифторацетамидо- L-ликсогекс-1-ерпирано:юй, как описано в примере 1, получают «-7,9-бис-эпи-4-деметоксидауномицин-М-трифторацетат (2 Rj R2 R3 Н, R, СОСРз),. 210-215 С а -91° (с 0,1 в диоксане) вместе с /3-7,9-бис-зпи-4-деметоксидауномицин- N- трифторацетатом (2, R,, R4 COCF3), т.Ш1. 165 167°С а -91 (с 0,1 в диоксане). Эти соединения путем хроматографии на силикагеле при применении хлороформ : ацетон (80:20 по объему) в качестве элюирующего средства разделяют. . Последующий гидролиз соединений 0,1 н. NaOH, как описано в принтере 1, дает гидрохлорид а-7, 9-бис-эпи-4-деметоксидауномицин (2, R,), Т.Ш1. 205-207°С, о -80° (с 0,1 в СНзОН) и гидрохлорид -7,9-бис-эпи-4-деметоксидауномицин (2, ), Т.Ш1. 186-187°С, 250° , (с 0,1 в СНзОН). П р н м е р 3. 1-Метоксидауномицин-гвдрохлорид (1, , ). При проведении способа по примеру 1, но с применением 1-метоксидауномИцинона, получают указанное соединение, т.пл. 195°С, М +200° (с 0,1 в СНзОП), выход 25%. . Пример 4. 4-Дeмeтoкcи-l,4-димeтилдayнoмицин-гидpoxлopид (1, , СНз). При проведении способа по примеру 1, но при применении 4„-деметокси-1,4-диметилдауномицинона получают указанное соединение, т.пл. Т83-185°С, +-175° (с 0.1 CHjOH), выход 30%. П р и м е р 5. 4-Деметокси-1,4-диметнл-7,9-бис-эпидауномшщн-гидрохлррид (2, , ). При проведении способа по примеру I, но при применении 4-деметокси-1,4-димегил-7,9бис-эпидауномицинока получают укачанное (соединение. П р и м е р 6.4-Деметоксн-1,4-дихлордауномицин-гидрохлорид (1, , ). При Проведении способа по примеру 1, но при применении 4-деметокси-1,4-дихлордауноми1шнона получают указанное соединение,j т.пл. 184-185°С +175°, выход 27% (с 0,1 СНзОН). П р и м е р 7. 4-Деметокси-1,4-дихлор-7,9-бис-эпидауномицин-гидрохлорид (2, , R2 ).. .10 При проведении способа по примеру 1, не с применением 4-деметокси-1,4-дихлор-7,9-бис-эпидауномицинона получают указанное соединение. П р и м е р 8. 4-Деметокси-2,3-диметил- is дауномицин-гидрохлорид (1, , ). При проведении способа по пр1имеру 1, но с применением 4-деметокси-2,3-диметилдауномицинона выделяют о:-4-деметокси-2,3-диметил- 20 дауноми1ш -М-трифторацетат (1, , R2 , R4 COOF3), т.пл. 233-235°С, а + 181° (с 0,1 в диоксане), из которого путем последующего тидролиза 0,1 н. NaOH получают гидрохлорид а-4-деметокси-2,3-диме- 25 тилдауномицина (1, , )H), Т.Ш7. I90-192°C +180° (с 0,1 в СНС1з) . выход 35%. П р и м е р 9. 4-Деметокси-2,3-диметил-7,9-бис-эпидауномицин-гидрохлорид (2, СНз, ). При проведении способа по примеру 1, но с применением 4-деметокси-2,3-диметил-7,9-бис-эпидауномицииона получают указанное соединение.35 Пример 10. 4-Диметокси-2,3-дихлордауномицин-гидрохлорид (1, , Н). При проведерши способа по примеру 1, но с применением 4-деметокси-2,3-дихлордауно- 40 мицинона выделяют а-4-деметокси-2,3-дихлордаупомицин N-трифторацетат (1, ,, R5 COCF3), т.пл. 238-240°С а +170° (с 0,1 в диоксане), из которого путем последующего гидролиза 0,1 н. NaOH получают 45 гидрохлорид а-4-деметокси- 2,3-дихлордауномицина (1, R, С1, ), а +180° (с 0,1 в СНзОН), т.пл. 258-260°С, выход 23%. Пример 11. 4-Деметокси-2,3-дихлор-7,9бис-эпидауномицин-гидрохлорид (2, ,50 R R R4 ) При проведении способа по примеру 1, но с применением 4-деметокси-2,3-дихлор-7,9бис-)пидауномицинона получают указанное соединение.55 Формула изобретения 1. Способ nojryMeHHH гилрохлорида оптически активных дауносаминилпроизводных антра


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гидрохлоридов оптически активных антрациклинонгликозидов | 1976 |
|
SU646914A3 |
| Способ получения оптически активных антрациклинонов | 1977 |
|
SU776557A3 |
| Способ получения гликозидов антрациклина | 1976 |
|
SU1014477A3 |
| ПРОИЗВОДНЫЕ АНТРАЦИКЛИНОНА И ИХ ИСПОЛЬЗОВАНИЕ ПРИ АМИЛОИДОЗЕ | 1995 |
|
RU2167661C2 |
| СПОСОБ ПОЛУЧЕНИЯ 4-ЗАМЕЩЕННЫХ АНТРАЦИКЛИНОНОВ | 1989 |
|
RU2071463C1 |
| Способ получения антрациклиновых гликозидов | 1986 |
|
SU1553015A3 |
| 4-ЗАМЕЩЕННЫЕ АНТРАЦИКЛИНОНЫ И ГЛИКОЗИД АНТРАЦИКЛИНА | 1991 |
|
RU2024483C1 |
| Способ получения рацемических аглюконов | 1983 |
|
SU1311616A3 |
| АНТРАЦИКЛИНОВЫЙ ГЛИКОЗИД И СПОСОБЫ ЕГО ПОЛУЧЕНИЯ | 1990 |
|
RU2073681C1 |
| Способ получения хлоргидратов замещенных антрациклинов | 1979 |
|
SU867315A3 |


Авторы
Даты
1980-03-25—Публикация
1977-10-11—Подача