XI
Изобретение относится к способу получения новых соединений - гидрохлоридов оптически активных антрациклинонгликозидов, обладающих ценными фармакологическими свойствами.
Основанный на известной реакции образования гликозидной связи , предлагаемый способ получения гидрохлоряда оптически активных антрадиклинон-гликозидов общих формул
о ОЛ
, ОН
liHKi
он
R, О Oft
,COdllg
ОН
R, О ОН О
И
о он
11.-1
СОСНз он
BHR4
Q ОН
III
COOHj
он
«HR4
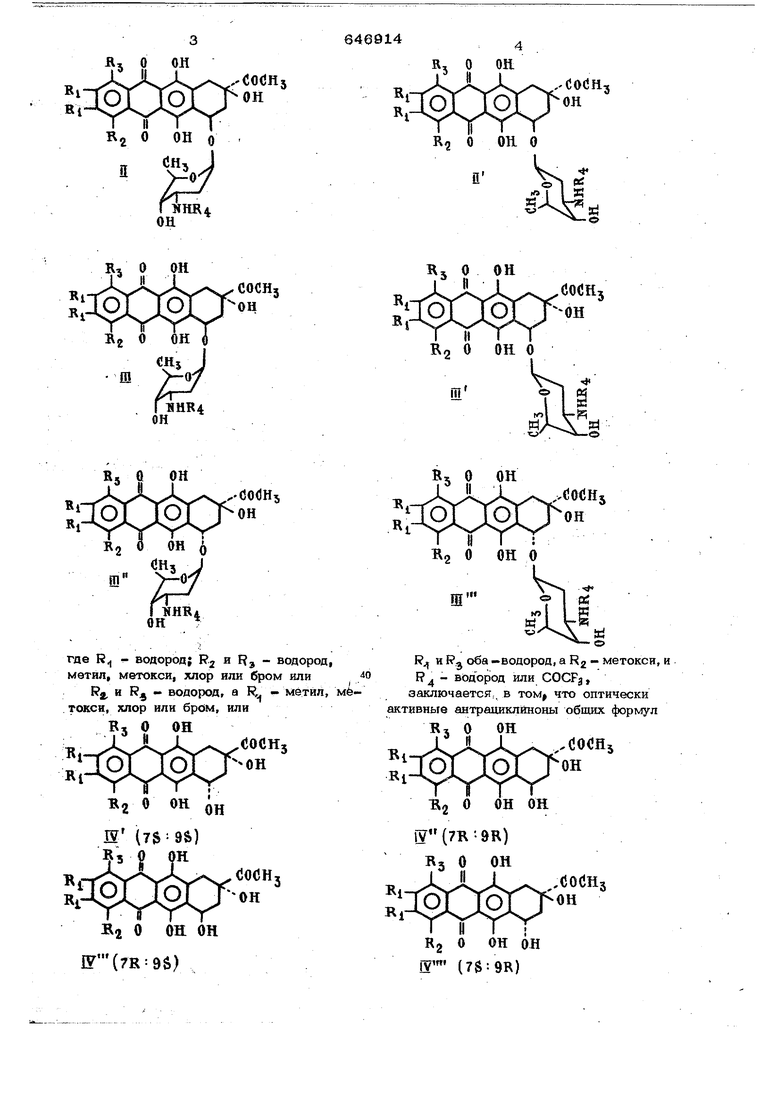
где R водородf R.j и R, - водород, метил, метокси, хлор или бром или
, и RJ - водород, а R, - метил, токси, хлор или бром, или
БЗ О ОН
}ОСШ
2
Ш () Ви О ОН
JOCHД2 о он он
iY(7R 9S)
Кч о он
сосн,
Rz О
R и Rj оба -водород, а R2 - метокси, и R - водород или COCFg, заключается,, в том что оптически активные антрациклйноны общих формул ОН
,.( ОН
он он
W(7R-9R)
R
,,СОСНз
он
R2 О ОН ОН
(7S:9R)
где I , и Sj имеют вышеуказанные значения, подвергают взаимодействию с 1,2,3,6-тетрадеокси-4--О-трифторацет1Ш-З- рифторадетиламидо- Ь -ликсо-гексен-1-йираноэой в безводном бензоле или нитрЪметане в присутствии п-толуолсульфокислоты, полученное 7-(4 -О-трифторадетил-3 -трифторацетамидо- L -ликсо-пираноаш1)нлроизводное обрабатывают метанолом, затем в случае необходимости удаляют трифторацетильные защитные группы гидролизом 0,1 н.раствором едкого натра и полученное основание обрабатывают 0,1 н.метанольным раствором соляной кислоты.
Пример 1.К 4-даметоксидауномицинону (VJ, где ,) (1г) в бензоле (200 мл) добавляют 1,2,3,6-тетрадеокси-4-0-трифторадетил- -трифторадетамидо- L -ликсо-гексен-1-пиранозу (3 г) и п-толуолсульфокислоту (30 мг).
Раствор нагревают 8 ч с обратным холодильником в темноте, добавляют пиридин {О,1 мл) и выпаривают в ваку-уме. Остаток растворяют в хлороформе, отмывают водой и 5%-ным раствором бикарбоната натрия. Растворитель выпаривают в вш :ууме, остаток растворяют в метаноле (350 мл) и оставляют на ночь при комнатной температуре. После , выпаривания растворителя остаток хро Матографируют на силикагеде (2О г), элюируя вначале хлороформом, а затем смесью хлороформ -ацетон (19:1){ и получают 0,6 г cd -(-)-даунозаминил-4-деметоксидауномицинон- N-трифтораие- тата (I, где Ri-. . т,Ш1. 155-158°C;tot +20О с 0,1 дноксан), и 0,3 г |3-(-)-изомера (J где R, а-Н; R iCOCF 5 т.пл 148-15О°С; о(.3 1° +1ОО (сО,, диоксан). Полученный трифторацетат растворяют в 40 мл О,1 н.раствора едкого натра, выдерживают 30 мин при комнатной температуре, добавляют соляную кислоту до рН 8 и экстрагируют хлороформом. После выпаривания растворителя остаток помещают в небольшое количест- во смеси хлороформ-метанол; 0,1 н.метанольный раствор соляной кислоты добавляют до рН 4,5, затем приливают этиловый эфир до осаждения гидрохлорВДа (-).5Даунозаминил-4-деметоксидауномидинона (4тдеметоксидауномидин, X где R, ). Выход О,35 г; Т.Ш1. 183-185 C; ci. +210° (,1, метанол). Аналогичным образом
псшучают гидрохлорид jS -()-даунозаминил-4-дёметоксидауномицинона ( р-4-деметоксидауноминин, J, где R,-, ),Ы 1,° (,1 этанол).
Для 4-деметоксидауномицина . 256, 460, 486, 52О нм.
В примерах 2-19 проводят опыт, как ъ примере 1.
П р и м е р 2, При конденсации 4-деметокси-7,9-бис-эпи-дауномицинона (IV, где ) с 1,2,3,6-тетрад еокси-4 0-трифторадетил-3 -трифторацетамидо- U -ликсо-гексен-1-пиранозой получают сзС -7,9-бис-эпи-4-деметоксвдауномицин-N-трифторадетат (Д , где R,.p.j Рд-СХ)СРз), Т.ПЛ. 210-215 Сг СоСДд (,1 диоксан), и р, -изомер i где , 1 4 СОСР|), Т.ПЛ. 165-16 rolj -270 (с
ЮД, диоксан).
ti - и |Ь -Изомеры разделяют на колонке с силикагелем, элюируя смесью хлороформ - адетон (80:20) по объему). После гидролиза получают гидрохлорид
oL -7,9-бис-эш1 4-деметоксидауномицина (f , где R, т.пл. 205 207 С;Го13 -80 (,1, метанол), и гидрохлорвд Э ,9-бис-эпи-4-деметоксидауномицина (|, где R, Р -Rj-1 4.-Н), Т.ПЛ, 185-187 С;Г АЛ -250С (,1, метанол).
П р ер 3, Гидрохлорид 7,9-бис-эпи-д номицина (|, где Р «-Р R,-OCH) получают из дауномицинона. Пример 4. Гкдрохлорид 1-метоксвдауномиыйна (I , где Н; R -Rj-OCHj), получают из 1-метокскдауномицинона (Sv, где R jcHiRa Ps i
Пример 5, Гидрохлорид JL-метокси-7,9-бис-эпи-дауномивдша (| , где , RjsRjaOCH,) синтезируют, исnoJbaya в качестве исходного соединения 1-метокси-7,9-бнс-эпи-дауномидинон (IV, где ,).
П р и м е р 6. Гидрохлорид 4-деметокси-1,4-йиметилдауномиаина (I, где ) получают, исходя из 4-деметокси-1,4-йЯметилдауномицинона (IV( где R,H; R2-Rj CH,). Для целевого продуктаЛ; „.256, 472,495, 530 нм..
Пример 7. Гидрохлорид 4н емвтокси-1,4 йиметил-7,9-биc-aпи- ayнoмидана (1 , где R.R,CH3) синтезируют из 4-деметокси-1,4; диметял-7,9-бис-эпи-дауномишгаона ОУ, где R.). Прим ер 8. Гидрохлорид 4-двмвт окси-1,4-лихлордауномицина (I, где Р ) получают из 4--. .еметоксвч1,4 вхлораауномицшона j , гдв R,eH; RjsRjT :;); Для целевого про дукта Д 262, 48О, 508, 545 нм. Пример 9. Гидрохлорид 4-де-метокси-1,4-дихлор-7,9-бис-эпигяауно, мяцииа (| , где .nO лучают, исходя на 4-деметокси-1,4-ди хлор-7|9-бис-эпидауномицинона (W , где ,Ce). Пример 10, Гвдрохлорвд 4-деметокси-1,4-дибромдауномицина (1,гдв Rj R ssBt-) получают, используя в качестве исходного соединения 4-деметокси-1,4-йнбр6мдауномицинон (,гдв R-jfia-Bh). Пример 11. Гидрохлорид 4-деметокси-1,4-дибром-7,9-5ис-эпи-дауномицина (| , где ) получают иэ 4-дeмeтoкcи-l,4-дибpoм 7i9r-биc-aпи-flayнoмицинoнa (wt где R.). Пример 12. Гидрохлорид 4-деметокси-2,3-диметилдауномиш1на (1 , где R aCHj; 2 R3-R4 H) синтезируют, исходя из 4-дегаетокси-2,3-Дйметипдау. ромвдинона (ivi где R.j5.p.H). После гидролиза оС - -деметокси-2,3-димэтилдауномишш- Ы -трифторацетата (I , где , R4 COCFj), . 233-235С, +181 (с- Ю,1, диоксаи), получают гидрохлорид -4-деметокси-2,3-дкметилдауномицина, Т.ПЛ. 190-192 0; dlj +180° (с°Ю,1, метеиол). Для 4-деметокси-2,3-.диметилдауномицинаАд д с 268, 458, 485, 528 нм. Пример 13. Гадрохлорид 4-деметокси-2,3 -ди метш1 7,9- бис-эпи-д аун мицина (I , где R aCHj; ) получают из 2,3-диметил-7,9-бис-эпи«ваУномицинона (IV, где R,CHj Rx RffJX, Пример 14. Гидрохлорид 4-деметокси 2,3-диметоксидауномицина (I где R -OCHj; ) синтезируют, исходя из 4-деметокси-2,3-дим оксидауномицинона (IV { .где .; Rj.H). Пример 15. Гидрохлорид 4-деметокси-2,3-диметокси-7,9-бис-эпи-дауномицина (Н , где ; е-Н) получают из 4-деметокси-2,3-диметокеи-7,9-.6ис-эпи-дауномицинона (|у, где -Н). П р и м ё р 16. Гидрохлорид 4-деметокси-2,3-аихлордауномицина (I ,где J .) получают из 4-аеметокси-2,3-дихлордауномицинона (IV, где R jdPj-ssH) через oL-4-деметокси-2,3-дихлордауномицин- N-трифтор- i ацетат ( I, где Р. :Н; R СОСРэ), Т.ПЛ. 238-240 C; :dj2j +170 с г 0,1, диоксан). Для гидрохлорида dL-изомера ciJ +170® (,1 метанол). Для 4-деметокси-2,3-дйхлордауномицинаЛ 272, 466, 494, 53О нм, Пример17, Гидрохлорид 4-демето$сси-2,3-дихлор-7,9-бис-эпи-дауномицина (н , где 1 i Р д Н) получают, используя в качестве исходного соединения 4-деметокси-2,3-дихлор-7,9-бис-эпи-дауномицин (IV. где R, -се; ). При м ё р 18. Гидрохлорид 4-деметокси-2,3-дибромдауномицина (I, где RI -Вг; Rj-Р| R4-Н) синтезируют из 4-деметокси-2,3-дибромдауномицина {IV где ), Пример 19. Гидрохлорид 4-деметокси-2,3-дибром-7,9-бис-эпи-д ауномицина (I , где ) получают, исходя из 4-деметокси-2,3-дйбром-7,9-бис-эпи-дауномицинона ( , где ). Фор. мула изобретения Способ получения гидрохлоридов оптически активных антрациклинон-гликозидов общих формул
О ОН
11I
,dOCH5 ОН
СОСИ
3
О ОН
,
СНч J
RS о он
к« о он о
о
I «
S
и
о
в, о он
RS О ОН
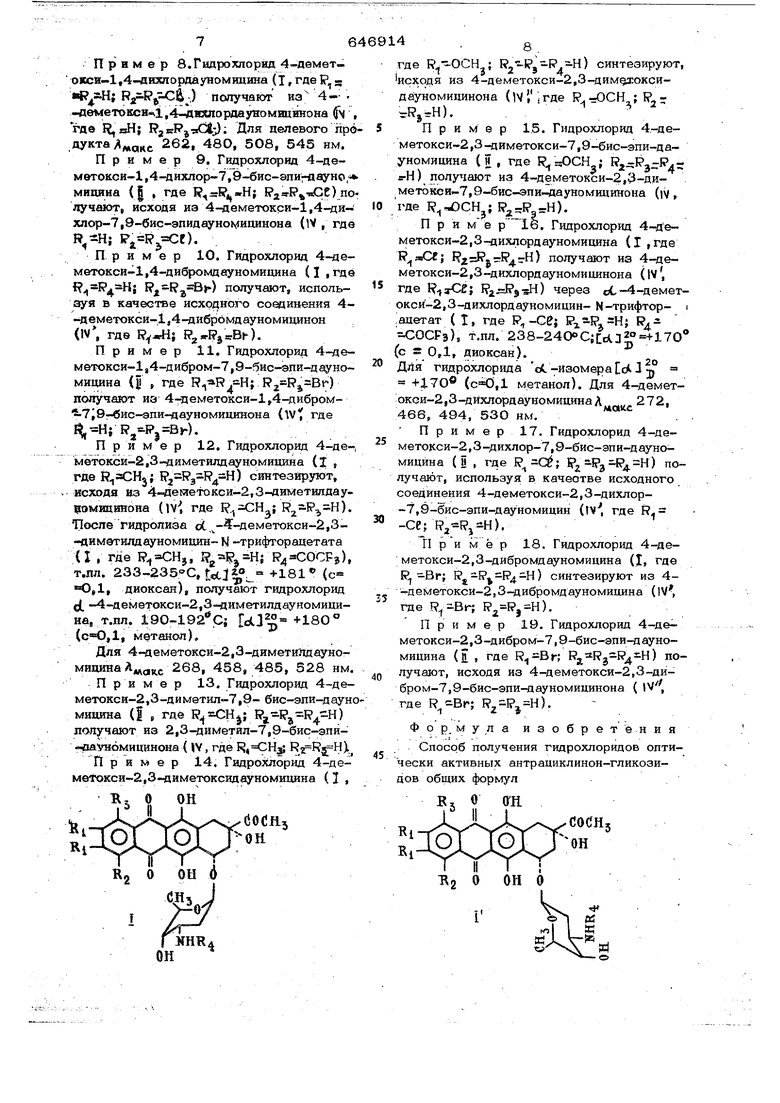
где R - водород; R и Rj - водород, метил, метокси, хлор или бром, или R и RJ оба являются водородом, а R метил, метокси, хлор или бром, или
Rj О ОН
doCHj -он
R2 о он он
Ш (7&:9§) RS О ОН
,
О ОН ОН S ()
Р И R- оба являются, водородом,а 1 метокси R J. - водород иди COCF , о т- личающий с я тем, что оптически активные антрацикпиноны общих формул
..СОСНз
он
он он
fV (7R-9H)
,,СОСНз
он
он он
S (7S :9R)
гае Ri|, f,, R имеют вышеуказанные зяачения, подвергают взаимодействию с 1,2,3,6-тетрад еокси-4-Оттрифторацетил -3-трифторадетиламвдо- i - иксо-гексен -1--п11реюеэрй в безводном бензоле или нмтрометсше в присутствии И -толуолсудьфокислоты (,полученное 7-(4;|-0-трифторааетил-З -трифтораиетамидо- Ь-ликсо виравоэил)-производное офабатыва IOT метанолом, с последующим в случае
необходимости снятием трифторацётильных защитных групп гидролизом 0,1 н. NaOH и полученное основание обрабатывают 0,1 н.метанольным раствором соляной кислоты.
Источники информации, принятые во внимание при экспертизе
1. Н. Кочетков и др. Химия углеводов, М., Химия, 1967, с. 208.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения гидрохлорида оптически активных дауносаминилпроизводных антрациклинонов | 1977 |
|
SU724087A3 |
| Способ получения оптически активных антрациклинонов | 1977 |
|
SU776557A3 |
| Способ получения гликозидов антрациклина | 1976 |
|
SU1014477A3 |
| Способ получения оптически активных антрациклинонов | 1977 |
|
SU650498A3 |
| СПОСОБ ПОЛУЧЕНИЯ ГИДРОХЛОРИДА АНТРАЦИКЛИНгЖ5^ИДА | 1977 |
|
SU826956A3 |
| Способ получения гидрохлорида 4 -эпи-6оксидауномицина | 1975 |
|
SU646913A3 |
| Способ получения гликозидов антрациклина | 1976 |
|
SU728719A3 |
| Способ получения аналога дауномицина или его хлоргидрата | 1975 |
|
SU645588A3 |
| Способ получения гликозидов антрациклина | 1980 |
|
SU993822A3 |
| Способ получения гликозидов | 1979 |
|
SU963471A3 |


Авторы
Даты
1979-02-05—Публикация
1976-12-03—Подача