Заместитель у фенильного кольца может находиться в орто-, мета- или ггараположении. . Пиридильный радикал может быть связан с пиперазиназотом в 2-, 3или 4-положении. Новые соединения получают путем взаимодействия триазолотиенодиазепи ИОВ общей формулы 11 23.. где R и R имеют вышеуказан-ные зна чения и Н-а&.-/атом галогена, с пипе разином общей формулы III О ;где R имеет вышеуказанные зйачения Вза:имодействие соединений общей формулы II с пиперазином формулы II .проводят без растворителя или в бо-лее..высок.окипящих растворителях таких как бензол, тОлуол, дйоксан, те рагидрофуран, хлорпроизводные угЛев iQOpoflOB,. например четырёххлорнстый углерод:, илй ;метиленхл6рйд, прёдпо.чт тельно при температуре кипения соот ветствующего .растворителя. Время ре акции зависит от используемогоисхо його Материала .и мржёт составлять о йесксЗлькйх минут до . нёскольких часов ...Те целевыепродукты об14ейформулы 1,-в которых R означает йодород аЛКил;.окСиалкил, галойдалкил или д алкйламиноа.пкил, образуют стабильные водорастворимые, соли. Для солеобраз вания пригодны все кислоты, образую щие физирлогически переносимые кисЛОтйоаддитивные сОли,,; такие как гал гёнводородные кислоты, -.серная, фосфорная, азотная, цйклогексилсульфами новая, лимонная,. винная, аскорбинова малеинОвая/ муравьиная, салицилов.ая кислоты, метан-, или тОлуолсульфокис лбта.-, . : Таким способом могут быть получен целевые продукты,, в случае необходи мости ё виде |)изирлогически-. переносимой кислотноаддитивной соли: . 8-б ом-6-(о-хлорфенил)-1- N-{п-хлорфенил) -пиперазинил -4Н-3-триазоло 3 ,4-с тиено.12 ,3-е 1, 4-диазепин 8-бром-б-(о-хлорфенил)-1-(N-фенил пиперазинил) -4H-S -триа.золо 3 ,4-с J тиено12,3-eJl,4-диазепин; 8-бром-6-(о-хлорфенил)(оТ Олил) -пиперазинил -4Н-3-триазоло 3 ,4-cJ тиено 2 ,,4-диазепин; 8-бром-б-.(о-хлорфенил)(о.т-хлорфенил) -пиперазинил -4Н-3-трйазоло 3,4-с тиенЬI2,,4-диазепин 8-бром-6-(о-хлорфенил)(2-метоксифенил)-пиперазинил -4H-S-триазолр 3,4-с тиено 2,,4-диазепин;8-бром-б-(о-хлорфенил)(п- фторфенил) -пиперазинил -4Н-5-триазол о 3 ,4-с тиено 2 ,3-е 1, 4-диазепин, 8-бром-б- (о-хлорфенил) -1- N-(2-гидроксизтил)-пиперазинил -4H-S-триазоло 3,4-с тиено 2,,4-диазепин ..... 8-бром-б-(о-хлорфенил)(о-нитрофенил) -пиперазинил -4Н-3Триазоло 3,4-с тиено 2,,4-диазепин; 8-бром-б-(о-бромфенил)-1-(N-фенилпиперазинил) -4Н-Б-гтриазоло 3 ,4-с тиено12,3 е 1,.4-диазепин; . . -; 8-бррм-б-(о-бромфенил)(2-пиридил)-пиперазинил -4Н-3-триазоло 3 ,4-с тиено 2 ,3-е 1, 4-диазепин; 8-хлор-б-(о-хлорфенил)(3-пиридил)-пиперазинил -4Н-5-триазоло 3,4-с тиено 2,,4-диазепин; 8-бром-б-(о-хлорфенил)(4.-пиридил).-пиперазинил -4Н-.5-триазоло 3 ,4-с тиено 2,3-е 1, 4-диазепин; 8-бром-б-(о-фторфенил)-пиперазинил- 4Н-3-триазоло 3 , 4-с тиёно 2, 3-е 1,4-диазепин; 8-метил-б-(о-хлорфенил)-1-(N-метилпиперазинил)-4Н-3-триазоло 3,4-с тиено 2 ,,4-диазепин; 8-бром-б-(о-хлорфенил)-1-(N-этилпиперазинил)-4Н-3-триазоло 3,4-с тиено 2 ,,4-диазепин; 8-бром-б- (о-хлорфенил) -1- (N-изопропилпйперазинил) - 4Н-3-триазоло 3 ,4-с тиено 2 ,,4-диазепин; 8-бром-б-(о-бромфенил)-1-пиперазинил-4Н-3-триазол6 3,4-с тиено 2 ,3-е 1,4-диазепин; 8-бром-б-(о-хлорфенил)-1-IN-(р-гидроксиизопропил) -пиперазинил. -4Н-3-триазоло 3,4-с тиеноС 2 ,,4-диазепин; . . 8-бром-б- (о-хлорфёнил) -Д- N- С/3-хлб)этил) -пиперазинил -4Н-3-триазоло 3 ,4-с тиено 2 ,,4-диазепин; 8-хлор-б- (о-хлорфенил) -1-пиперазинил-4Н-3-триазоло 3 ,4-с тиено 2 ,3-е 1,4-диазепин; . 8-бром-б- (о-хлорфенил) -1- N-(5-диметиламиноэтил)-пиперазинил -4Нг-3-триазоло 3 ,4-с тиено 2 ,3-е 1, 4-диазепин; . 8-бром-б-(о-хлорфенил)(диметиламинометил)-пиперазинил -4H-S-трйазоло13,4-с тиено 2 ,,4-диазепин;8-бром-б-(р-хлорфенил)-Г-Ы-формилпиперазино-4Н-3-триазолр 3,4-с тиейо 2 ,3-е 1, 4.-диазепин; .1-(N-ацётйлпиперазино)-8-бром-б- (р-хлррфенил) -4Н-3-триазоло 3 ,4-с тиено12 ,,4-диазепин; . 1- (N-аде.тйлпиперазинр) -8-зтил-б-(о-хлорфенил)-4Н-3-триазрло 3,4-с тиенр 2 ,3-е 1, 4-диазепин;,
. 1-(N-ацетилпиперазино)-8-хлор-6- (р-хлорфенил) -4Н-5-триазол.о 3 ,4-с тиено 2 ,,4-диазелин;
1-(Н-ацетилпипераэино)-8-бром-б-(о-фторфенил)-4Н-5-триаэоло 3,4-с тиено 2 ,,4-диазепин;
1-(Ы-ацетилпипераэино)-8-бром-6-(о-бромфенил)-4Н-8-триаэоло 3,4-с тиено(2 ,,4-диазепин;
8-бром-6-(о-хл6рфенил)-1- N-С -гидроксипропил)-пиперазинил -4H-S-триазоло 3/4-с тиено 2 ,,4-диазепин;
8,-бром-6-(о-хлорфенил) -1- (N-стеарилпиперазино)-4Н-8-триазоло 3,4-с тиено 2,,4-диазепин;
8-бром-1-(К-капроилпиперазино)-6-(о-хлорфенил)-4Н-3-триазоло 3,4-с тиено 2 ,3-е 1, 4-диазепин; .
8-бром-б-(о-хлорфенил)-1-(Ы-бензоилпиперазино)-4Н-3-триазоло 3,4-с , тиено 2,,4-диазепин;
В-бром-6-(о-хлорфенил)(л-фторбензоил)-пиперазино -4Н-5-три- азоло(3,4-с тиено 2 ,,4-диазепин;
8-бром-б-(о-хлорфенил)-1- N-{o-метилбензоил)-пиперазино -4Н-5-триазоло 3,4-с тиено 2 ,,4-диазепин;
8-бром-б-(о-хлорфенил)(о-хлорбензоил)-пиперазино -4Н-8-триазоло 3 ,4-с тиено. 2,3-е 1, 4-диазепин;
8-бром-б-(о-хлорфенил)(п-нитробензоил)-пиперазино -4Н-8-триазоло 3,4-с тиено 2 ,,4-диазепин;
8-бром-б-(о-хлорфенил)-1-(N-нйкотиноил-пиперйзино)-4Н-3-триазоло 3 ,4-с тиено 2 ,,4-диазепин;
8-бром-б-(о-хлорфенил)-1-(N-пиколиноилпиперазйно)-4Н-8-триазоло 3,4-с тиено 2,,4-диазепин; 1-(N-этоксикарбонилпиперазино)-8-бром-6-(о-хлорфенил)-4Н-8-триазоло 3 ,4-с тиено 2 ,,4-диазепин.
Исходные соединения общей формулы 11 известны из литературы.
Целевые продукты общейформулы I имеют ценные терапевтические свойства и могут быть применены в качестве подавляющёго страх средства, транквилизатора, седативного средства и нейроплегического средства. Главное действие при отдельных соединениях различно, т.е. у одного соединения преобладает нейроплегическое, у другого снотворное действие и так далее.
Так, например, соединения, в которых R означает низший алкильный радикал, -преобладают подавляющее чувст во страха действие. Они могут образовывать соли и в качестве соли являются водорастворимыми.
Те соединения с оксиалкилом,которые в виде соли являютсятакже водорастворимыми, имеют благоприятное действие на состояния бодрствование кошек, причем SWS (slow Wave sleep) удлиняется, состояние активного и ослабленного бодрствования-сокращается и фазы REM (rapid eye
movement) незначительно удлиняются или остаются неизменными.
Производные, в которых К означает ацил и гете.роацил, наряду с выраженным транквилизирующим и подавляющим чувство страха компонентами имеют также хорошее действие на реакцию избежания наказания (activeavoidance) крыс, а именно максимумы этих двух действий наблюдаются по
разным временам, сначала нейроплегйческая и затем подавляющее чувство . страха действия,
Также биохимическими методами можно доказать нейроплегические свойства ацилпиперазинилсоединений,
Новые соединения в частности пригодны для устрайения психомоторных состояний возбуждения и страха, выступающих, например, у больных шизофренией, и кроме того,, для лечения
спастических состояний и расстройства сйа, -
Соединения, в которых R означает водород, алкил, оксиалкил, галоидалкил или диалкиламиноалкил, наряду с
с тем могут быть переведены в стабильные водорастворимые кислотнрадцитивные соли, вследствие чего становится .возможным парентеральная дача и таким образом применение этих соединений в качестве наркотического средства короткого или ультракороткого действия.
Особенно эффективными оказались такие целевые продукты общейформулы 1, в которых R означает водород, алкильную или гидрбксйалкильную группу, фенильный или пиридил ный радикал или радикал R-СО-, К -хлор, R -бром и R -водород или метил. Разовая доза предлагаемого, вещества составляет 0,05-50, предпочтительно 0,1-25 мл (орально), и 5-150 мг дневная доза.. . . Пример 1, 8-Вром-б-(о-хлорфенил) -1- N- (2-оксиэтил) -пиперазинил -4Н-8-триазоло 3,4-с тиено 2,,3-диазепин.
0,07 моль (31 г) 1,8-дибром-б-(о-хлорфенил)-4Н-3-триазоло 3,4-с тиено
2,3 ,4-диазепина, 17 г(0,14 моль) N-(2-оксиэтил)-пиперазина и 800 мп ксилола в течение 24 ч нагревают с обратнымхолодильником. Отсасывают реакционную смесь еще теплой .над углем кизельгура и упаривают фильтрат в вакууме. Остаток поглощают в метиленхлориде .и раствор промывают водой. После сушкй И:упаривания получают 28,5 г (81% от теории) соединения; т.пл. 125-12бс (из уксусного эфира).
Основание суспендируют с помощью небольшого количества спирта и затем добавляют незначительный избыток насыщенного нее спирта. После добавления простого эфира кристаллизуется
хороши водорастворимый гидрохлорид : т.пл. 211-22оt: (разлосоединения;жение).. Аналогичным способом из растворен горячем спир±е основания добавдением 1 моль малеиновой кислоты винной кислоты соответственно метансульфокислоты получают соответствующие соли,с количественным выходом. точка плавления 201-202 0 г Тартрат: точка плавления 228-229 Метансульфонат. точка пдавления 241-242®С. . . .л I .Пример 2. 8-Бром-б-(о-хлорфенил)-1-пиперазинил-4н-3-триазоло 13,4-с тиено 2,,4-диаз епин. 0,01 моль (.4,5 г) 1,8-дибром-б-(о-хлорфенил)-4Н-3-триазоло 3,4-с тиено 2,3-е)1,4-диаэепина растирают с 0,02 моль (1,8 г) пиперазина и в те.чёние 15 мин нагревают до . Охлажденный расплав смешивают с метиле.нхлоридом и водой. После отделения водной фазы метиленхлоридный .слой экстрагируют с помощью ЮО мл 2 н. СОЛЯНОЙ кислоты. Экстракты подщелачивают аммиаком и реакционный продукт повторно поглощают в метилен хлориде. После сушки и упаривания получают из уксусного эфира 3,8 г (82% от теории) желаемого соединения;, т.пл. 246-248°С. Добавлением спи ртовой соляной кислОты получают гидрохлорид; т.пл. (разложение) . Пример 3. 8-Бром-6- (о-хлорфенил) (2-пиридил)-пиперазинил -4Н-8-триазоло 3,4-с тивно 2 ,,4диазепин. 0,04 моль (19 г) 1,8 дибpoм-б-(o-xлopфeнил) -4Н-5-триазоло 3 ,4-с)тиено 2,,4-диазепина с 0,08 моль (13,4 г) N- пиридил-(2)-пиперазина и 150 мл ксилола в течение 24 ч нагревают с обратным холодильником. Выделившийся гидробромид М- пиридил-(2)-пиперазина отсасывают. В фильтрате находится вышеуказанное соединение, которое упариванием и перекристаллизацией выделяют и очищают. Вы ход 13,2 г (61% от теории);т.пл. 215216С.. Согласно указанным методам получены соединения общей формулы I, привеДенные в таблице.


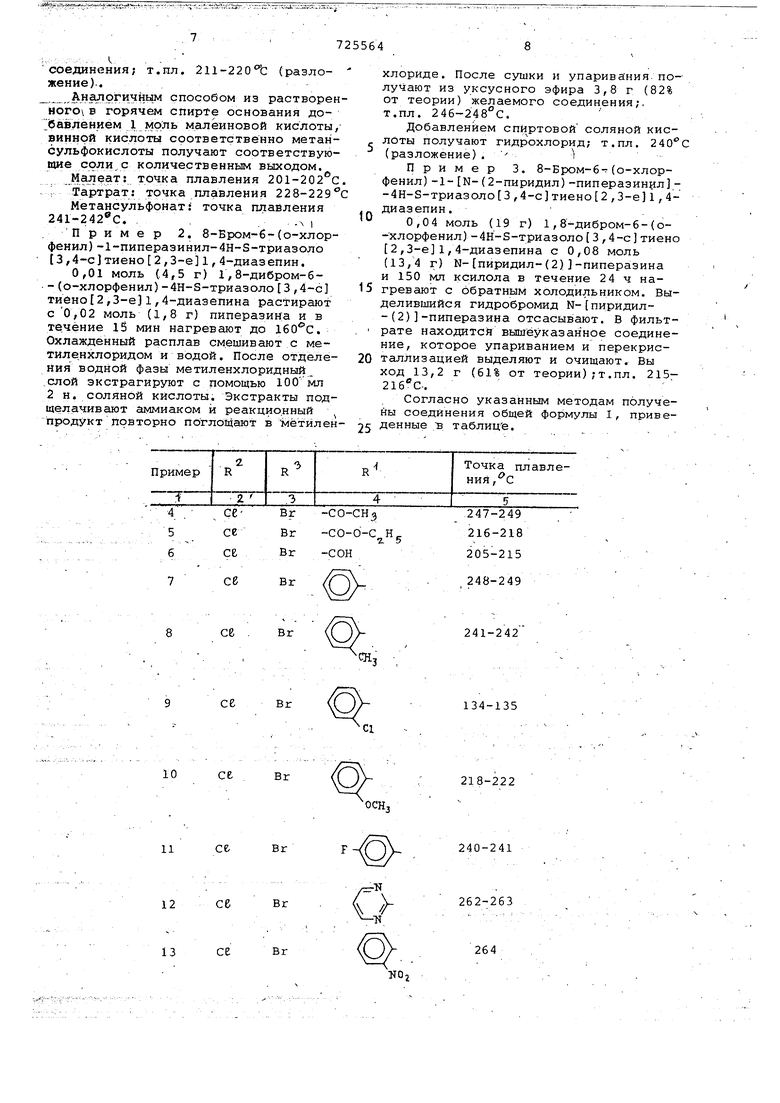
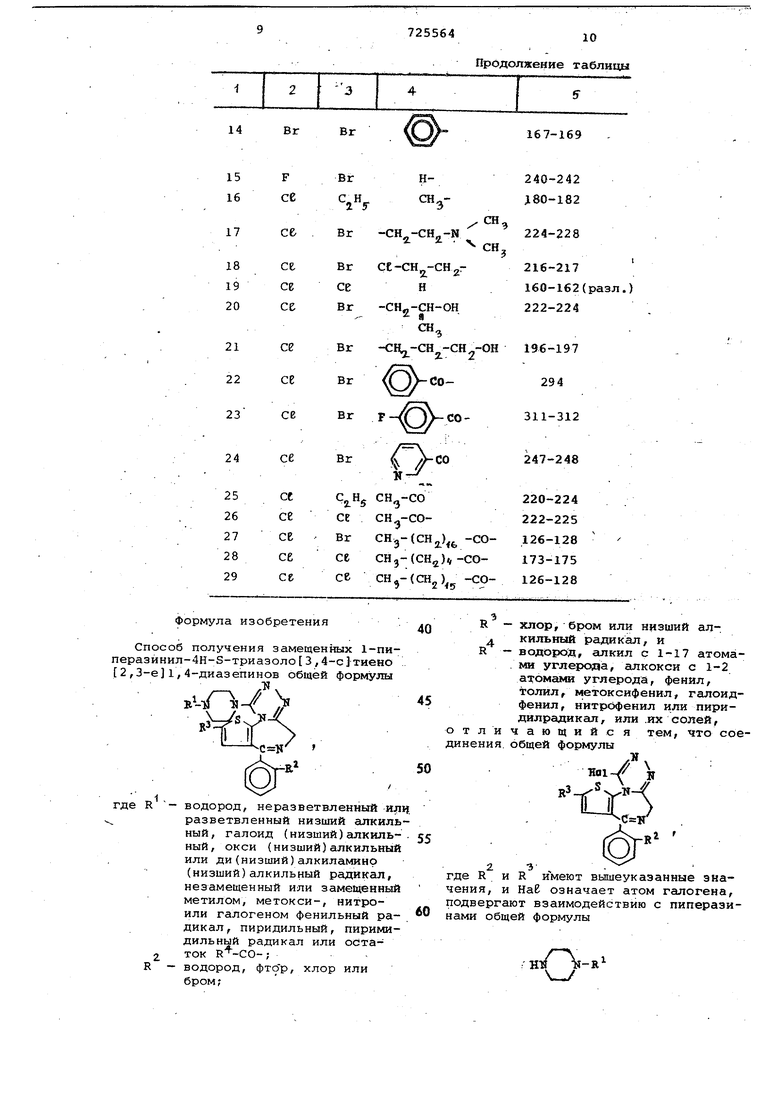


се
Вг
Вг
се
се
Вг
248-249
241-242
134-135
10
се
Вг
218-222
Вг
се
11
Вг
се
12
Вг
се
13
240-241
262-263
264
72556410
Продолжение таблицы
14Br
Br
167-169
F
Вг
се
SH
се
Вг
ВгCC-CH -CHgr
сг се се
сен
в г-CHg-CH-OH
Вг 196-197
се
С6
Вг
Вг
се
се
Вг перазйнил-4Н-3-триазоло 3,4-с тиено 2 ,,4-диазепинов общей формулы где R - водород, не разветвленный и.пч . разветвленный низший алкильный, галоид (низший)алкильный, окси (низший)алкильный или ди(низший)алкиламино (низший)алкильный радикал, незамещенный или замещенный метилом, метокси-, нитроили галогеном фенильный радикал, пиридильный, пиримидильный радикал или оста2 ток R -CO-; R - водород, фтсрр, хлор или бром
240-242
н- э Д80-182
/СН,
224-228
СИ,
216-217 160-162(разл.) 222-224
сн
294
СО311-312
СО247-248о ди гд ч по на с 1-17 атомами углерода, алкокси с 1-2 атомами углерода, фенил, толил, метоксифенил, галоидфенил, нитрофенил или пиридилрадикап, или .их солей, тли чающий с я тем, что соенения, общей формулы -W . Hoi-V 2 3 е R и R имеют вышеуказанные знания, и Наб означает атом галогена, двергают взаимодействию с пиперазими общей формулы .
;,.;;,:.; ,,,.,;, „ii.,,,.- ., . . -.. 725564 .12
где R ийеёТ .Вйшеукаээнные значения,Источники информации ,
&Ш 13 1 & КёШё1Л iieyfeuoroпринятые во внимание при экспертизе ntSOiiyKTa в свободном виде или в виде,1. Патент Великобритании №1410963,
f;Qjl кл. С 07 D 495/04, опублик. 1975.
Авторы
Даты
1980-03-30—Публикация
1978-07-19—Подача