Предлагаемые -соединения получают путем ацилирования соединения об1дей формулы где R и R имеют указанные значения, муравьиной кислотой или реакционноспособным производным. Кислоты общей формулы R -COOH, где R имеет указанные значения. Ацилирование соединений формулы галогенидом, соответственно ангидррдом карбоновой кислоты, может быть осуществлено с применением избытка ацилирующего средства или также в пригодном инертном растворителе, таком как диоксан, тетрагидрофуран, бензол, толуол или ксилол. В некоторых случаях целесообразно добавление неорганического или органического ос нования, например пиридина, триэтил амина, поташа или бикарбоната калия для удаления кислоты. Температуру и время реакции можно варьировать в широких пределах в зависимости от используемого исходного материала. Так температура реакции может лежат между комнатной температурой и точко кипения используемого растворителя, соответственно ацилирующего средства. Время реакции может составлять от нескольких минут до нескольких часов. Исходные соединения общей формулы ij могут быть получены, например путем взаимодействия соответственно замещенных 1-галоген 4Н-5-триаг Оло 4с тиено 2 , ,4-диазепинов с пипе разином или путем дегидрирования 1-пиперазинил-4Н-5-триазоло З , но 2 , Зе 5 , б-дигидро-1,4-диазепина. Целевые продукты общей формулы J имеют ценные терапевтические свойст ва и могут быть применены в качест ве подавляющего страх средства тран квилизатора, седативного средства и нейроплегического средства. Главное действие при отдельных соединениях различно, т.е. у одного соединения преобладает нейроплегическое, у дру го4о. снотворное действие и так далее . Данные соединения наряду с выраж нием транквилизирующим и подавляющи чувство страха компонентами имеют также хорошее действие на реакцию избежания наказания (active avoidan ce) крыс. Также биохимическими методами мо но доказать нейроплегические свойст ва ацилпиперазинилсоединений. Предлагаемые соединения поэтому в частности пригодны для устранения сихомоторных состояний возбуждения и страха, выступающих, например, у больных шизофренией и, кроме того, для лечения спастических состояний и расстройства сна. Разовая доза предлагаемого вещества составляет 0,05 до 50, предпочтительно 0,1 до 25 мг (орально), и 5 до 150 мг- дневная доза. Пример 1. 1-(N-Ацетилпиперазино)-8-бром-6-{о-хлорфенил)-4Н-5-триазоло 3,4с тиено С2,3е 1,4-диазепин. 4,6 г (0,01 моль) 8-бром-6-(о-хлорфенил)-1-пиперазино-4Н-5-триазоло З , 4 с тиено 2 , Зе 1, 4-диазепина в течение 20 мин перемешивают в 100 мл ангидрида уксусной кислоты. Выливают реакционную смесь на лед и подщелачивают аммкаком. Ацетильное соединение поглощают в метиленхлорие, метиленхлоридную фазу сушат и статок путем добавления простого эфира доводят до кристаллизации. ВЫ1СОД 3,8 г (76% теории); т. пл. 247-249°С. П р и м е р 2. 8-Бром-6-(о-хлор фенил) -1- (N-этоксикарбонилпиперазино) -4Н-vS-триазоло 3,4с тиено 2, Зе 1,4-диазепин. 4,6 г (0,01 моль) 8-бром-б-(о-хлорфенил) -1-пиперазино-4Н-5- триазоло З , 4 с тиено 2 , Зе 1, 4-диазепина перемешивают в течение 30 мин при комнатной температуре в 100 мл тетрагидрофурана с 2 мл этилового эфира хпормуравьйной кислоты. Упаривают, добавляют метиленхлорид, подщелачинаюг аммиаком и остаток от высушенной метиленхлоридной фазы подвергают хрома ографии на S i Q,-,, причем элюируют смесью из 98% метиленхлорида и 2% метанола. Выход 4,8 г (91% теории); т.пл. 21б-218 С. Rr-. 0,38 (пластинки из силикагеля типа 60 Р254Ф Р Мерк, ФРГ). Растворитель: метиленхлорид - метанол (95:5) . Пример 3, 1-(N-Формилпиперазино)-8-бром-6-(о-хлорфенид)-4H-S-триазоло 3,4с тиено 2,3е 1,4-диазепин. . 4,6 г (0,01 моль) 8-бром-б-(о-хлорфенил)-1-пиперазино-4H-S-триазоло Г3,4 с 1,4-диазепина в 100 мл муравьиной кислоты в течение 3 ч нагревают с обратньм холодильником. Вы-, лияают на лед, подщелачивают 2 н. натровым щелоком, поглощают формильное соединение в метиленхлориде и перерабатывают в метиленхлориде, сушат метиленхлоридную фазу и остаток доводят до кристаллизации путем добавки простого эфира. BbixoJ3 3 ,9 г (80% теории); т.пл. 205-215°С.
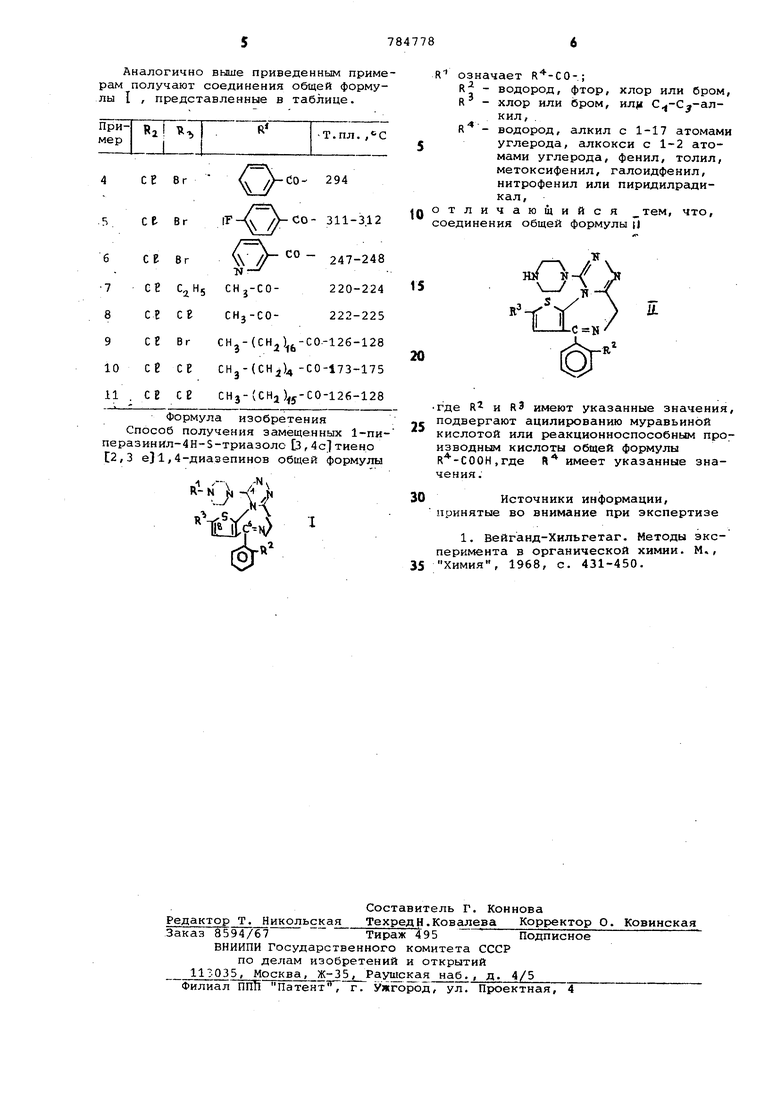
Аналогично выше приведенным примерам получают соединения общей формулы I , представленные в таблице.
R означает R-СО-;
R - водород, фтор, хлор или бром, R - хлор или бром, С -С -алкил, .
я - водород, ал к ил с 1-17 атомами 5 углерода, алкокси с 1-2 атомами углерода, фенил, толил, метоксифенил, галоидфенил, нитрофенил или пиридилрадикал,
отличаю1аийся тем, что, соединения общей формулы tJ
Q co247-248
СЕ Вг N-
СЕ С,Н5 CHj-CO220-224
-3
СЕ ееСНзСО-222-225
СЕ Вг CHj-(CH.l,.-126-128 се СЕ CHj-iCHi) -СО-173-175
11 . се СЕ CH3-(CHj)5-CO-126-128
Формула изобретения Способ получения замещенных 1-пиперазинил-4Н-5-триазоло 3,4с тиено С2,3 е)1,4-диазепинов общей формулы
01
43i
T-i:. иггде R и яЗ имеют указанные значения, подвергают ацилированию муравьиной
25 кислотой или реакционноспособным производным кислоты общей формулы Я -СООН,где Л имеет указанные значения.
Источники информации,
принятые во внимание при экспертизе
1. Вейганд-Хильгетаг, Методы эксперимента в органической химии. М,, Химия, 1968, с. 431-450.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения замещенных 1пиперазинил-4н- -триазоло/3,4-с/ тиено/2,3-е/-1,4-диазепинов или их солей | 1978 |
|
SU725564A1 |
| Способ получения производных 1,4-диазепина или их солей | 1975 |
|
SU583758A3 |
| Способ получения производных 1,4-диазепина | 1980 |
|
SU1056904A3 |
| Способ получения производных 1,4-диазепина | 1975 |
|
SU648104A3 |
| Способ получения производных тиенотриазолодиазепина или их кислотно-аддитивных солей | 1978 |
|
SU1060115A3 |
| Способ получения производных 1-пиперазинил-4н- -триазоло/3,4с/-тиено/2,3е/-1,4-диазепина | 1979 |
|
SU793402A3 |
| Способ получения замещенных -6-арил4н- -триазоло/3,4-с/тиено /2,3-с/-1,4диазепинов или их солей | 1976 |
|
SU622406A3 |
| Способ получения производных гетразепина | 1989 |
|
SU1738089A3 |
| СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ НАПРАВЛЕННОЙ ДЕГРАДАЦИИ БЕЛКА | 2020 |
|
RU2820673C2 |
| ПРИМЕНЕНИЕ ДИАЗЕПИНОВ ДЛЯ ПРИГОТОВЛЕНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ ИЛИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С ДЕЙСТВИЕМ ОДНОГО ИЗ РЕЦЕПТОРОВ СОМАТОСТАТИНА | 1999 |
|
RU2229299C2 |


Авторы
Даты
1980-11-30—Публикация
1979-04-04—Подача