(54) СШИТЫЕ СОПОЛИМЕРЫ ХИТОЗАНА


| название | год | авторы | номер документа |
|---|---|---|---|
| Биоспецифический полимерный адсорбент для выделения протеиназ (его варианты) | 1982 |
|
SU1137388A1 |
| СПОСОБ ПОЛУЧЕНИЯ ГЕМОСОВМЕСТИМЫХ ПОЛИМЕРНЫХ ГИДРОГЕЛЕЙ | 1982 |
|
SU1078894A1 |
| ИОННЫЕ МОЛЕКУЛЯРНЫЕ КОНЪЮГАТЫ N-АЦИЛИРОВАННЫХ ПРОИЗВОДНЫХ ПОЛИ(2-АМИНО-2-ДЕОКСИ-D-ГЛЮКОЗЫ) И ПОЛИПЕПТИДОВ | 1996 |
|
RU2172323C2 |
| Способ получения макропористых полимерных материалов | 1982 |
|
SU1008214A1 |
| АФФИННЫЙ АДСОРБЕНТ ДЛЯ УДАЛЕНИЯ ИЗ КРОВИ БИЛИРУБИНА И ДРУГИХ ТОКСИЧНЫХ ПРОДУКТОВ И СПОСОБ ЕГО ПОЛУЧЕНИЯ | 1978 |
|
SU731752A1 |
| Способ получения водонерастворимых протеиновых препаратов | 1973 |
|
SU576959A3 |
| Препарат фермента | 1977 |
|
SU687080A1 |
| Способ получения иммобилизованной глюкоамилазы | 1976 |
|
SU601286A1 |
| Модифицированный полимерами макропористый кремнезем в качестве носителя для дисульфидно-обменной ковалентной хроматографии белков и способ его получения | 1977 |
|
SU687081A1 |
| Полиациламидонитросалициловый альдегид как катализатор для рацемизации оптически активных аминокислот и способ его получения | 1976 |
|
SU657841A1 |

Изобретение атносится к получению сшитых полимеров, Известны сшитые подимеры хитозана СН,-СН,-СН-СН-СИ7-С J 2 г I г I CONH2 - амидная группа N- I пирролидонил , Сшитые полимеры указанной обшей формулы могут быть использованы в качестве носителей для иммобилизации ферментов. Известный полимерный носитель ферментов блоиль Р-300 обладает недостаточно высокой активностью. -CH Щ, аналированного малеиновым ангидридом, и вин ильных мономеров обшей формулы:I I -CH-CH-CHj-CHI I СООН Н Для повышения активности носителей для иммобилизации ферментов, а также расширения ассортимента полимерных носителей полимеры получают радикальной сопопимеризацией акриламида и винилпирролидона с малеильным производным хигозана, содержащим кратные связи. Это производное получают путем ацилирования хитозана, выделенного вз панцирей криля. Ацилирование проводят в формамиде при температуре от 2О до 6О®С. 37 Степень ацилироваиия получающегося производного может меняться в пределах от 5 до 1ОО%. Реакцию сополимеризации проводят в водном растворе или в среде органическо го растворителя (формамид, N ,N-диме- тилформамид), а также в водноорганических смесях. Для лучшего протекания процесса сополимеризацию проводят в атмоС фере инертного газа. Весовое соотношение компонентов реакции (винильного мономера и ацилированного хитозана) может меняться в. пределах от 1 : 10 до 100 ; 1, а их концентрация в растворе от 3 до 20 вес.%. Процесс сополимеризации проводят в зависимости от типа применяемого инициатора при температур от 2О до . Образующийся в процессе сополимеризации продукт представляет собой набухший прозрачный гель, который дробят на кусочки желаемой величины, промывают и высушивают. Для получения конечного продукта в форме сферических гранул исходных раствор реагентов диспергируют в несмешива юшейся с используемым растворителем жидкости, например в силиконовой жидкости. Сополимеры ацилированного хитозана и винильных мономеров указанной общей формулы хорошо набухают в воде и могут быть использованы для иммобилизации ферментов. Полимерный носитель, содержащий три сии, иммобилизованный на сополимере аци лированного хитозана и акриламида, имее активность, составляющую 83% от активности нативного фермента при содержании фермента 2 мг на грамм носителя, что превышает процент сохранения активности трипсина, иммобилизованного в обычном акриламидном теле методом включения. Если в качестве винильного мономера используют Н -винилпирролиды, сохранение активности препарата иммобилизованного трипсина на таком носителе достигает 76% при содержании фермента 2,5 м на Грамм носителя. Для сравнения трипсин иммобилизуется в тех же условиях на поливиниллирролидоне, сохранение активности препарата при этом составляет 24%. Таким образом, вышесказанное свидетельствует о перспективности использования синтезированных полимеров в ка|Честве носителей для иммобилизации ферментов. 7 Ниже приводятся примеры получения сополимеров на основе малеилированного хитозана и винильных мономеров. Пример 1. Смесь 1,78 г (0,01 м) хитозана, 1,96 г (Oj02 м) малеинового ангидрида и 100 мл формамида перемешивают при в течение 5 ч. Полученный раствор выливают в 5ОО мл воды. Вьшавший полимер отделяют центрифугированием и промывают водой до нейтральной реакции. Степень ацилирования полученного продукта составляет 100% Рассчитано,% Найдено, % С43,4043,34 И5,115,18 N5,075,13 К водной суспензии полученного ацилированного хитозана добавляют О,4 г (0,01 м) N аОН и воды до обшего веса смеси 39 г. К полученному раствору добавляют 0,71 г (О,01 м) акриламида и 0,О1 г (Нд) После растворения всех компонентов смесь нагревают в чение 3 ч при 60 С в атмосфере азота. Полученный гель дробят и промывают водой, высушивают. Объемная набухаемость полим.ера в воде равна 12. Полученный сополимер используют для иммобилизации трипсина. 0,3 г хлористого цианнура растворяют в Ю мл диоксана, добавляют 0,1 г сухого сополимера, 5 мл воды, перемешивают 5 мин при комнатной температуре, затем промывают смесью диоксан-вода 1:1 (1ОО мл), диоксаном, высушивают. О,1 г полученного активированного носителя и О,О01 г ферментного препарата трипсина перемешивают в 5 мл фосфатного буфера рН 9,18 в течение 2 ч при . Сохранение активности у полученного препарата составляет 83% при содержании фермента 2 мг/г носителя. Пример2. К раствору 2,75 г хитоаана, ацилированного малеиновым ангидридом (см, пример 1) в 30 мл воды, содержащей 0,4 г V4 аОН, добавляют О,276 г N-винилпирролидона, 0,03 г аскорбиновой кислоты, 0,О08 г FeSOn и 0,03 г 30%-ного раствора . Раствор тщательно перемешивают, обезгаживают и оставляют стоять при 20 С в течен:;е 4 ч. Полученный гель дробят, промывают водой и высушивают. Объемная набухаемость полимера в воде равна 8. Сополи-. мер активируют хлористым цианнуром и иммобилизуют трипсин (как описано в примере 1), Сохранение активности у полу57ченного препарата составляет 76% при с держании фермента 2,5 мг/г носителе. Пример 3, 0,276 г хитозана, ацилированного малеиновым ангидридом (см. пример 1), растворяют в ЗО мл во ды, содержащей 0,О4 г bSaOH, Затем добавляют ЗО г акриламида 0,1 г ( и 97О мл . Полученны раствор диспергируют в 2,5 л силиконовой жидкости. Полимеризацию ведут при непрерывном перемешивании в течение 6 ч при 6О С. Полученный в форме сферических гранул полимер отфильтровывают, тщательно промывают бензолом, диоксаном, водой, диоксанами и высушивают. Объемная набухаемость полимера в. воде равна 13. Пример 4. Смесь 1,78 г (0,О1 м) хитоэана, 1,96 г (0,02 м) м леинового ангидрида и 1ОО мл формамид перемешивают при 6О С в течение ЗО м Полученный раствор выливают в 50О мл воды. Вьшавший полимер отделяют центрифугированием и промывают водой до нейтральной реакции. Степень ацилирова ния полученного продукта составляет 100%. Найдено; % Вычислено, % С46,4246,55 Н6,166,08 Ы6,136,03 К раствору 0,28 г полученного моле щхированного хитозана в 13,9 г формами да добавляют 3,19 г акриламида, 0,О1 динитрила ааоизомасляной кислоты. Полу ченный раствор выдерживают при в течение 4 ч и при в течение 2 ч Образовавшийся гель дробят, промывают водой и высушивают. Объемная набухав- мость полимера в воде равна 7. П р и м е р 5.1,78 г (0,О1 м) хитоз на, 0,196 г (0,002) мапеинового ангид рида и 8О мл формамида перемешивают при 2О С в течение 5 ч. Полимер осаждают в 4ОО мл воды, отделяют центрифу гированием, промывают водой и высушивают. Степень ацилирования полученного продукта 5%. Найдено, % Рассчитано, % С4О,564О,68 Н6,736,66 Н7,627,65 К раствору 1,8 г полученного продук та в 30 мл смеси - диметилформамид вода (3:1) добавляют 0,9 г винилпирро- лидона, Oj05 г динитрила азоизомасляно кислоты. Полученный раствор выдержива;ют при 80 С в течение 4 ч. Образовав- 7 шийся гапь дробят, промывают водой и высушивают. Объемная набухаемость полимера в воде равна 12. П р и м е р 6, Смесь 1,78 г (О,01 м) хитозана, 0,55 г (0,0055 м) малеинового ангидрида и 1ОО мл формами- да перемешивают при 20 С в течение 5ч. Полученный раствор выливают в 500 мл воды. Выпавший полимер отделяют центрифугированием и промывают ьодой до нейтральной реакции. Степень ацилирова- ния полученного продукта сос- авляет 50%. рассчитано, %Найдено, % С42,2542,43 Н5,725,9О N6,166,21 К водной суспензии полученного аци- лированного хитозана добавляют 0,2 г (О,О05 м) КаОН и воды до общего веса 25 г. К пол;;/чеиному раствору добавляют О,71 г (О,01 м) акриламида и 0,01 г (NH)2U2 QS После растворения всех компонентов смесь нагревают 3 ч при в атмосфере азота. Полученный гель дробят, промывают водой и высушивают. Объемная набухаемость полимера в воде равна 13,5., Пример 7. Смесь 1,78 г(О,О1 м) хитозана, 0,22 г (0,ОО22 м) малеинового ангидрида и 10О мл формамида пере мешивают при 20 в течение 6 ч. Полученный раствор выливают в 50О мл воды. Вьшавший полимер отделяют центрифугированием и промывают водой до нейтральной реакции. Степень ацилирования полученного продукта составляет 20%. Рассчитано, %Найдено, % С41,2541,41 И6,276,32 Н7,086,91 К водной суспензии полученного аципированного хитозена добавляют 0,1 г (О,ОО25 м) N аОН и воды до общего веса ЗО г. К полученном - раствору доба&ляют О,3 г N-винилпирролидона и О,О1 г (HH)jSgOg. После растворения смесь нагревают в течение 4 ч при в атмосфере азота. Полученный гель дробят, промывают водой и высушивают. Объемная кабухаемость в воде равна 14, Предложенные соединения могут быть легко получены в технологических условиях благодаря простоте синтеза сополимеров.. Исходные реагенты - малеиновый ан- гидрид, акриламид, Н-винилпирролидон и хитозан (который является продуктом переработки хитина, остающегося как от-
ход при выделении белка из кридя) дешевы и доступны.
Синтезированные сополимеры имеют большое значеине при использовании в на родном хозяйстве, особенно в пишевой и фармацевтической промышленности. Потребность в эффективных носителях для имCHjon
СН2 СН2-СН-СН-СЧ2 НСООН
- СН - СН -СН2- СН-яО
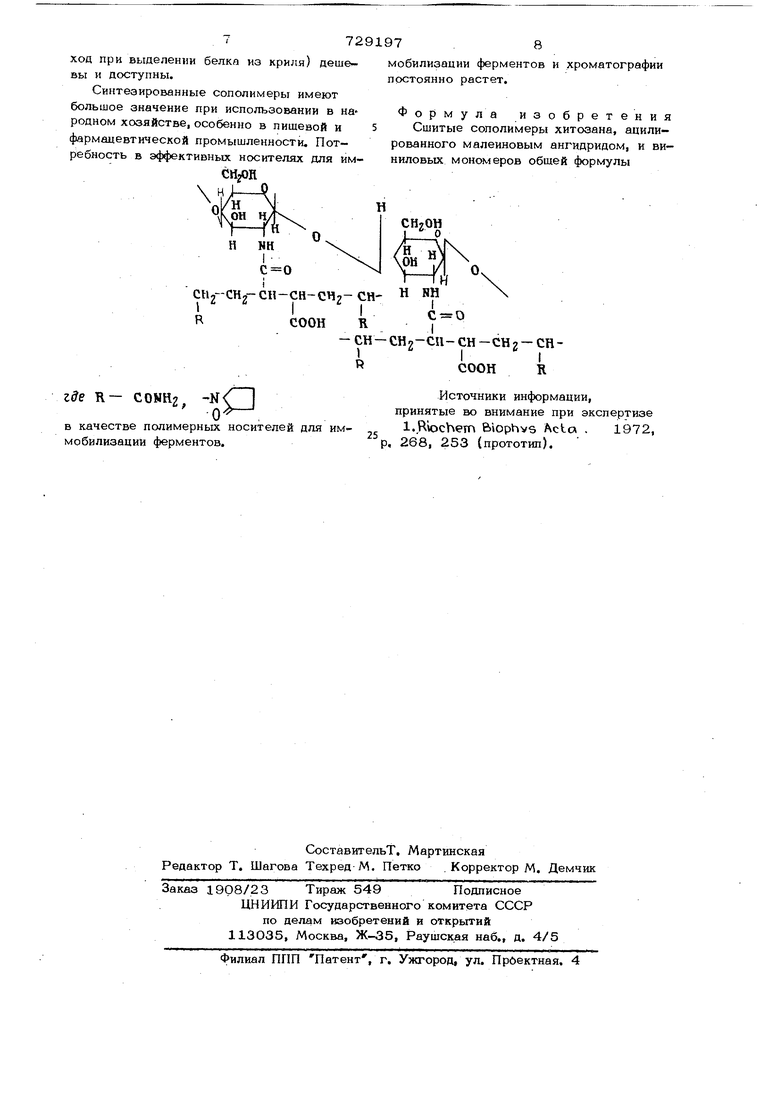
где R -
СОЫН2,
0
в качестве полимерных носителей для мобилизации ферментов.
мобилизации ферментов и хроматографии постоянно растет.
Формула изобретения Сшитые сополимеры хитозана, ацилированного малеиновым ангидридом, и виниловых мономеров обшей формулы
Н ЯН
СООНR
Источники информации, принятые во внимание при экспертизе l.R ochem Biophvs Acta . 1972, , 268, 253 (прототип).
Авторы
Даты
1980-04-25—Публикация
1977-07-05—Подача