1
Изобретение относится к новому способу получения дитиенилалкиламинов общей формулы
(I)
В-А1К NHY
где А и В вместе -,,группа )С{ОН)-СН2или
-неразветвленный
А1 k или разветвленный С| -Cj -алкил;
-неразветвленный или разветвленный С, -С jj -алкил
или группа общей формулы
,ORi
(а).
,-CHlRl-CH-(01l)где R - водород или -алкил;
RI - водород или С2 -С -ацил, или группа -NHY означает группу
формулы
/ -К N-Rj (5
где Rn - незамещенныйили зa eщeнный
одной, двумяили тремя метоксигруппамифенил или бензил,
или их солей, которые обладают биологической активностью и поэтому могут найти применение в медицине.
Известен один способ получения дитиенильных производных общей формулы
О
10B-CH -y-ClT-Cll-f
I.I I Rj Kj j
где оба тиенильных остатка могут быть замещены одним или более низ15 шими алкилами, мостик А-В - группа
)с (ОН) или
атом водорода у В - или СНг,-группы может замещаться низшим алкилом;
Ry и 2 водород или низший алкил;, 20 водород или оксигруппа;
R и Rf, - водород, галоид, оксигруппа, низший алкил, низший галогенированный алкил или низшая алкоксигруппа, заключающийся вовзаимодействии тие25 ни.г1магнийгалогенида с соответствующим кетоном.
Выход целевых продуктов не превышает 8% l .
Недостатком этого способа является низкий выход целевого продукта. Кроме того, по такому способу получ ют относительно ограниченное количество целевых продуктов. Целью изобретения является повыш ние выхода и расширение ассортимента целевых продуктов. Предлагается способ получения дитиенилалкиламинов формулы I или и солей, заключающийся в том, что соо ветствующий тиениллитий подвергают взаимодействию с соединением общей формулы C-diig-AlK-jiail {Ц где Alk имеет вышеуказанные значени Z - хлор, бром, йоДу низшая алкокси- или тиенилгруппа На1 - хлор, бром или йоц, в смеси растворителей, состоящей из простого насыщенного эфира и насыще ного углеводорода, и/или моно- или ди -C -С4-алкилбензола , при температу ре (-50 ) -(-80 ) и полученное при эт соединение общей формулы бН., где Alk имеет вышеуказанные значени X - хлор, бром или йод, обрабатывают амином общей формулы (s где Y и группа -NHY имеют вышеуказан ные значения, с последующим выделением целевого продукта и в случае необходимости де гидратаций последнего до целевого с единения общей формулы Т, где лив вместе означают группу , н выделением целевого продукта в свободном виде или в виде соли, используя для этого такие кислоты, как соляная малеиновая и др. Выход целевого продукта 15-90,4% Отличительным признаком способа: является то, что взаимодействию с тиениллитием подвергают соединение формулы М с последующей обработкой полученного при этом соединения формулы lT( амином формулы |у. Пример 1. 1,1-ДитиениЛ(3 -1-оксипропил-(3)- 1-окси 1(п-оксифенил)-пропил-(2) -амин. 25 г (0,15 моль) п-окси-нор-эфедрина, 22 f 5 мл триэтиламина и 4 5,, 5 г (0,15 моль) 1,1-дитиенил-(З)-З-бромлропанола-(1) нагревают в 80 мл диоксана при перемешивании в течение 8 ч при 100°С. Затем смесь упаривают S значительной степени во вращающемся испарителе, остаток смешивают с 150 мл воды и трижды встряхивают каждый раз с 100 мл диэтилового эфира. Объединенные эфирные экстракты высушивают сульфатом магния. Через несколько часов при выкристг1Ллизовывается слаРо окрашенное вещество, которое перекристаллизовывают из ацетона.Получают 15 г бесцветного кристаллического вещества, т.пл. 174-175 С. Для получения кислой малеиновокислой соли взмучивают 5,0 г основания в 30 мл этилацетона. После добавления 1,5 г малеиновой кислоты получают прозрачный раствор, который начинают сме1Уивать с диэтиловым эфиром до ясно различимого начинающегося помутнения. После выдержки в течение 12 ч отсасывают кристаллизат, промывают этилацетатом и высушивают. Получают 4,0 г кислрй малеиновокислой соли, т.пл. 198-К) 9°С. Получение исходного вещества - 1,1-дитие11ил- (3 ) - 3-бромпропанола- (1). В четырехгорлои колбе объемом 1,5 л,снабжержой капельной воронкой, сушильной трубкой, мешал-кой, термометром и трубкой для подачи азота, охлаждают в атмосфере азота 300 мл абсолютного диизопропилового эфира в охлаждающей ванне, используя смесь метанола с твердой углекислотой. Во время охлаждения добавляют раствор 335,2 мл н-бутиллития в гексане (0,55 моль); при этом эфир охлал-чцают до -75-С. Затем прикапывают в течение 90 мин раствор 81,5 г 3-бромтиофена (0,5 моль) в 100 мл абсолютного диизопропилового эфира с таким расчетом, чтобы температура не превышала . После этого выдерживают реакционную смесь в течение 1 ч при (-70)-(-75)С для дополнительного протекания реакции. Далее добавляют по каплям в течение 90 мин раствор 36,2 г этилового эфира 6-бромпропионовой кислоты (0,2 моль) в 60 мл абсолютного диизопропилового эфира так, чтобы температура не превышала -70с. После этого смесь выдерживают 4 ч для дальнейшего прохождения реакции. Затем удаляют охлаждающую ванну и реакционную смесь растворяют в 160 мл воды. Температура повышается до . Далее перемешивают еще некоторое время, пока температура не повысится до О-С, после чего отделяют органическую фазу, высушивают сульфатом магния, фильтруют и все легкокипящие вещества отгоняют в вакууме, во вращающемся испарителе. В остатке получают светлое масло. Выход 54 г (96%,считая на сложный эфир бромпропионовой кислоты). Так же получают 1,1-дитиенил-(3)-4-бромбутанол-(1) и 1,1-дитиенил... (3 )5-бромпентанс)Л-(1) в виде светлого масла. Пример 2, 1,1-Дитиенил-(3)-1-ОКСИ--4- (4-фенилпиперазино) -бутан. Раствор 16,2 г (0,1 моль) 4-фенилпиперазина, 14 мл триэтиламина и 1,7 ptO, моль) 1,1-дитиенил-(3)-1-окси-4-бромбутана в ВО мл диизопропилового эфира оставляют стоять 3 дня при комнатной температуре. Кристаллический продукт отсасывают, промывают эфиром, высушивают, взмучивают в воде, отсасывают, промывают и высушивают. Выход сырого-продукта 24,4 г (61,3%)i.
8 г (0,02 моль) сырого основания растворяют в 50 мл ацетона. После добавления ацетонового раствора, содержащего 2,32 г (0,02 моль) малеиновой кислоты, подогревания и фильтрования добавляют эфир до начинающегося помутнения. Через короткое время кристаллизуется вещество, которое
отсасывают, промывают смесью ацетонэфир (1:1) и высушивают. Выход 8,3 г (81%), т.пл. малеата 110-111 с.
Пример 3. 1,1-Дитиенил-(3)-1-ОКСИ-4- 4-(3-метоксифенил)-пиперазино -бутан.
Это соединение получают аналогично примеру 2, применяя 0,1 моль 4-(3-метоксифенил)-пипераэина. Температура плавления малеата 149-150С, выход 94%.
Пример 4. Получение других 1,1-дитиенил- (3 )-1-оксипропил- ( 3) -аминов формулы Т (значения -NHY приведены в табл.1)
Таблица 1



| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения /3,3-ди (тиенил-3)-3- оксипропил /-(1-фенил-1-оксипропил-2) амина или /3,3-ди (тиенил-3) пропен-2-ил/ - (1-фенил-1-оксипропил-2) амина или их солей | 1978 |
|
SU784774A3 |
| Способ получения дитиенильных производных | 1970 |
|
SU457221A3 |
| ПРОИЗВОДНЫЕ НИТРАТОАЛКАНОВЫХ КИСЛОТ ИЛИ ИХ ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМЫЕ СОЛИ | 1991 |
|
RU2017748C1 |
| Способ получения производных тиено (3,2-с)пиридина или их солей | 1976 |
|
SU640665A3 |
| СПОСОБ ПОЛУЧЕНИЯ АМИНОКЕТОНОВ | 1974 |
|
SU440826A1 |
| Способ получения производных индолизина или их фармацевтически приемлемых солей | 1987 |
|
SU1528321A3 |
| ПРОИЗВОДНЫЕ АМИНОФОСФОНОВЫХ И -ФОСФИНОВЫХ КИСЛОТ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ СОСТАВЫ НА ИХ ОСНОВЕ | 1997 |
|
RU2181362C2 |
| СПОСОБ ПОЛУЧЕНИЯ КАРБАМОИЛОКСИМА | 1972 |
|
SU328576A1 |
| ПРОИЗВОДНЫЕ КСАНТИНА В ВИДЕ СМЕСИ ИЗОМЕРОВ ИЛИ ИНДИВИДУАЛЬНЫХ ИЗОМЕРОВ, ОБЛАДАЮЩИЕ СВОЙСТВАМИ АНТАГОНИСТОВ АДЕНОЗИНА | 1992 |
|
RU2057752C1 |
| Способ получения 1-фенил-2-аминокарбонилиндольных соединений или их кислотно-аддитивных солей | 1983 |
|
SU1223843A3 |

То же
Этанол-эфир
140-141
51,0
186-187
45,0 Метанол-эфир 130-131 39,9
Соединения, приведенные в табл.1 получают по следующей методике.
0,1 моль 1,1-дитиенил-(3)-3-бромпропанол-(1), 0,11 моль триэтиламина и 0,1 моль первичного или вторичного амина (см.колонку 2 табл.1) нагревают в 60 мл диизопропилового эфира примерно 12-13 ч при перемешивании и действии обратного холодильника. После охлаждения отсасывают кристаллы, промывают их диизопропиловым эфиром и высушивают. Затем взмучивают в воде, отсасывают, промывают водой, высушивают, перекристаллизовывают и получают, как указано в примере 1, в данном случае соль малеиновой кислоты.
Пример 5. 1,1-Дитиенил-(3)-l-пpoпeнил- (3)- 1-ОКСИ-1-(п-оксифенил)-пропил-(2) -амин.
23 г (0,15 моль) п-окси-нор-эфедрина, 22/5 мл триэтиламина и 45,5 г (0,15 моль) 1,1-дитиенил-(З)-З-бромЬропанола-(1) нагревают в 80 мл диоксана при перемешивании 8 ч при 100°С. Затем смесь в значительной степени упаривают во вращающемся ис.парителе и сиропообразный остаток
дважды обрабатывают порциями по 250 мл диэтилового эфира. Объединенны эфирные растворы подкисляют изопропанольным раствором хлористого водоро.да, причем высаживается высоковязкий продукт. После сливания растворителя остаток переносят в 100 мл эталона, нагревают 10 мин при кипении и действии обратного холодильника, затем концентрируют раствор во вращающемся испарителе. Остаток растворяют в 100 мл теплого ацетона, причем после
СН.2НСе Метанол
СН 2НСе То же
СН 2Нсе ИзопропанолТ J
СН 2НСР Метанол NIL-Cil СН НС НзСО ОСНз CHj нее N11-Он, (СН)2 нее
ОСИ:
(СН,, ) 2НСе Метанол-эфир 212-213
(CHj )j 2НСЕ Метанол
СН::
I /г-
CH-CH-f V
(СН) НСР То же
-он I /
он
охлаждения медленно выкристаллизовывается вещество. После перекристаллизации из изопропанола получают соединение в виде хлористоводородной соли в виде бесцветных кристаллов.
Выход 10,2 г; т.пл. гидрохлорида 138-140°С.
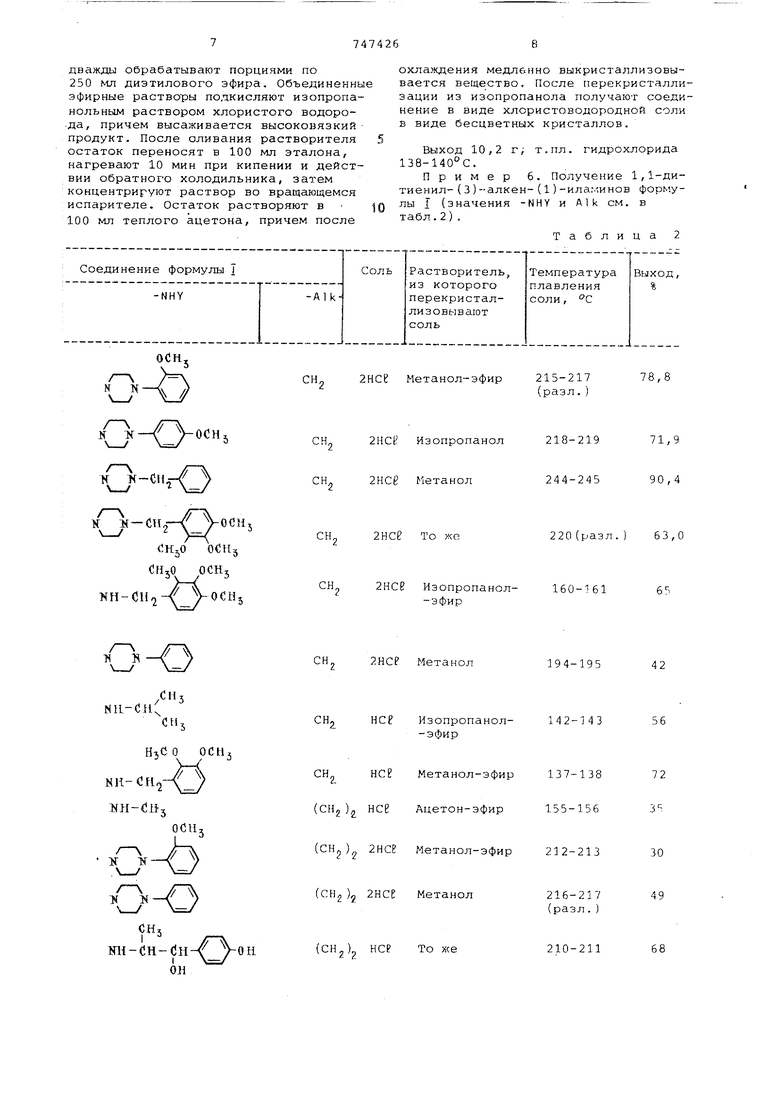
Пример 6. Получение 1,1-дитиенил-(З)-алкен-(1)-иламинов формулы I {значения -NHY и Alk см. в табл.2).
Таблица 2
90,4
244-245
220(разл.) 63,0
160-161
65
-эфир
194-195
42
56
72
30
216-217
49 (разл.)
68
210-211 Изопропанол- 142-143 -эфир Метанол-эфир 137-138 Ацетон-эфир 155-156
Продолжение табл.2
Авторы
Даты
1980-07-23—Публикация
1978-01-11—Подача