(54) СПОСОБ ПОЛУЧЕНИЯ 1,2,5,5,9-ПЕНТАМЕТИЛ-3-КЕТО-Л -ОКТАГИДРОНАФТАЛЕНА

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных простанкарбоновой кислоты | 1971 |
|
SU439962A1 |
| Производные 2,3,4,9-тетрагидро-1Н-карбазол-1-уксусной кислоты, проявляющие болеутоляющее и противовоспалительное действие и метиловый эфир 2,3,4,9-тетрагидро-1Н-карбазол-1-уксусной кислоты как промежуточный продукт для синтеза производных 2,3,4,9-тетрагидро-1Н-карбазол-1-уксусной кислоты, проявляющих болеутоляющее и противовоспалительное действие | 1986 |
|
SU1482915A1 |
| Способ получения производныхфузидОВОй КиСлОТы или EE СОлЕй | 1976 |
|
SU799670A3 |
| Способ получения эпимерных производных простановой кислоты или их солей | 1972 |
|
SU662007A3 |
| Способ получения 9-дезокси-9 @ -метиленизостеров @ или их лактонов или их солей | 1979 |
|
SU1053745A3 |
| Способ получения производных конденсированных индолов или инденов | 1973 |
|
SU728716A3 |
| Способ получения производных -фенилжирной кислоты | 1969 |
|
SU528864A3 |
| Способ получения гетероциклических амидов или их солей | 1987 |
|
SU1595338A3 |
| Способ получения арахидоновой кислоты | 1977 |
|
SU897766A1 |
| Способ получения алкиловых эфиров 3,7,11-триметил-2,4-додекадиеновых кислот или их 11-метоксипроизводных | 1977 |
|
SU727624A1 |

1
Изобретение относится к химии сесквитерпеновых .соединений, конкретно к синтезу ненасыщенного кетона формулы 1,
ся оксиацетат (IX), который окисляют . до ненасыщенного кетоацетата (Х), гидрргенолиз которого цинковой пьшью в уксусной кислоте дает непредельный кетон (I). Вьщеленный природный продукт не обладает запахом {Ti .
Недостатками способа получения соединения (I ) являются труднодоступность исходного дименола (М), выделяемого с низким выходом из Южноамериканского дерева Drimys wintert; многостадийность процесса, включающего 9 стадий, применение взрывоопасных реагентов (м-хлорпербензойной кислоты и натрийборгидрида) ; необходимость применения низких температур , необходимость проведения селективных реакций ацетилирования, даквдих низкий выход промежуточных продуктов, а также нeзriaчитeлJЬJный выход целево- . го соединения. , ...,.. ,.,
Цель изобретения - упрощение прог цесса.
Поставленная цель достигается тем, что, согласно способу получения 1,2,5,5,9-пентаметил-З-кето-Д -6ктагидронаФталена формулы 1 на основе замещенного октагидронафталена, .смесь изомерных метиловых эфиров бициклогомофарнезеновцх кислот формулы В COjCH
а
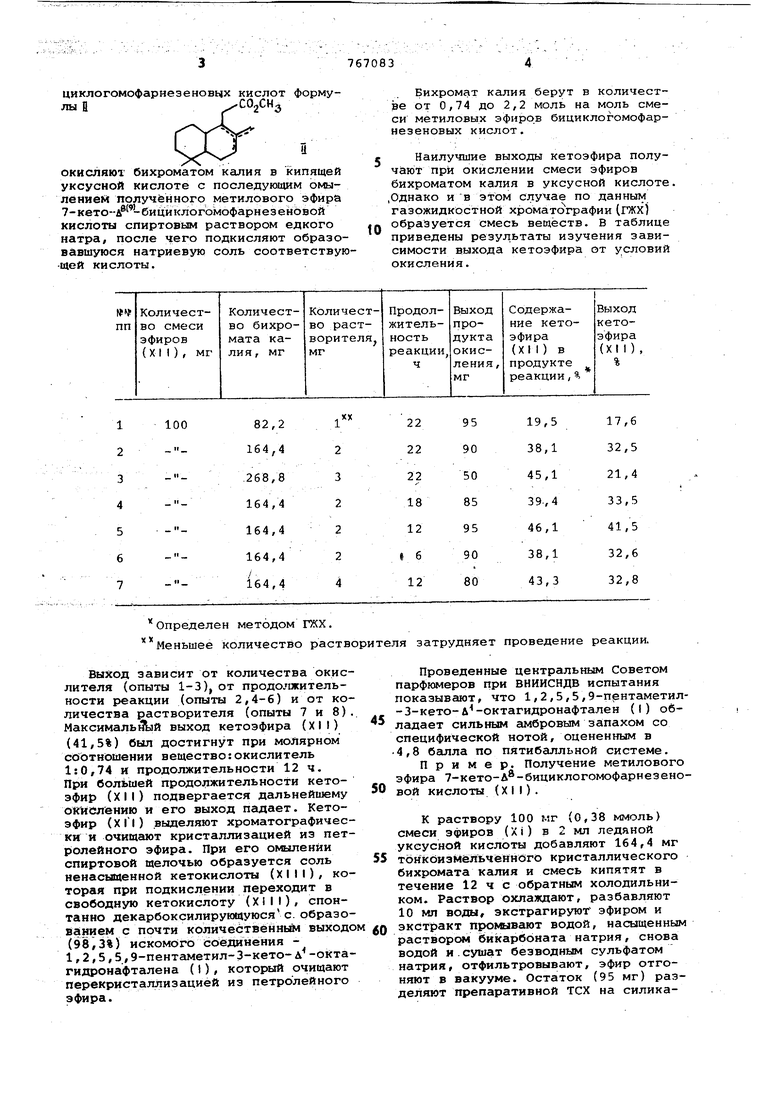
окисляют бихроматом калия в кипящей уксусной кислоте с последующим омылёниеМ полученного метилового эфира 7-кето--д -бициклогомофарнезеновой кислоты спиртовым раствором едкого натра, после чего подкисляют образовавшуюся натриевую соль соответствующей кислоты. Определен методом ГЖХ. Меньшее количество растворителя затрудняет Выход зависит от количества окислителя (опыты 1-3), от продолжительности реакции (опыты 2,4-6) и от количества растворителя (опыты 7 и 8). МаксималыЗУй выход кетоэфира (XII) (41,5%) был достигнут при молярном соотношении вещество:окислитель 1:0,74 и продолжительности 12 ч. При большей продолжительности кетоэфир (XII) подвергается дальнейшему окйелению и его выход падает. Кетоэфир (ХГ|) выделяют хроматографически и очищают кристаллизацией из петрояейного эфира. При его омылении спиртовой щелочью образуется соль ненасыщенной кетокислоты (XIII), которая при подкислении переходит в свободную кетокислоту (XIII), спонтанно декарбоксилирующуюсяс. образованием с почти количественным выходо (98,3%) искомого соединения 1,2,5,5,9-пентаметил-З-кето- л -октагидронафталена (I), который очищают перекристаллизацией из петролейного эфира.
Бихромат калия берут в количестве от 0,74 до 2,2 моль на моль смеси метиловых эфнров бициклогомофарнезеновых кислот.
Наилучшие выходы кетоэфира получают при окислении смеси эфиров бихроматом калия в уксусной кислоте, .Однако и в этом случае по данным газожидкостной х эоматографии (ГЖХ) образуется смесь веществ. В таблице приведены результаты изучения зависимости выхода кетоэфира от у;словий окисления. проведение реакции. Проведенные центральным Советом парфюмеров при ВНИИСНДВ испытания показывают, что 1,2,5,5,9-пpнтaмeтил-3-кeтo- д -октагидронафтален (I) обладает сильным с1Мбровым запахом со специфической нотой, оцененным в 4,8 балла по пятибалльной системе. Пример. Получение метилового эфира 7-кето-Л®-бициклогомофарнезеновой кислоты (XII). К раствору 100 мг (0,38 ммоль) смеси эфиров (Xi) в 2 мл ледяной уксусной кислоты добавляют 164,4 мг тонкоизмёЛЬЧённОго кристаллического бихромата калия и смесь кипятят в течение 12 ч с обратным холодильником. Раствор охлаждают, разбавляют 10 МП воды, экстрагируют эфиром и экстракт промывают водой, насыщенным раствором бикарбоната натрия, снова водой и.сушат безводным сульфатом натрия, отфильтровывают, эфир отгоняют в вакууме. Остаток (95 мг) разделяют препаративной ТСХ на силикагеле с люминофором. Растворитель: бензол петролейный эфир-этилацетат 90:10:5. Зону с R 0,43 собирают, и вещество вымывают эфиром. Получают 40 мг кристаллического продукта (XI.I) (выход 38) (по данным ГЖХ выход эфира (XII) составляет I , который перекристаллизовывают из легкого петролейного эфира, т,пл. 99-100,5°C, +124,3°С (с 2,6 СНС Найдено,%: С 73,67 Н 9,65 п Н2оОзВычислено,%: С 73,34, Н 9,41. м кс248 им (Ig е 3,75) ИК-спектр (. см ) : 1627, 1680 (кетогруппа, сопряженная с дво ной связью); 1750 (сложноэфирная группа). . ЯМР-спектр (снят с CCfi на прибо ре РС-60, внутренний стандарт ТМС, S М.Д.): синглеты при 0,95 (6Н, С4-гемциметильная группа); 1,07 (ЗН, С,о-СНз); 1,68 (ЗН, Cg-СНз); 3,24 (2Н, ), 3,73 (ЗН, ОСНэ) , мультиплет с центром при 2,36 (2Н, Сб-снг). Получение 1,2,5,5,9-пентаметИл-3-кето-д -октагидронафталена (1) . Кетоэфир (XII) (0,18 г) кипятят с раствором 0,75 г едкого натра в 6,75 г этилового спирта с обратным холодильником в течение 3 ч. Раство разбавляют водой, подкисляют соляной кислотой и экстрагируют эфиром Эфирный экстракт промывают водой, насыщенным раствором бикарбоната натрия, снова водой, сушат безводны сульфатом натрия, отфильтровывают, эфир отгоняют в вакууме и остаток перекристаллизовывают из легкого петролейного эфира. Получают 140 мг (98,3%) кетона (I), т.пл. 51-52с, чистого по данным ГЖХ (ХРОМ-4, 5% ХЕ-60, на хроматоне N-AN- DMCS, сте лянная колонка длиной 2 м и диамет ром 4 мм, температура колонки 1302бО°С,скорость нагревания 3°С в ми температура испарителя 200° С, газ-носитель гелий, скорость 60 мл/мин, время удерживания кетон (I) 3,5 мин),ос +86 (с 4; СНС«з S,«7J249,5 нм (IgE «, 1 ) . ИК-спектр (. см ): 1975, 1390 (гемдиметильная группа), 1610 1660 (oL,|b -ненасыщенный кетон) . Не посредственное спектральное и хром тографическое сравнение полученног продукта с заведомым образцом кето (|) показывает, что они идентичны. Смешанная проба плавится без депре сии . Использование предлагаемого способа обеспечивает применение для синтеза легкодоступного исходного вещества, которое получается простым известным способом из выпускаемых отечественной промышленностью соединений; синтез в 3 стадии вместо 9 в известном} максимальный вЫход целевого продукта в расчете на исходное соединение составляет 37,5%, что при синтезе дорогостоящих душистых веществ с амбровым запахом вполне приемлемо . Формула изобретения 1. Способ получения 1,2,5,5,9-пентаметил-3-кето-д-октагидронафталена формулы I , на основе замещенного октагидронафталена, отличающийся тем, что, с целью упрощения процесса, смесь изомерных метиловых эфиров бициклогомофарнезеновых кислот формулы П окисляют бихроматом калия в кипящей уксусной кислоте с последующим омылением полученного метилового эфира 7-кето-д®-бициклогомофарнезеновой кислоты спиртовым раствором едкого натра, после чего подкисляют образующуюся натриевую соль соответству1ощей кислоты. 2. Способ ПОП.1, отличающийся тем, что бихромат калия берут в количестве от 0,74 до 2,2 моля на моль смеси метиловых эфиров бициклогомофарнезеновых кислот. Источники информации, принятые во внимание при экспертизе 1. A.I.Aasen, C.H.G. Vogt, CR. Enzell Tobacco chemistry, 28. Structure and Synthesis of Orim-8-en-7-one , a New Tobacco Constituent, Acta Chemica Scand, B-29, № 1, 1975, p. 51-55 (прототип).
Авторы
Даты
1980-09-30—Публикация
1979-01-29—Подача