среде, с последующим гидролизом бисульфитного соединения едким натром Пример1, А. Получение бисульфитного соеди не-ния резорцина. В круглодонной колбе емкостью 150 мл, соединенной,с обратным холо дильником, нагревали раствор 9,3 г (0,084 моль) резорцина и 33,9 г (О ,14 моль) метабисульфита калия в 60 мл воды при и непрерывном перемешивании в течение 10 ч. Полученный светло-желтый раствор калиевой соли бисульфитНого соединения подкисляли небольшим количеством концентрированной соляной кислоты до рН 2,О (для разложения избытка сульфита калия). Затем добавляли осторожно в количестве, не обходимом для получения рН раствора 6,5-7,0 (при щелочном значении рН раствора бисульфитные. соединения ре зорцина разлагаются). Б. Получение бисульфитного соеди нения 3 -оксифенилен-3 -оксигепта- (4-амино-4-фениленаминодифенилмета на) .,- V К полученному раствору бисульфит ного соединения резорцина добавляли 14,6 г (О,-0735 моль) 4,4-дйаминодифанйлметана в 29,4 мл 22%-ной соляной кислоты. Синтез вели в кругло донной колбе .емкостью 250 мл, соёди нённой с обратным холодильником,при непрерывном перемешивании в течение 15 ч. Полученную суспензию охлаждали, отфильтровывали и отмывали водой Ът резорцина (до исчезновения фиолетового окрашивания с FeClg).Не прореагировавший диамин отмывали со лянокислым раствором () до исчезновения реакции на вытек диазо раствора со щелочным раствором/Ь на тола. Осадок сушили при комнатной температуре.Наличие серы в полученн продукте доказывает качественная ре акция с н итропруссидом натрия. Выход 21,1 г (78,2%). Пройуй порошок желтого цвета с т.пл.287-С Найдено, % : С 62 ,1: В 5 , 2 ; N 7,2; S 9,8. Вычислено,%: С 62,45;Н 5,1; N 7,3; S 9,6, . 1V )ЪЛ 1Ь SB .В.Гидролиз бисульфитного соедине ния З -оксифенилен-З -оксигепта-(4-амино-4-фениленаминодифенилметана) Гидролиз вели в круглодонной кол бе емкостью 500 мл, соединенной, с обратным.холодильником, в растворе NaOH (рН среды 11-12) при в течение 2-3 ч. Полученную щелочную суспензиюохлаждали, выливали в стакан с холодной дистиллированной водой, подкисленной соляной кислотой до рН 2,о, нейтрализуя кислый раствор до рН ,0-7,0. Стакан поме шгши в лед и выпавший осадок отфиль тровывали и отмывали водой от сульат ионов доисчезновения реакции с BaClr; . Осадок сушили при . При наличии серы в полученном продукте проводили гидролиз дополнительно. Гидролиз Идет неполностью. Очистку продукта осуществляли путем перекристаллизации из ацетона. Доказательством наличия ОН-группы в полученном продукте служит реакция сочетания елочного раствора полученного соединения с диазораствором п-нитроанилина. З -оксифенилен-з -оксигепта- (4-амино-4 -фениленаминодифениЛметан) - светло-коричневый порошок т.пл. 150-152 С. . Пример 2. А, Получение бисульфитного соединения резорцина. В круглодонной колбе емкостью 150 мл, соединенной с обратным холодильником, нагревали раствор 9,3 г (0,084 моль) резорцина и 33,9 г (0,14 моль) метабисульфита калия к 60 мл воды при 100°С и непрерывном перемешивании R течение 10 ч. Полученный светло-желтый раствор калиевой соли бисульфитного .соединения резорцина (,5) охлаждали, подкисляли небольшим количеством концентркрб8;анной соляной .кислоты до рН 2,0 №ля разложения избытка сульфи- , та калия). Затем добавляли осторожно в количестве, необходимом дли получения рН раствора 6,5-7,0 (при щелочном значении рН раствора бисульфитное соединение резорцина разлагается) . в. Получение бисульфитного соединения З -оксифенилен-3 -оксигепта-4- (амино-4 -фениленаминодифенилового эфира). К полученному раствору бисульфитHoto соединения резорцина добавляли 14,7 г (0,0735 моль) 4,4 -диаминоди- фенилового эфира в 29,4 мл 22%-ной соляной кислоты. Синтез вели в круглодонной колбе емкостью 250 мл, соединенной с обратным холодильником, при непрерывном перемешивании в течение 15 ч. Полученную суспензию охлаяодали, отфильтровывали и отмывали водой от резорцина (до-исчезновения фиолетово-|го окрашивания с РеСЦ) .Непрореагировавший диамин отмывали солянокислым раствором (рН 3-4) до исчезновения реакций на вытек диазо4эаствора со щелочным раствором |Ь-нафтола. Осадок сушили при комнатной температуре. Наличие серы в полученном продукте доказывает количественная реакция с нитропруссидом натрия. Выход 21,4 г (79,9%). Продукт-порошок желтого цвета с т.пл. 273 С. Найдено, %:С58,9;Н4,5; N 7,4; S 9,3. Вычислено, %;С 59,0; И 4,5; N 7,3 S 9,5. Cibl 120 14 О
В. Гидролиз бисульфитного соединения З -оксифенилен-з -оксигепта-(4-амино-4-фениленаминодифенилсвого эфира).
Гидролиз вели.в круглодонной колбе емкостью 500 мл. ,соединенной с обратным холодильником в растворе NaOH (рН среды ivll-12) при в течение 2-3 ч. Полученную щелочную суспензию охлаждали, выливали в стакан с холодной дистиллированной водой, подкисленной соляной кислотой до рН л2,0 нейтрализуя кислый раствор до рН 6,77,0. Стакан помещали в лед и выпавший осадок отфильтровывали и отмывали водой от сульфат ионов до исчезновения реакции с ВаС. Осадок сушили при . Очистку продукта осуществляли путем перекристаллизации из -ацетона. Доказательством наличия ОН-группы в полученном пpoдyктe служит реакция сочетания щелочного раствора полученногр соединения с диазораствором п-нитроанилина.
3 -Оксифенилен-з -оксигепта-(4-амино-4-фениленаминодифениловый эфир порошок бежевого цвета с серым оттенком с т.пл. 200-202°С.
Указанное соединение, его свойства в литературе не описаны.
3 -Оксифенилен-З-оксигепта-(4-амино-4-фениленаминодифенш1метан) указанной формулы получают конденсацией бисульфитного соединения резорцина с 4,4-диаминодифенилметаном при мольном соотношении 8:7 в солянокислой среде,с последующим гидролизом полученного бисульфитного соединения NaOH при . рН 11-12 при нагревании.
Мол.вес полученного соединения: найдено 2134,1 вычислено 2016,45.
Найдено, % : С 82,6; Н 6,1; N 9,9.
Вычислено,%: С 82,8; Н 5,9; N 9,7,
Предлагаемые соединения были испытаны как термостабилизаторы пбликапроамидной нити.
Соединение вводили в мономер перед полиамидированием (температура полиамидирования 260±1°с) в количестве 0,5% от массы мономера. Получение полимера осуществлялось на Лабораторной установке. .
Эффективность стабилизирующего действия испытуемого соединения определили по сохранению исхЬдной прочности волокна после прогЕ ева в атмосфере воздуха при 200С в течение 2 ч Эталоном сравнения является термостабилизатор Н-1 - 2,2-бис-(п-фениламинофенокси)-диэтиловый эфир.
Полученные данные приведены в таблице .
Термостойкость поликапроамидной мононити.


| название | год | авторы | номер документа |
|---|---|---|---|
| 3 , 3 -Ди(оксифенил)-3,3 дихлор-4,4 -диаминодифенилметан в качестве термостабилизатора нитрильного каучука | 1977 |
|
SU654611A1 |
| Способ получения 2-[4-(2-фуроил)-пиперазин-1-ил-4-АМИНО-6,7-ДИМЕТОКСИХИНАЗОЛИНА | 1978 |
|
SU946402A3 |
| Способ получения 3(или 5)-метил-1Н-пиразол- @ 5-(или 3)-азо-1 @ -2-нафтола | 1986 |
|
SU1361145A1 |
| СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ АМИНОБЕНЗОЙНЫХ КИСЛОТ | 1995 |
|
RU2096403C1 |
| Способ получения 2-меркаптобензимидазолов | 1990 |
|
SU1825787A1 |
| 2,2,6,6-Тетраметилпиперидиламид 2,2,6,6-тетраметилпиперидиламиноуксусной кислоты в качестве неокрашивающего свето-термостабилизатора полимерных материалов | 1978 |
|
SU671245A1 |
| Способ получения производных пиразола | 1975 |
|
SU582758A3 |
| Бис-(диалкиламиноалкиламиды) @ -труксилловой кислоты, проявляющие курареподобную активность | 1973 |
|
SU522597A1 |
| ПРОИЗВОДНЫЕ 2-АМИНОПИРАЗИН-5-КАРБОКСАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И СОДЕРЖАЩИЕ ИХ МЕДИЦИНСКИЙ ПРЕПАРАТ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ | 1994 |
|
RU2128176C1 |
| Способ получения производных фенилалкиламина | 1978 |
|
SU745360A3 |

Н-1 .
-Оксифенилен-3 -оксигепта(4-амино-4-фениленаминодифенилметан) Из данных таблицы следует, что лредлагаемое соединение является хорошим термостабилизатором поликапроамидной нити, не уступающим Н-1. По данным термограмм летучесть описываемого соединения 3-оксифенил ен-3 -оксигепта (4-амино-4-фенилен
96
99,5 аминодифенилметана) меньше, чем Н-1. . Описываемое соединение нерастворимо $ обьгчных органических растворителях. Таким образом, предлагаемое сойди Пение имеет ряд преимуществ в сравне НИИ.с Н-1 и может быть использовано в качестве термостабилизатора поликапроамидной нити.
Формула изобретения 3 г з-Ди-(Ьксифенилен) диамин общей .фйрмулы
проявляющий свойство термостабилизатора поликапроадгадной нити.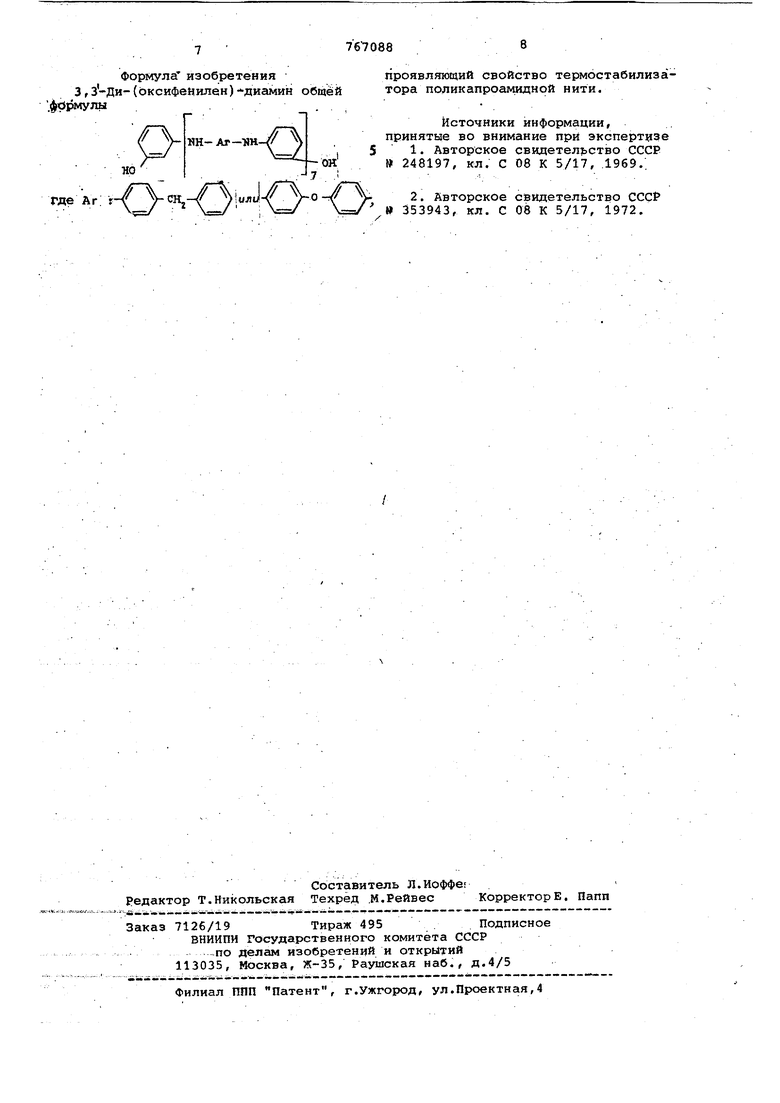
Авторы
Даты
1980-09-30—Публикация
1977-06-06—Подача