379931
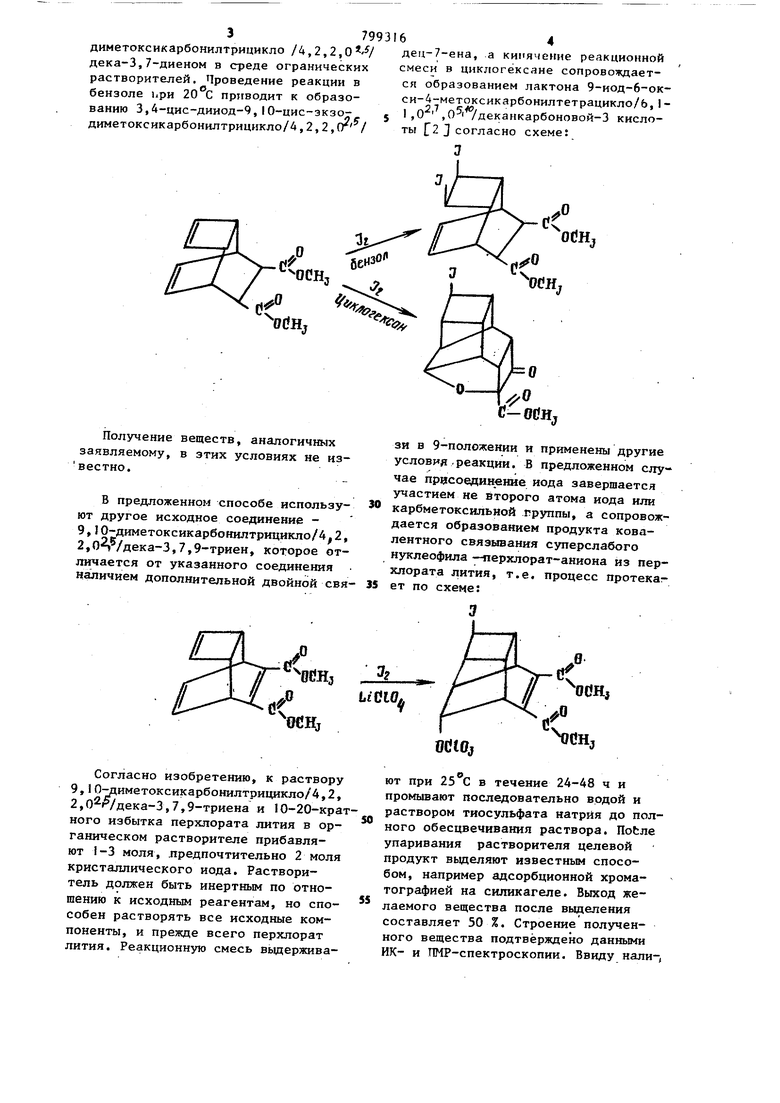
диметоксикарбонилтрицикло /4,2,2,0 1 дека-3,7-диеном в среде огранических растворителей. Проведение реакции в бензоле ьри 20 С приводит к образованию 3,4-цис-дииод-9,10-цис-экзо- j диметоксикарбонилтрицикло/4,2,2, / С б OCHj odH, Получение веществ, аналогичных заявляемому, в этих условиях не известно. В предложенном способе используют другое исходное соединение 9,10-диметоксикарбонилтрицикло/4 2, 2,о2 /дека-3,7,9-триен, которое отличается от указанного соединения наличием дополнительной двойной свя
eCHj
Согласно изобретению, к раствору 9,10--/ иметоксикарбонилтрицикло/4,2, 2,о2р/дека-3,7,9-триена и 10-20-кратного избытка перхлората лития в органическом растворителе прибавляют 1-3 моля, .предпочтительно 2 моля кристаллического иода. Растворитель должен быть инертным по отношению к исходным реагентам, но способен растворять все исходные компоненты, и прежде всего перхлорат лития. Реакционную смесь вьщержива64
дец-7-ена, а ки1яче гне реакционной смеси в циклогексане сопровождается образованием лактона 9-иод-6-окси-4-метоксикарбонилтетрацикло/6,I 1,0 , /деканкарбоновой-3 кислоты f2 3 согласно схеме
J
od(0j
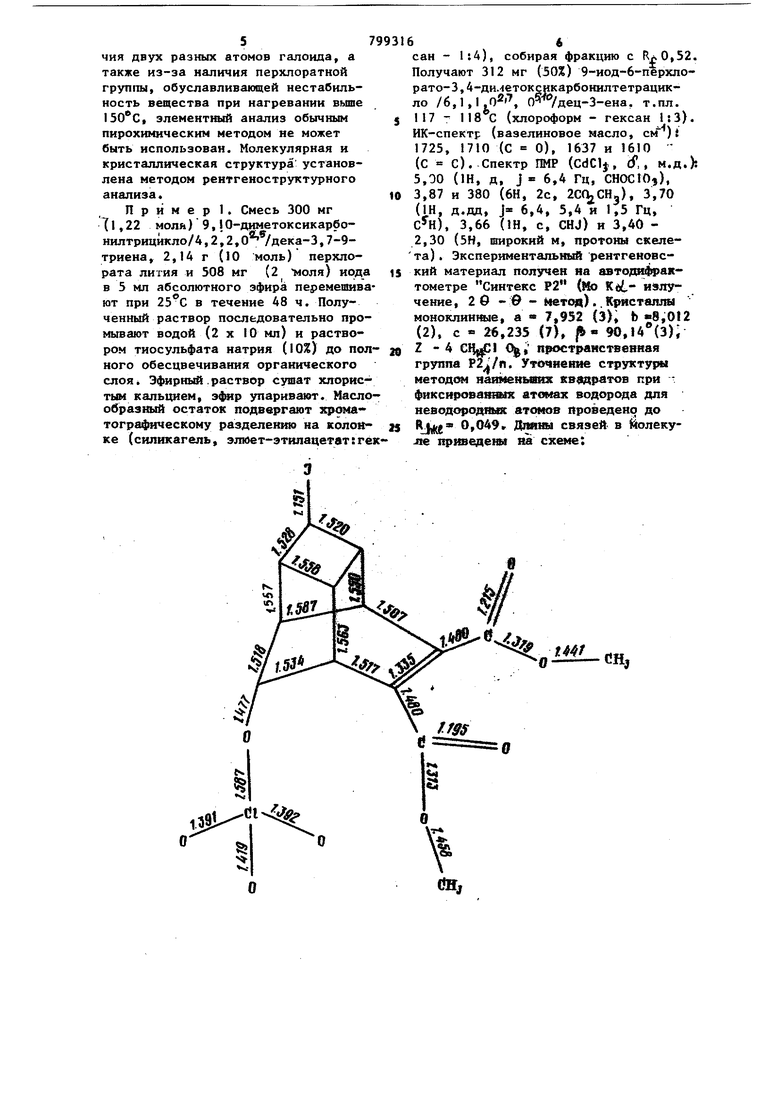
ют при 25 с в течение 24-48 ч и промывают последовательно водой и раствором тиосульфата натрия до полного обесцвечивания раствора. ПоЬле упаривания растворителя целевой продукт вьщеляют известным способом, например адсорбционной хроматографией на силикагеле. Выход желаемого вещества после выделения составляет 50 %. Строение полученного вещества подтверждено данными ИК- и ПМР-спектроскопии. Ввиду налив/. (/-odHj аи в 9-положении и применены другие условил реакции. В предложенном случае присоединение иода завершается участием не второго атома иода или карбметоксильной группы, а сопровождается образованием продукта ковалентного связывания суперслабого нуклеофила -перхлорат-аниона из перхлората лития, т.е. процесс протекагет по схеме: чия двух разных атомов галоида, а также из-за наличия перхлоратной группы, обуславливающей нестабильность вещества при нагревании вьппе , злементный анализ обычным пирохимическим методом не может быть использован. Молекулярная и кристаллическая структура установлена методом рентгеноструктурного анализа. Пример 1. Смесь 300 мг 7l,22 моля) 9,10-диметоксикарбоншттрицикло/4,2,2,0 /дека-3,7-9триена, 2,14 г (10 моль) перхлората лития и 508 мг (2 1оля) иода в 5 мл абсолютного зфира перемешива ют при в течение 48 ч. Полученный раствор последовательно промывают водой (2 X 10 мл) и раствором тиосульфата натрия (10%) до пол ного обесцвечивания органического слоя Эфирный.раствор сушат хлористым кальцием, упаривают. Масло образный остаток подвергают хроматографическому разделению на колон ке (силикагель, элюет-этилацвтвт:г
, 6 сан - 1:4), собирая фракцию с ,52. Получают 312 мг (50%) 9-иод-6-перхлорато-3,4-ди.1етоксцкарбонилтетрацикло /6,1,1,, 0 /дец-З-ена, т.пл. 117 - 118 С (хлороформ - гексан 1;3). ИК-спектр (вазелиновое масло, см )i 1725, 1710 (С 0), 1637 и 1610 (с с). Спектр ПМР (CdClj:, сГ,, м.д,): 5,00 (1Н, д, j 6,4 Гц, СНОСЮ,), 3,87 и 380 (6Н, 2с, ), 3,70 (1Н, д.дд, J 6,4, 5,4 и 1,5 Гц, СН), 3,66 (1Н, с, CHJ) и 3,40 2,30 (5Н, широкий м, протоны скелета). Экспериментальный рентгеновский материал получен на автода актометре Синтекс Р2 (йо излучение, 2 б -0 - «4етоя) .. KfNKCTamibi моноклинкые, а 7,952 (3) Ь «8,012 (2), с « 26.235 (7), /Ь« 90.14(3); Z 4 0 простраиствевиая грзгапа . Уточиение структуры методом яаяменившЕ квадратов при фиксировашшх атомах водорода для неводород1В|ас атомов проведено до Rj 0,049 ДПйШ связей в молекуле пр1юеденм яа схеме: Т1ример2. В условиях, анало гичных для примера 1, из 300 мг (1,22 моля) 9,Ю-диметоксикарбонил трицикло/А , 2,2, О -Д/дека-3,7,9-триена. А,28 г (20 молей) перхлората лития и 508 мг (2 . моля) иода в 8 м этилацетата получают 300 мг (48%) 9-иод-6-перхлорато-3,4-диметоксикарбонилтетрацикло/6,1,1,0 , (Л / дец-3-ена, т. пл. 117 - В. Иммунотропную активность заявляемого препарата определяли по его .способности влиять на антителообразование (титры антител) в сыворотке крови и количеству антиген - связывающих и розеткообразуюпшх клеток (РОК) в селезенках мышей, иммунизированных эритроцитами барана (эталонный тест - антиген). Эксперименты были проведены на белых мышахсамцах, весом 18 - 20 г. Животных иммунизировали внутрибрюшинным введ ниe стандартной дозы эритроцитов (5 10 клеток). На седьмой день после антигенного стимула животных забивали. От каждой мьппи в отдельную пробирку собирали кровь, в сыворотке которой при помощи микротитратора Такачи общепринятым методом определяли титры антител :(темагглютининов). Одновременно извлекали селе зевки и готовили суспензии селезёноч ных клеток, в которых ставдартным методом выявляли клетки, связывающие эритроциты барана и формирующие розетки, то есть розеткообразующие клетки (РОК), Вводимое вещество
Заявляемое вещест- 3,6 (5,7-,5)
во
1,2(2,25-0,15)
Т, 2(2,25-0,15)
23,2(26,5-19,9)
Эта иммунодепрессивная активность нового вещества сходна с действием циклофосфаиа. При комбинированном применении нового вещества и циклофосфана потенцирование действия циклофосфана не наблюдается.
Заявляемое вещество имеет существенное преимущество с эталонным веществом циклофосфаном в том, что
0,57
. 0,46 0,46
оно малотоксично. Оно не вызывает гибели мьшей даже в такой высокой дозе как 1000 мг/кг. Для цифлофосфана LDiY)составляет 500 мг/кг.
Таким образом, заявляемое вещест во обладает достаточно высоким иммунодепрёссивным действием,-сочетающимся с крайне низкой токсичностью, что отличает его от всех известных Количество РОК-10 леариых клеток Результаты экспериментов по определению количества РОК обрабатывали статистически. Титры антител выражали в виде супрессивных индексов (си), которые получали делени ем средней величины loq титров антител в опыте на среднюю величиИУ ос| титров антител в контроле. Величина индекса 0,7 и менее свидетельствует о наличии иммунодепрес сивного эффекта. Испытьшаемое вещество вводили внутрибрюшинио а течение трех дней перед иммунизацией в дозе 150 мг/кг в виде суспензии в 3 %-ном водном растворе крахмала. Инъекцию антитела производили через 24 ч после введения испытываемого вещества. Кроме того, было изучено влияние на иммунитет комбинированного применения испытьюаемого вещества (150 мг/кг). и циклофосфана (100 мг/кг). Производилось также сравнение иммунодепрессивной активности нового вещества с эталонным иммунодепрессантом -циклофосфаиом (додл 500 мг/кг}. Результаты эксперимента, представленные в таблице, свидетельствуют о том, что заявляемое вещество проявляет иммунодепрессивную активность: снижает титры антител (СИ 0,57), а также резко уменьшает количество РОК в селезенке. Титры мононукгемагглютининов (СИ) 9 нммунодепрессивных препаратов, ко рые, как правило, обладают высоко токсичностью. формула изобретения 1. 9-Иод-6-перхлорато-3,4-пиметоксикарбонилтетрацикло/6,1 ,1.0 дец-З-ен формулы 9 OdiCb обладающий иммуиодепрессивиой акт ностью. 2. Способ получения соединения по п. I, отличающийся И) тем, что 9,I0-пнметокснкар6онилтрицикло/4,2,2,0 /дека-3,7,9 триен подвергают вэаимодейстпию с иодом и перхлоратом лития в инертном орга-. ннческом растворителе при комиатной температуре. Источники информации, принятые во внимание при экспертизе 1 .Ковалев И,Е. и др.Введение в иммунофармакологию, Изд-во Казанского госуниверситета, Казань, 1972. V 2. Л. Kondo и др. Электрофильное присоединение в системе трицикло |,4,2,2,(Л дека-3,7 диена. Структуры и некоторые комментарии относительно природы п-участия, J. Org. Chen. 43, (6) 1180, 1978.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения 9-галоид-6-перхлорилокси-3,4-диметоксикарбонилтетрацикло [6,1,1,0 @ , @ 0 @ , @ ] дец-3-ена и 4,9-дигалоид-5,6-диметоксикарбонилтетрацикло[5,3,0,0 @ ,0 @ ' @ 0 @ ,8]дец -5-ена | 1979 |
|
SU883011A1 |
| Способ получения 9(2-нитрофенилтио) -6 - перхлорато - 3,4- диметоксикарбонилтетрацикло 6,1,1,0 ,0 дец-3-ена | 1979 |
|
SU725401A1 |
| Способ получения лактонов 9-арилтио-6-окси-4-метоксикарбонилтетрацикло (6,1,1,0,2,7,0,5,10)-деканрбоновых-3-кислот | 1980 |
|
SU891610A1 |
| @ -Хлоралкил- или циклоалкилперхлораты,обладающие иммунодепрессивной активностью,и способ их получения | 1979 |
|
SU809810A1 |
| Способ получения диметилового эфира трицикло /4,2,2,0 @ /-дека-3,7-диен-9,10-цис-эндо-дикарбоновой кислоты | 1981 |
|
SU973524A1 |
| Дигидрохлориды 9-замещенных 2(1-адамантил)имидазо (1,2- @ )бензимидазолов, обладающие иммунодепрессивным действием | 1983 |
|
SU1143039A1 |
| 3,4,9,10-Аллилтрицикло (4,2,2,0 @ )-дец-7-ен-карбоксилат в качестве связующего в литьевых пресс-композициях | 1981 |
|
SU1004353A1 |
| ИММУНОСТИМУЛЯТОР | 1993 |
|
RU2077339C1 |
| ПРОИЗВОДНЫЕ 8-КАРБАМОИЛ-2-(2,3-ДИЗАМЕЩЕННОГО ПИРИД-6-ИЛ)-1,2,3,4-ТЕТРАГИДРОИЗОХИНОЛИНА В КАЧЕСТВЕ ИНДУЦИРУЮЩИХ АПОПТОЗ СРЕДСТВ ДЛЯ ЛЕЧЕНИЯ РАКА | 2012 |
|
RU2625315C2 |
| СТЕРЕОИЗОМЕРЫ ТРИЦИКЛОДЕКАН-9-ИЛКСАНТОГЕНАТА | 2008 |
|
RU2470915C2 |


Авторы
Даты
1982-01-07—Публикация
1979-09-24—Подача