Изобретение относится к способу получения новых производных 3-уреидо(тио)хрюмонов общей формулы ,-t Rj ) о KI где X - кислород или сера; Ю 2 - галоген, алкил с 1-4 атомами углерода или алкоксил с 1-3-атомами углерода; П - равно 0,1 или 2; j Т, - водород; и, и - одинаковые или различные и означают водород, еилкил с. 1-4 aтoм€uv и углерода, алкоксил с 1-3 20 атомами углерода или вместе с атомом азота образуют 5- или 6-членное кольцо, или морфолиновое кольцо,25 которые проявляют гербицидную активность и могут поэтому найти применение в сельском хозяйстве. Известны реакции взаимодействия аминов с фосгеном с получением соот- jQ вётствуюцих изоциатов Г, которые при обработке их амином дают соответствующие уреидопроизводные 2. Цель изобретения - получение новых производных З-уреидо(тио)хромонов, обладаюашх ценными свойствами. Поставленная цель достигается тем, что при получении производных З-уреидо(тио)хромонов формулы (I) соединение-формулы где X , Z и п - имеют вьваеуказанные значения, подвергают взаимодействию с фос.геном в среде инертного органического растворителя при 50-120®С с последующей обработкой полученного продукта ё1мином формулы « , где имеют вышеуказанные значения,
в среде безводного инертного органического растворителя при 20-120с,
Предпочтительно в качестве инертного органического растворителя используют ароматический, алифатический или хлорированный алифатический углеводороды, простой эфир или нитрил. Представителями растворителей являются бензол, толуол, ксилолы, хлорбензол, гексан, гептан, цнклогексан, метилциклогексан, дихлорэтан, дихлорэтилен, четыреххлористый углерод, перхлорэтилен, диоксан, тетрагидрофуран, диэтиловый или изопропиловый эфиры, или ацетонитрил.
В случае соединений, для которых Х означает атом кислорода, предпочтительно используют эквимолекулярны количества амина формулы (111) и полученного на первой стадии 3-изоционатохромона, В случае соединений для которых X означает атом серы, используют молярный избыток амина формулы (ГЦ) по отношению к соединению, полученному на первой стадии Предпочтительно используют по меньшей мере два молярных эквивалента амина формулы (Г11) на молярный эквивалент соединения, полученного на первой стадии.
Пример 1. Получение 3-(3 ,-диметилуреидо)хромона (соединение 1) о
В 150 мл 2М раствора фосгена в толуоле вносят 14,5 г 3-аминохромон и кипятят с обратным холодильником в колбе, снабженной системой охлаждения посредством сухого льда. Заменяют охлгикдение сухим льдом на охлаждение водой для завершения Дегазации, доводят до комнатной температуры и фильтруют через стеклянный фильтр. После промывки 100 м толуола и высушивания под вакуумом получают 13 г 3-изоцианатохромона с т.пл. 130°С. Выход 77,4%.
К раствору 13 г 3-изоцианатохромона в 50 мл толуола быстро добавляют раствор 7,5 г безводного диметиламина в 100 мл безводного толуола. Температура реакционной смес быстро повышается от 20 до . Затем происходит кристаллизация продукта. Перемешивают еще 20 мин до тех пор, пока температура реакционной среды не снизится до . После отсасывания и перекристаллизации из 1000 мл диизопропилового эфира и высушивания получают 5,4 г 3- (З, /-диметилуреидо)хромона с т.пл, ,
Найдено,%: С 62,10; Н 5,25; N 11,95.
Вычислено,%: С 62,06; Н 5,21; N 12,06,
Исходный 3-аминохромон, плавящийся при 124°С, получают путем восстановления 3-нитрохромона с
помощью бисульфита натрия в воднойсреде по известному способу, при этом 3-нитрохромон получается(по известному способу из 2 -окси-2 --нитроацетофенона.
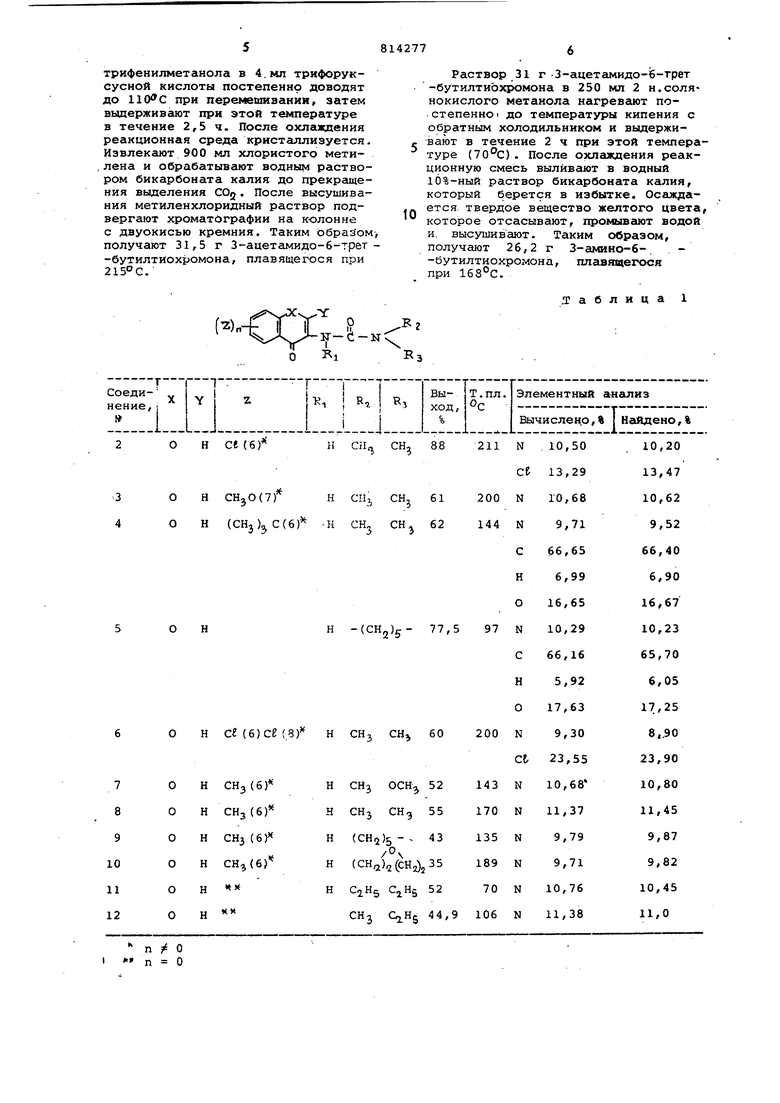
Пример 2. Аналогично примеру 1 из соответствующих исходных веществ получают соединения 2-12, характеристики которых приведены в табл. 1.
3-Аминохромоны, используемые в качестве исходного вещества для получения соединений 2-12, получаются описанным выше способом.
Пример 3. Получение 3-(3,3-диметилуреидо)тиохромона (соединение 13) ,
Суспензию 9,3 г 3-аминотиохромон в 129 мл раствора фосгена в толуоле постоянно нагревают до температуры кипения с обратным холодильником при охлаждении холодильника сухим льдом вплоть до прекращения выделения газов. Эта операция вызывает необходимость длительного нагревания (12 ч). Затем удаляют избыток фосгена кипячением с обратным холодильником (охлаждение водой), После охлаждения отсасывают осадок зеленовато-желтого цвета и промывают его раза 50 мл хлористого метилена. После высушивания получают таким образом 10.0 г 2,3-дигидробензотиопиран 3, 4-с1 -5-оксазолийхлорид.
Выход 83,6%, т,пл, 160°С.
К суспензии 9 г полученного ранее продукта в 50 мл безводного толуола добавляют по каплям раствор 2,25 г безводного диметиламина в 41 мл безводного толуола, OodJie охлаждения до комнатной температуры смесь выливают на расколотый лед, , затем разбавляют 100 мл воды и нейтрализуют избытком бикарбоната калия. Водную фазу экстрагируют 2X500 мл эфира для анестезии и декантируют. Экстракты затем высушивают и фильтруют, а выкристаллизовавшийся остаток обрабатывают 2x20 диизопропилового эфира. После фильтрования и высушивания получают таким образом 5,3 г 3-метиламинотиохромона с т.пл, 134с.
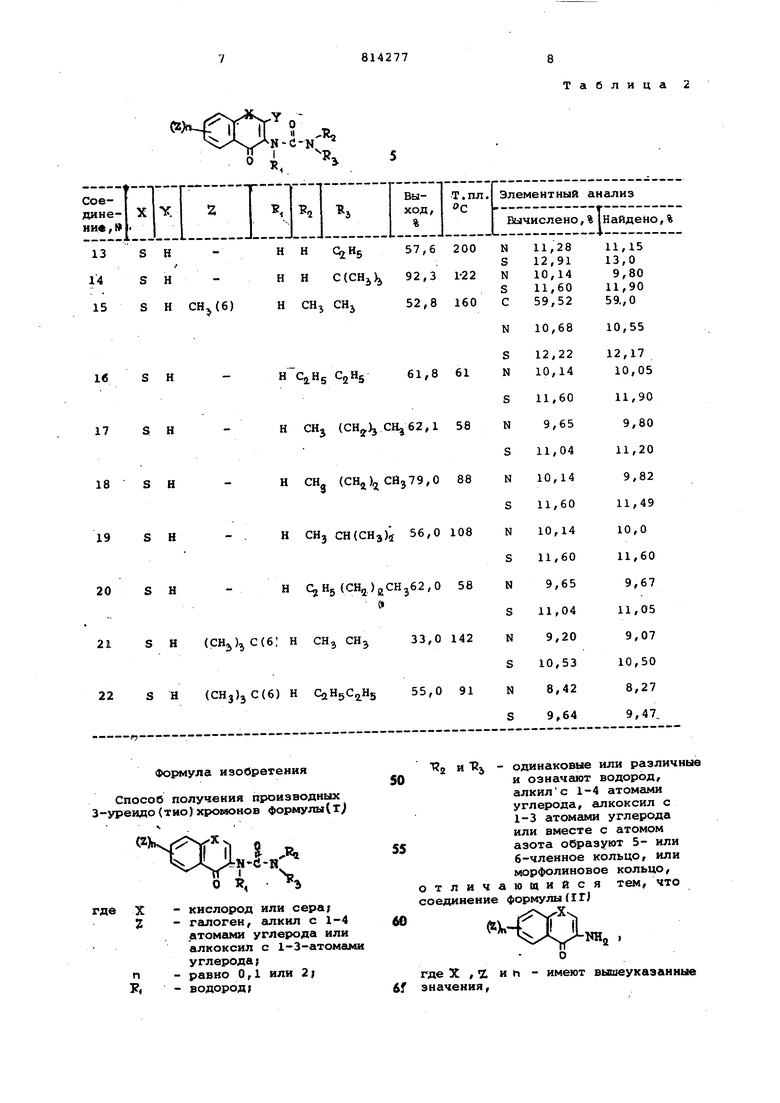
Пример 4. Следуя методике условий примера 3 из соответствующих исходных веществ получают соединения 14-22, указанные в табл.2, Замещенные З-аминотиохромоны, используемые в качестве исходных веществ для получения соединений 14-21, получают каталитическим гидрированием соответствующих 2-галоид-З-амино(тио)хромонов, З-Амино-6- -трет -бутилтиохромон, исходное соединение для получения соединения 22, получают - следующим образом, : Суспензию 44,6 г 3-ацетамидо-6-трет -бутилтиохромона-4 и 46,8 г
трифенилметанола в 4. мл трифорукеусной кислоты постепенно доводят до ll(flc при перемешивании, затем выдерживают при этой температуре в течение 2,5 ч. После охлаждения реакционная среда кристаллизуется. Извлекают 900 мл хлористого мети, лена и обрабатывают водным раствором бикарбоната калия до прекраидения выделения COg. После высушивания метиленхлоридный раствор подвергают хроматографии на колонне с двуокисью кремния. Таким образом получают 31,5 г З-ацетамидо-6-трет-бутилтиох;ромона, плавящегося при 215С.
Раствор 31 г -З-ацетамидо-б-трет -бутилтиохромона в 250 мл 2 н.солянокислого метанола нагревают постепенно до температуры кипения с обратнЕом холодильником и выдержи, вают в течение 2 ч при этой температуре (70с) . После охлаждения реакционную смесь выливают в водный 1б%-ннй раствор бикарбоната калия, который берется в избытке. Осаждается твердое вещество желтого цвета, которое отсасывают, промывают водой и. высушивают. Таким образом, получают 26,2 г З-амино-6-. -бутилтиохромона, плавящегося при 168°С.
.Таблица 1
Кг


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных (5-алкилуреидо-1,3,4-тиадиазол2-ил-сульфонил) уксусной кислоты | 1977 |
|
SU645575A3 |
| Способ получения производных цефалоспорина | 1980 |
|
SU1138031A3 |
| Способ получения производных цефалоспорина | 1979 |
|
SU1118289A3 |
| ПРОИЗВОДНЫЕ N-ФЕНИЛГЛИЦИНАМИДА, СПОСОБ ИХ ПОЛУЧЕНИЯ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ СРОДСТВОМ К РЕЦЕПТОРАМ ХЦК И ГАСТРИНА | 1991 |
|
RU2076108C1 |
| Способ получения водорастворимых производ-НыХ НиТРОзОМОчЕВиНы | 1977 |
|
SU849999A3 |
| Способ получения производныхоксадиазолина | 1973 |
|
SU509232A3 |
| Способ получения бис-(1,3-дизамещенных мочевино) сульфидов | 1975 |
|
SU580833A3 |
| Способ получения аминопроизводных бензофенона | 1973 |
|
SU508176A3 |
| Способ получения производных имидазо/ , -B/ ТиАзОлА | 1972 |
|
SU847915A3 |
| Способ получения производных цефалоспорина или их фармацевтически приемлемых солей | 1981 |
|
SU1095879A3 |

п 5 О I п О
Таблица 2 9814 подвергают взаимодействию с Фосгеном в среде инертного органической го растворителя при 50 120с о последующей обработкой полученного продукта амином формулыflU) ,, Кй омп -в -у ъ где RI и «5 - имеют вышеуказанные значения, 27.7 10 в среде безводного инертного органического растворителе при 20-120 С. источники инЛоомаиии источники информации, принятые ВО. внимание при экспертизе . 5 .1. Войганд-Хильгетаг. Методы эксперимента в органической химии, м., Хюия, 1968, с. 438-439. 2. Там же, с. 377. .
Авторы
Даты
1981-03-15—Публикация
1979-04-06—Подача