Ье5разуют вторую C-G связь, если Z и z образуют вторую С-С связь, то и обозначают каждый в отпельности водшюла или.образую или образуют вторую С-С связь, вводят во взаимодействие G згиолом обще формулы III. в которой R имеет вышеприведенные значения. Реакция может быть осуществлена в присутствии или отсутствии раство рителя, а также с использованием катализатора, В соответствии с описываемым спо собом , -, - или й -ненасы щенный стероид-спиро-оксазоладзинон общей формулы И обрабатывают С,.,|-ти алканкарбоновой кислото, например тиоуксусной кислотой или тиопропйон вой кислотой и отделяют полученный продукт присоединения, ЕСЛИ приводят во взаимодействие соединения общей формулы II с алкил меркаптаном, то обычно требуется про должительный нагрев для завершения реакции, В таких случаях реакцию предпочтительно осуществляют в присутствии основного катализатора, например, пиперидина или ионообменнoй смолы типа четвертичного аммония в гидроксильном цикле. Целевые продукты могут -быть выделены в виде стереоизомеров. АНтиальдостероновое действие новых соединений исследуется следующим образом. Надпочечная железа крыс удаляется за 18 ч до обработки. Подлежащее исследованию соединение вводят животным вместе с подкожным введением 12,5 мг аЦетата дезоксикортикостерона (ДОКА) вётцества, способного дополнять действие сшьдостерона, и содержание натрия и калия в моче определяют методом пламенной фотометрии. В сравнительном опыте вводят оральную дозу 400 мкг спиронелактона (17ог-карбоксиэтил-178-окси-Яз -ацетилтио-андрост-4-ен-3-онлактона). Результаты оценивают путем вычисления значений fog (10 Na/К), Результаты представлены в таблице.


| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения стероидных спирооксазолидинов или их стереоизомеров | 1978 |
|
SU931109A3 |
| Способ получения -гомостероидов | 1975 |
|
SU626706A3 |
| Способ получения производных стероидспирооксатиазолидинов в виде их стереоизомеров или их смесей или их солей | 1981 |
|
SU1079177A3 |
| СПОСОБ ЛЕЧЕНИЯ ДОБРОКАЧЕСТВЕННОЙ ГИПЕРПЛАЗИИ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ, ФАРМАЦЕВТИЧЕСКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ИНГИБИТОР 5-АЛЬФА-РЕДУКТАЗЫ | 1992 |
|
RU2125879C1 |
| Способ получения производных прегнана | 1978 |
|
SU786906A3 |
| Способ получения тиоацетил-или меркаптопроизводных стероидных лактонов | 1974 |
|
SU517262A3 |
| 19,11-ПЕРЕКРЫТЫЕ МОСТИКАМИ 4-ЭСТРЕНЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ, ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ | 1993 |
|
RU2157814C2 |
| Способ получения производных прегн-4-ена | 1978 |
|
SU826958A3 |
| Способ получения производных 6-оксо-17 @ -этинил-17 @ -трифторацетоксигонана | 1982 |
|
SU1176845A3 |
| Способ получения 17-галогенэтинилстероидов | 1984 |
|
SU1389681A3 |

ДОКА
480
Спиронолактон
7с ацетилтиоэcтp-4-eн-4-oн-17Ь-спиро-5 -{2 -оксо-З-метилоксазолидин) 480
ДОКА :
«
480
Спиронолактон
7c3t-этил тиоанд рос т 4-ен-3-он-17Ь-спиро-5 -(2 -оксо-3-метилоксазолидин)480 И/Сп - испытуемое вещество/с Из таблищд внцнр, что То -ацетилтиоэстр-4-ен-3-он-17Ь-спиро-5-(2 -оксо-З -метилоксазолидин) и 7С| зтил-. -тио-андрост-4-ен-3-он-17 Ь -спиро-5 -; -(2-оксо-3-метилоксазолидин) значительно подавляют действие ДОКА на крыс. Утеротропическое и антиэстрогенное действия соединения были изучены на мышах-самках младенческого возраста по методике Эдгрена, При подкожном введении соединения в суточных дозах 30 мг/кг не наблюдается никакого утеротропического эффекта, Исследование антиэстрогенного эффекта показы- 6$
0,73
108
1,52
0,94
96
1,43
0,60
75 1,05.
1,04
82
1,09 jftO пиронолактон. вает, что данное соединение не вызыВовет значительного уменьшения утеротропического действия бензоата зстрадиола при одновременном введении в течение 3 сут суточными дозами 0,1 мкг/животное, Андрогенное и антиандрогенное действие данного соединения были исследованы на кастрированных самцах крыс по методике Дорфмана. При введении соединения в течение 7 сут подкожно суточньали дозами 1 мг/животное не наблюдается никакого андрогенного эффекта, В этом опыте соединение не подавляет действие пропионата тестостерона, введенного в суточных дозах 50 мкг.
При подкожном введении животньлм спиронолактона суточными дозами 1 мг наблюдалось значительное уменьшение андрогенного эффекта пропионата тестостерона, введенного одновременно со спиронолактоном.
Пример 1. То -Ацетилтко-андpocT-4-eH-3-oH-17t -cnMpo-5 -(2 -оксо-З-метилоксазолидин) .
Смесь 3,50 г андрост-4,6-диeн-3-oн-17%-cпиpo-5 - { 2 -оксо-З -метилоксазолидина) и 3,5 мл тиоуксусной кислоты нагревают -на паровой бане в течение 1,5 ч. Избыток тиоуксусной кислоты отгоняют под вакуумом, остаток растирают с изопропиловь м эфиром и о делившееся вещество отфильтровывают.Полученный сырой продукт (4,0 г) растворяют в 120 мл тешього этилацетата, раствор обесцвечивают при помощи активированного угля,,отфильтровывают и упаривают до конечного объема приблизительно 35 мл. 2,20 г Idr-ацетилтио-андрост-4-ен-3-он-17ф-спиро-5 -(2 -оксо-з -метилоксазолидина) вЕдцеляют из концентрата. Т.пл. 218-219° С, -48(,5 в хлороформе), УФ-спектр i.Jf 237мм {Е 16,500).
Пример2. 1 -Ацетилтио-андрост-4-ен-3-он-17}7-спиро-5 - (2 -оксо-З -метил-оксазолидин) .
Опыт проводят так же, как в примере 1, но в качестве исходного вещества берут 4,0 г андрост-1,4-диен-3-он-17Ь-спиро-5 -(2 -оксо-з-метилоксазолиди 1а) . Получают 3,55 г сырого 1о6-ацетилтиоандрост-4-ен-3-он-17 -спиро-5 -(2 -оксо-З -метилоксазолидина) ; т.пл. 2.04-205 С. . Этот сырой продукт растворяют в 35 мл этилацетата и раствор упаривают до одной четверти первоначального объема. Получают 2,37 г очищенного продукта; т.пл. 204-2060С,/ 0 /g +З Е-«Н (с 1 в хлороформу), Уф-спектр Х р, 240 JUM ( 300) .
Пример 3. 1 (ацетилтио) -андрост-4-ен-З-он- 17Ь-спиро-5 -(2 -оксо-з-метилоксазолидин),
Смесь 1,20 г андрост-1,4,6-триен 3-он-17Тэ-спиро-5 -(2 -оксо-З -метилоксазолидина) и 2 мл тиоуксусной кислоты нагревают на паровой бане в течение 1., 5 ч:. Избыток тиоуксусной кислоты отгоняют под вакуумом, маслянистый остаток растирают с изопропиловым эфиром, затем отделившееся кристаллическое вещество отфильтровывают и промывают холодным изопропиловым эфиром. Полученный сырой продукт весом 1,64 г .растворяют в 10 tvui ацетона при комнатной температуре, раствор обесцвечивают активированным углем, отфильтровывают, упаривают до половины первоначального объема при комнатной температуре под пониженным давлением и к концентрату добавляют 14 мл изопропилового эфира. Отделившийся продукт отфильтровывают и получают 1,10 г чистого 1,(ацетилтио -андрост-4-ен-3-он-17Ь-спиро-5 - (2 -оксо-З -метилоксазолидина). Спектроскопические данные продукта следующие: 237 им (Е ); ИКтах -1б15 (), 1760 и 1690 ТС О см ). ,
ЯМР(СОСЕ,3) : cf 2,85 (ЗН, S ,-NCHj ) ,
o 2,40 (6Н,Ъ, ацетилтио} , 5,75 (1К, уширенный, 4 Гц, СН) м.д.
Пример 4. 7об-Ацетилтио-эстр-4-ен-3-он-171 -спиро-5 -(2 -оксо- з -метилоксазолидин).
Смесь 0,96 г эстр-4,6-диен-З-он-17Ь-спиро-5 -(2 -оксо-Згсметилоксазолидина) и 1 мл тиоуксусной кислоты нагревают на паровой бане в течение 1 ч. Избыток тиоуксусной кислоты отгоняют при и пониженном давлении,
0 остаток подвергают двукратной перекристаллизации из ацетона. Получают ,, 0,17 г 7с1С.-ацетилтио-эстр-4-ен-3-он-17&-спиро-5 -(2 -оксо-З -метил-оксазолидина); т.пл: 203 20бОс
5 -89,7° (с 0,5 в хлороформе), 236 JV/M (Е 20,600).
Пример 5. 7о.-Ацетилтио-136-этил-гон-4-ен-3-он-17Ъ-спиро-5 -{2-оксо-3-метилоксазолидин) ,
0
Смесь 1,4 г 13В-ЭТИЛ-ГОН-4,6-диен-3-он-17Ь-спиро-5 - (2 -оксо-3-метилоксазолидина) и 1,4 мл тиоуксусной кислоты нагревают на паровой бане в. течение 1 ч. Избыток тиоуксусной кис5лоты отгоняют ..под . вакуумом рри 50С и маслянистый остаток растирают со смесью 1:1 этилацетата и изопропилового эфира. Полученное твердое веще- ство перекристаллизовывают из смеси
0 1:1 метанола и изопропилового эфира. Получают 0,71 г 7ct-ацетилтио-138-этил-гон-4-ен-3-.он-17Ъ-спиро-5 -(2 -оксо-З -метилоксазолийина) ;, т.пл. 135-1 , -73,1°(с 0,5 в хлороформе). УФ 236|UM
5 (Е 18 800)
Пример 6, 7Q -Этилтиo-aндpocт-4-ен-3-он-17Ь-спиро-5 - (2 -оксо-З -метилоксазолидин).
Смесь 2,1 г анцрост-4,6-диен-З-он-17г -спиро-5 -(2 -оксо-З -метилоксазолидина) , 1,3. мл пиперидина и 12 мл этк.лмеркаптана нагревают с. обратным холодильником в течение 48 ч. В, течение этого времени из смеси выделяется твердое вещество желтого цвета. К концу реакции вьщелиБшееся твердое вещество растворяют путем добавления к смеси 50 мл банзола и полученный
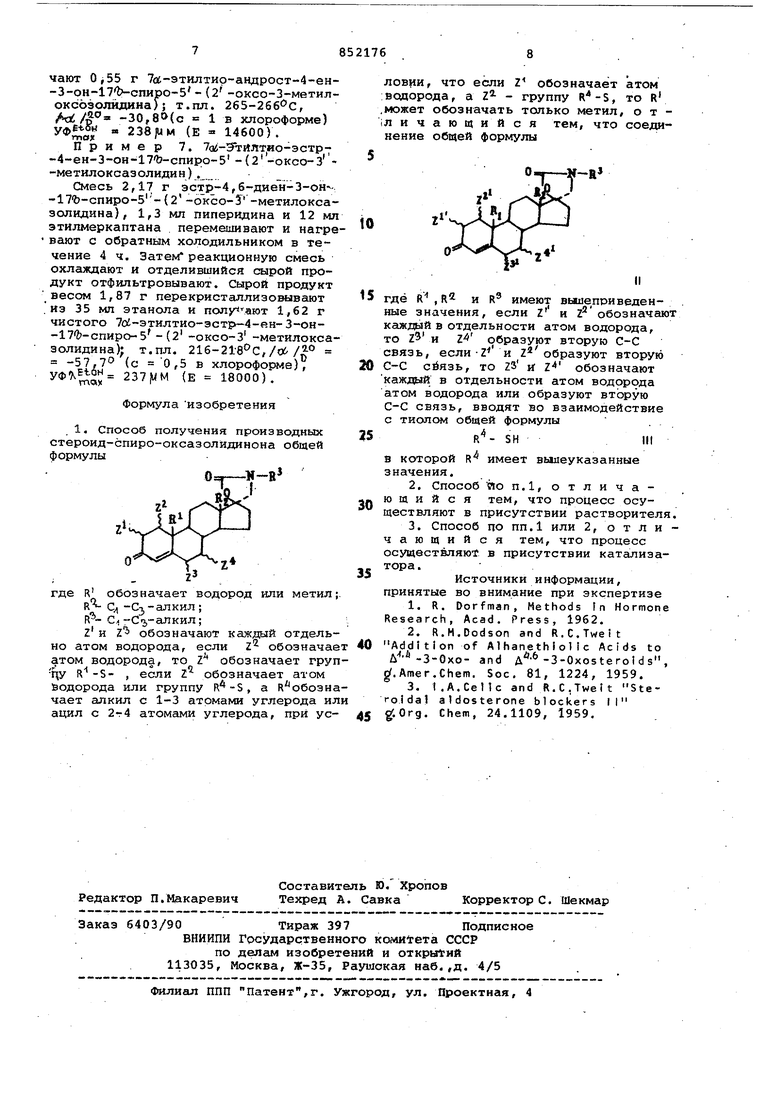
раствор выпаривают в вакууме. Остаток кристаллизуют путем растирания с холодным этилацетатом. Отделившийся кристаллический сырой продукт весом 1,02 г отфильтровывают и перекристаллизовывают из 35 мл этилацетата. Получают Oj55 г 7а-этилтир-андрост-4-ен-3-он-171 -спиро-5 - (2 -оксо-3-метилоксозолидина); т.пл. 2б5-266 с, -30,80(0 1 в хлороформе) « м (Е 14600). Пример 7. 7сй-дтгйлт,ио-эстр7 -4-ен-3-он-17Ь-спиро-5 -(2-оксо-3 -метилоксазолидин) . Смесь 2,17 г эстр-4,6-диен-3-он--; -17Ь-спиро-5- (2 -оксо-J -метилоксазолидина), 1,3 мл пиперидина и 12 мл этилмеркаптана перемешивают и нагре вают с обратным холодильником в течение 4 ч. Затем реакционную смесь охлаждают и отделившийся сырой продукт отфильтровывают. Сырой продукт весом 1,87 г перекристаллизовывают из 35 мл этанола и 1,62 г чистого 7о -этилтио-эстЕ -4-ен- 3-он-17Ь-спиро-5- (2 -оксо-З -метилоксазолидина); т.пл. 216-218 C, -57.7 (с 0,5 в хлороформе), 237 VM (Е 18000). Формула изобретения 1. Способ получения производных стероид-спиро-оксазолйдинона общей формулы 0, где R обозначает водород или метил R Ci-С-1,-алкил; ,-апкил; Z и 1 обозначают каждый отдельно атом водорода, если l обозначае атом водорода, то Z обозначает груп цу R -S- , если Z обозначает атом йодорода или группу , а Я обозна чает алкил с 1-3 атомами углерода ил ацил с 2т4 атомами углерода, при условии, что если Z обозначает атом водорода, а Z- - группу К-5, то R может обозначать только метил, о т личаю1цийся тем, что соединение общей формулы оЛА,4 где К , R и R имеют выше приведенные значения, если Z и Z обозначают каждый в отдельности атом водорода, то и образуют вторую С-С связь, если-Z и Z образуют вторую С-С сйязь, то Z3 иг обозначают каждый в отдельности атом водорода атом водорода или образуют втсурую С-С связь, вводят во взаимодействие с тиолом общей формулы 4 SH в которой R имеет вышеуказанные значения. 2.Способ По п.1, отличают и и с я тем, что процесс осуществляют в присутствии растворителя. 3.Способ по ПП.1 или 2, о т л и чающийся тем, что процесс осуществляют в присутствии катализатора. Источники информации, принятые во внимание при экспертизе 1.R. Dorfman, Methods tn Hormone Research, Acad. Press, 1962. 2.R.M.Dodson and R.C.Tweit Addition of AlhanethiolIc Acids to Л- -3-0x0- and A -3-Oxo5terolds, .Amer.Chem. Soc. 81, 1224, 1959. 3.I.A.Cellc and R.C.Tweit Steroidal aidosterone blockers II giOrg. Chem, 24.1109, 1959.
Авторы
Даты
1981-07-30—Публикация
1979-03-29—Подача