Пример 2 , AHflpocT- t-eH, 3-он-175-спиро-5-(2-оксо-3метилоксазолидин). Способ А. Смесь 9 г андрост-5-ен-3(1-ол-175 .спиро-5-(2-оксо-З -метилоксазолидина), полученного по примеру 1, 10,2 г изопропилата алюминия и 52 мл циклогексанона кипятят в 200 мл сухого толуола в течение 13 ч. После охлаждения реакционную смесь экстра гируют тремя порциями по 50 мл раствором соляной кислоты, 15 мл воды и 15 мл насыщенного раствора кислого углекислого натрия и водой. Органическую фазу сушат, выпаривают и полученный маслянистый остаток растирают с изопропиловым эфирюм. Полученный кристаллический продукт промывают изопропиловым эфиром и фильтруют, в результате перекристаллизации неочищенного продукта из этилацетата получают k,2 г чистого соединения. Т.пл. 189°С; oCJ +kk°(,S, хлороформ). Если неочи щенный продукт перекристаллизовывают из метанола при добавлении изопропилового эфира, то точка плавления продукта, получаемого по примеру, равна . Способ В. Смесь 2,03 г М-этоксикарбонил-17 х метил-аминометиландрост-.Б-ен-Зр-ола, 5,2 мл с-гексанона и 2,0 г изопропилата алюминия в 30 мл сухого толуола кипятят в течение 7 ч. Реакционную смесь экстрагируют 5%-ным раство ром соляной кислоты..После этого органическую фазу встряхивают до нейтральной реакции с насыщенным водным раствором кислого углекислого натрия и водой, сушат и выпаривают. После растирания маслянистого остатка с изопропиловым эфиром получают 1,08 г неочищенного ан);рост- -ен-3-он-175-ч:пиро-5 - (2-оксо-З -метилоксазолидина). Т. пл. (после перекристаллизации из этилацетата) 188-189 C; (,5, хлороформ). П р и м е р . 3 . 3(-0ксиандрост 5-ен-175-спиро-5 -(2 -оксо-З-аллил оксазолидин). Стадия А. По способу, описанному в примере 1, проводят стадию А, однако в каче стве исходного соединения берут 9;06 г Зй-оксианДрост-5-ен-175-спир оксирана и используют 25 мл аллил 96 амина и 0,90 г -толуолсульфокислоты, при этом после перекристаллизации из этилацетата получают 7,72 г 17ot-алиламинометиландрост-5 ен-3/5, Ог.г.,т20 17(Ь-Диола. Т.пл. ,5, хлороформ). Стадия В., По способу, описанному в примере 1, стадия В, однако исходя из 7/18 г 17оС-аллиламинометиландрост-5 ен-3 17(2 -Диола и перекристаллизовывая неочищенный сырой продукт из этилацетата при добавлении изопропилового эфира, получают 6,92 г N-этоксикарбоИИЛ-.17(Л-аллиламинометиландрост-5-енЗр, 17(3-диьла. Т.пл. Й8°С;И2О -57°(,5, хлороформ). Стадия С. Замыкание кольца указанного N-этоксикарбонил-17оС-аллиламинометильногосоединения проводят, как описано в примере 1, стадия С, в результате чего получают требуемое по примеру соединение. Т.пл. 259 С; о ,5, хлороформ). П р и м е р ij. З-З-Оксиандрост-5-ен-175-спиро-5-(2-оксо-3-изопропиЛ7 оксазолидин). Стадия А. По способу, описанному в примере 1, стадия А, исходя из 6,0 г Зр-оксиандрост-5-ен-175-спирооксирана и 17 мл изопропиламина и используя в качестве катализатора 0,60 гп-толуолсульфокислоты, получают 7,11 г 17о1;-изопропиламинометиландрост-5-ен-3(, 17(3-диола. После перекристаллизации из этилацетата при добавлении эквивалентного объема Н-гексана продукт плавится при 112-113c;i:oC3 j° -76,(,5,хлороформ). Стадия В. Исходя из продукта, полученного со стадии А, и по методике примера.. 1 , стадия В, получают Н-это1 сикарбонил-17(Х.ИЗОпропиламиномет-иландрост-5-ен-З . 17 -диол,. который после перекристаллизации из этилацетата плавится при С; л. (,5, хлороформ). Стадия С. Замыкание кольца указанного со.единения проводят, как описано в . примере 1, стадия С, в результате чего получают требуемое соединение.
79
которое после перекристаллизации из этилацетата плавится при 222-223°С; -117°(,5, хлороформ).
Пример 5 . 3(Ь-Фтораидрост-5-ен- 175-спиро-5- (2-оксо-3-метилоксазолидин).
Стадия Д.
К перемешиваемой суспензии 8,85 г 3(1-фторандрост-5-ен-17-она и 14,Об г триметилсульфонийиодида в 100 мл сухо го диметилформамида добавляют за четверть часа 8,50 г калий- трет-бутилата при . Полученную смесь перемешивают в течение 2,5 ч, а затем выливают в 1700 мл ледяной воды. Осажденные кристаллы отфильтровывают и промывают водой до нейтральной реакции. После перекристаллизации неочи ценного продукта из метанола получают 7,15 г чистого 3(Ь-фторандрост5-ен-1 75-спирооксирана. Т.пл. ос -9(,5, хлороформ)
Стадия В.
По способу, описанному в примере 1, стадия А, исходя йз 6,1 г 3(Ь фторандрост-5-ен-175-спирооксирана и 50 мл жидкого метиламина и используя 0,60 гп -толуолсульфокислоты в качестве катализатора, после перекристаллизации из метанола получают 5,1 г 3ft -фтор-17(1-метиламинометиландрост-5-ен-17р-ола. Т.пл. 175°С; Ы -1 О0-( ,5 , хлороформ).
Стадия С.
По способу, описанному в примере 1, стадия В, однако исходя из Зр-фтор-1 -метиламинометиландрост-5-ен-17 3-ола, полученного на указанной стадии В, получают соответствуюи;ее N-этоксикарбониль.ное производное После перекристаллизации из метанола продукт плавится при 172 С; обД -77°(,5, хлороформ).
Стадия Д.
2,10 г 3 3-фтор-М-этоксикарбонил 1 .-метиламинометиландрост-5-ен-17Э-ола, полученного как для стадии С, обрабатывают в соответствии со способом, описанным в примере 1, стадия С, и после перекристаллизации из изопропилового эфира получают 1,79 г требуемого соединения. Т.пл. W D -127°(,5, хлороформ).
Пример 6 . Андрост- -ен-3-он-175-спиро-5-(2-оксо-3-аллилоксазолидин).
2,16 г М-этоксикарбонил-17с.-аллиламинометиландрост-5-ен-Зр, 17р-диола
98
полученного как указано в примере 3, стадия В, окисляют в соответствии со способом, изложенным в примере 2, стадия В. Получают 1,3 г неочищенного продукта. После перекристаллизации из этилацетата и добавления изопропилового эфира получают 1 г продукта. Т.пл. 13Ы32С;Ы +7,2 (,5, хлороформ).
Пример 7 . Андрост- -ен3 он-175-спиро-5-(2-оксо-3-изопропилоксазолидин).
2,1 г М-этоксикарбонил-17с1 -изопропиламинометиланд рост-5-ен-3(3, 17/ -Диола, полученного в соответствии с примером 1, на стадии В, окисляют, как описано в примере 2, стадия В. Полученный продукт перекристаллизовывают из этилацетата при добавлении изопропилового эфира, в результате чего получают 0,90 г требуемого соединения. Т.пл. 177-179°С; об (,5, хлороформ).
Приме Р 8.Aндpocт-A,6-диeн-3-oн17S-cпиpo-5-(2-oкco-з-мeтилoкcaзoлидин) Способ А.
Смесь 3,15 г андрост-4-ен-3-он1 75-спиро-5-(2-оксо-З-метил-оксазолидина), полученного, как описано в примере 2, и 13 г хлоранила в k мл трет.-бутанола кипятят в течение 3 ч при перемешивании. Реакционной смеси дают остыть до комнатнс$й температуры, фильтруют и полученный фильтрат выпаривают. Остаток растворяют в хлороформе, нерастворимую часть отфильтровывают и хлорофориовый раствор экстрагируют четырьмя порциями 5 -ного раствора гидроокиси натрия по 12мл каждая, а затем двумя порциями воды по 10 мл, после чего сушат сыльфатом магния. Полученный экстракт концентрируют, а остаток переводят в кристаллическое состояние за счет растирания, в результате чего получают 2,75 г неочищенного продукта. После перекристаллизации из этилацетата, повторенной дважды, полученный продукт плавится при 212-213С; -20,3(,5, хлороформ).
а к -2в2Аллл.
Способ В.
К перемешиваемой суспензии 7,18 г андрост-5-ен-Зр-ол-17-5-спиро-5-{2оксо-ЗМетилоксазолидина), полученного по способу, описанному в примере 1, и 0,28 г порошкообразного сухого ацетата натрия в 70 мл сухого тетрагидрофурана по каплям добавляют смесь 3,2 г брома и 10 мл ледяной уксусной кислоты. При 10°С, спустя несколько минут после того, как растворится стероид, можно наблюдать желть)й осадок. Спустя 0,5 ч, при перемешивании реакционную смесь выливают на 900 мл ледяной воды, оставляют на некоторое время, и осадо отфильтровывают. Сырой продукт поме щают в too мл ледяной уксусной кислоты и полученную суспензию нагревают до 6ofc, 6,56 г бихромата натрия, содержащего 2 моль кристаллизационной воды в 20 мл ледяной кисл ты, нагревают до 80°С и добавляют к указанной суспензии при перемешивании. Полученный темный раствор пере мешивают при в течение получас охлаждают и выливают в 800 мл ледян воды. Выпавшее в осадок кристалличе ское вещество фильтруют и промывают водой. 9,5 г полученного неочищенно дибромкетона растворяют в 100 мл диметилформамида, добавляют 9,5 г бромистого лития и 9,5 г карбоната лития. Полученную смесь кипятят в течение 1,5 ч при перемешивании. Неочищенный продукт выливают в ледяную воду и выделяют фильтровани ем. Выход (после перекристаллизации из этилацетата с использованием дре весного угля при обеспечивании) составляет «,32 г. Т.пл. 212°С; -21°(,5, хлороформ). Пример 9. Андрост-1,Ч-диeн 3-oн-17S-cпиpo-5-(2-oкco-3-мeтил.oкcaзoлидин) . 2,18 г андрост- -ен-3-он-17Sспиро-5-{2-оксо-3-метилоксазолидина) полученного по примеру 3, кипятят в Зб мл сухого диоксана с 1,5 г 2,3-дихлор-5,6-дициано-1 , -бензохино на в течение tO ч. Смеси позволяют остыть до комнатной температуры, оса док отфильтровывают и полученный фильтрат выпаривают. Выпаренный остаток растворяют в 70 мл дихлорметана и экстрагируют пятью порциями до 10м 1%-ного раствора гидроокиси натрия и после этого тремя порциями воды по 10 мл. Дихлорметановый раствор сушат пропускают через силикагель и выпаривают, в результате чего получают 1,5 г желтого кристаллического продукта. После перекристаллизации из этилйцетата (перекристаллизацию проводят дважды) получают 0,2 г чистого продукта . Т.пл. (,5, хлороформ); ° нм. Пример 10. Андрост-1 .tjS-триен-3-он-175-спиро-5-(2-оксо-Зметилоксазолидин). Смесь ,28 г 3(3-оксиандро,ст-5-ен175-спиро-5-(2-оксо-З-метилоксазолидина) , полученного в примере 1, и 8,15 г 2,3-Дихлор-5,6-дициано-1 ,«бензохинона в 120 мл диоксана кипятят в течение 80 ч. Реакционную смесь обрабатывают, как описано в примере 9, за исключением того, что дихлорметановый раствор неочищенного продукта пропускают через нейтральную окись алюминия. Полученный продукт перекристаллизовывают из этилацетата, в результате чего получают 0,90 г требуемого соединения. Т.пл. 22322г °С;И 1 (,5,xлopoФoP Ь 298 , 221 нм. Пример 11. 1Зр-этил-З-метоксигона-2,5-(Ю)-диен-175-спиро5-(2-оксо-З-метилоксазолидин). Способ А. Стадия А. К перемешиваемой суспензии kk,0 г 1 3(5-этил-3-метоксигона-2,5(10) диен17-она 118,8 г триметилсульфонийиодида в 660 мл сухого диметилформамида добавляют г калий -трет-бутилата за полчаса при . Перемешивание продолжают в течение 2 ч. Затем реакционную смесь выливают в ледяную воду, и осажденный белый кристаллический продукт отфильтровывают и промывают водой. Неочищенный продукт сушат, кипятят с двукратным объемом метанола и фильтруют в горячем состоянии. В результате получают 3,1 г 13fi этил-3-метоксигона-2,5(10)-диен-17Sспирооксирана с т.пл. 183°С. Для получения соединения аналитической степени чистоты около 1 г неочищенного продукта перекристаллизовывают из 30-кратного объема этилацетата. Т.пл. полученного соединения 187189°С; ос +106° (,5, хлороформ) .i Стадия В. В соответствии с процедурой, описанной в примере 1, стадия А однако, сходя из 30 г полученного 13р -этил3-метоксигона-2,5(10)-диен-175-спироксирана и 90 мл жидкого метиламина, используя 3 г п-толуолсульфокислоы в качестве катализатора, получают 26 г 13|1-этил-3-метокси-17об-метил11 .аминометилгона-2,5Ч10)-диен-17Э Ола Для аналитических целей около 1 г неочищенного продукта перекристал)1изовывают из этилацетата, в результате чего получают продукт с т.пл. 188:-189 С; +67 (,5, хлоро.форм) . Стадия С. 13,5 г 13 5-этил-3-метокси-17о:-метиламинометилгонадиен-17(Ь-ола, полученного в стадии В, подвергают взаимодействию с диэтиловым сложным эфиром пироугольной кислоты, как описан в примере 1, стадия В. Полученный пр дукт перекристаллизовывают из метанола, в результате чего получают N-эYoкcикapбoнил-13p-этил-3-мeтoкcи-17о6-метиламинометилгона-2,5 (10) диен-17 5-о л. Выход 11 г, т.пл. 137°С; D +25°(,5, хлороформ). Стадия Д. Раствор IjOt г N-этоксикарбонил-13 1-этия-3-метокси-17о -метиламинометилгона-2,5(10)-диен-17р)-ола в 15 мл , . этанола, содержащего 0,5 г гидроокис калия, кипятят в течение 1 ч. Реакци онную смесь обрабатывают в соответствии с примером 1, стадия С, и полу ченный продукт перекристаллизовывают из этилацетата до получения 0,60 г 13р|-этил-3-метоксигона-2,5 (10) -диен175-спиро-5-(2-оксо-З-метйлоксазолидина). Т.пл. 207°С; +17° (,5, хлороформ). Пример 12. 13/ -9тйл-4-ен-3-он-175-спиро-5-(2-оксо-З-метилоксазолидин). ,0 г 13р-этил-3-метоксигона-2,5(10)-диен-175-спиро-5-(2-оксо-3-метилоксазолидина), полученного в соответствии с примером 11, перемешивают в смеси с АО мл метанола, 4 м воды и 2 мл концентрированной соляно кислоты в течение 1 ч при . Реакционную смесь выпаривают, затем остаток помещают в воду. Полученное кристаллическое вещество отфильтровывают, сушат и перекристаллизовывают из этилацетата. В результате получают 2,5 г чистого соединения с т.пл. 192°С; оС1 -ifl4°(,5 хлороформ). Пример 13. 13р -Этилгон-5 (10)-ен-3-он-175-спиро-5-(2-оксо-3-метилоксазолидин). Смесь ,2 г малоновой кислоты, 70 мл воды и 170 мл этанола нагревают до и при перемешивании добав 912 ляют суспензию 7,t г 13р-этил-3-метоксигона-2,5(10)-диен-175-спиро-5{2-оксо-З-метил-оксазолидина), полученного, как описано в примере 11, в 80 мл этанола. За несколько минут получают раствор, который затем поддерживают при 70 С в течение дальнейших 20 мин. 200 мл насыщенного раствора кислого углекислого натрия, а затем ЦОО мл воды по каплям добавляют раствору при охлаждении его льдом, Образовавшийся осадок отфильтровывают и промывают водой, в результате чего получают 6,8 г требуемого соединения с т.пл. 1б2-1б6 С. Аналитический образец получают, растворяя около 1 г вещества в холодном ацетоне и добавляя изопропиловый эфир. Выпавшие в осадок при охлаждении кристаллы отфильтровывают. Полученный продукт плавится при {OL +51°(с хлороформ). Пример 1. 13|5-Этилгона4,9(ТО)-диеч-3-он-175-спиро-5-(2оксо-3-метилоксазолидин). К перемешиваемому раствору 11,1 г 1315-этил гона-5-( 10) -ен-З-он-175-спиро5-(2-оксо-3-метилоксазолидина), полученного в примере 13, в 50 мл сухого пиридина по каплям добавляют раствор 10 г пиридинийпербромида в 50 мл пиридина за 0 мин при 20с. Затем реакционную смесь перемешивают в течение 3,5 ч при комнатной температуре и выливают в 1 л.воды Маслянистая жидкость кристаллизуется при соскабливании. Посл# перекристаллизации 8,38 г неочищенного продукта из этилацетата получают 6,3 г чистого соединения. Т.пл. 165 167С; 1 2б5{с 0,5, хлороформ); Э1аноА -, А макс 301 нм. П р и м е р 15. 13(-Этил-3метоксигона-1,3,5(10)-триен-175-спир -5-(2-оксо-3-метилоксазолидин) . Исходя из 1,78 г 13 -этил-3-метоксигона-2,5(10)-диен-1 7S-спиро-5(2-оксо-З-метилоксазолидина), полученного по примеру 11, и в соответствии с процедурой, описанной в примере И, после перекристаллизации неочищенного продукта из этилацетата получают 1,19 г чистого продукта с т.пл. 197-193 С; -29°{с(5, хлороформ); яУдГс 276, 28k нм. Пример 16. 13р-Этилгона,9(10)-11-триен-3-он-175-спиро-5-(2-оксо-З-метилоксазолидин). 13 К перемешиваемому раствору 13р-этилгона-,9(10)-диен-3-он-175-спиро-5- (2-оксо-3-метилоксазолидина полученного в соответствии с примером И, в 35 мл сухого этанола при комнатной температуре добавляют 0,5 г пирролидина в атмосфере азота Спустя ц суспензию охлаждают на бане с ледяной водой, после чего промывают охлажденным льдом метанолом.Получают 2,6Б гаминосоединения. К перемешиваемой суспензии указанного енаминосоединения с 5 мл метанола и 2,5 мл воды добавляют 1 ,20 мл уксусной кислоты в атмосфере азота при 20с. Спустя 2 ч при перемешивании добавляют еще порцию воды (25 мл) и перемешивание продол жают еще в течение 12 ч. Реакционну смесь разбавляют еще 100 мл воды, осадок отфильтровывают и промывают водой. Полученный неочищенный 13(5 этилгона-5(10), 9(11)-диен-3-он-17S -спиро-5- (2-оксо,-3-метилоксазолидин) сушат, растворяют в ацетоне при ком натной температуре, обесцвечивают с помощью древесного угля, концентр руют до Vt его исходного объема и наконец, разбавляют изопропиловым эфиром. Выпавшие в осадок I, г 13Й этилгона-5-(Ю), 9(11)-диен-3-он175-спиро-5-(2-оксо-3-метилоксазолидина) плавятся при 17 -17б°С. К рас вору О,Э этого соединения в 10 мл сухого диоксана добавляют раствор 0,62 г 2-3-Дихлор-5,6-дициано-1 .tбензохинона в мл диоксана в атмо фере азота. Реакционную смесь перем шивают в течение 2 ч а темноте, затем фильтруют и диоксановый фильтра выпаривают. Остаток растворяют в дихлорметане и полученный раствор экстрагируют 1%-ным водным раствором гидроокиси натрия, а затем водой. После сушки и выпаривания экстракта получают желтое маслянистое вещество, которое кристаллизует ся при растирании с Изопропиловым эфиром, получают 0,3 г неочищенного 13 -этилгона-,9(10), 11-трйенЗ-он-1 75-спиро-5-(2 -оксо-З -метилоксазолидина),который появится посл перекристаллизации из этилацетата пр 225-226°С; об Ь° -83(,5, хлороформ); 335, 235 нм Пример 17. 13/ -Этилгона,6-диен-З-он-175-спиро-5-(2-оксо 3-метилоксазолидин). 9 1 Г 13|3-этилгона-4-ен-3-он-175спиро-5-(2-оксо-З-метилоксазолидина) растборяют в 20 мл сухого диоксана, 1 мл этилового эфира ортомуравьиной кислоты и 0,1 мл раствора, полученного из 0,35 мл концентрированной серной кислоты и 7 мл сухого диоксана, добавляют к раствору, который перемешивают в течение одного часа при комнатной температуре, затем добавляют две капли пиридина и полученную смесь выливают в 200 мл ледяной воды. Образовавшийся осадок отфильтровывают, промывают водой и растворяют в 7,3 мл ацетона. Затем добавляют0,39 г хлоранила и раствор перемешивают при комнатной температуре в течение 1,5 ч в темноте. Затем его выпаривают, и остаток растворяют в 200 мл дихлорметана. Дихлорметановый раствор сушат, пропускают через нейтральную окись алюминия и выпаривают. После перекристаллизации выпаренного остатка из этилацетата получают 0,17 г чистого продукта. Т.пл. 2б7-2б8°С,Соср: -Э2° ,5, хлороформ) 282 нм. Пример 18. 3-Метоксиэстра1,3,5(10), 9(11)-тeтpaeн-17S-cпиp65- (2-оксо-З-метилоксазолидин). Стадия А. В соответствии с процедурой, описанной в примере 11, способ А, стадия А, исходя из 3-метоксиэстра1,3,5(10), 9(11)тетраен-17/5-она получают 3-метоксиэстра-1,3,5(10), 9(11)-тетраен-175-спирооксиран, который после перекристаллизации из метанола плавится при l42C;| oC3 +12б°(,5, хлороформ). Стадия В. В соответствии с процедурой, описанной в примере 11, способ А, стадия В, из ,80 г 3-метокси-эстра1,3,5(10), 9(11)-тетраен-175-спирооксирана получают 3,0 г 3-метокси17о метиламинометилоэстра-1,3,5(10), 9(11)-тетраен-17|5-ола с т.пл. 13 135°С; оС120 +90°(,5, хлороформ) Стадия С. В соответствии с процедурой, опианной в примере 1, стадия В, однако, сходя из 3,0 г З-метокси-17оС-метилминометилэстра-1,3,5(10) , 9(11)етраен-17(5-ола, получают соответстующее N-карбэтоксипроизводное. Нечищенный продукт превращают в соот15ветствующее спиросоединение в этаноле по способу, описанному в примере 1, стадия С. Полученный продукт пере кристаллизовывают из метанола, в результате чего получают 2,21 г требуемого соединения с т.пл. 187C; О +10°(,5, хлороформ). Пример 19. 3-0кси-5р, 19 Циклоандрост-6-ен-175-спиро-5 2-оксо-З-метилоксазолидин). Стадия А. К суспензии S,t7 г Зй-ацетокси5(, 19-Циклоандрост-6-ен-17-она и 6,8 г триметилсульфонийиодида в 53 м сухого диметилформамида добавляют 5,6 г калий-трет-бутанола при в течение 10 мин. Полученную смесь перемешивают еще в течение 15 мин, а затем выливают в ледяную воду. Выпавшее в осадок вещество отфильтро вывают, промывают до нейтральной реакции водой и сушат. После перекристаллизации из этилацетата получают 2,147 г Зр -окси-5р, 19-циклоандрост-6-ен-175-спирооксирана с т.пл. 18018lOc;Co l ° -15,70(,5, хлороформ). Стадия В. В соответствии с процедурой, описанной в примере 1, стадия А, исходя из 2,7 г Зр-окси-5р, 49-Циклоандрост-6-ен-175-спирооксирана, получают 3, 173-диокси-17об 1етиламинометил-5 f, 19-Циклоандрост6-ен. Неочищенный продукт перекриста лизовывают из этилацетата и получают 1,88 г чистого продукта с т.пл. 198-199°С; IOL -k3° (,5, хлороформ). Стадия С. 1,80 г 3 - 17 -диокси-17 -метиламинометил-5, 19-циклоандрост-6-она полученного на стадии В, превращают в соответствуквдее N-этоксикарбонильное соединение в соответствии с процедурой, описанной в примере 1, стадия В, И после выделения сырого продукта его превращают в Зр-окси-5р, 19-Циклоандрост-6-ен-175-спиро-5-(2-оксо-3-метилоксазолидин), как опи сано в примере 1, стадия С. После перекристаллизации неочищенного продукта из этилацетата получают 1,17 г чистого продукта, который плавится при 228-229®С; ос 20 „ -79(с-0,5, хлороформ). П.р и м е р 20. З-окср-5-3. 19-ЦИКлоандрост-6-ен-175-5-(2-оксо-З-метилоксазолидин). 9 К .перемешиваемой суспензии 5,30 г комплекса трехокись хрома-пиридин в 80 мл сухого дихлорметана добавляют по каплям при комнатной температуре раствор 0,85 г 3-fi окси-5р. .19-циклоандрост-6-ен-175-спиро-5-(2-оксо-З-метилоксазвлидина;, полученного в соответствии с примером 19, в 18 мл сухого дихлорметана. Реакционную смесь перемешивают в течение 20 ч и затем отфильтровывают. Дихлорметановый раствор встряхивают с водой, сушат и пропускают через слон нейтральной окиси алюминия. Затем раствор выпаривают и полученный сухой остаток перекристаллизовывают из этилацетата, в результате чего получают 0,50 г чистого соединения с т.пл. 164°С; ,5° (,5, хлороформ). Пример 21. Энт. 13| -этилгoнa-4-eн-3-oн-17S:cпиpo-5-(2-oкco3-мeтилoкcaзoлидин) . Стадия Л. в соответствии с процедурой, описанной в примере 11, способ А, стадия А,исходя из энт.13 -этил-3-метоксигона-2,5{1О)-диен-17-она,получают энт.13 -этил-3-метоксигона-2,5(10)диен-1 75-спирооксиран.Т.пл. С, Мо -109(,5, хлороформ). Стадия В. Знт. 13р-этил-3-метоксигона-2,5 (10)диен-17S-спирооксиран,полученный на стадии А, подвергают взаимодействию сметилам1 ном, как описано в примере 11, способ А, стадия В, и полученный продукт затем превращают В соответствующее N-спирооксиран, произвольное по процедуре, описанной в примере 11, способ А, стадия С. Превращение этого соединения в соответствии с примером 11, способом А, стадией Д приводит к получению энт. 1Зр-этил-З-метоксигона-2,5(10)-диена175-спиро-5Ч2-оксо-3-метилоксазолидина) с т.пл. 208°С;Сос12° -19° (,5, хлороформ). Стадия С. Энт. 13 -этил-3-метоксигона-2,5 (10)-диен-175-спиро-5-(2-оксо-З-метилоксазолидин) гидролизуют соляной кислотой в водном метанольном растворе, как описано в примере 12, в результате чего получают энт.13(9тилгон- -ен-3-он-175-спиро-5-(2оксо-3 метилоксазолидин 191 C,3j + (,5, хлороформ). Пример 22, 13 -Этил-Зоксиминогон- 1-ен-175-спиро-5-(2-оксо-3-метилоксазолидин). Способ А. Раствор 0,9, г 13| -этилгон- -ен-3 ои-1 75-спиро-5-(2-оксо-3 метил зксазолидина),0,2 г хлоргидрата гидроксиламина и 0,25 г сухого ацетата натрия в смеси 3 мл воды и 20 мл этанола кипятят на водяной бане в те чение одного маса. Реакционную смесь выпаривают, кристаллический остаток промывают, сушат и перекристаллизовывают из метанола, в результате чег получают 0,50 г продукта с т.пл. 28 :286°С;М -н86(,5, хлороформ Способ В, Раствор 1 г 13(Ь-этил-3-метоксигона-2,5(ТО)-диен-175-спиро-5-(2-оксо-3-метилоксазолидина) и 1 г хлорогидрата гидроксиламина в 10 мл сухого пиридина перемешивают при 50°С в течение 0,5 ч и при 80°С еще в течение ч. Реакционную смесь выпаривают. Остаток растворяют в хлороформе и затем раствор встряхивают с 2, водным раствором соляной кислоты, затем с насыщенным раствором бикарбоната натрия и с водой. Хлороформенный раствор сушат и выпаривают. После перекристаллизации остатка из метанола получают 0,5 г 13(Ь-этил-3-оксиминогон-4-ен-17S-спиро-5-(2-оксо-З-метилоксазолидина) который плавится при 283С; j-J +70° (,5, хлороформ). Оксимы, полученные по способам А и В., являются смесями 2- и Е-изомеров в различных соотношениях. Пример 23. 13 -этил-3 метюксииминогонг1+-ен-1 75-спиро-5-(2оксо-З-метилоксазолидин), В соответствии с процедурой, описанной в примере 22, способ А, используя О-метилгидроксиламинхлоргмцрат и продолжая реакцию 5 ч, получают требуемое соединение, которое после перекристаллизации из зтилацетата плавится при 180-182°C; оС. +85 (,5, хлороформ). Пример 24. 13р-.Этил-3-аплилоксиминогон-4-ен-175-спиро-5-(2-оксо-З-метилоксазолидин). В соответствии с процедурой, описанной в примере 22, способ А, используя О-аллилгидроксиламинхлоргидрат, получают требуемое соединение ст. пл. I после перекристаллизации . ИЗ метан-олаТ 1ЬЗ-165С; +73° (,5, хлороформ). П р и м е р 25. 3 0ксиминоандрост-,6-диен- 17S-cпиpo-5-(2-oкco3-мeтилoкcaзoлидин) . Исходят из 7,1 г полученного по примеру 8 андрост-,6-диен-3-он-175пиро-5-(2-оксо-З-метилоксазолидина), и по способу, описанному в примере 22, стадия А, получают 7,5 г сырого продукта, который перекристаллизовывают из этанола. Т.пл. С (разложение). LOC -57,3°(, в хлороформе). П р и м е р 26. ир-Этил-З оксимино-г6на-,9(10), 11-триен-175спиро-5-(2-оксо-3-метилоксазолидин). Исходят из 1,77 г полученного по примеру 16 13р-этилгона-,9(10) , 11триеи-3-он-175-спиро-5- (2-оксо-Зметилоксазолидина), и по способу, описанному в примере 22, стадия А, получают сырой продукт (1,88 г), коорый перекристаялизовывают из этилацетата. Выход 1,55 г; т.пл. 273-275С (разложение)iM2j° -108°(, в хлороформе). Формула изобретения 1. Способ получения стероидных спирооксазолидинов общей формулы . где алкил с 1- атомами углерода; R,- В9ДОРОД, алкил с I- атомами углерода, алкенил с 2- атомами углерода; Z - одна из групп, представленных общими формулами
19
R.J- водород или метил;
фтор, гидроксил, ацилоксил с 2-3 атомами углерода, алкоксикарбонилоксил с 2- атомами углерода, оксогруппа, оксииминогруппа или алкоксииминогруппа с 1-3 атомами углерода;
3110920
оксогруппа, оксиминогруппа или алкоксиминогруппа с 1-3 атомами углерода; алкил с 1-3 атомами углеро5да
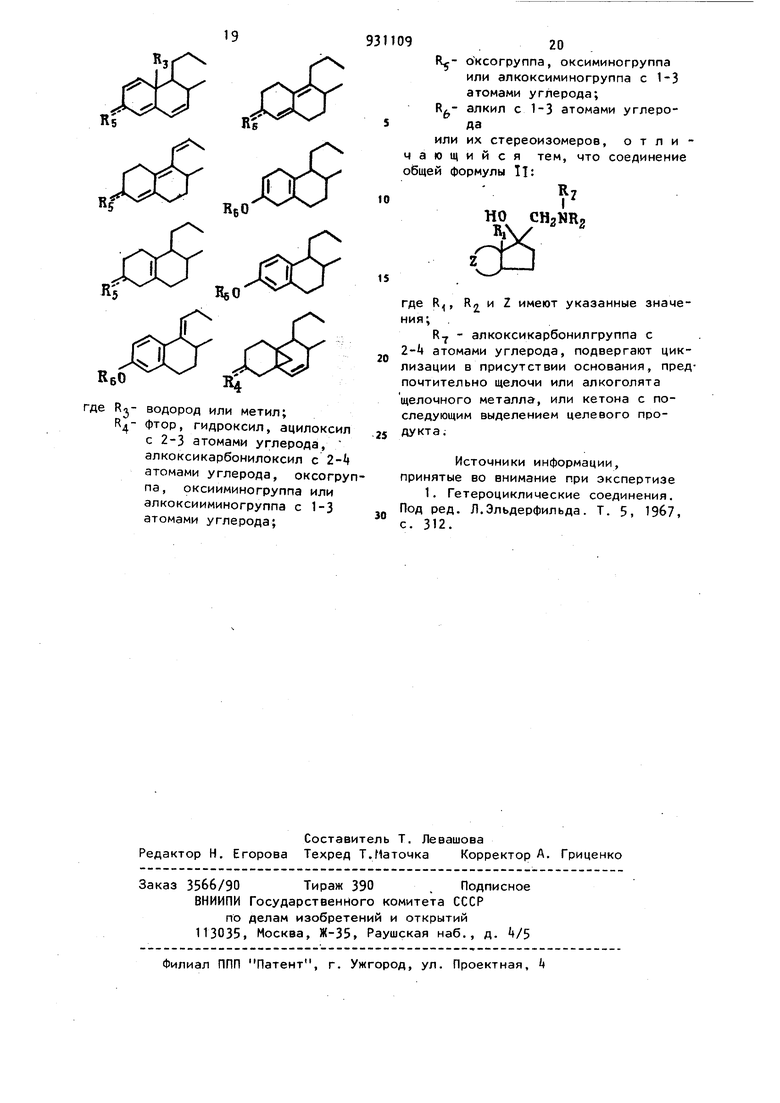
или их стереоизомеров, отличающийся тем, что соединение общей формулы Ц:
но сНгИНг
«Г
где R, Rrt и Z имеют указанные значения;
RY - алкоксикарбонилгруппа с атомами углерода, подвергают циклизации в присутствии основания, предпочтительно щелочи или алкоголята щелочного металла, или кетона с последующим выделением целевого продукта;
Источники информации, принятые во внимание при экспертизе 1. Гетероциклические соединения. Под ред. Л.Эльдерфильда. Т. 5, 19б7, с. 312.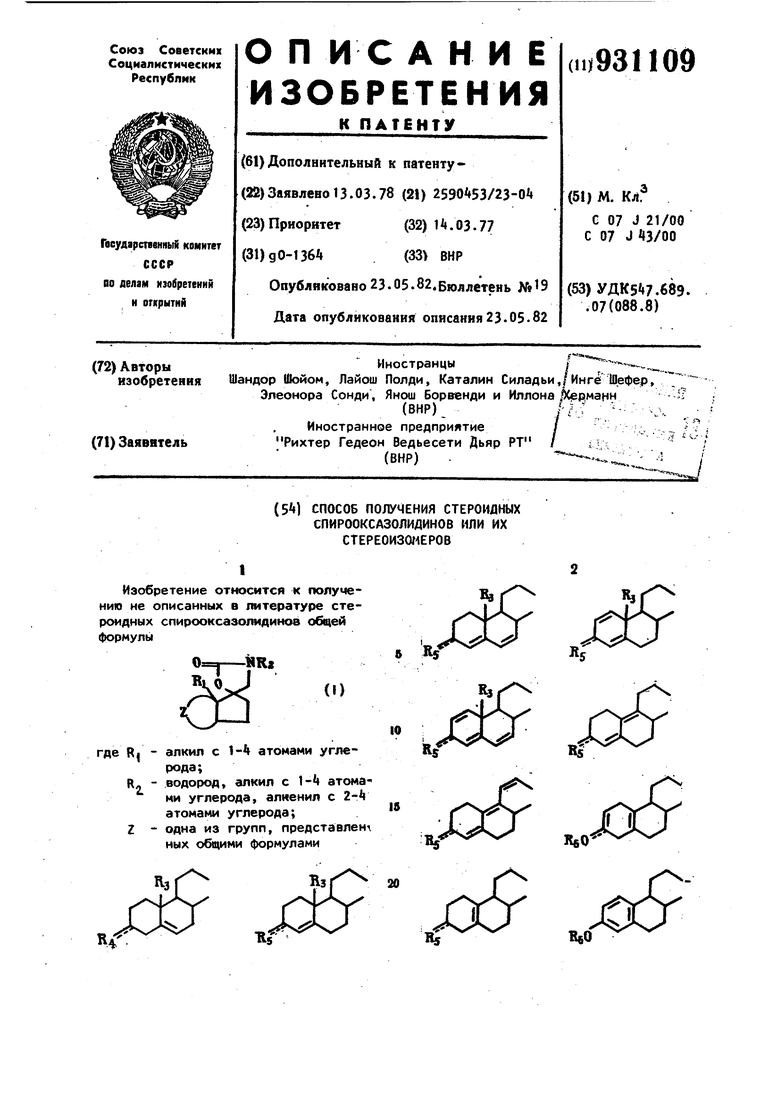










Авторы
Даты
1982-05-23—Публикация
1978-03-13—Подача