(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 21-ОКСИ-20Изобретение относится к усовершенствованному способу получения производных 21-окси-20-метилпрегнана общей формулы (1) «JHjOH где пунктирная линия означает возмо; ную двойную связь, обладающих фармакологической активностью. Известен способ получения производных 21-окси-20-метилпрегнана общей формулы (1), заключающийся в том, что ситостерин или Д -холестен-3-он подвергают ферментации с помощью культуры Mycobacterium spec. NRRL e-3583 или B-3B05 или ее вариантов или мутантов fl . Выход целевого про дукта не превышает 1%. Недостатком этого способа является низкий выход целевого продукта. Цель изобретения - повышение выхо да целевого продукта., Поставленная цель достигается опи сываемым способом по.лууения производ ных 21-окси-20-метилпрегнана общей
-МЕТИЛПРБГНАНА формулы сI), заключающимся в том, что ситостерин или Д -холестен-3-он подвергают ферментации с помощью культуры Mycobacterium spec.NRRL Б-3583 или В-3805 или ее вариантов или мутантов при рН 6-8 в присутствии тетрабората или трифенилбората, или метабората натрия, или метабората кальция в расчете 1-5 г на 1 h куль-. туры. Пригодными растворителями для субстрата являются, например, метанол, этанол, гликольмонометиловый эфир, диметилформамид или диметилсульфоксид. Эмульгирование субстрата осуществляют расплавлением его в микронизированной форме или растворенным в смеишваюцемся с водой растворителе {метанол, этанол, ацетон, гликольмонометиловый эфир, диметилформамид или диметилсульфоксид). предпочтительно в умягченной воде, которая содержит обычные эмульгаторы. Пригодными эмульгаторами являются неиногеннуе эмульгаторы, например адцукты этиленоксида или сложные эфиры жирных кисуют с многоатомными спиртами. Mycobacter luffl spec. NRRL В-3805 целесообразно после обработки мутагенами наносить на кровяные агаровые пластинки. Таким образом получают отдельные колонки различного морфологического вида. Эти колонии вьвдёляют и испытывают на способность к образованию производных 21-окси-20-метилпрегиана общей формулы(I). Среди салекционгалх , которые образуют круглые колонии, получают штаммы, которые образуют производные 21-окси-20-метилпрегнана с выходо1у в 1,5-3. раза больше, чем неселекционированные штаммы.
Пример 1. а. В колбу Эрленмеера емкостью 2 л с 500 мл стерильной питательной среды, содержащей, 1% дрожжевого экстракта, 0,45% вторичного фосфата натрия, 0,34% первичного фосфата калия, 0,2% Тагат З/ 02 и в которой установлено рН 6,7, производят посев путем отмучивания (промывки-декантацией) сухой культуры Mycobactertum spec. NRRL Вт3805 и встряхивают в течение 3 дней при 30t с скоростью 190,об/мин,
б.22 г ситостерина эмульгируют с 4,4 г Тегина® и 430 мл воды при с помощью U11га-Тиггах® в течение 25 мин и затем доливают до 513 г водой. Стерилизуют эмульсию в течение 20 мин при 120°С.
в.В колбу Эрленмейера емкостью 500 мл с 65 мл стерильной питательной среды, содержащей 2 г Cornsteep liqudr, 0,3 г вторичного фосфата аммония, 0,25 г Тагатз QZ и в которой установлено рН 6,5, производят посев вырапи1ваемЬй культуры Мусоbacterium spec.
Затем добавляют 28 мл приготовленной в примере 16 суспензии (соответствует 1,2 г ситостерина) и спустя 24 ч - 4 мл 4%-ного водного раствора тетрабората натрия и ферментируют в течение 120 ч при 30°С с встряхиванием.
После ферментации бульон культуры экстрагируют 2 раза по 100 мл хлористым этиленом. Объединенные этиленхлоридные экстракты затем смешивают с 11 г активного угля и фильтруют через складчатый фильтр. Фильтрат концентрируют при на роторном испарителе и хрсялатографируют на окиси алюминия. После хроматографирова;ния получают 135 мг 21-окси-20-ме тил- -претнен-З-она с т.пл. 140141 С (из этил ацетата) .
Бели реакцию проводят при таких же условиях, но без добавки раствора тетрабората натрия, то получают 45 мг 21-окси-20-метил-4-првгнен-3-она.
П р и м е р. 2. а. Из 22 г 4-холестен-3-она готовят, как описано в примере 1б, 513 г эмульсия.
б. В условиях примера 1в выращивают 70 мл культуры Hycobacterlum spec. NRRL В-3805,смешивают с 28 мл
эмульсии 4-холестен-З-она и спустя 24 ч - с 4 мл 4%-ного водного раствора тетрабората натрия и ферментируют в течение 120 ч при 30°С и с встряхиванием.
Обрабатывают смесь после ферментации, как описано в примере 1в, и получают 95 мг 21-окси-20-метил-4-прегнен-3-она с т.пл. 142-144°С.Если проводят реакцию в таких же условиях, но без добавки раствора тетрабората натрия, то получают 40мг 21-окси-20-метил-4-прегнен-3-она.
Примерз. 28 МП приготовленной согласно примеру 16 эмульсии ситостерина ферментируют, как описано в примере 1в, с помощью культуры Mycobacter i urn spe.c. NRRL B-3805, причем вместо водного раствора тетрабората натрия используют добавку 6 МП 4%-ной суспензии метабората калция в воде. После обработки смеси после ферментации, как описано в примере 1в, получают 120 мг 21-окси-20-метил-4-прегнен-З-она с т.пл.141143°С.
Пример 4. 28 мл приготовленной согласно примеру 16 эмульсии ситстерина ферментируют, как описано в примере 1в, с помощью 7Q мл культуры Mycobacteriurn spec,NRRL B-3805, прич вместо водного раствора тетрабората натрия добавляют 5 мл 4%-ного раствора трифенилбората.
После обработки смеси после ферментации, как описано в примере 1в, получают 125 мг 21-окси-20-метил-4-прёгнен-3-она с т.пл. 142-143с.
П р и ме р.5.а. В условиях примера 1а выращивают культуру МусоЬасterium spec. NRRL В-3683.
б. 65 мл описанной в примере 1в питательной среды смешивают с 5 мл выращенной культуры Mycobacterium spec,N.RRL В-3683. Затем к культуре добавляют 28 мл полученной по примеру 16 эмульсии ситостерина и спустя 24 ч - 4мл 4%-ного раствора тетрабората натрия и ферментируют в течение 120 ч. Обрабатывают смесь после ферментации, как описано в примере 1 В, и получают 90 мг 21-окси-20-метил-1,4-прегнадиен-3-она с т.ш1,180182°С(из смеси этилацетата с ацетоном) .
Примере. 40 мл выращенной культуры Mycobacter1 urn spec. NRRL B-3805, полученной согласно примеру la, центрифугируют со скоростью 4000 об/мин, полученную бактериальную массу затем дважды проыывахт буферйрованньи до рп 6 солевым раствором, содержсцдим 0,5% хлористого натрия, 0,012% сульфата магния (гептагидрата) и 1,36% первичного фосфата калия, суспендируют в 40 мл этого солевого раствора и смешивают с 10 м 0,5%-ного 1-метил-3-нитро-1-нитрозо17уанидина. .
Инкубируют бактериальную суспензию в течение 1 ч при 30°С, отделяют бактерии центрифугированием, промывают их дваяд:;ы вышеуказанным солевым раствором и помещают их на кровяные агаровые пластинки. Из образовавшихся
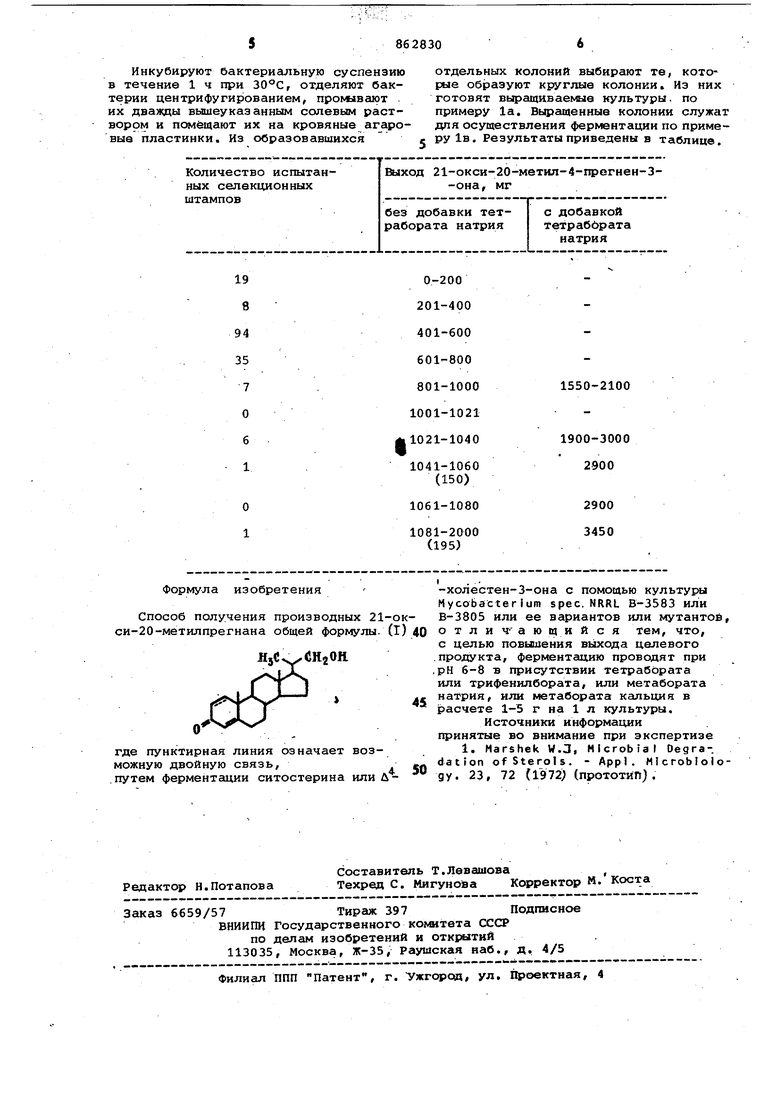
отдельных колоний выбирают те, которые образуют круглые колонии. Из них готовят выращиваемые культуры, по примеру 1а. Выращенные колонии служат для осуществления ферментации по примеру 1в, Результаты приведены в таблице.

| название | год | авторы | номер документа |
|---|---|---|---|
| Способ получения производных андростан-17-она | 1977 |
|
SU980628A3 |
| Способ получения производных 5андростен-17-она | 1976 |
|
SU697053A3 |
| Способ получения 11 -гидроксистероидов | 1979 |
|
SU876059A3 |
| СПОСОБ ПОЛУЧЕНИЯ 17-ОКСОСТЕРОИДОВ | 1991 |
|
RU2082762C1 |
| Способ получения 4-андростен-3,17-диона или 1,4-андростадиен-3,17-диона | 1987 |
|
SU1679977A3 |
| Способ получения -гомостероидов или их 1,2-дегидропроизводных | 1973 |
|
SU697054A3 |
| РЕКОМБИНАНТНЫЕ МИКОБАКТЕРИАЛЬНЫЕ ШТАММЫ-ПРОДУЦЕНТЫ И ИХ ИСПОЛЬЗОВАНИЕ ДЛЯ ПОЛУЧЕНИЯ 22-ФУНКЦИОНАЛИЗИРОВАННЫХ СТЕРОИДОВ | 2019 |
|
RU2767610C2 |
| Способ получения стероидов | 1979 |
|
SU860708A1 |
| Способ получения 11 @ -оксистероидов | 1980 |
|
SU940650A3 |
| СПОСОБ ПОЛУЧЕНИЯ АНДРОСТА-1,4-ДИЕН-3,17-ДИОНА | 1993 |
|
RU2039824C1 |

19 8
94 35 7 О б 1
О 1 Формула изобретения Способ получения производных 21-о си-20-метилпрегнана общей формулы. (I СНгОЯ где пунктирная линия означает возможную двойную связь, путем ферментации ситостерина или Л1550-2100
1900-3000 2900
2900 3450 -холестен-3-она с помощью культуры Mycobacterium spec. NRRL В-3583 или В-3805 или ее вариантов или мутантой, отлич-ающийся тем, что, с целью повышения выхода целевого продукта, ферментсщию проводят при рН 6-8 в присутствии тетрабората или трифенилбората, или метабората натрия, И.ПИ метабората кальция в расчете 1-5 г на 1 л культуры. Источники информации принятые во внимание при экспертизе 1. Harshek W.3, Mlcrobtal Oegra-. dation ofSterols. - Appl. Microbiology. 23, 72 (1972) (прототип).
Авторы
Даты
1981-09-07—Публикация
1978-12-04—Подача