(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ
ТЕТРАГИДРО-1,3,5-ТРИАЗИН-2,6-ДИОНА ИЛИ ИХ ОСНОВНЫХ СОЛЕЙ
t
Изобретение относится к синтезу новых производных тетрагидро-1,3,5триазин-2,6-диона, которые могут найти применение в медицине.
Известен способ ацилирования аминов реакцией переамидирования при нагревании - .
Целью изобретения является синтез новых биологически активных производных тетрагидро-1, 3,.5-триазин-2,6дион а.
Поставленная цель достигается тем, что согласно способу получения производных тетрагидро-1,3,5-триазин2,6-дионов формулы
„.-М-ж-/У-Но
где R -алкильный радикал алкильный радикал , несущий а-лкокси-радикал , циклоалкил или алкенил или алкильный радикал г ле связывающий dуглеродный атом является вторичным, бензил или 1-(фенил)-этилрадикал, или фенил радикал незамещенный или
замещенный атомом галогена, или алкокси , осуществляют перегруппировку соединения формулы
f Л
R-ii //-w«%
И ,
10 где R имеют указанные выше значения, при нагревании в интервале температур 60-15 , и целевые продукты выделяют или переводят в основные соли.
15
Процесс предпочтительно проводят в присутствии высококипящего разбавителя или растворителя. В качестве исходного соединения предпочтительно используют соединение формулы II ,гдв R представляет собой изопропильный
20 или н-пропильный радикал и R явля- ется пент-3-ильным или гекс-3-ильным радикалом. ,
Аддитивной солью основания соеди- .
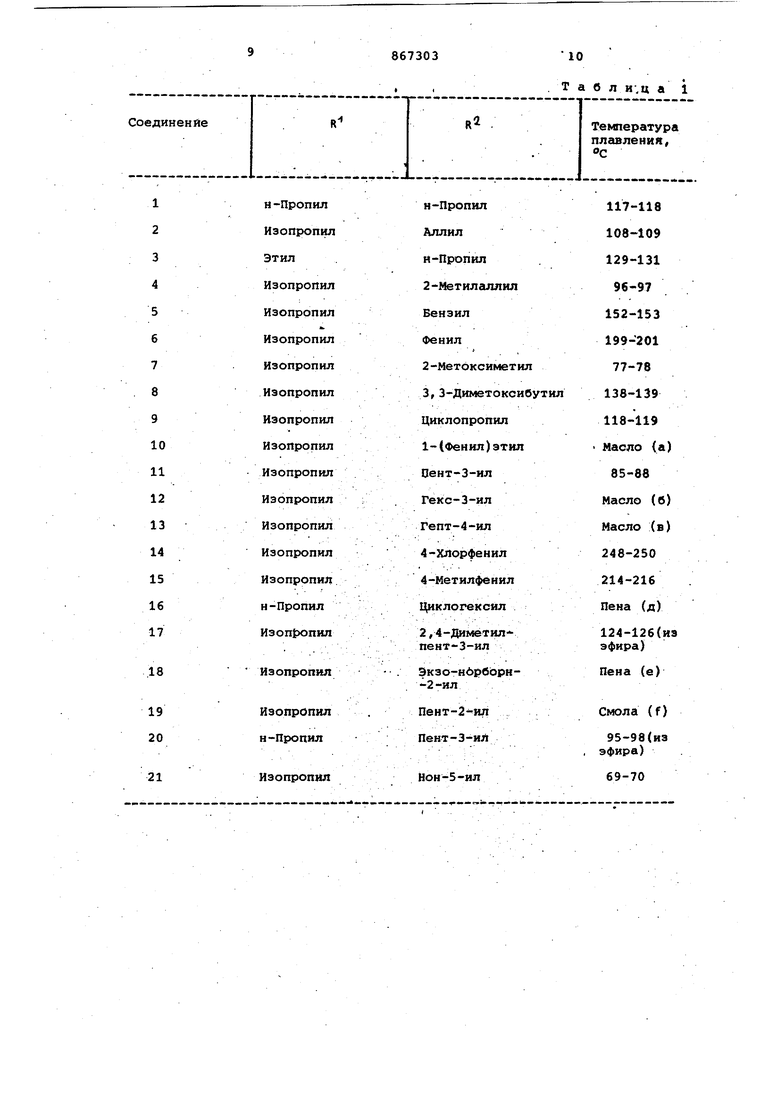
25 нения формулы 1 являются, например, щелочной металл или соль щелочногг емельного металла, например, натрия, калия, кальция или соль магния, алюминия, например двойная соль гидро30 1ркисиалюминия, соль меди или комплек,с ее, или соль с органическим основани ем, фармацевтически приемлемый катион, например, триэтаноламин Или бензиламин. Предпочтительными группс1ми новых соединений по формуле I являются соединения, где К соответствует изопропилу или н-пропильному радикалу; R5 соответствует пент-3-илу, гекс-3-илу или циклогексильному радикалу и в каж дой группе, другие R и R соответствуют любому одному из ранее указанных значений, вместе сЬриемлемыми для при готовления лекарств солями этих соединений, полученных присоединением ос нования. Новые типы соединений по формуле I описаны в примерах, причем из них наиболее предпочтительным является 1-изопропил-4-(N- ацетил )ци клопропиламино-тетрагидро-1,3,5-триазин-2,6дион, 1-ИЗОПРОПИЛ-4- (М-ацетил)-пент 3-иламино7 -тетрагидро-1,3,5-триазин 2,6-дион и. 1-ИЗОПРОПИЛ-4-(N-ацетил)циклогексиламино-тетрагидро-1, 3,5триазин-2,6-дион, и фармацевтически приемлемые аддитивные соли основания этих соединений. Требуемые исходные материалы формулы J могут быть получены путем реакции 4 алкиламиносоединения формулы О Гпн .y-ff где R и R имеют значения, указанны выше, с кетеном предпочтительно при комнатной температуре и в разбавител или растворителе, например хлористом метилене. Во многих случаях удобно приготавливать исходный материал фор мулы /I In situ и использовать в пре ложенном способе без очистки. 4-алкиламиносоединения формулы К могут быть получены путем реакции ам на формулы .J обычно как его ацетат соли с производным 4-метилтио1,3,5-триазина формулы где R и R имеют значения, указанны выше, при температуре в пределах 10О и подходящем растворителе, та|сом как диметилформамиде. 4-алкилтио Соединения формулы И могут быть полу чены методом синтеза аналогичных 1,3,5-триазин-2,6-дионов. Соединения по формуле Г являются умеренно кислыми и реагируют со слабыми основаниями, например карбонатами водорода щелочных металлов, образуя при этом соответствующие соли щелочных металлов. Если необходимо получить приемлемую с точки зрения фармацевтических требований соль, полученную присоединением основания, проводят реакцию соединения по формуле I с подходящим для этой цели основанием. Болеутоляющие свойства соединений формулы I могут быть продемонстрированы в ходе проведения стандартного теста путем измерения периода, прекращения корчей мыши, которой была сделана интраперитональная инъекция ацетилхолина. Соединения формулы показывают наличие значительной активности при проведении этого теста при введении noj onHTHOMy животному через рот дозы, составляимдей 50 мг/кг веса или менее, при полном отсутствии каких-либо токсичных эффектов при использовании активной дозы, причем предпочтительные соединения по формуле 1 , например, 1-изопропил-4С(N-ацетил)-пент-З-иламино -тетрагидро-1, 3,5-триазин-2,б-дион проявляют значительную активность при введении через рот дозы, составляющей 5 мг/кг веса или много менее. В дополнение к болеутоляющим свойствам, определенные соединения по формуле I обладают противовоспалительным действием, которые могут быть продемонстрированы при использовании любого из двух обоих стандартных тестов S а)при создании у крыс артритов с покющью стимуляторов б)отека у крыс, вызываемого введением исландского мха. Соединения по формуле I , обладающие хорошими противовоспалительными свойствами, демонстрируют активность как в любом из двух, так и в обоих указанных тестах при лозе- вещества. Вводимого через рот, равной или меньшей 50 мг/кг веса, которая вводится в виде ежедневной дозы в течение 14 х;ней в ходе теста а) или в качестве разовой дозы при тесте б) безо всяких побочных токсичных воздействий при использовании этой дозы. Новыми соединениями формулы 1 , обладающими хорошими противовоспалительными свойствами, являются 1-этил4-(М-ацетил)-н-пропиламино-, 1-н-пропил-4-(М-ацетил)-н-пропиламино- и 1изопропил-4-(N-ацетил)бензиламинотетрагидро-1,3,5-триазин-2,6-дион. Некоторые из соединений формулы I 4также обладают свойствами пpeкpaщeниj синтетазы фермента простагландина. Это свойство может быть продемонстрировано в стандартном эксперименте, проводимом in vitro, который включает использование синтетазы простагландина, выделенной из зародышевого пузырька барана. Те соединения по формуле I , которые прекращают синтетазупростагландина, обеспечивают этот процесс при концентрации их in vitro в пределах 105м или менее. Примером соединения по формуле I , который пре ращает синтетазу простагландина, является 1-изопропил-4-(М-ацетил)-бензиламино-тетрагидро-1,3,5-триазина2,6-дион, Подавляющие синтетазу простагландИна соединения, например, индометцин или .флюфенамовая кислота, эффективны при клиническом применении в случае лечения при острых заболеваниях, свя занных с ненормально высоким содержанием простагландина в тканях, напри Мер dysmenorrhoca или menorronagia и при лечении сопровождающихся болезненными ощущениями воспалительных за болеваний суставов, например артритов или остоартритов, Для создания упомянутых фармакологических эффектов в теплокровных животных введение соединений формулы Г может осуществляться следующим образом: , а)для болеутоляющего действия при ежедневной дозе, например, 0,1-25 мг/ кг(для человека это эквивгшентно ежедневной дозе приема, составляющей 2,5-626 мг); б)для обеспечения противовоспали|Тельного действия при ежедневной дозе введения через рот, равной 1-50 мг/кг соединения по формуле I , обладающего противовоспалительным действием (для человека это соответствует полной ежедневной дозе приема, равной 25 1250 мг); в)для подавления синтетазы простагландина при ежедневной дозе 1 50 мг/кг соединения по формуле I , обладающего свойством подавлять синте тазу простагландина (для человека это эквивалентно полной дозе дневного приема, равной 25-1250 мг) активного ингредиента по формуле 1 или его аддитивной соли основания. Соединения формулы Г, обычно используемые в форме обычных фармацевти ческих соединений, могут быть нспользованы, при лечении сопровождающихся болевыми ощущениями воспалениях суставов , таких как артриты и остоартриты. , . . , П р им е р 1. Раствор 1-изс)пропил-3-ацетйл-4-циклогексилгининотетрагидро-1,3,5-триазин-2,6-диона (12,0 г в сухом толуоле (150 мл) кипятят с Ьбратным холодильником в течении 16 .ч После охлаждения добавляют дополнительное количество толуола (50 мп), затем раствор последовательно npojifcjвают 10 об. % водным раствором соляной кислоты (3x80 мл), водой (80 мп) и насыщенным раствором хлористого натрия (go мл). Затем толуольный раствор сушат (MgS04) и испаряют. Остаток кристаллизуют из смеси хлористого метилена-петрс5лейнрго эфира (т.кип 40-60с), получают 1-йзопропил-4-(Нацетил) циклогексиламинотетрагидро1,3,5-Т1риазин-2,6-дион (2,0 г), т.пл. 129-131 С. Исходное вещество получают следующим образом. Газообразный кетен, образованный пиролизом ацетона при бОО-ТОО С в приборе, основанном на аппарате Вильямса и Хурда, пропускают через раствор 1-изопропил-4-циклогексиламинотетра-. гидро-1,3,5-триазин-2,6-диона (10,0 г) в хлористом метилене (150 мп) до завершения реакции (1 ч 40 мин), еудя по анализу с помощью тонкослойной хроматографии (S1022уксусная кислота/ этнлацетат/толуол, 2:35t63 по объему)./ Избыток кетена удаляют пропусканием газообразного аргона через рвдкционный растйор в течение 15 мин. При выпаривании растворителя получают 1-изопропил-3-ацетил-4-циклогекйиламино,тетрагндро-1, 3,5-триазин-2,6-дион (14,2 г) удовлетворительной для последующих реакций чистоты. Чистый препарат (0,4 г) с т.пл. 105-107«С получают при растирании неочищенного твердого образца (2,2 г) со смесью эфира и петролейного эфира (т.кип, 40-60 С). В табл. 1 приведеньь соединения общей формулы I с выходами 10-40%. Примечание. Не кристаллические вещества были гомогенными судя по данным тонкослойной хроматогоафии (S iO :уксусная кислота/этилацетат/толуол, 2:80:18 по объему) и нкюли следукнцие ПМР-спектральные характеристики (определены в растворе CDCl-j с использованием тетрамеТилсилана (ТМС) в качестве внутреннего стандарта): а)(м.д,) (60 MHZ) :1.4,1.5 (дублет(д), 6 протонов, {СН)СН -,1,77, 1.9 Соублет (д), 3 протона, СН 2.0 Гсинглет(с), 3 протона, NCOCHj ; 4.7-5.3 Смультиплет(м), 1 протон, ( 6.5-6.9 квадруплет(к), 1 протон, ; 7,26 синглет(с), 5ароматических npOTOHoaJ; б)ofr (м.д.) (100 MHZ): 0.86-1.0 Гтриплет(т), 6 протонов, СНз( ,,; 1,15-1,35Гм, 2 протона, CKaCHijCH-iCHC HyJ 1,42-1.50 д,6 протонов, (CH-J)2CHJ 1,65-2.35 CM, 4 протона, CHjCH/j.CHjCHCHrtCHjJ; 2,43Гс, 3 протона), NCOCHj 4.05-4.40 Гм, 1 , ротон, CH4(CHci.)aCHCH2CHj f 4.8-5.2 Гм, 1 протон, ( с) СГ-(м.д.) (60 MHZ): 0,7-1.1 Гг, 6протонов,CHjCHnCH/jCH- ; 1.1-1.7 (м, 4 протона, CH CHjCHjCH); 1,421,53 Гя. 6 протонов, (CHa)iCH3; 1.772,35 (м, 4 протона, CHjCH CHjCH); 2.47 (с, 3 протона, NCOCHj); 4,054,60 Гм, 1 протон, СНзСНзСНоСН J 4.735.40 Гм., 1 ripoTOH, CH CHaCHiCHj; 4.73-5.40 м, 1 протон, ) д) А (м.д.)/(100 MHZ): 0.8-1.15 (т, 3 протона, .); 1.18-2.15 м, 12 протонов, CHjCHo. + -(сн)а)5- ; 2.43 Гс, 3 протона, СОСНз ; 3.78-4.32 IM, 3 протона, в) Л (м.д.) (100 MHZ):1.50 Гд, 6 протонов, {CHi)aCHj; 2.22 с, 3 протона, COCHj:;/ 2,30 4- 2.42 2с, 2 протона, норборнил С1 и С4-н)j 4.0 . (т., 1 протон, норборнил С2-ЭНДО-Н)} 5.0 гептет, 1 протон, (СН з)iCHJ f 11.1 (широкий с., 1 протон, NH-)j f) (Л(м.д.) (100 MHZ) 0.83-1.07 IT,, 3 протона, CH(CHi)-i3 1.12-1.68 Ift, б протонов, (CHJ)lCHJ+д, 3 протона, CHjCH. (СН 2)aCHj; + м, 2 протона,, CH-jCHCHiCHjCH J 1.72-2.3 (м, 2 протона, CH CHCHiCH-j) 2.45 (с, 3 протона СОСН) 4.28-4,67 (секстет, 1 протон, {СН„), 4.78-5.27 гептет, 1 протон, ( СН . Исходные вещества формулы W можно получить аналогично описанному по реакции соответствугацих 4-алкиламинОпроизводных формул JJL с кетеном. Они получаются обычно в виде липких твердых веществ, в основном гомогенных по данным тонкослойной хроматографии их использовали в процессе перегруп-. пировкй без дальнейшей очистки. Получение требуемых 4-алкиламино-производных формулы Щ проиллюстрировано следующим: 1-изопропил-4-метилтиотетрагидро1,3, 5-триазин-2,6-дион (6,0 г)и цикло пропиламин ацетат (17,85 г) совместно нагревают с перемешиванием при 150С в течение 3 ч. Смесь охлаждают и добавляют воду (150 мл) Образующееся при этом белое твердое вещество собиpatoT, промывают водой и сушат; полу чают 1-изопропил-4-циклопропиламинотетрагидро-1, 3,5-ТЕ иазин-2,6-дион, с т.пл. 237-238 С. Аналогичным образом получают исход ные вещества общей формулы ДГ из соот ветствующих 4-метилтиосоединений формулы JV по реакции с избыточным количеством соответствукядего амина, в ви де его ацетата: Прим. е чан и е. Смолы были гомогенными, судя по данным тонкослдй ной хроматографии (S jOtjtyKcyCHaK кислота /зтилацетат/ толуол) - 2:35:62 в ббъемном отношении) и имели следую е-ПМР-спектральные характеристики (определение в растворе CDCI с использованием ТМС в качестве внутреннего стандарта); . а)60 MHZ: oft. (м.д.): 0.77-1.17 т, 6 протонов, CHjCHQCHiCHCHiCH з 1.42 И 1.52 д, 6 протонов, (СНз)1СНЗ 1.17-2.07 м. , 6 протонов, СНСНяСНО 3.62-4.32 м, широкий, 1 .протон, CH CHjCHiCHCHoCHj J 4.72-5.3 Гм, 1 протон, (СН)СНЗ 8.17 Хд, ши рокий, I протон - NH-3 б)60 MHZ: f (м.д .): 0.7-9.1 т, 6 протонов, CH CHiCHiCH-l 1.1-1.9 Гм, 8 протонов, CHftCHjj CHuCHl 1.4 1.53 д, 6 протонов, (CHjl/ CHj; 3.64.3 м, широкий, 1 протон, CHjCH/jiCH . СН J 4.7-5.3 м, 1 протон, (СНз)оСН1. с) 90 MHZ: (f- (м.д.) : 0.7-1.05 Гт, 3 протона, CH3CH/CH,2/rtCH3J S 1.11.72 д, 6 протонов, (CHjljCHj +м, 4 протона СНэСН(СН,)СНз +д., 3 протона CHjCH(CHa),;iCH3 ; 3.78-4.2 Гм, широкий, 1 протон, СНзСН(СН2) 4.73-5.28 Ггептет, 1 протон, (СНа), СН (100 MHZ); д) 60 MHZ: r (м.д.): 0.8-1.1 (т,широкий, 6 протонов, СНз(СН2)зСН f 1,21.7 (м, 12 протонов, СНз(СН2)з CHj+д, 6 протонов, (СНэ)о.СНД; 3.76-4.27 м, широкий, 1 протон, СН5(СН1)зСН ; 4. 87-5.32 гептет, 1 протон, (CHaJo СН ; (100 MHZ). Пример 4. Готовят суспензию 1-ИЗОПРОПИЛ-4-(N-ацетил)циклогексиламинотетрагидро-1,3,5-триазин-2,6диона (10 мМ) в смейи воды (50 мл) и 1,2йиметоксиэтана (10 мл). Затем к перемешанной суспензии добавляют бикарбонат натрия (10 мМ) в воде (50 4п) . После выдерживания в течение 1ч при комнатной температуре/раствор отфильтровывают и испаряют фильтрат в вакууме. Твердый остаток обрабатывают небольшим количеством 1,2диметоксиэтана с тем, чтобы получить натриевую соль 1-изопропил-4-(N-ацетил )циклогексиламино-тетрагидро-1 3 , 5-триазин-2,6-диона при значительном количественном Выходе в виде твердого вещества белого цвета, микроанализ которого дал удовлетворительные результаты. Примерз. Раствор 1-изопропил-3-ацетил-4-циклогексиламинотетрагидро-1,3,5-триазин-2,6-диона (1,0 г) в сухом толуоле (20 мл) нагревают до ВО°С в течение 24 ч, когда по данным тонкослойной хроматографии (ТСХ)(на силикагеле, с использОва|1ием-в качестве элюента смеси этанол-гуксусная кислота:трлуол 59:1:40 (объемные доли) в {зеакционной смеси исчезает исходное вещество и появляется основной, новый, медленно выходящий компонент, идентичный по значению Rf С 1изопропил-4-(N-ацетил)-циклогексилами(ИОТетрагидро-1,3,5-триазин-2,6-дионоН (пример 1). Смесь охлаждают до ком,натн6й температуры и обрабатывают,как описано в 1. Таким образом, после перекристаллизации из смеси хлористого метилена с петролейным эфиром (т.кип. 40-60С) пoлyчkют 1изопропил-4-(N-ацетил)-циклогексиламинотетрагидро-1,3,5-триазин-2,6дион (0,15 г), т.пл. 128-131 с. Аналогичным образом, но при использовании кипящего ксилола (v 145 с) в течение 2 ч (после этого времени по данным ТСХ в смеси отсутствует исходное вещество), целевое соединение получают с выходом 12%.
10
867303
Т а б л и,ц а i






Изопропйя
21
69-70
Нон-5-ил
R - алкильный радикал , несущий алкокси-радикал С.|-С4, циклоалкил или алкенил или алкильный радикал Cg-Cig , где связываюгде R и R4 имеют указанные выше 65 значения при нагревании в интервале температур 60-150 С с последующим вьвделением целевого продукта в свободном виде или в виде основной соли.

Авторы
Даты
1981-09-23—Публикация
1979-02-13—Подача