3
R2NCO,
где R2 имеет указавные значения, с последующим получением соли с кислотой и выделяют целевые иродукты известными приемами.
Пригодным тином R, когда он является хлорфеннльным радикалом, может быть, например 4-хлорфенильный радикал. ПригодныМ типом R2, когда он является хлорфен-нльиым рад1п алом, может быть, наприлгер 2-, 4-хло,рфе11Ильные радикалы.
В том случае, когда R представляет собой бром.февильный, нит1рофбнильный, это-ксифеиильный или толильный радикал, R может быть, наоример 4-брО|Мфенил, 4-НИтрофен«л, 4-этоксифенил или 4-толлильным радикалом.
Когда R2 нредставляет собой алкил Сз- Сю, то могут применять: а) радикалы, преимущественно содержащие 4-8 атомов углерода, то есть н-бутил, изобутил или н-октильный радикал.
Однако предпочитают группу соединений, которые получают по предлагаемому способу и которые содержат R представляющий собой изобутильный радикал, а R хлорфенильиый, бромфенильный, нитрофенильпый, этоксифенильный или толяльный радикалы, и в которых группа - NH-СО-NHR находится в жета-положении.
Предлагаемым способом были получены: 1-(3-этилепгуа«иди«о)-3-(3-и - бромфенилуреидо)бензол.
1-(3-изопропилгуа«иди1Но)-3-(3 - /г-хлорфеиилуреидо)бензол.
1-(3-изобутилгуанидино)-3 - (3 - п - хлорфенил)реидо) бензол.
1-(3-изобутилгуаиидино)-3-(3 - ..w - хлорфеП1илуреидо) бензол.
1-(3-изобутилгуанидийо)-3-(3 - о - хлорфенилуреидо) бензол.
1-{3-изобутилгуаниди1Но)-3-(3 - п - брОМфеНилуреидо) бе1нзол.
1-(3-изобутилгуа нидино)-3-(3 -/г - нитрофенилуреидо)бензол.
1 - {3-изобутилгуаниди1но)-3-(3-п - толилиуреидо)бензол.
1-(3-изобутилгуаИидшю)-3-(3-/г - этоксифепилуреидо)бензол.
1-(3-фенилгуанидиио)-:3-(3 -/г - хлорфепилуреидо)бензол.
1-{3-/г-хлорфенИЛгуа1Н.иди«о)-3-(3-н - бутилуреидо)бензол.
1-(3-/г-хлорфенилгуаНидино)-3 - (3 - изобутилуреидо)бензол.
1-{3-/г-хлорфенилгуа«идино)-3-(3-н - октилуреидо)бензол.
1-(3-изопропилгуа«идино)-4-(3-rt - хлорфеннлуреидо) бензол.
1-(3-изобутилгуа1Нидино)-4 - (3 -/г - хлорфенилуреидо)бензол.
1-(3-изопент,илгуан1ИДино)-4-(3 - д - хлорфенилуреидо) бензол и 1-(3-изОбутилгуа«иди1Но)-4- (3-п-толилуреидо) бензол.
ЕсЛИ нужию получить соль, то продукт реакции подвергают взаимодействию с кислотой.
содержащей совместимый с фармацевтической точки зрения а«иоп.
Процесс получения соединений формулы П ведут преимущественно в И1нертном растворителе или разбавителе, например в пиридине, и при 25-:100°С.
Пример I. Павеску 0,7 г изобутилизацианата доба1вляют к раствору 2 г 1-(п-хлорфеиил)-3- (м - а1нилино)гуаниди1нодигидрохлорида в пиридине при комнатной температуре и перемешивают в течение 48 ч. Затем добавляют 0,7 г изобутилизодианата и полученную смесь выдерживают при 50°С в течение 9 дией. Пиридин выпаривают в небольшом вакууме, а
остаток растворяют в 30 мл метанола; раствор кипятят с а-ктивированным углем, фильтруют и упаревают досуха. Твердый остаток pacTiBoряют в метанол-соляной кислоте и подшелачивают раствор 10%-ной гидроокисью
натрия. Осадок отфильтровывают, промывают водой, сушат и превращают в гидрохлорид при помощи растворения твердого остатка в небольшом количестве этанола; добавляют эфир.иый раствор соляной кислоты, а осаждаЮЩ1ИЙСЯ твердый осадок промывают избытком сухого эфира. Этот осадок промывают небольшим количеством изопропилового спирта и получают 1- (З-п-хлорфенилгуаеидино) -3- (3-изобутилуреидо)-бензолгидрохлорид с т. пл.
207-209°С.
Пример 2. К раствору 19,6 г 1-изобутил- 3 - ж - аиилиногуанидинодигидрохлорида в 100 мл пиридина прибавляют по каплям раствор 11,5 г и- хлорфенилизоцианата в 25 мл пиридина при комнатной температуре. Смесь перемешивают в течение 16 ч и отгоняют пиридин в невысоком вакууме. Смолистый 01статок встряхивают со смесью 100 мл эфира и 10 мл 1%-ного водного раствора гидроокиси натрия
для удаления солянокислого пиридина, после чего кристаллизуют продукт. Твердый остаток отфильтровывают, промывают водой, эфиром и сушат. После перекристаллизации из смеси этанол/петролейпый эфир с т. кип. 40-60°С
получают 1-(3-изобутилгуанидино) - 3 - (3 - га-хлорфенилмочевино) бензол с т. пл. 215- 216°С.
Аналогично с применением соответствующих анилиногуанидинов и подходящих изоциапатов получают приведенные в табл. 1, соединения.
-NH-CO-NHR-HCl
R NH-C-NH55
II 5Н
Пример 3. Способ, описанный в примере 2, повторяют, но используют соотвбтствующий замещенный фениланилиеогуанидин и изоцианат вместо изобутилизоциаита. При этом получают соединения, приведенные в табл. 2.
Пример 4. Повторяют способ, описа.ппый в примере 2, используя соответствуюндий а ниi NH-c-NHIt
NH
NH-CO-NHR-HCl
Таблица 1

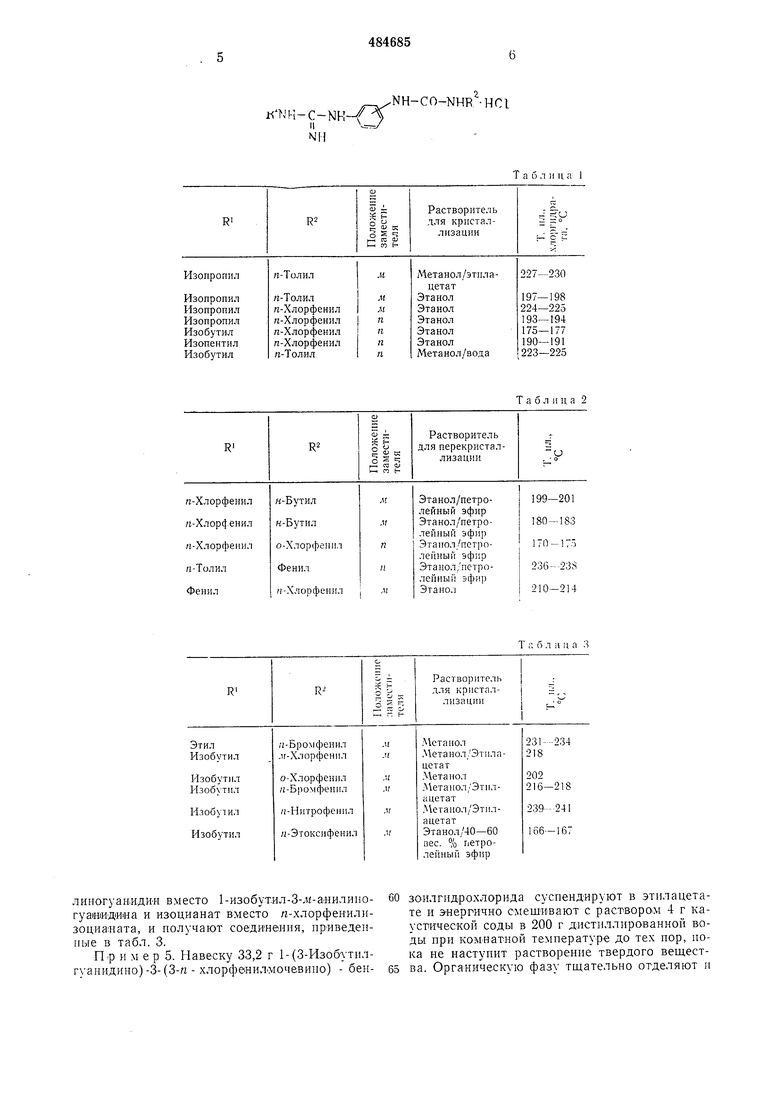


линогуанйдин вместо 1 -изобутил-З-.и-анилипогуаиидиНа и изоцианат вместо я-хлорфенилнзоциаиата, и получают соединения, ириведенIIые в табл. 3.
Пример 5. Навеску 33,2 г 1-(3-Изобутилгуанидино)-3-(3-п - хлорфениЛМочввино) - бенТаблица 2
Т a б л it ц а 3
зойлгидрохлорида суспендируют в этилацетате и энергично смешивают с раствором 4 г каусрической соды в 200 г дистиллированной воды при кoмa aтнoй температуре до тех пор, пока не наступит растворение твердого вещества. Органическую фазу тщательно отделяют и
7
перемешивают с раствО(ром 11,8 г глюко-нолактона ;в 250 мл дистпллнроваияой воды в течеНие 16 ч. ВоДНую фазу отделяют и вымораживают, получая 1-(3-|ИзобутилгуанИдино--3-(3-лхлорфениллючевино) бензолглюконат, который после кристаллизации из иебольшого объема абсолютного этанола имеет т. пл. 144-146°С.
Предмет изобретения
Способ получения заМещенНых гуаиидинофенилмочевины общей формулы I
JfH-CO-NHR2
-П
K-4 H-c-:Nii
II
NH
где R - этил, изолропил, изо бути л, изопе нТ1ИЛ, фенил, хлорфенил, талил; R2 - алкил, Сз-Сю фенил, хлорфенил, бромфенил, нитрофенкл, этоксифе«ил, тол.ил, причем
а) при R - Э1ТИЛ и R2 - броадфенил, группа - NH-СО-NHR2 находится в жега-иоложении;
8
б)при R - хлорфенил и R - алкил Сз-Сю, группа - NH-СО-NHR2 - находится в и ега-положбнии;
в)при R - изопропил, изобутил, изопе-нтил, фенил И R2 - хлорфенил, бромфенил, иитрофеиил, этокоифенйл, толил, группа - МЫ-СО-NHR2 находится в мета- или параноложении;
г)при R - толил, хлорфенил и R - фенил, о-хларфенил, группа-NH-СО-NHR - находится в пара-положенИ«, отличающийся тем, что амии общей формулы III
NH.
HNH-C-NH
/
т
где R имеет указанные значения, подвергают взаимодействию с изоцианатами формулы IV
R2NCO,
где R2 имеет указаиные значения, с последующим выделением целевого продукта или превращением его в соль известными приемами.
Авторы
Даты
1975-09-15—Публикация
1972-01-06—Подача