например из смеси хлороформа и гексана.
Соединения активны при лечении амебных инфекций слепой кишки и печени у теплокровных животных.
Две следующие пробы устанавливают эту активн ость.
В пробах использовали полученный из Национального Института Здоровья штамм EntamiеЬа histolitica. Этот штамм и неидентифицированную фекальную флору культивировали при 37°С на среде Кливленда-Коллиера. Эта среда состоит из печеночного отвара на агаровой основе, покрытого смесью лошадиной сыворотки и физиологического раствора (1:6), к которой добавлено несколько миллиграмм рисовой пудры. Бактерии пересевали на свежую среду два раза в неделю.
Инфекции слепдй кишки у самок белых крыс. Покрытие (0,25 мл), содержащее большие количества амеб, инъекцируют в слепые отростки прямой кишки анестезированных отнятых от самки в период кормления крыс. Лечение начинают на следующий после заражения день. Соединения растворяют в 0,2% водном агаре и дают один раз в день с едой в течение 5 дней последователно. Через 6 дней после введения амебной инфекции крыс умерщвляют и соскоб со стенки слепого отростка прямой кишки каждой крысы смешивают с каплей 0,85% физиологического (солевого) раствора и исследуют микроскопически на наличие амеб. Крыса считалась выздоровевшей, если в пробе не наблюдали наличия амеб. ДЙя каждого режима рассчитывают степень извлечения или очищения (отношение количества выздоровевших крыс к количеству подвергавшихся лечению) и соотносят эту величину с самопроизвольным выздоровлением, наблюдавшимся у не подвергавшихся лечению коатрольных крыс,, подвергнутых заражению. Активной считается самая малая доза, которая вызывает очищение или излечение 50% и более подвергнутых такому лечению крыс. Величина активной дозы измеряется в мг/кг/день. Результаты действия предлагаелих соединений совместно с результатами испытания для известных эффективных лекарственных препаратов приведены в табл. 1.
Гепатитные (печеночные) инфекции у самок золотистых хомячков.
Кусочек заполненной амебами губки пригодной для усвоения, площадью около 25 мм вжИвляют между средними долями печени инестезированных хомячков . Неподвергавшиеся лечению хомячки обычно умирают от следовавшей за вживлечием инфекции на 6 день. Лечение начинают в день введения инфекции, как только хомячки приходят
в себя после операционной анестезии. Испытываемые соединения растворяют или суспендируют в 0,2% водном агаре и дают животным дважды в день с едой в течение 5 дней последовательно. Эффективные дозы предотвращают смертность. Число выживших хомячков корректируют с учетом неспицйфичного выживания у группы контрольных животных, неподвергавшихсй лечению. Активной считается низшая доза, выраженная в мг/кг/день, которая предупреждает смертность 50% и более животных в течение 14 дней после заражения и лечения. Результаты испытаний типичных предлагаемых соединений в сопоставлении с активными дозами известных эффективных для лечения содинений приведены в табл. 2.
Новые 2,6-антрахинониленамидины полезны для лечения секальных и гепатитных амебных инфекций у теплокровных животных при их применении в количествах 0,5-40 мг на 1 кг живого веса животного в день. Предпочтительный диапазон доз, при котором достигнуты наилучшие результаты, составляет 2 - 29 мг/кг/день. Таким образом, дневная доза для субъекта весом 70 к составляет от 35 мг до 2,8 г а предпочтительно - от 140 мг до 2 грамм.
Подходящие для орального применения препараты могут быть в виде капсул, таблеток, суспензий, сиропов и т.п. В случае таблеток основной активный компонент смешивают с традиционными ингредиентами, такими, как крахмал, лактоза, сахароза, сорбит, тальк, стеариновая кислота, стеарат магния, дикальций фосфат и т.п. материалами, известными как нетоксичные фармацевтические носители или разбавители.
Пример. NN -2,6-Антрахинониленбис-(N,N-диметилциклопропан карбоксамидин).
К раствору 300 мл 40% водного диметиламина в 500 мл эфира добавляют по каплям при 10-25с 52,0 г хлорангидрида циклопропанкарбоновой кислоты в 100 мл эфира. Смесь перемешивают при комнатной температуре в тече.ние 2- ч, добавляют 50 мп воды. Эфирный слой отделяют, три раза промывают по 50 мл воды, сушат сульфатом натрия и фильтруют. Эфир отгоняют, остаток перегоняют и получают N,Nдиметилциклопропанкарбоксамид в виде бесцветного масла.
к раствору 34,0 г этого продукта в 200 МП ацетонитрила прибавляют при 5-:15°С за 30 мин 36,8 г хлорокиси фосфора, перемешивают 30 мин при комнатной температуре, прибавляют 23,8 г 2,6-диамин9антрахинона, перемешивают 20 ч, при 60°Cf вливают смесь в 500 мл воды со льдом, затем постепенно добавляют 75 мл 10 н. раствора едкого натра, осадок отфильтровывают, промывают водой и сушат. После перекристаллизации из 2-метоксиэтанола получают продукт в виде оранжевых кристаллов с т.пл. 241243°С. П р и м е р 2. N, 2,6-антрахино ниленбис (N,М-диэтилциклопропанкарбоксамидин). Реакцию раствора 134 мл диэтиламина в 600 мл эфира и 52,0 г хлорангидрида циклопропанкарбоновой кислоты проводят по примеру 1 и получают NIN-диэтилциклопропанкарбоксамид в виде бесцветного масла. Из 42f4 г вышеуказанного продукта 23,8 г 2,б-диаминоантрахинона,36,8 г хлорокиси фосфора и 200 мл ацетонит.рила, по примеру 1после перекристаллизации из 2-метоксиэтанола, получают продукт в виде оранжевых крис таллов с т. пл. 166-168°С. Примерз. N,,6-Антрахинониленбис-(Ы,Ы-диметилциклобутанкарбоксамидин). К раствору 19,1 г амида N, N-диметилциклобутанкарбоновой кислоты в 150 мл ацетонитрила добавляют 18,4 г хлорокиси фосфора при 5-10с.. Полученную смесь перемешивают при комнатной температуре 1 ч, затем добавляют 11,9 г 2,б-диаминоантрахинона. перемешивают при в течение 10 ч выливают в 600 мп ледяной воды и подшелачивают 5н NaOH. Оранжевые кристаллы собирают фильтрованием и промывают водой. Кристгшлы растворяют в хлороформе и фильтруют, хлороформ отгоняют при пониженном давлении. Остаток кристаллизуют из метилцеллозольва и получгиот 16,2 г оранжевых кристаллов с т.пл, 209-211°С.
Таблица П р и .м е р 4. N,,6-Антрахинрниленбис-(N, N-диметил-п-хлорбензамидин) . К перемешиваемому раствору 27,6 г N,N-диметил-п-хлорбензамида в 100 мл ацетонитрила, охлажденному до 515°С на бане с ледяной водой, в течение 30 мин добавляют 10,8 мл хлорокиси фосфора. Баню с ледяной водой снимают и продолжают перемешивание при комнатной температуре 30 мин, затем добавляют 11,9 г 2,6-диаминоантрахинона и продолжают перемешивание при комнатной температуре в течение 1 ч, и 20 ч при 60°С. Затем смесь осторожно выливают в смесь воды и льда, перемешивание продолжают в течение 1 ч, постепенно добавляя 75 мл Юн, гидроокиси натрия. Оранжевый осадок собирают фильтрованием, промывают водой и сушат в вакууме при 80°С. Высушенное вещество размешивают с хлороформом (300 мл) и фильтруют. Фильтрат 2 раза промывают водой, сушат над сульфатом магния, фильтруют и упаривают в вакууме до сиропа. Это вещество размешивают с 25 мл метилового спирта и образовавшиеся красные кристаллы собирают фильтрова нием. Продукт npONMBaroT диэтиловым эфиром и сушат в вакууме. Т.пл. 296298С. П р и м е р 5. N, N -2,6-Антрахйнониленбис (NIN-диметил-п-фторбензамидин). Это соединение получгиот по примеру 4, используя 32,8 г N,N-диметил-пфторбензамидина, 133 мл ацетонитрила, 14,7 мл хлорокиси фосфора и 15,9 г 2,6-диаминоатрахинона. Т.пл. 288-289°С (разложение).

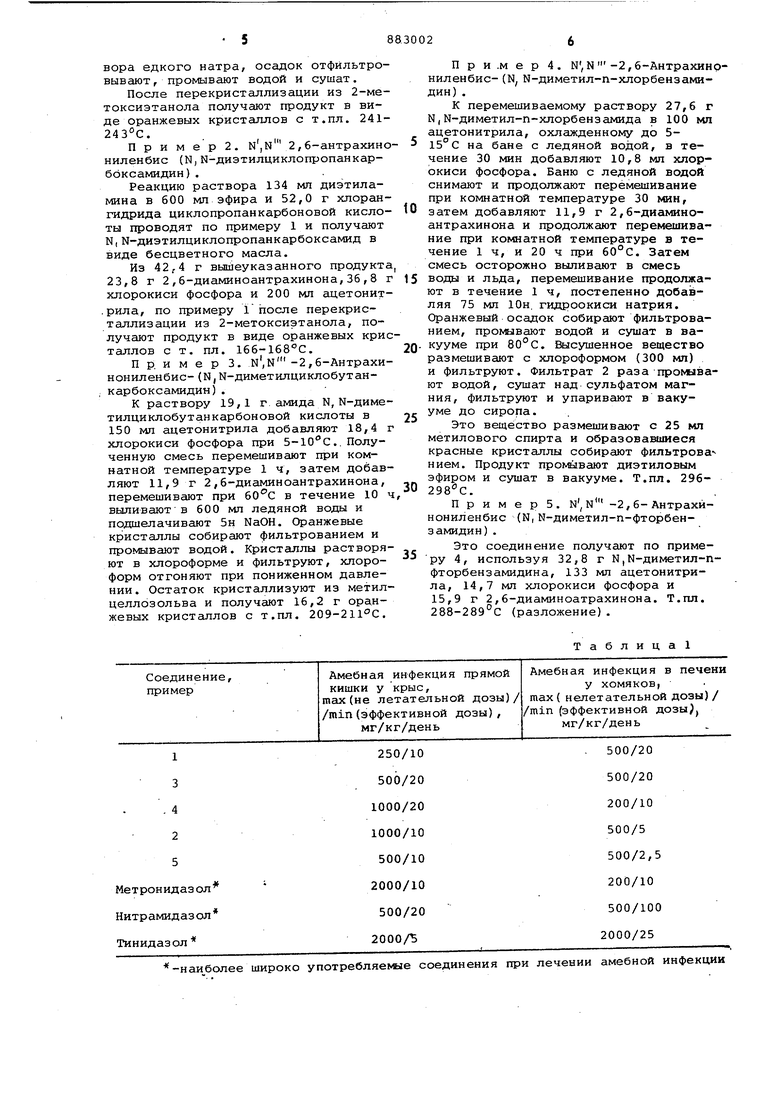
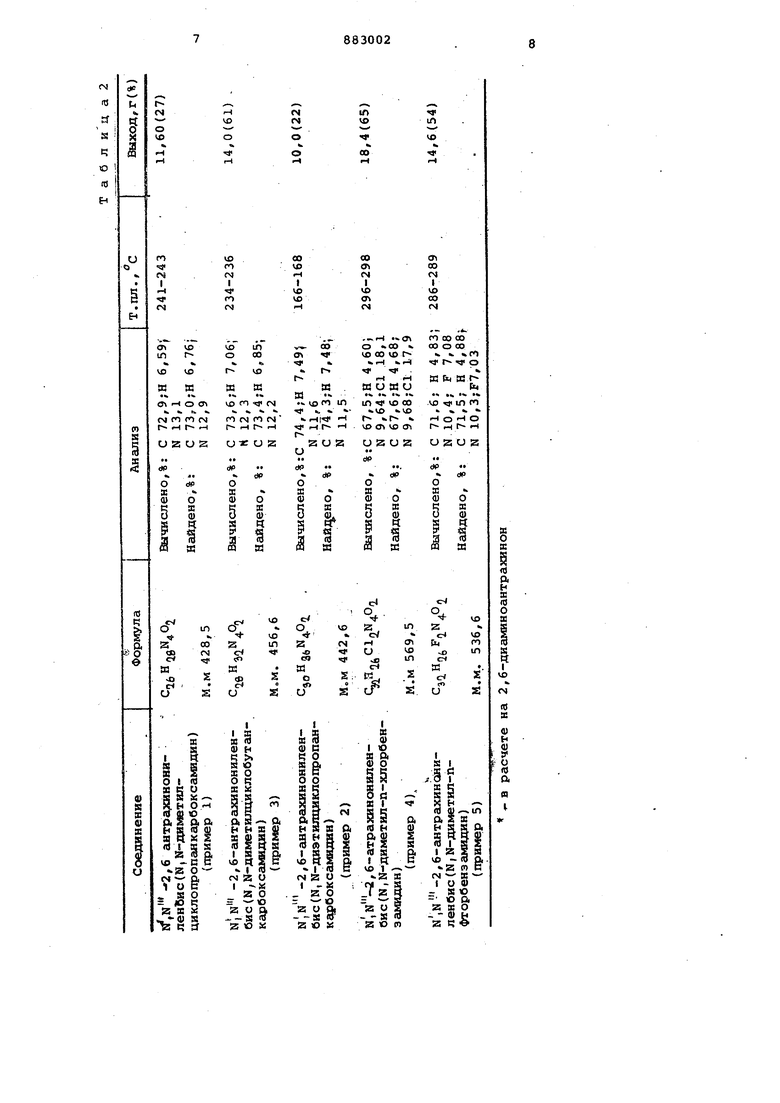


-наиболее широко употребляемые соединения при лечении амебной инфекции Формула изобретения Производные антрахинона общей фор О ft I 4y r -N t sN-lLJ К )Г .«N гп (i)i О - гг„ .L™T°Sooy Lrn хлорфенил- или п - фторфенил, Rn метил, обладающие противоамебной активностью в отношении Entamieba histolitica. Источники информации, принятые во внимание при экспертизе 1. Машковский М.Д. Лекарственные ;i -«««- .
Авторы
Даты
1981-11-23—Публикация
1976-08-19—Подача